非离子型聚丙烯酰胺单用及与纳米微粉硅胶联用对甘草次酸脂化乳稳定性的影响Δ
金粟,王秀丽,曲昌海,阮婧华(.北京中医药大学中药学院,北京0002;2.贵州省中国科学院天然产物化学重点实验室,贵阳 550002)
脂化乳与生物膜具有良好的生物相容性,将难溶性药物制备成脂化乳剂后,可以增加药物的溶解度,提升药物的胃肠道稳定性,降低刺激性,也可以促进药物的肠淋巴转运,提高生物利用度[1-2],因此具有良好的应用前景。通过提升脂化乳的稳定性,对于扩展其应用范围具有很大帮助。
甘草次酸的油水分配系数P的对数值lgP为6.57,其难溶于水,水中溶解度仅为6.32 mg/L[3],口服生物利用度低,适合包载于脂化乳,因此本文选择以甘草次酸为模型药,选择以非离子型聚丙烯酰胺(型号:NPAM 1400)为稳定辅料,加入到甘草次酸脂化乳中,考察其对脂化乳稳定性的提升效果,并以此浓度与前期[4]筛选的两种纳米微粉硅胶(nSiO2)进行组合,考察两种材料组合使用对甘草次酸脂化乳稳定性的影响,初步确定两种稳定辅料的加入浓度,以期对进一步提升脂化乳的体外稳定性提供依据。
1 材料
1.1 仪器
G16型医用离心机(北京白洋医疗器械有限公司);BS110S型万分之一电子分析天平(北京赛多利斯仪器系统有限公司);TU-1810型紫外-可见分光光度计(北京普析通用仪器有限责任公司);SCI-ENTZ-ⅡD型超声波细胞粉碎机(宁波新芝生物科技股份有限公司)。
1.2 药品与试剂
甘草次酸脂化乳(北京中医药大学中药学院实验室自制,批号:201604,规格:约含甘草次酸1.25 mg/mL);非离子型聚丙烯酰胺(上海麦克林生化技术有限公司,型号:NPAM 1400,批号:P821242);nSiO2(广州市敬益新材料有限公司,型号:亲水性-380、疏水性-215);水为纯净水。
2 方法与结果
2.1 稳定辅料的选择
2.1.1 非离子型聚丙烯酰胺 聚丙烯酰胺是丙烯酰胺均聚物或与其他单体共聚而成的线性高分子化合物的总称,是水溶性高分子化合物中应用最为广泛的品种之一。因为结构中具有酰胺键,易形成氢键,具有良好的水溶性,可以被用作有效的絮凝剂、增稠剂等。已有研究[5-6]报道,聚丙烯酰胺为无细胞毒性材料,并且对长期使用其的患者进行血常规和尿常规检查均显示无异常。故本文选择以非离子型聚丙烯酰胺为稳定辅料,将一定浓度的非离子型聚丙烯酰胺加入到甘草次酸脂化乳中,希望通过增加制剂的黏度,提升脂化乳的物理稳定性。
2.1.2 nSiO2nSiO2是一种具有良好生物相容性、物理化学稳定性的超微纳米材料,可以对脂化乳制剂稳定性提升起到一定的作用[4]。因此,本文选择亲水性和疏水性的nSiO2分别与非离子型聚丙烯酰胺组合使用,希望能进一步提高甘草次酸脂化乳的稳定性。
2.2 稳定性考察
2.2.1 稳定性系数 本文采用紫外-可见分光光度计,分别测定脂化乳离心前后稀释液在一定波长处的吸光度,计算稳定性系数(KE)[7],KE值越小,说明离心操作对制剂中分散颗粒上浮或下沉的影响越小,即制剂稳定性越高,以此来评判加入稳定辅料后甘草次酸脂化乳稳定性的提升效果。具体操作:取制剂1 mL于1.5 mL尖底离心管中,以离心半径为5.7 cm、4 000 r/min离心10min,精密移取下层制剂(取样深度1 cm处)至10 mL量瓶中,纯净水定容,使用紫外-可见分光光度计以纯净水调零,检测500 nm波长处的吸光度(A);另精密移取未离心的制剂1 mL于10 mL量瓶中,纯净水定容,同法检测500 nm波长处的吸光度(A0),按公式KE=(A0-A)/A0×100%计算KE。
2.2.2 稳定性系数之比 为了减小误差,消除每批空白制剂之间的差别,笔者还以稳定性系数之比(KE/KE空白)作为评价加入不同稳定辅料后甘草次酸脂化乳稳定效果的指标,公式为KE/KE空白=加入稳定辅料后制剂的KE/未加入稳定辅料的制剂的KE空白。
2.3 非离子型聚丙烯酰胺单用
2.3.1 非离子型聚丙烯酰胺浓度初筛 非离子型聚丙烯酰胺为水溶性高分子材料,本研究将非离子型聚丙烯酰胺隔夜充分溶胀作为水相,在预试验的基础上,与甘草次酸脂化乳剂混合制备得到含非离子型聚丙烯酰胺0、200、400、600 mg/L的甘草次酸脂化乳[8]。根据加入非离子型聚丙烯酰胺质量浓度不同,分为空白脂化乳组和非离子型聚丙烯酰胺200、400、600 mg/L脂化乳组,分别按“2.2.1”项下方法计算KE,比较各组制剂的稳定性,结果见表1。
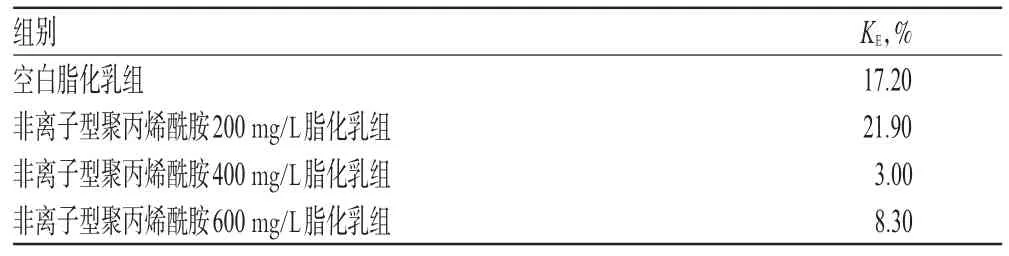
表1 200、400、600 mg/L非离子型聚丙烯酰胺对甘草次酸脂化乳稳定性的影响(n=3)Tab 1 Effects of 200,400,600 mg/L non-ionic polyacrylamide on the stability of Glycyrrhetinic acid lipo-emulsion(n=3)
由表1结果可以看出,空白脂化乳组的KE为17.20%,加入非离子型聚丙烯酰胺后,除非离子型聚丙烯酰胺200 mg/L脂化乳组的KE大于空白脂化乳组外,其余两组脂化乳的KE均减小,表明加入400、600 mg/L非离子型聚丙烯酰胺可提高甘草次酸脂化乳的稳定性,其中400 mg/L时对稳定性的提升效果较明显。
2.3.2 非离子型聚丙烯酰胺浓度的确定 在“2.3.1”项下结果的基础上,再次制备含非离子型聚丙烯酰胺0、300、400、500 mg/L的甘草次酸脂化乳,根据加入非离子型聚丙烯酰胺质量浓度不同,分为空白脂化乳组和非离子型聚丙烯酰胺300、400、500 mg/L脂化乳组,分别按“2.2.1”项下方法计算KE,比较各组制剂的稳定性,结果见表2。
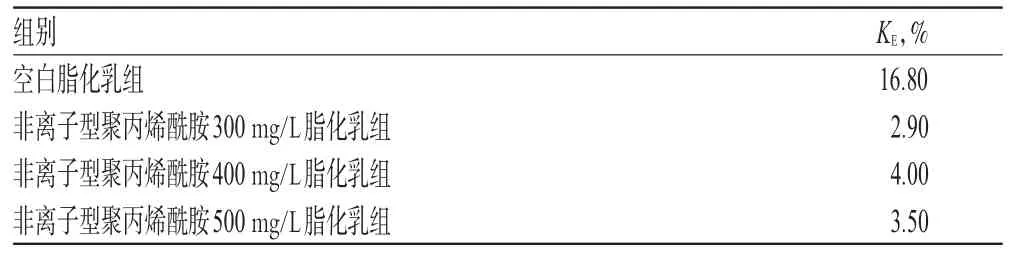
表2 300、400、500 mg/L非离子型聚丙烯酰胺对甘草次酸脂化乳稳定性的影响(n=3)Tab 2 Effects of 300,400,500 mg/L non-ionic polyacrylamide on the stability of Glycyrrhetinic acid lipo-emulsion(n=3)
由表2结果可以看出,加入非离子型聚丙烯酰胺的甘草次酸脂化乳的KE均小于空白脂化乳组,说明加入非离子型聚丙烯酰胺可以有效提升甘草次酸脂化乳的离心稳定性。通过比较KE的差异,可以发现随着非离子型聚丙烯酰胺加入质量浓度的增加,KE表现出先增大后减小的现象,但3个质量浓度之间差别不大。遵循尽量减少应用辅料原则,最终确定非离子型聚丙烯酰胺加入质量浓度为300 mg/L。
2.3.3 验证试验 平行制备3批非离子型聚丙烯酰胺加入质量浓度为300 mg/L的甘草次酸脂化乳及不加非离子型聚丙烯酰胺的甘草次酸脂化乳(空白脂化乳),分别按“2.2”项下方法计算KE和KE/KE空白。结果显示,空白脂化乳的KE空白为17.6%,3批含非离子型聚丙烯酰胺300mg/L的甘草次酸脂化乳的KE分别为3.8%、3.9%、3.3%(RSD=9%,n=3),KE/KE空白分别为0.22、0.22、0.19,结果均在可接受范围内,表明该方法基本稳定。由此确定,非离子型聚丙烯酰胺可提高甘草次酸脂化乳的离心稳定性,其加入质量浓度为300 mg/L。
2.4 非离子型聚丙烯酰胺与nSiO2联用
根据“2.3”项下结果和预试验结果,考察300 mg/L非离子型聚丙烯酰胺分别与不同浓度nSiO2[亲水性(0.2%、0.3%、0.4%)和疏水性(0.2%、0.3%、0.5%)]联用对甘草次酸脂化乳稳定性的影响。试验分为空白脂化乳组,低、中、高浓度亲水性nSiO2脂化乳组,低、中、高浓度疏水性nSiO2脂化乳组,非离子型聚丙烯酰胺+低、中、高浓度亲水性nSiO2脂化乳组,非离子型聚丙烯酰胺+低、中、高浓度疏水性nSiO2脂化乳组,分别按“2.2”项下方法计算KE和KE/KE空白,比较各组制剂的稳定性,结果见表3。

表3 300 mg/L非离子型聚丙烯酰胺与nSiO2联用对甘草次酸脂化乳稳定性的影响Tab 3 Effects of 300 mg/L non-ionic polyacrylamide combined with different concentrations nSiO2 on the stability of Glycyrrhetinic acid lipoemulsion
由表3结果可以看出,在甘草次酸脂化乳只加入nSiO2时,低浓度疏水性nSiO2脂化乳组的KE最小;非离子型聚丙烯酰胺与nSiO2联用时,非离子型聚丙烯酰胺+低浓度疏水性nSiO2脂化乳组的KE最小。但是结合“2.3.3”项下结果,单独使用非离子型聚丙烯酰胺的甘草次酸脂化乳的KE/KE空白约为0.22,而非离子型聚丙烯酰胺+0.20%疏水性nSiO2脂化乳的KE/KE空白为0.27,排除空白脂质体的干扰后可以看出,非离子型聚丙烯酰胺与疏水性nSiO2联用时甘草次酸脂化乳的稳定性并没有比单用非离子型聚丙烯酰胺时提高。综合考虑,单用300 mg/L非离子型聚丙烯酰胺时甘草次酸脂化乳的稳定性最好。
3 讨论
稳定体系对提高脂化乳制剂稳定性作用明显,本课题组已经进行了大量的稳定辅料的考察,筛选出了nSiO2和聚丙烯酰胺的增加稳定性效果较为突出[4]。nSiO2是通过物理包裹的方式提高脂化乳的稳定性。聚丙烯酰胺溶于水后可以形成网状的立体结构,避免了脂化乳粒相互聚集,聚丙烯酰胺黏度随温度降低而增大[9],脂化乳放置在室温下,温度降低可以更好地发挥聚丙烯酰胺提高脂化乳稳定性的效果。
笔者在预试验中对聚丙烯酰胺的种类也进行了筛选,分别考察了非离子型和阴离子型两种聚丙烯酰胺单独使用对甘草次酸脂化乳离心稳定性的影响,结果显示,非离子型聚丙烯酰胺提高脂化乳稳定性的效果更好,因此本研究仅对非离子型聚丙烯酰胺开展进一步的试验,比较了非离子型聚丙烯酰胺单独使用及其与nSiO2联合使用时对甘草次酸脂化乳离心稳定性的影响。
本研究结果发现,联合使用nSiO2和聚丙烯酰胺两种稳定辅料时,脂化乳的稳定性没有明显的提高,考虑原因可能是nSiO2与聚丙烯酰胺提高稳定性的原理不同所致,具体原因有待进一步研究。最终结果显示,单用300 mg/L非离子型聚丙烯酰胺时甘草次酸脂化乳的稳定性最好。
[1]陈芳宁,张秀荣,王秀丽,等.丹酚酸B脂化乳的制备及其稳定性研究[J].现代药物与临床,2017,32(2):179-182.
[2]李士远.抗癌先导物T-OA脂质体及甘草次酸脂质体的肠淋巴转运研究[D].北京:北京中医药大学,2017.
[3]曹姗.口服甘草次酸急性毒性、体内分布及对血清离子元素含量影响的研究[D].哈尔滨:东北林业大学,2012.
[4]李士远,金粟,陈芳宁,等.不同加入量亲水性/疏水性纳米二氧化硅对甘草次酸脂化乳稳定性的影响研究[J].中国药房,2017,28(7):951-953.
[5]田菲,吴军正,鲁开化,等.聚丙烯酰胺水凝胶对L929细胞的细胞毒性研究[C].长春:首届国际医用聚丙烯酰胺水凝胶--奥美定学术研讨会,2000:326-329.
[6]VON BUELOW S,VON HEIMBURG D,PALLUA N.Efficacy and safety of polyacrylamide hydrogel for facial softtissue augmentation[J].Plast Reconstr Surg,2005,116(4):1137-1146.
[7]马萍,辛艳茹,杨京燕,等.离心分光光度法测定乳剂的稳定性[J].药学实践杂志,2001,19(1):23.
[8]金粟,李士远,张秀荣,等.甘草次酸脂化乳的质量评价指标探讨[J].中国药房,2017,28(6):800-803.
[9]孙红英,陈红祥,李金波,等.聚丙烯酰胺溶液粘度的影响因素[J].精细石油化工进展,2005,6(9):1-3.

