雷公藤多苷对贝伐珠单抗诱导的小鼠蛋白尿的影响及其相关机制的研究
闻 妹,陈映霞,马兴群,黄 勇,曹梦苒,江 超
过去十年中,血管形成抑制剂已广泛应用于临床,贝伐珠单抗(bevacizumab,BEV)为新型抗血管内皮生长因子(vascular endothelial growth factor,VEGF)的人源化单克隆抗体,通过选择性地结合VEGF,阻止VEGF与其受体结合,进而抑制新生血管的形成,达到抑制肿瘤生长的目的。蛋白尿是BEV较常见的不良反应之一,通过抑制血管内皮生长因子信号通路,导致肾功能损伤。这一不良反应目前尚无有效预防及治疗方法,一旦出现3级及3级以上蛋白尿,建议停用血管形成抑制剂,很大程度上降低了其临床治疗效果[1]。多项研究[2-3]证实雷公藤多苷片(Tripterysiumwilfordiipolyglucoside,TWP)可以通过维持肾小球足细胞的功能,降低糖尿病肾病相关蛋白尿。该研究在体外研究的基础上[4],观测TWP对BEV相关小鼠肾损伤的修复作用并探索讨论其作用机制。
1 材料与方法
1.1材料选用清洁级雄性ICR(institute of cancer research)小鼠30只,由南京军区总院实验动物中心提供。BEV注射液购自瑞士罗氏制药公司;雷公藤多苷片购自上海复旦复华有限公司;cDNA第一链合成试剂盒购自美国 Thermo Fisher (K1622)公司;氯仿(500 ml)、异丙醇(500 ml)购自中国南京化学试剂有限公司;兔抗鼠VEGF单克隆抗体、兔抗鼠nephrin单克隆抗体、兔抗鼠podocin单克隆抗体购自美国Abcam公司。
1.2实验分组30只健康清洁级实验小鼠适应性喂养1周后,随机分为5组: 对照组:尾静脉注射相同体积生理盐水,1次/周,共4周;BEV组:尾静脉注射BEV 60 mg/(kg·周),共4周;BEV+TWP1组:尾静脉注射BEV 60 mg/(kg·周),喂服TWP 4 mg/(kg·d),共4周;BEV+TWP2组:尾静脉注射BEV 60 mg/(kg·周),喂服TWP 8 mg/(kg·d),共4周; BEV+TWP3组:尾静脉注射BEV 60 mg/(kg·周),喂服TWP 16 mg/(kg·d),共4周;每周称体重调整用药剂量。4周后采集小鼠24 h尿液,测量尿蛋白总量;采集小鼠血液标本,检测血液中血尿素氮(blood ureanitrogen,BUN)、血肌酐(serum creatinine scr,Scr)、谷草转氨酶(glutamic oxalacetic transaminase,AST)、谷丙转氨酶(glutamic-pyruvic transaminase,ALT)等生化指标。最后解剖小鼠,取出肾组织,HE染色方法观察肾小球结构改变,通过电镜观察足细胞超微结构变化,免疫组化方法观测肾组织VEGF、nephrin及podocin蛋白表达变化,Q-PCR方法检测VEGF mRNA、podocin mRNA及nephrin mRNA表达。实验观察过程中,动物自由活动、饮水、进食。
1.3标本收集4周末收集24 h尿液,测尿中蛋白总量,眼球取血,检测血液中Scr、BUN、AST、ALT等指标。解剖小鼠,取出肾组织,行免疫组化及分子检测。
1.424h尿蛋白测定根据试剂盒说明书测定。
1.5血生化指标血清Scr、BUN、AST、AST等生化指标按照试剂说明书在全自动化生化仪上检测。
1.6肾组织的光镜检查取一部分肾组织,大小约0.5 cm,10%福尔马林固定,石蜡包埋,切片厚度2 μm,行HE染色后光镜下观察。
1.7电镜检测足细胞超微结构改变取小于1 mm3肾组织块,用2.5%戊二醛固定,用0.1 mol/L磷酸漂洗液漂洗3次。1%锇酸固定液固定2~3 h,再用0.1 mol/L 磷酸漂洗液漂洗3次;最后经脱水、烘烤、染色后,Hitachi7500透射电镜下观察足突和基膜改变,拍片。
1.8免疫组化法观察肾组织VEGF、nephrin、podocin分布将石蜡切片脱蜡,加入兔抗鼠抗体(VEGF、podocin、nephrin稀释浓度均为1 ∶100)孵育4 ℃过夜,严格按照试剂盒说明操作,切片完成后光镜下观察。
1.9Q-PCR分析VEGF、nephrin、podocinmRNA的表达操作严格按照Q-PCR试剂盒说明书进行,引物均由南京思普金科技有限公司提供。逆转录反应:起始模板RNA 2 ng,反应体系为10 μl,每个检验指标做3个复孔。反应条件为:95 ℃预变性2 min,95 ℃变性15 s,60 ℃退火20 s,72 ℃延伸40 s。引物分别是qmPodocin(123 bp) F:5′-GACCAGAGGAAGGCATCAAGC-3′,R:5′-GCACAACCTTTATGCAGAACCAG-3′;qmVEGF(105 bp) F:5′-CACATAGAGAGAATGAGCTTCC-3′,R:5′-CTCCGCTCTGAACAAGGCT-3′;qmNephrin(87 bp) F:5′-TCTGGGTCCAAACCCTAAGATT-3′,R:5′-TCAATAAGCAGGTGGAACTCAC-3′。
2 结果
2.124h尿蛋白比较BEV组24 h尿蛋白量显著高于对照组;与BEV组比较,BEV+TWP2、BEV-TWP3组24 h尿蛋白量明显降低,差异具有统计学意义(P<0.01);BEV+TWP1 24 h尿蛋白量差异无统计学意义。见图1。

图1 各组小鼠24 h尿蛋白量的变化
A:对照组;B:BEV 组;C: BEV-TWP1组;D:BEV-TWP2组;E: BEV-TWP3组;与对照组比较:**P<0.01;与BEV组比较:##P<0.01
2.2血生化分析各组小鼠ALT、AST、BUN、CREA差异无统计学意义(P>0.05)(表 1)。
2.3肾组织病理变化光镜下观察对照组小鼠肾组织结构正常;BEV+TWP1、BEV组小鼠肾小球内皮细胞缩小,改变后的结构呈空泡状;与BEV组比较,BEV+TWP2、BEV-TWP3组肾小球结构有明显恢复,见图2。
2.4电镜方法观察肾足细胞超微结构对照组:足细胞形态结构正常;BEV组、BEV-TWP1组:足细胞足突显著减少、广泛融合,微绒毛减少、变短,内皮孔明显增多、扩大、不规则,基底膜局部增厚;BEV-TWP2组、BEV-TWP3组:足细胞足突融合、微绒毛减少、基底膜增厚均明显改善,内皮孔分布正常,BEV-TWP3组小鼠的足细胞接近正常。见图3。
阳极浸在稀硫酸溶液中,电解过程中生成较多H+,H+可透过阳离子交换膜定向迁移到产品室。阴极浸在氢氧化钠溶液中,电解过程中生成较多的OH-,由于阳离子交换膜的限制,只可能是原料室中Na+定向迁移到阴极室,以使阴极室正、负电荷保持平衡。这导致原料室中向产品室定向迁移,必定会跟阳极室迁移过来的H+反应生成次磷酸。强还原性微粒容易在阳极被氧化,若将阳极直接浸入次磷酸溶液中,必定会有次磷酸直接被氧化成亚磷酸、磷酸等,产品就会有多种杂质。
2.5免疫组化检测VEGF、nephrin、podocin蛋白的表达免疫组化结果:对照组、BEV+TWP2、BEV-TWP3组小鼠肾组织VEGF的表达为中、强阳性,BEV组为阴性或弱阳性。见图4~6。
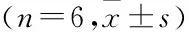
表1 各组小鼠血清生化指标的比较

图2 小鼠肾小球变化 HE×400
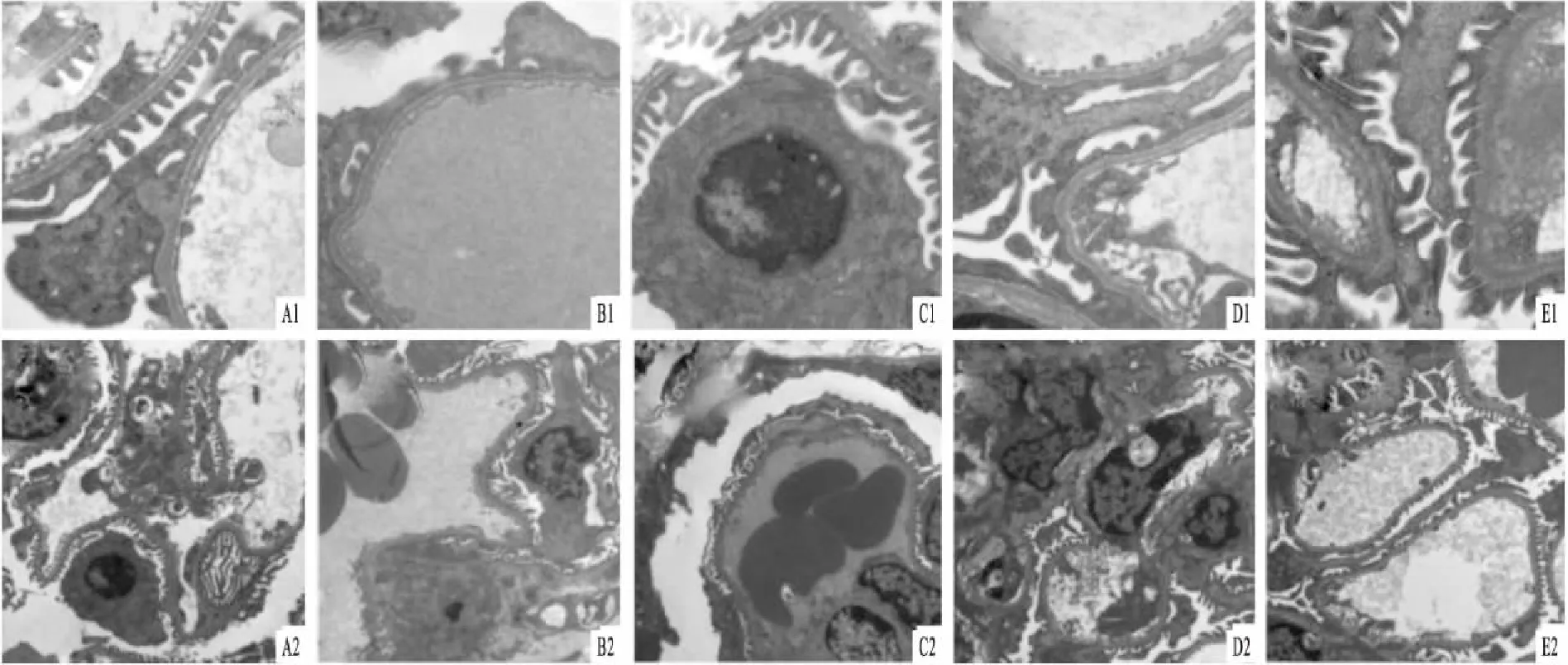
图3 各组小鼠电镜下足细胞结构变化
2.6Q-PCR检测小鼠肾组织VEGF、nephrin、podocinmRNA表达VEGF、nephrin、podocin蛋白与mRNA表达量情况,BEV组较对照组明显降低,BEV+TWP2、BEV-TWP3较BEV组显著升高,差异具有统计学意义(P<0.01);BEV+TWP1组差异无统计学意义。见图7。
3 讨论
BEV在应用4周后其24 h蛋白尿的发生率显著升高。参照相关研究,根据BEV临床使用剂量,在预实验中设计了三组不同的剂量来诱导蛋白尿的产生。结果显示,小鼠被注射BEV 4周后,肾脏出现肾小球内皮细胞萎缩、空泡状改变等病理变化。电镜下显示肾足细胞出现足突明显减少、足突融合增宽、微绒毛稀疏变短、基底膜局部增厚等超微结构改变。这些异常均表明蛋白尿的发生与BEV对足细胞损伤密切相关。且BEV导致的损伤具有剂量相关性。而各组小鼠的Scr、BUN、ALT、AST无显著差异,表明足细胞结构的损伤不至于引起明显的肾功能变化。临床上也显示,蛋白尿的产生并不意味着肾功能会在短期内出现明显变化。
VEGF家族是血小板源生长因子超家族中最重要的成员,肾小球足细胞和肾小管上皮细胞VEGF的表达最显著,VEGF有助于促进血管内皮细胞增殖和新生血管的形成,在维持足细胞功能与基底膜蛋白方面具有重要作用[5-8]。将足细胞VEGF基因敲除,会降低肾小球基底膜重要组成部分、裂隙孔膜相关蛋白nephrin的表达,最终导致蛋白尿的形成[9]。在本实验中,通过免疫组化、Q-PCR显示VEGF蛋白和mRNA表达量与蛋白尿具有相关性。这与之前的研究[10]结果吻合。

图4 各组小鼠足细胞VEGF蛋白表达 免疫组化×400
图5 各组小鼠足细胞nephrin蛋白表达 免疫组化×400
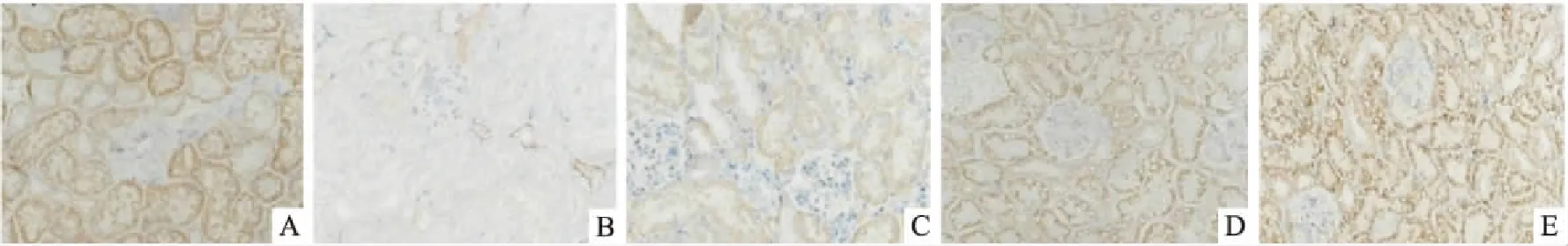
图6 各组小鼠足细胞podocin蛋白表达 免疫组化×400

图7 Q-PCR检测VEGF、nephrin、podocin 基因表达
A:VEGF mRNA;B:nephrin mRNA;C:podocin mRNA;1:对照组;2:BEV 组;3: BEV-TWP1组;4:BEV-TWP2组;5: BEV-TWP3组;与对照组比较:**P<0.01;与BEV组比较:##P<0.01
本实验显示,BEV可降低足细胞VEGF的表达,抑制足细胞相关蛋白nephrin、podocin的表达,进而造成足细胞损伤,最后导致蛋白尿。
TWP具有保护和修复肾小球电荷屏障、抑制免疫应答、改变肾小球机械屏障的损伤等作用,是治疗糖尿病肾病等蛋白尿临床常用药物之一,其疗效和安全性得到大多数学者的认可[11]。本试验证实足细胞损伤是BEV相关蛋白尿主要发生机制之一,nephrin与podocin的表达降低将引起裂孔膜疏松、消失,滤过屏障损坏,从而出现蛋白尿。文献[12]报道TWP具有上调nephrin、podocin表达,改善足细胞损伤的作用。本研究在使用BEV的基础上采用不同剂量的TWP[4、8、16 mg/(kg·d)]干预,结果显示小鼠24 h尿蛋白明显下降。光镜下显示中、高剂量TWP导致的一系列病理改变病变明显缓解,Q-PCR、免疫组化结果显示经过TWP干预的小鼠VEGF、nephrin、podocin表达明显恢复。小鼠足细胞病变改善程度与TWP剂量正相关,主要的机制是TWP通过修复小鼠足细胞损伤,增加肾小球nephrin、podocin表达。
TWP的毒性始终是人们关注的问题,尤其是肝肾功能,本文采用的TWP剂量参考了大量糖尿病肾病的实验研究,证明采用的剂量未引起明显不良反应[13-14]。TWP(20 mg, 口服TID)治疗BEV诱导的蛋白尿个案中,患者服用TWP期间定期检查生化指标,无明显异常,说明TWP是治疗BEV相关蛋白尿的有效药物,有进一步研究的价值。

