乙二醛双氧水氧化萃取制备乙醛酸研究
王 萌,刘少文
(武汉工程大学 化工与制药学院,湖北 武汉 430073)
乙醛酸(Glyoxylic acid,GA)是最简单的酮酸,是重要的有机合成中间体。乙醛酸的工业生产方法有乙二醛硝酸氧化法、草酸电解还原法和顺酐臭氧氧化法等[1-3]。目前国内多采用硝酸氧化法,国外多采用草酸电解还原法和顺酐臭氧氧化法。草酸电解还原法对环境污染较小,但耗电量大,乙醛酸质量不稳定;乙二醛硝酸氧化法,虽然乙二醛价格便宜,但安全性差且设备腐蚀严重;顺酐臭氧氧化法,虽产品质量好,但投资较大、电耗高。乙二醛双氧水氧化法成本低、无污染、投资小,不失为生产GA的一种好的途径。
因为乙二醛特殊的结构,易产生草酸等副产物,传统方法合成乙醛酸的方法都选择性较差。与传统方法相比,反应萃取技术作为一种新兴耦合技术能显著提高选择性,是一种高效、节能、清洁、安全、可持续发展的化工新技术[4]。通过查阅大量相关于草酸-乙醛酸的萃取分离技术,乙醇酸-乙醛酸的萃取分离技术等文献,发现萃取剂对乙醛酸选择效果较好,这充分证实了采用反应萃取合成乙醛酸的可行性[5-7]。利用反应萃取技术合成乙醛酸,其优点在于:可以及时将乙醛酸移出反应相不断萃入萃取相,维持反应相中产物的浓度小于平衡浓度,就能打破化学平衡推动反应向右进行,提高平衡转化率及乙醛酸收率;可以有效避免乙二醛过度氧化生成乙二酸,大大简化后续分离工艺。
1 实验
1.1 实验装置
实验装置见图1。
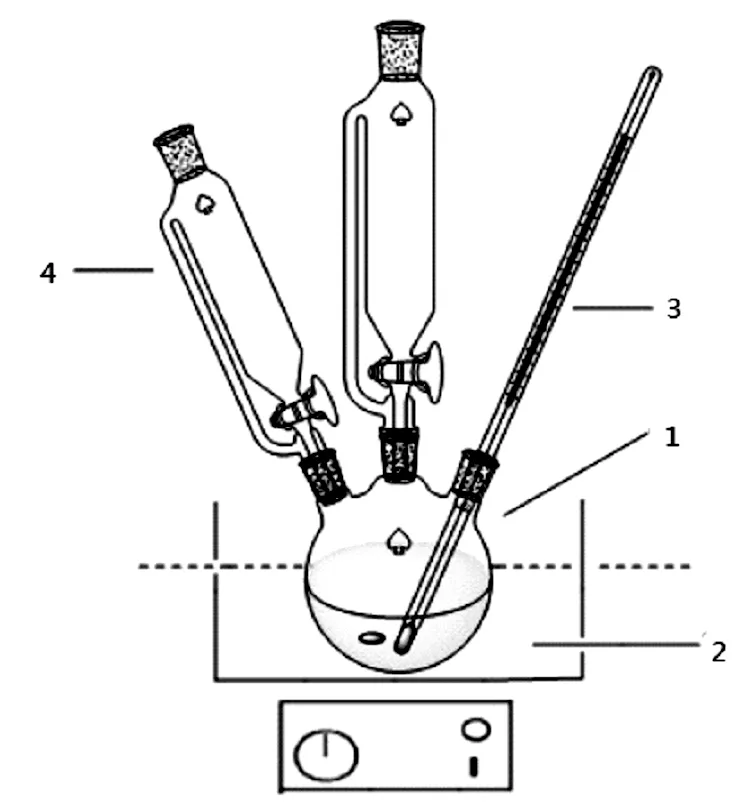
1.三口烧瓶;2.水浴磁力搅拌器;3.温度计;4.恒压滴液漏斗图1 实验装置图
1.2 实验步骤
1.2.1 乙二醛双氧水氧化制乙醛酸反应步骤
乙二醛双氧水氧化反应是在是氮气保护和无氮气保护条件下进行的。称取4.671g硫酸亚铁,溶于50mL的蒸馏水,置于100mL的滴液漏斗中备用;称取41.90g30%(质量分数)双氧水置于另一个100mL滴液漏斗中备用。在四口烧瓶中加入60mL30%(质量分数)的乙二醛,用冰水冷却,开始同时滴加硫酸亚铁和双氧水,保持反应温度控制在3~8℃,滴加速度控制在2h内滴加完毕。滴加完成后继续反应3h。在反应时间为10、20、30、60、90、120、180、240、300min时取样送高效液相色谱进行分析,并计算各组分含量。
1.2.2 乙二醛双氧水氧化萃取制乙醛酸反应步骤
按照上述的乙二醛双氧水氧化反应步骤,在反应烧瓶中添加乙二醛的同时按体积比1∶1比例添加三辛胺萃取剂,并以萃取剂与稀释剂的体积比分别为1∶1~3加入稀释剂,用冰水冷却,使其温度保持在3~8℃。分别反应30、60、120、180min,取反应产物静置分离,用乙醛酸溶液进行萃洗,再用水进行反萃取,分离,样品用高效液相色谱进行分析,计算各组分含量。
2 实验结果与讨论
2.1 氧化气氛对反应的影响
实验考察了氧化气氛(即氮气保护和无氮气保护)对反应的影响如图2所示。
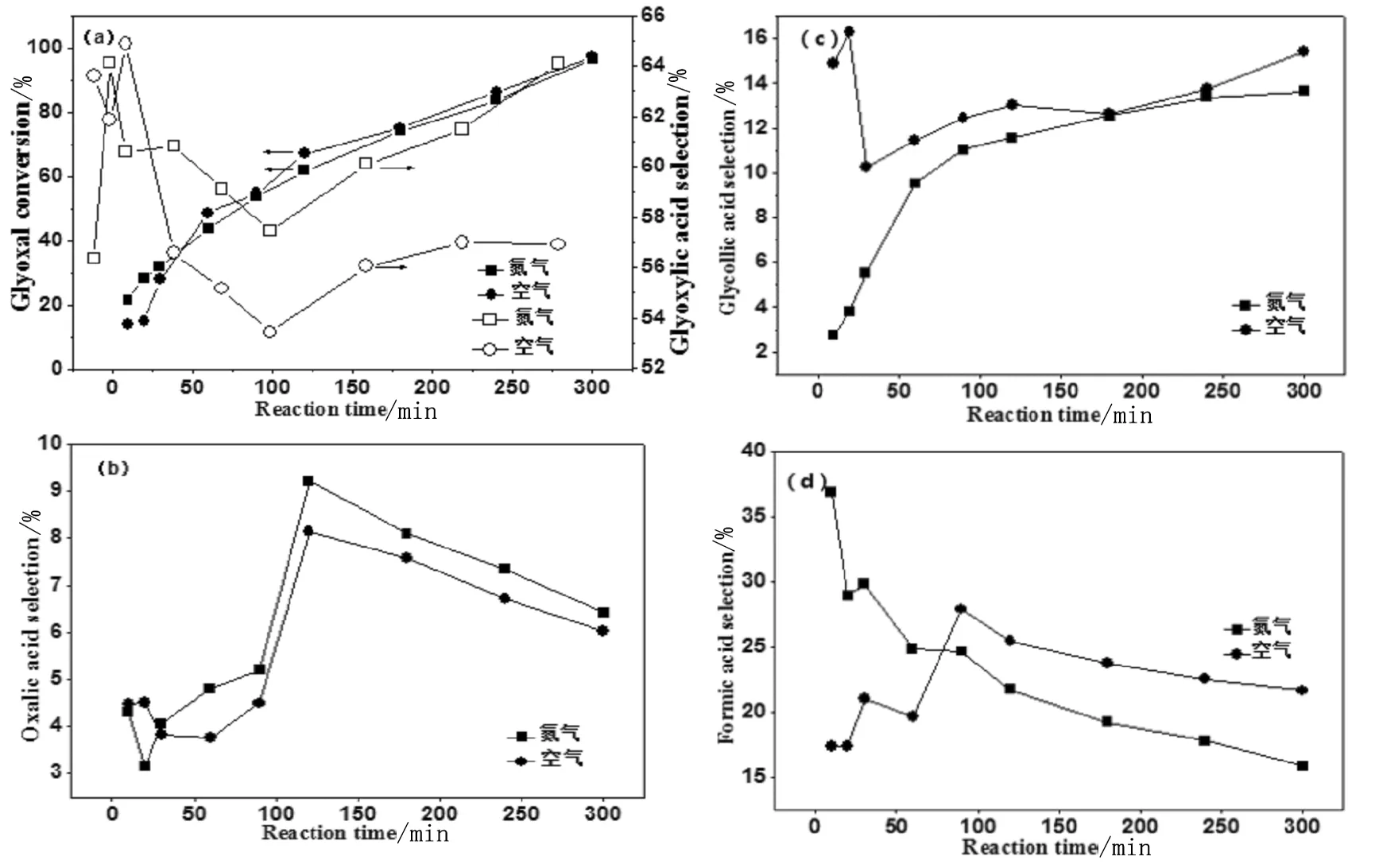
(a)主反应;(b)副产物草酸;(c)副产物乙醇酸;(d)副产物甲酸
图2 氧化气氛对反应的影响
从图2可以看出,随着反应时间的延长,乙二醛转化率在有无氮气保护时均呈现上升的态势,且两者的转化率比较接近。但乙醛酸选择性却呈现较大的差异,反应开始时乙醛酸选择性较高,随着反应进行逐步降低,反应100min后选择性逐步增加。在有氮气保护的条件下乙醛酸选择性比无氮气保护时高5个百分点,这说明氮气保护有利于乙醛酸的生成。
氧化气氛对草酸选择性的影响似乎不大,即有无氮气保护时草酸选择性变化不大,随着反应时间增加,草酸选择性先增加,反应100min后呈下降趋势,这说明通过控制反应在较短或较长时间时可以抑制副产物草酸的生成。氮气保护可以在一定程度上抑制乙醇酸的生成,但随着反应时间的延长,有利于乙醇酸的生成,即乙醇酸选择性明显增加。氧化气氛对甲酸选择性的影响则比较复杂,反应时间较短时,氮气保护有利于甲酸副产物的生成,反应时间较长时,氮气保护可以抑制甲酸的生成。
2.2 萃取剂对反应的影响
氧化体系中各组分在三辛胺萃取剂中的分配系数如表1所示。
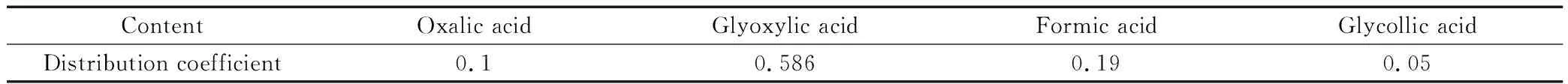
表1 各组分分配系数
由表1可以看出,三辛胺对羧酸的萃取效果乙醛酸>甲酸>草酸>乙醇酸,也印证了加入萃取剂能让反应产生的乙醛酸进入有机相,避免其被氧化成其他副产物,这样就能提高乙醛酸的选择性和乙二醛的转化率。
乙二醛双氧水氧化反应体系添加三辛胺萃取剂的影响如图3所示。
从图3可以看出,当双氧水氧化乙二醛添加三辛胺萃取剂时,乙乙二醛转化率和乙醛酸选择性显著增加,反应180min后乙二醛转化率由75.37%提高到79.61%,乙醛酸选择性由56.07%提高到67.52%,萃取反应效果十分显著。从前面的反应产物在三辛胺萃取剂中的分配系数可以得知,该萃取剂对乙醛酸具有较高的分配系数,随着反应的进行,反应生成的乙醛酸进入有机相,一方面避免乙醛酸进一步氧化生成其它有机酸,另一方面在反应的同时进行了产物分离,这样在提高转化率的同时,也提高了乙醛酸的选择性,同时大大减少了副产物的产生。
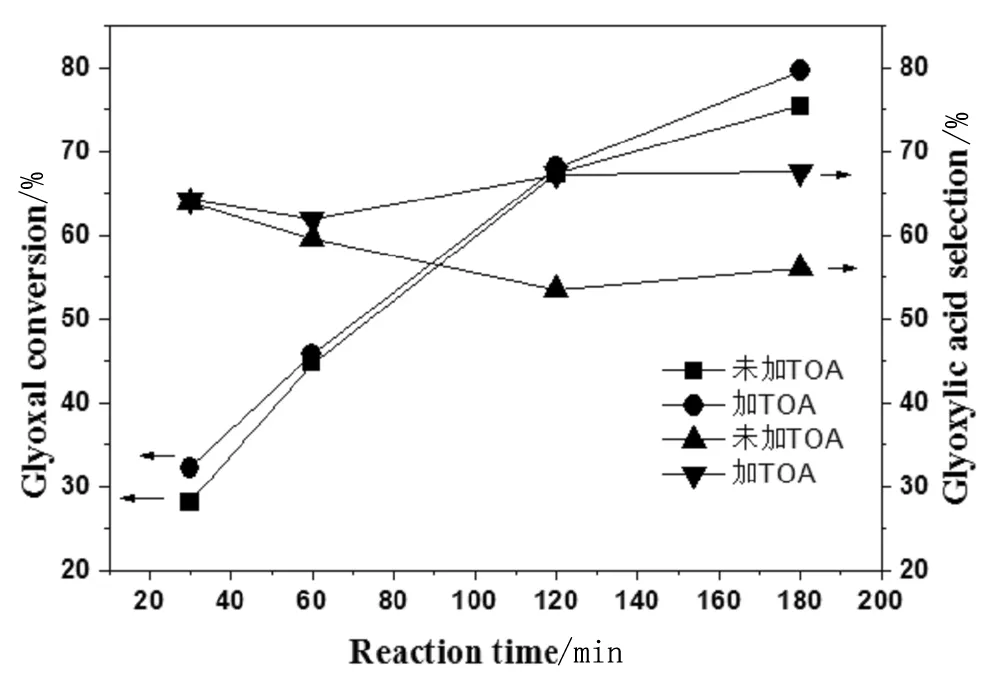
图3 萃取剂对萃取氧化反应的影响
由于乙二醛双氧水氧化萃取反应受氧化气氛的影响,所以考察了氧化气氛对萃取反应的影响如图4所示。
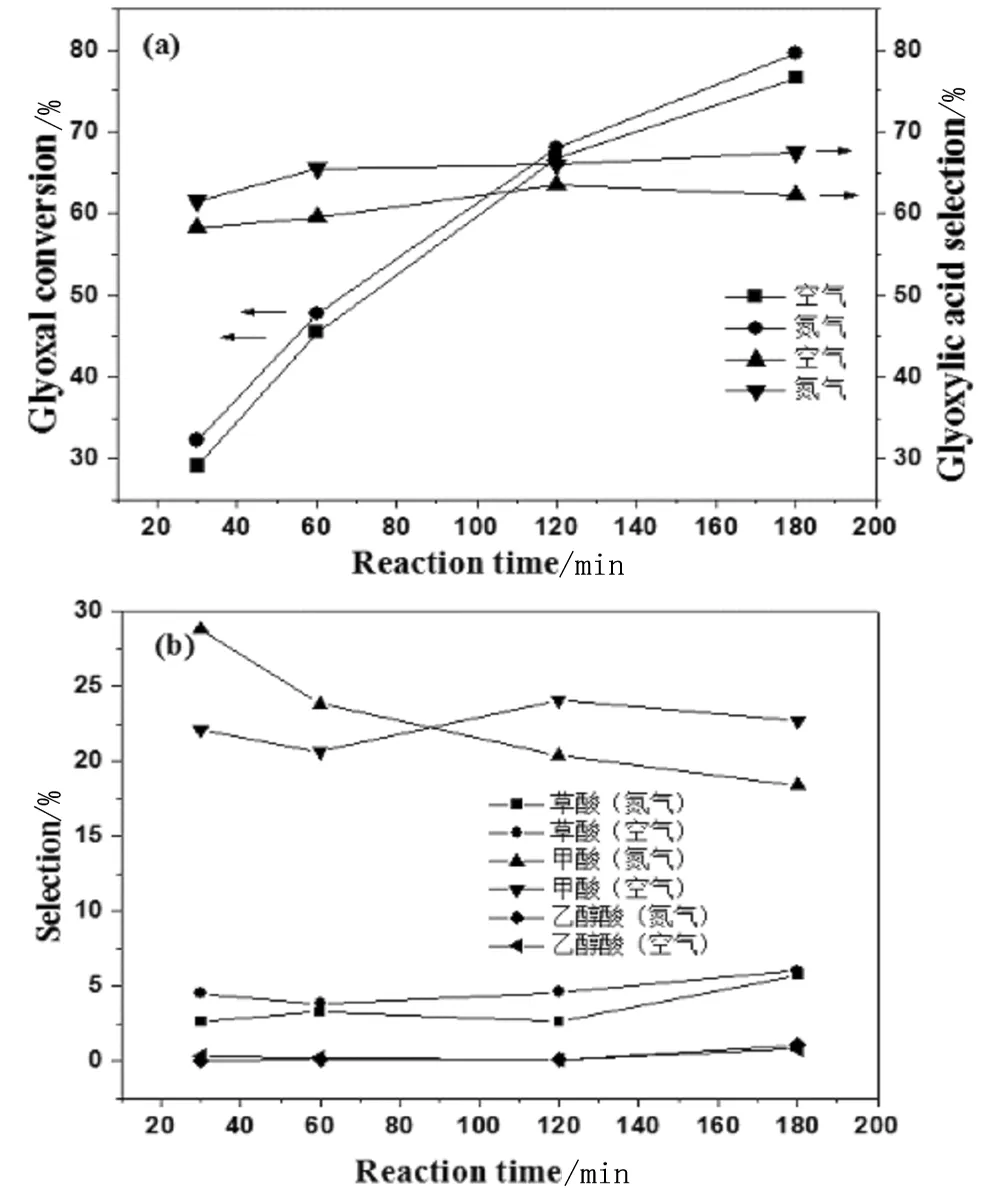
(a)主反应;(b)副反应;图4 氧化气氛对萃取反应的影响
由图4可以看出,随着反应时间的延长,乙二醛转化率和乙醛酸选择性在有无氮气保护时均呈现上升的态势,且在有氮气保护的条件下乙二醛转化率和乙醛酸选择性都比无氮气保护时高,这说明在双氧水萃取氧化体系中氮气保护也有利于乙醛酸的生成。
而在双氧水萃取氧化体系中,有氮气保护时草酸选择性比无氮气保护时低,说明氮气会在一定程度上抑制副产物草酸的产生,且明显抑制乙醇酸的生成。氧化气氛对甲酸选择性的影响则比较复杂,反应时间较短时,氮气保护有利于甲酸副产物的生成,反应时间较长时,氮气保护可以抑制甲酸的生成,这点与双氧水氧化体系类似。
2.3 稀释剂种类对反应的影响
稀释剂种类对分配系数的影响如表2所示,对反应的影响如表3。
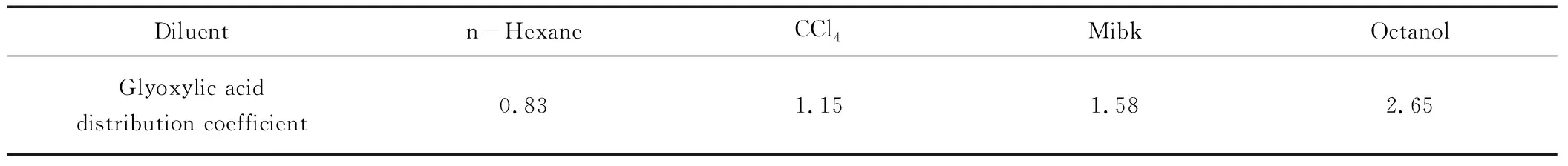
表2 反应萃取中稀释剂对分配系数的影响
三辛胺∶稀释剂=1∶1(V/V);T=3~8℃;通N2
由表2可以看出,在不同性质的稀释剂中,三辛胺萃取乙醛酸的分配比相差很多,稀释剂效应十分显著。通过比较不同稀释剂参加的氧化萃取反应参加萃取反应中乙醛酸的分配系数,可以发现稀释剂的效果正辛醇>甲基异丁基酮>四氯化碳>正己烷。
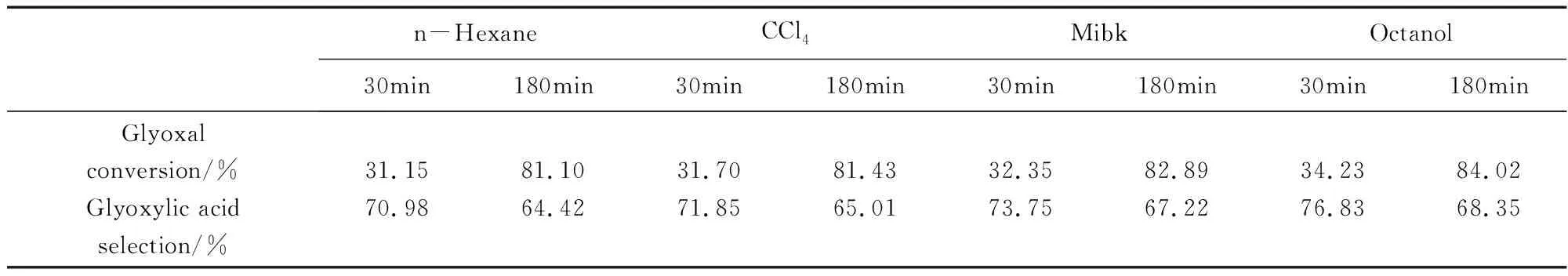
表3 稀释剂种类对萃取氧化反应的影响
由表3可以看出,加入稀释剂乙二醛转化率和乙醛酸选择性明显增加。这是因为TOA是一种对羧酸比较有效的萃取剂,但由于其操作性能不够好,需要加以稀释,选择一种好的稀释剂可以改善萃取操作性能,还会产生很强的稀释剂效应,改善萃取剂的的萃取性能,提高其萃取能力。一般认为稀释剂的偶极矩、介电常数和溶解度参数是影响萃取平衡,产生稀释剂效应的主要因素。通常都是用稀释剂的极性参数、溶剂化作用、电子对的给予能力等来解释。萃合物与稀释剂的相互作用能力及其在稀释剂中的疏溶作用是影响三辛胺萃取羧酸,产生稀释剂效应的主要因素。通过比较不同稀释剂参加的氧化萃取反应的乙二醛转化率和乙醛酸选择性可以看出反应30min时,正辛醇作为催化剂时,乙二醛的转化率和选择性最高;反应180min时,也是正辛醇作为催化剂时,乙二醛的转化率和选择性最高。但正辛醇作为稀释剂反应30min乙二醛的转化率太低了只有34.23%而反应180min时乙二醛转化率很高的同时乙醛酸选择性也不低,因此综合考虑选择正辛醇为稀释剂反应180min为适宜的萃取反应条件。
2.4 萃取剂浓度对反应的影响
萃取剂和稀释剂的不同配比对反应结果有很大影响,分别取三辛胺与正辛醇的体积比为1∶1,1∶1.5,1∶2和1∶3进行实验,实验结果对分配系数的影响如表4所示,对乙二醛转化率和乙醛酸选择性的影响如表5所示。

表4 反应萃取中萃取剂浓度对分配系数的影响
T=3~8℃;通N2
根据表4,乙醛酸分配系数随着萃取剂浓度先升高后降低。这是因为,由于三辛胺是一种分子量高、憎水性很强的叔胺,当稀释剂中含水量升高时,由于水和三辛胺萃合物的极大的不相溶性,溶解了水的稀释剂不利于萃合物分子溶解到有机相,使得萃取能力下降,这种现象称之为疏溶作用,这种疏溶作用越大越不利于萃取。萃合物与稀释剂的相互作用能力越大及其在稀释剂中的疏溶作用越小,稀释剂效应越显著,越有利于萃取。因此三辛胺浓度越大,其萃取能力越强。但随萃取反应剂浓度的增大,草酸和乙醛酸的分配系数皆随之增大,但随着萃取剂浓度增到到一定程度时,草酸的变化幅度较乙醛酸的变化幅度大,即萃取剂对乙醛酸和草酸的分离能力就降低了,随即分配系数降低。因此,乙醛酸分配系数随着萃取剂浓度先升高后降低。
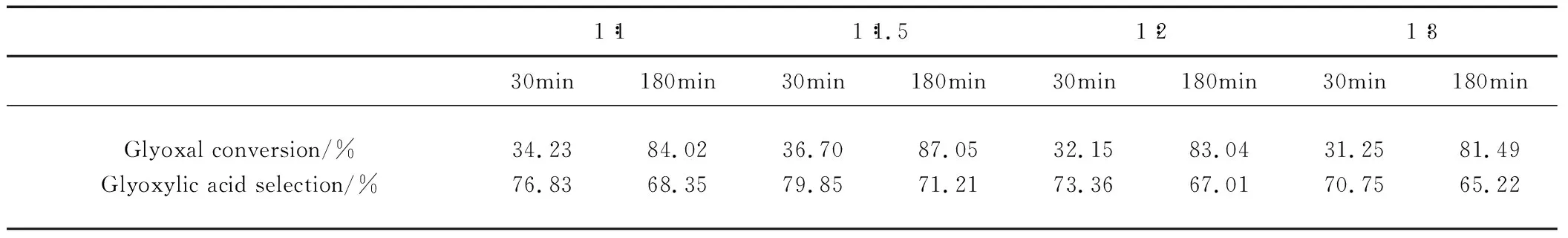
表5 萃取剂浓度对萃取氧化反应的影响
由表5可以看出,TOA与正辛醇的体积比依次为1∶3,1∶2,
1∶1.5和1∶1时,乙二醛的转化率和乙醛酸的选择性先增高后降低。这是因为乙醛酸分配系数随着萃取剂浓度先升高后降低,乙二醛的转化率和选择性就随之改变了。三辛胺与正辛醇体积比为1∶1.5时乙二醛的转化率和乙醛酸的选择性最高,当反应30min时乙醛酸的选择性最高,但此时乙二醛的转化率很低,而反应180min时,此时乙二醛的转化率和乙醛酸的选择性分别为为87.05%和71.21%,因此综合考虑萃取剂TOA与稀释剂正辛醇的配比为1∶1.5反应180min为较适宜的实验条件。
3 结论
通过对乙二醛双氧水氧化萃取制备乙醛酸过程的研究,考察了各因素对实验结果的影响,可得出反应的优化实验条件为:通N2条件下,选用三辛胺为萃取剂剂,正辛醇为稀释剂,三辛胺与正辛醇的体积比为1∶1.5,在3~8℃下反应3h,乙二醛转换率为87.05%,乙醛酸选择性为71.21%。反应设备简单经济,反应副产物少,所得产物明显优于其他传统工艺,值得进一步推广应用。
[1] 高会元.乙醛酸生产、应用研究新进展[J].上海化工,2002,27(15):51-54.
[2] 陆军民.国内乙醛酸衍生产品的现状与展望(一)[J].精细与专用化学品,2002(6):8-10.
[3] 陈银生,张新生,戴迎春,等.乙醛酸合成方法最新进展[J].精细与专用化学品,2002,10(1):1617.
[4] 冯 霞,梁晓贤.反应萃取技术的研究现状[J].精细与专用化学品,2012,32(4):301-304.
[5] 罗 津 A M.萃取手册[M]. 袁承业,译.北京:原子能出版社,1988.
[6] 秦 炜,张 英,罗学辉,等.草酸与乙醛酸的萃取分离[J].化工学报,2001(2):135-140.
[7] 张宏耀,秦 炜,戴猷元.乙醇酸与乙醛酸的萃取分离[J].化工学报,2003,54(11):1552-1557.
[8] Waghmare M, Wasewar K, Sonawane S,et al.Natural non-toxic solvents for recovery of picolinic acidby reactive extraction[J].Ind Eng Chem Res,2011,50(23):13526-13537.

