白蛋白结合型紫杉醇对晚期乳腺癌患者的疗效及安全性分析
康芦兵
(枣庄市立医院药剂科 山东 枣庄 277101)
近年来,新辅助化疗方案被广泛应用于临床中乳腺癌的治疗,不但使治疗效果显著提升,也极大的减轻了化疗药物的不良反应。本文对2014年6月—2016年6月医院收治的晚期乳腺癌患者46例,应用白蛋白结合型紫杉醇治疗,取得了理想的疗效,现报道如下。
1.资料与方法
1.1 一般资料
回顾性分析2014年6月—2016年6月医院肿瘤科收治的46例晚期乳腺癌患者资料,均为女性,患者确诊年龄为29~70岁,中位年龄53岁;病理分型浸润性导管癌39例,腺癌2例,髓样癌5例;接受二线化疗者12例,三线及三线以上化疗者34例;乳腺癌转移程度肺转移16例,骨转移13例,肝转移6例,淋巴结转移11例,其中≥2个部位发生转移者24例;入组研究的所有患者均经过蒽环类或传统溶剂型紫杉烷类药物化疗失败。
1.2 纳入标准
a.所有患者均经过病理组织学确诊为乳腺癌Ⅳ期;b.患者均有客观肿瘤指标以评价治疗效果(具有CT或MRI可以测量的客观病灶);c.Karnofsky评分≥70分;d.预计生存时间≥3个月;e.血常规及肝、肾、心脏功能指标正常;f.所有患者均符合本院伦理委员会相关要求,签署知情同意书[3]。
1.3 治疗方案
所有患者均使用白蛋白结合型紫杉醇(Abraxane,美国阿博利斯生物科学公司,H20091059,规格100mg)进行单药化疗,每周使用治疗剂量为260mg/m2,用50ml生理盐水稀释后静脉滴注30min,每21d给药1次为1个治疗周期,在进行化疗的同时,给予保护胃肠黏膜的药物,并进行补液水化处理。每治疗1个周期后评价治疗毒性,完成2个周期治疗后评价疗效,对于该化疗方案有效的病例继续采用该方案化疗4~12个周期。
1.4 疗效及不良反应评定标准
根据WHO制定的实体瘤客观疗效评定标准对治疗疗效进行评价,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)及进展(PD),总有效率(ORR)按照CR+PR进行统计,临床获益(CBR)=CR+PR+SD,无疾病进展生存期(PFS)定义为从治疗开始到疾病进展的时间或从治疗开始到没有进展情况下出现的任何原因引起的死亡时间。对患者不良反应的判断按照NCL抗癌药物毒性判定标准划分为0~Ⅳ度[1]。
1.5 统计学分析
采用SPSS19.0统计学软件对数据进行分析,计数资料以百分比(%)形式来表示,组间比较采用χ2检验,P<0.05表示有统计学差异。
2.结果
2.1 患者近期治疗效果比较
全组46例患者共完成252个周期的化疗,平均化疗周期数为5.5个,所有患者均可评价治疗效果,其中PR 15例(32.61%)、SD 28例(60.87%)、PD 3例(6.52%),ORR为32.61%,CBR高达93.48%,中位PFS为5.9个月。
2.2 不良反应评价
化疗过程中主要的不良反应为骨髓抑制,其中Ⅲ~Ⅳ级白细胞减少发生率为56.52%,Ⅲ~Ⅳ级粒细胞减少发生率为47.83%,Ⅲ~Ⅳ级血小板减少和贫血的发生率均为4.35%,骨髓抑制的不良反应经粒细胞集落刺激因子治疗后症状均有所缓解,均能继续进行化疗治疗,详见表。
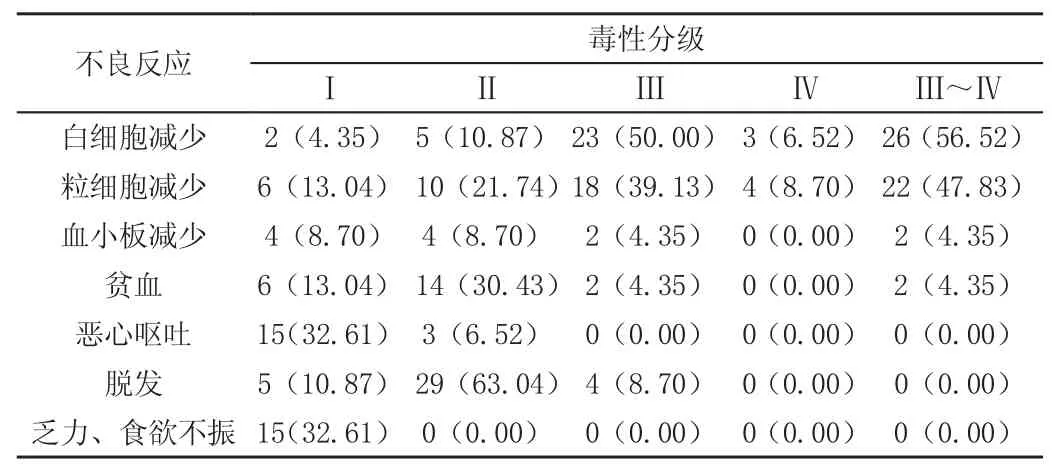
表 白蛋白结合型紫杉醇化疗方案常见不良反应(例,%)
3.讨论
紫杉醇化疗药物对乳腺癌有较好的治疗效果,但传统的紫杉醇类药物因使用时需聚氧乙烯蓖麻油作为助溶剂,明显的增加了药物毒性,从而限制了药物的使用剂量,影响药物在化疗中的疗效和安全性[2]。
白蛋白结合型紫杉醇以人血白蛋白作为药物的载体与稳定剂,将紫杉醇和人血白蛋白通过高压振动方式制成纳米微粒,白蛋白结合型紫杉醇与传统溶剂型紫杉醇比较,药物滴注时间可显著缩短,肿瘤细胞的局部药物浓度可显著增加,提高了对肿瘤的杀伤能力,且临床使用中毒性降低。
本研究中的所有患者均为乳腺癌晚期,以往均接受过化疗,采用白蛋白结合型紫杉醇化疗的有效率达32.61%,主要不良反应为Ⅲ~Ⅳ级骨髓抑制,经过积极对症支持治疗后仍可继续治疗,非血液学毒性轻微,患者可耐受,故白蛋白结合型紫杉醇可以考虑作为晚期乳腺癌的解救化疗方案。
[1]林志武.白蛋白结合型紫杉醇治疗晚期难治性乳腺癌的疗效及安全性分析[J].中外医疗,2015(25):52-54.
[2]吴永勇,杨林,李慧,等.白蛋白结合型紫杉醇联合奥沙利铂二线治疗吉西他滨耐药的晚期胆系肿瘤的临床观察[J].国际肿瘤学杂志,2015,42(6):478-479.

