人工全膝关节表面置换术后连续股神经阻滞与经静脉患者自控镇痛的随机对照研究*
冯宾张博 任毅赵潇雄彭慧明曲铁兵**翁习生**
(1.中国医学科学院北京协和医学院北京协和医院骨科,北京100730;2.首都医科大学附属北京朝阳医院骨科,北京100020)
全膝关节表面置换术(total knee arthroplasty,TKA)后重度疼痛的发生率可高达60%,并可导致呼吸系统、心血管系统和泌尿系统的严重并发症,影响术后功能锻炼以及远期疗效[1]。有效的术后镇痛对于早期进行患膝康复锻炼、缩短平均住院日等有利[2,3]。患者静脉自控镇痛(patient control analgesia,PCA)是全膝关节置换术常用的术后镇痛方法,但可引起恶心、呕吐、头晕等不良反应,严重时可出现呼吸抑制。近年来,越来越多的医生采用连续股神经阻滞(continuous femoral nerve block,CFNB)的方法进行术后镇痛,这种方式的镇痛效果确切,副作用少,有利于患者术后早期功能锻炼和功能恢复[4]。本研究旨在对比静脉PCA与CFNB在TKA术后的镇痛效果、并发症、膝关节功能恢复情况等方面的差异,为临床应用提供参考。
1 资料与方法
1.1 纳入与排除标准
本研究经北京协和医院及首都医科大学附属北京朝阳医院伦理委员会批准,将2014年6月至2015年6月于北京朝阳医院骨科接受初次单侧全膝关节表面置换的患者纳入研究。所有患者均知情同意并签署同意书。
纳入标准:①年龄<80岁;②体重40~80 kg;③术前明确诊断为骨关节炎,以一侧症状为主,经保守治疗无效;④术前美国麻醉师协会(American Society of Anesthesiologists,ASA)病情分级为Ⅰ或Ⅱ级;⑤手术采用前正中切口和髌旁内侧入路;⑥采用后稳定型固定平台膝关节假体。
排除标准:①双侧膝骨关节炎需行双侧TKA者;②既往有麻醉药品依赖、药物滥用史及正在使用激素、阿片类药物治疗者;③有凝血功能异常者;④神经阻滞穿刺点局部皮肤感染;⑤术前肝、肾功能异常者;⑥未控制的心绞痛或急性心梗发病6个月内;⑦卒中发作6个月内,或合并精神系统疾病者;⑧有明显的固定性畸形或严重的韧带不稳定者。
1.2 分组方法
本研究为随机对照试验。采用随机数字表的方法进行随机分组。数据收集者与数据统计分析者之间采用盲法,数据统计由第三方进行。共120例患者入组,随机分为A组(CFNB组),B组(静脉PCA组),C组(单次FNB联合静脉PCA组),每组40例。
手术由首都医科大学附属北京朝阳医院关节中心3个手术组完成。采用全身麻醉,平卧位。使用气囊式止血带,压力设置为收缩压+100 mmHg。手术采用标准膝前正中切口,髌旁内侧入路。假体使用后稳定型骨水泥固定平台假体,不置换髌骨。关节腔放置引流管,术后24 h拔除。所有患者遵循同样的术后功能锻炼方案,麻醉清醒后即开始活动踝关节,行下肢肌肉等长收缩锻炼。术后第1天开始直腿抬高锻炼及关节活动度锻炼,术后第1~3天在助行器辅助下行走。
1.3 麻醉及镇痛方法
1.3.1 麻醉方案:所有患者均采用全身麻醉。麻醉诱导采用咪达唑仑20 μg/kg、芬太尼1 μg/kg、昂丹司琼4 mg,随后以丙泊酚2 mg/kg和罗库溴铵0.6 mg/kg进行诱导插管。麻醉维持吸入氧气/笑气浓度比为1∶1,期间根据需要间断追加芬太尼加强镇痛,确保血流动力学稳定。
1.3.2 连续股神经阻滞:术前行股神经定位置管,在超声引导下在腹股沟韧带水平探及股动脉及股神经,穿刺点局部用2%利多卡因浸润麻醉。与皮肤呈30°向头侧刺入已连接神经刺激器(MultiStim Vario,Pajunk,#61650)的神经刺激阻滞针,初始刺激电流设定为1 mA,若减小到0.3 mA时仍可引出股四头肌收缩,则经刺激针给予0.4%罗哌卡因(瑞典阿斯利康公司)100 mg。然后置入连续神经阻滞导管,置入长度为超过针尖6~8 cm,在体表进行妥善固定并保留至术后用于镇痛。镇痛药物选择0.2%罗哌卡因。待手术结束前将导管连接至电子镇痛泵(Abbot GEMSTARTM,Hospira),同时给予负荷剂量10 ml,并开始持续输注10 ml/h。
1.3.3 静脉PCA泵:待手术结束前将Gomedical一次性使用镇痛泵连接至患者的静脉通路,药物为吗啡2 mg/ml+昂丹司琼0.3 mg/ml,单次剂量0.5 ml,锁定时间5 min,无背景输注。
1.3.4 单次股神经阻滞联合静脉PCA组:股神经阻滞为单次阻滞,穿刺方法同前,给予100 mg的罗哌卡因。术后联合静脉PCA泵,药物及剂量同前,锁定时间5 min,无背景输注。
1.3.5 基础镇痛及补救镇痛方案:手术结束时常规静脉注射帕瑞昔布钠40 mg,之后每12 h注射一次,至术后第3天。术后第4~14天口服NSAIDs药物镇痛。当疼痛VAS评分大于5分时,早期可追加PCA镇痛,待正常进食后给予氨酚羟考酮片口服进行补救镇痛。
1.4 观察指标
1.4.1 疼痛指标:采用疼痛视觉模拟评分(visual analogue scale,VAS)进行疼痛评分。分别在术后即刻、术后12 h、24 h、48 h、72 h、4 d、5 d、6 d进行随访,记录患者在静息和活动状态下的疼痛情况。记录术后静脉PCA泵的开启时间、按压次数、频率,并计算药物用量。记录补救镇痛使用情况。
1.4.2 功能康复指标:记录术后第3天和第6天患者进行膝关节主动活动的范围。记录术后完成主动直腿抬高时间、下地时间及术后住院日。
1.4.3 安全性指标:①生命体征:入院后至出院每天至少1次体温、心率、血压监测,术后1~3 d每天至少2次。②术前、术后第1、3、5天常规行血常规、凝血功能、肝肾功能检查。③记录不良事件发生情况,包括穿刺操作副损伤,药物相关的不良反应,如恶心、呕吐、皮疹、嗜睡、低血压、心血管事件。
1.5 统计学分析
采用SPSS 16.0统计软件对数据进行统计学处理。计量资料采用均数±标准差表示,组间比较采用独立样本t检验,组内两两比较采用方差分析。计数资料的组间比较采用χ2检验。检验水准α值取双侧0.05。
2 结果
2.1 一般资料
三组患者的年龄、BMI、手术时间、术后引流量、术后住院天数比较无统计学差异。人口学资料见表1。
2.2 膝关节功能
方差分析显示,术后第3天,C组关节活动度最高,但与A组间无统计学差异(P=0.368);A组与B组间的关节活动度比较无统计学差异(P=0.071),而B组与C组比较有统计学差异(P=0.014)。术后第6天,三组之间无明显统计学差异(P=0.069),B组的关节活动度最低。三组术后血红蛋白变化无统计学差异,术后完成直腿抬高时间与下地时间无统计学差异(表2)。
表1 三组患者人口学资料及手术相关信息(±s,n=40)
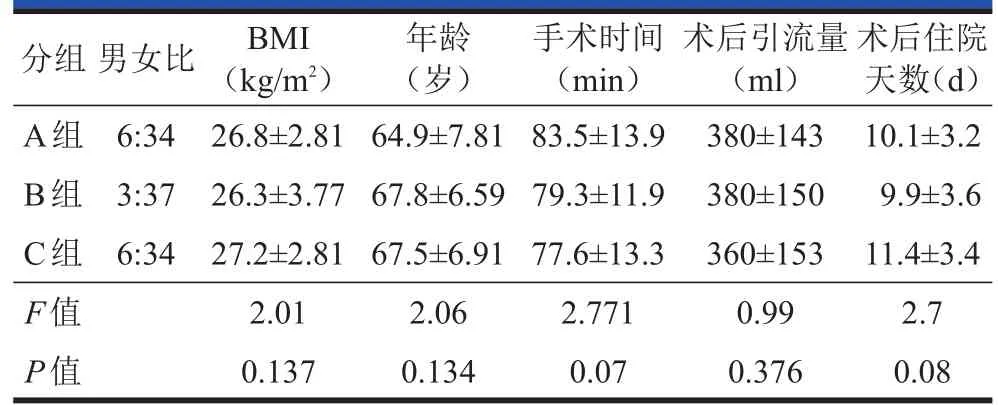
表1 三组患者人口学资料及手术相关信息(±s,n=40)
A组:股神经阻滞;B组:静脉PCA;C组:单次神经阻滞+静脉PCA
分组A组B组C组F值P值男女比6:34 3:37 6:34 BMI(kg/m2)26.8±2.81 26.3±3.77 27.2±2.81 2.01 0.137年龄(岁)64.9±7.81 67.8±6.59 67.5±6.91 2.06 0.134手术时间(min)83.5±13.9 79.3±11.9 77.6±13.3 2.771 0.07术后引流量(ml)380±143 380±150 360±153 0.99 0.376术后住院天数(d)10.1±3.2 9.9±3.6 11.4±3.4 2.7 0.08
表2 三组患者术后功能康复相关指标(±s)
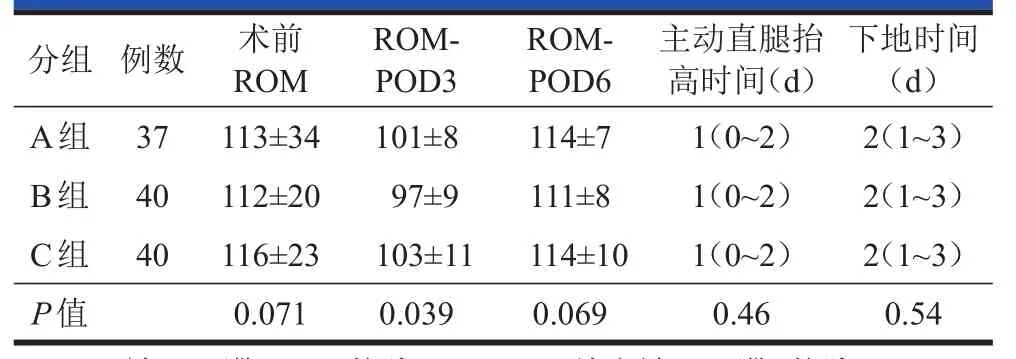
表2 三组患者术后功能康复相关指标(±s)
A组:股神经阻滞;B组:静脉PCA;C组:单次神经阻滞+静脉PCA;ROM:关节活动度;POD:术后天数
?
2.3 静脉PCA泵的使用
记录术后PCA使用量(表3),C组PCA使用量及按压次数少于B组,二者之间有统计学差异。A组有2例患者(5%)因阻滞镇痛效果不满意,术后24 h内疼痛控制不满意,采用静脉PCA补救镇痛。
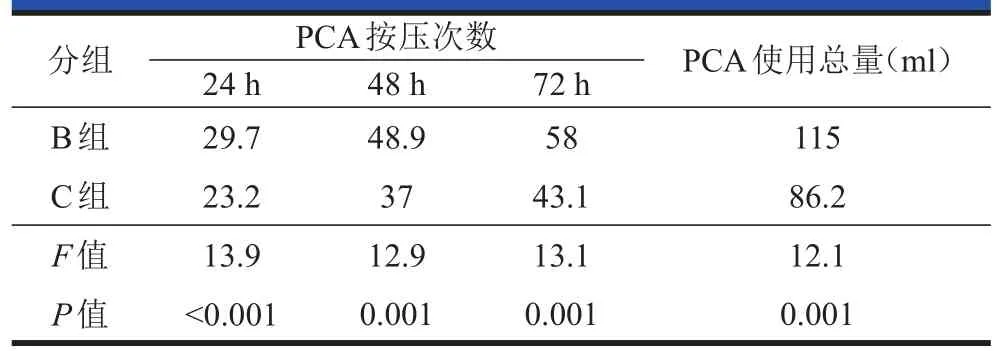
表3 B、C组静脉PCA按压次数及术后PCA用量(n=40)
2.4 疼痛评分
统计三组术前及术后静态VAS评分及动态VAS评分。所有病例动态VAS评分高于静态VAS评分,采用方差分析,三组术前静态VAS评分及动态VAS评分无差异。术后各观察时间点,B组静态及动态VAS评分均高于A组、C组,差异具有统计学意义,而A组与C组VAS评分均无统计学差异(表4)。术后72 h内,C组VAS评分低于A组,术后72 h后,C组VAS评分高于A组,差异无统计学意义。对比术后24 h、72 h、6 d动态VAS评分与静态VAS评分差值(Δ动态VAS-静态VAS),术后第1天和第3天,A组VAS评分差值最小,与B组、C组有统计学差异。术后第6天,三组VAS评分差值无统计学差异(表4)。
2.5 不良反应
A组有1例患者术后出现神经阻滞导管脱落,给予静脉PCA补救镇痛,余无穿刺部位相关并发症。A、B、C组术后恶心、呕吐的发生率分别为8%(3/37)、42%(17/40)、25%(10/40)。B组和C组恶心、呕吐的发生率无统计学差异(χ2=2.73,P=0.098),A组显著低于B组(χ2=13.1,P=0.001)和C组(χ2=4.5,P=0.034)。A、B、C组分别有1、5、3例术后出现头晕,三组头晕的发生率无统计学差异(χ2=2.883,P=0.237)。以上并发症经对症处理后恢复。
表4 三组患者术后不同时间点动静态VAS评分结果(±s)
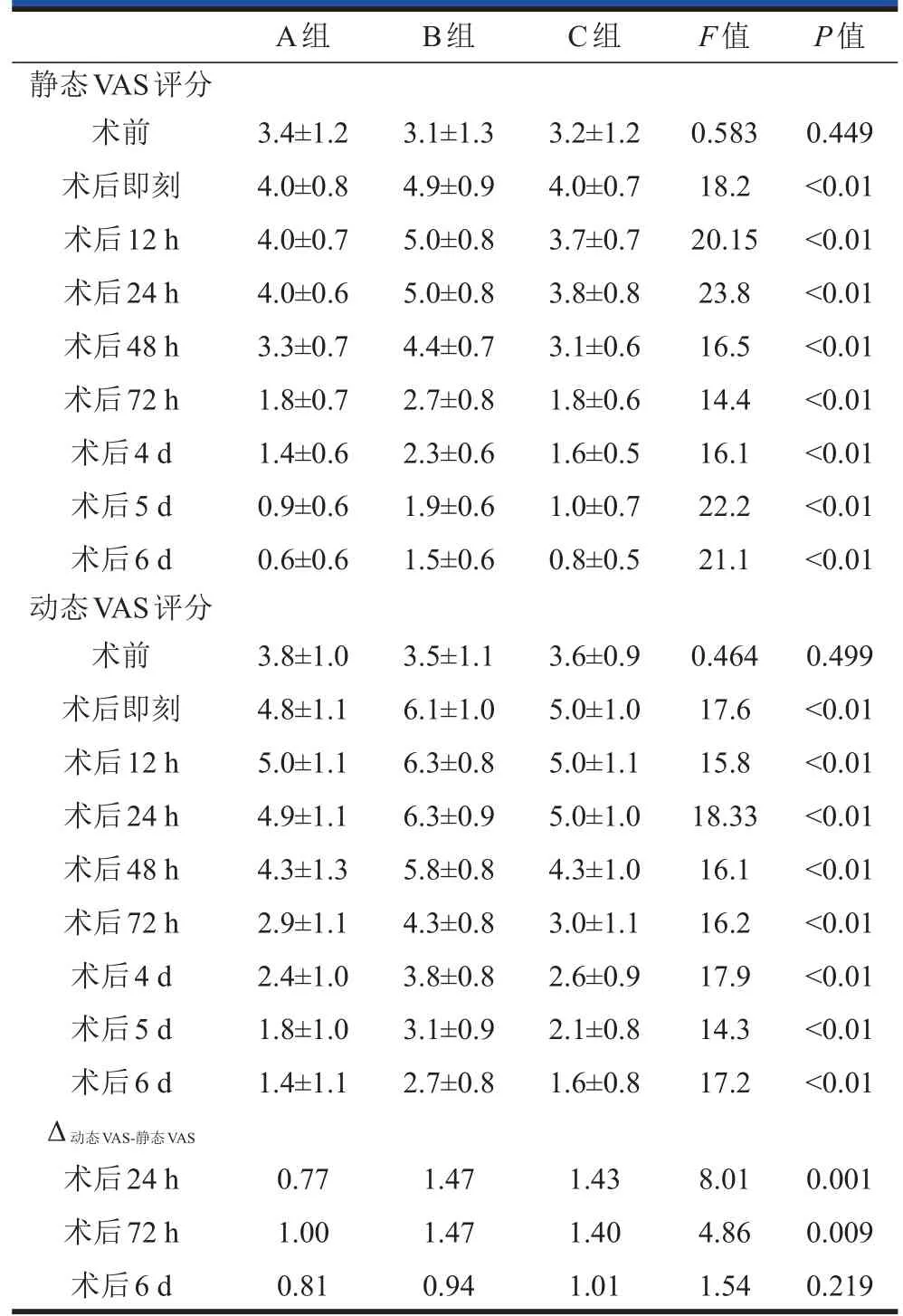
表4 三组患者术后不同时间点动静态VAS评分结果(±s)
Δ动态VAS-静态VAS:动态VAS评分与静态VAS评分差值
静态VAS评分术前术后即刻术后12 h术后24 h术后48 h术后72 h术后4 d术后5 d术后6 d动态VAS评分术前术后即刻术后12 h术后24 h术后48 h术后72 h术后4 d术后5 d术后6 d Δ动态VAS-静态VAS术后24 h术后72 h术后6 d A组3.4±1.2 4.0±0.8 4.0±0.7 4.0±0.6 3.3±0.7 1.8±0.7 1.4±0.6 0.9±0.6 0.6±0.6 3.8±1.0 4.8±1.1 5.0±1.1 4.9±1.1 4.3±1.3 2.9±1.1 2.4±1.0 1.8±1.0 1.4±1.1 0.77 1.00 0.81 B组3.1±1.3 4.9±0.9 5.0±0.8 5.0±0.8 4.4±0.7 2.7±0.8 2.3±0.6 1.9±0.6 1.5±0.6 3.5±1.1 6.1±1.0 6.3±0.8 6.3±0.9 5.8±0.8 4.3±0.8 3.8±0.8 3.1±0.9 2.7±0.8 1.47 1.47 0.94 C组3.2±1.2 4.0±0.7 3.7±0.7 3.8±0.8 3.1±0.6 1.8±0.6 1.6±0.5 1.0±0.7 0.8±0.5 3.6±0.9 5.0±1.0 5.0±1.1 5.0±1.0 4.3±1.0 3.0±1.1 2.6±0.9 2.1±0.8 1.6±0.8 1.43 1.40 1.01 F值0.583 18.2 20.15 23.8 16.5 14.4 16.1 22.2 21.1 0.464 17.6 15.8 18.33 16.1 16.2 17.9 14.3 17.2 8.01 4.86 1.54 P值0.449<0.01<0.01<0.01<0.01<0.01<0.01<0.01<0.01 0.499<0.01<0.01<0.01<0.01<0.01<0.01<0.01<0.01 0.001 0.009 0.219
3 讨论
近年来,TKA已经逐渐成为治疗膝关节中重度骨关节炎主要手段。然而,术后疼痛成为患者畏惧手术、影响手术疗效的重要因素。围手术期良好的镇痛可以减少患者的躯体及心理上的痛苦,减少创伤应激、降低术后全身并发症、促进早期进行康复锻炼,进而对防止术后粘连,缩短术后恢复时间及住院时间等具有积极意义[5]。
连续股神经阻滞(CFNB)对于全膝关节置换术后疼痛具有良好的镇痛效果,同时也能够达到理想的功能恢复效果[6]。文献报道CFNB不仅有助于患者术后早期功能恢复,且与传统阿片类药物镇痛相比,在术后1个月患者的SF-36评分、HSS评分以及行走距离和时间、关节活动度及肌肉力量方面均有显著的提高[7]。本研究结果发现在关节活动度方面,术后第3天,FNB+PCA组关节活动度最高,FNB+PCA组与静脉PCA组差异具有统计学意义,其余各组之间无统计学差异。术后第6天三组关节活动度无统计学差异。单独应用连续股神经阻滞与股神经阻滞联合静脉PCA,在术后早期功能恢复方面并无明显差异,术后3天联合方案功能活动度略好。股神经阻滞镇痛组术后关节活动度优于静脉PCA组。
静脉PCA操作比较简单,通过患者自己给药减少不同个体药代动力学与药效学差异的影响[8]。术后更易于管理,但术后存在一定的不良反应[9]。PCA使用中阿片类药物常见的不良反应有恶心、呕吐、便秘、皮肤瘙痒、呼吸抑制、头晕、意识障碍等[10]。其中术后早期若出现恶心、呕吐,将延迟术后患者正常进食、早期下地活动,影响口服药物吸收,影响关节置换患者的快速康复。McNicol等[11]报道的一项系统评价中,关节置换患者使用PCA进行镇痛,恶心呕吐的发生率可高达30%,其他常见的并发症有尿潴留(23%),意识障碍(15%),皮肤瘙痒(15%),戒断症状(2.5%),呼吸抑制(2.3%)。严重并发症甚至导致术后死亡。作者认为,降低阿片类药物的应用剂量可以预防上述并发症的发生,使患者术后获得平稳康复。本研究发现,静脉PCA组术后并发症发生率明显高于CFNB组及联合用药组,联合静脉PCA+FNB组较单独应用静脉PCA组,可减少PCA的使用次数和吗啡的使用剂量,减少术后并发症的发生率。该结果提示,应用CFNB可以在保证患者有效镇痛的基础上,减少镇痛相关并发症。以单次FNB作为镇痛的基础麻醉配合静脉PCA的术后镇痛方法,可获得与CFNB接近的镇痛效果,同时减少单纯使用静脉PCA的并发症。
动态VAS评分可真实反映患者术后主动进行功能锻炼的疼痛感受。静脉PCA在患者休息时能产生稳定的止痛效果,但对运动疼痛的止痛效果不满意[9]。本研究中,CFNB在术后24 h、72 h、6 d动态与静态VAS评分的差值最小,而静脉PCA组的VAS评分差值最大,72 h内三组差异有统计学意义,3天之后三组差异无统计学意义,与文献报道结果相符[9,12]。本研究结果提示CFNB可以为TKA患者提供更为满意的功能锻炼时的镇痛。
CFNB镇痛的效果不仅与该镇痛方法的有效性有关,同时也与该方法应用的局部麻醉药物种类及各自的性质、患者的痛阈大小以及操作者的技术相关。通常连续股神经阻滞需要操作者具备丰富的临床操作经验。股神经的痛觉支配部位是膝关节前部,后部、内侧、外侧痛觉分别由股后皮神经、闭孔神经、股外侧皮神经支配,因此CFNB镇痛范围的大小也决定了其镇痛的有效性。可能因操作精度、镇痛范围变异出现阻滞不满意。同时术后护理不当也可能出现术后导管脱落的情况。针对接受CFNB而镇痛不满意的患者,可以考虑联合其他镇痛方法如静脉PCA、口服NSAIDs或同时进行闭孔神经和坐骨神经连续阻滞,以获得满意的术后镇痛效果[13]。Calin等[14]报道CFNB镇痛失败的发生率从0%~67%不等。本研究中,CFNB组有2例镇痛不满意及1例导管脱落通过静脉PCA进行补救,镇痛失败率为7.5%。相对CFNB组,联合镇痛组,可获得相近的镇痛效果,避免了镇痛失败的并发症。同时文献报道CFNB可能出现股四头肌无力,导致术后跌倒[8]。而应用收肌管阻滞(ACB)理论上可减少术后股四头肌无力的症状[15]。David等进行的一项关于CFNB与ACB的随机对照研究,显示二者在疼痛评分及吗啡使用量之间无差异,ACB组术后8 h内股四头肌肌力稍优于CFNB,之后无明显差异[16]。本研究中统计术后完成直腿抬高时间及下地时间,术后1 d,CFNB组无明显抬腿无力情况。需要进一步试验对比CFNB与ACB对术后肌力恢复的影响。
本研究的局限性:①由三名主刀医师完成手术,神经阻滞操作由多名麻醉医生完成,操作者的个体差异可能对镇痛效果的评估产生影响。②本研究仅统计术后完成直腿抬高及下地时间,未统计术后不同时间点股四头肌肌力的变化,不能准确反映术后肌力的变化。
总之,根据本研究,我们认为TKA术后使用CFNB进行镇痛,可以获得满意的静息与运动镇痛效果,同时镇痛药物相关不良反应低,可满足术后早期康复锻炼的要求。联合单次神经阻滞与静脉PCA的镇痛方法,可提供与CFNB相近的镇痛效果。
[1]Singelyn FJ,Deyaert M,Joris D,et al.Effects of intravenous patient-controlled analgesia with morphine,continuous epidural analgesia,and continuous three-in-one block on postoperative pain and knee rehabilitation after unilateral total knee arthroplasty.AnesthAnalg,1998,87(1):88-92.
[2]Capdevila X,Barthelet Y,Biboulet P,et al.Effects of perioperative analgesic technique on the surgical outcome and duration of rehabilitation after major knee surgery.Anesthesiology,1999,91(1):8-15.
[3]Chelly JE,Greger J,Gebhard R,et al.Continuous femoral blocks improve recovery and outcome of patients undergoing total knee arthroplasty.J Arthroplasty,2001,16(4):436-445.
[4]Paul JE,Arya A,Hurlburt L,et al.Femoral nerve block improves analgesia outcomes after total knee arthroplasty:a meta-analysis of randomized controlled trials.Anesthesiology,2010,113(5):1144-1162.
[5]张伟,胡焱,刘雪冰,等.持续股神经阻滞用于全膝关节置换术后镇痛的效果分析.北京医学,2013,35(11):942-944.
[6]Zinkus J,Mockutė L,Gelmanas A,et al.Comparison of 2 analgesia modalities in total knee replacement surgery:Is there an effect on knee function rehabilitation?Med Sci Monit,2017,23:3019-3025.
[7]Wang F,Zhou Y,Sun J,et al.Influences of continuous femoral nerve block on knee function and quality of life in patients following total knee arthroplasty.Int J Clin Exp Med,2015,8(10):19120-19125.
[8]Momeni M,Crucitti M,De Kock M.Patient-controlled analgesia in the management of postoperative pain.Drugs,2006,66(18):2321-2337.
[9] 于华鹏,刘朝晖,郭万首,等.连续股神经阻滞在全膝关节置换术后镇痛及早期康复锻炼中的作用.中国骨伤,2010,23(11):825-827.
[10]Dias AS,Rinaldi T,Barbosa LG.The impact of patients controlled analgesia undergoing orthopedic surgery.Braz J Anesthesiol,2016,66(3):265-271.
[11]McNicol ED,Ferguson MC,Hudcova J.Patient controlled opioid analgesia versus non-patient controlled opioid analgesia for postoperative pain.Cochrane Database Syst Rev,2015,(6):CD003348.
[12]Ng FY,Chiu KY,Yan CH,et al.Continuous femoral nerve block versus patient-controlled analgesia following total knee arthroplasty.J Orthop Surg(Hong Kong),2012,20(1):23-26.
[13]Chan EY,Fransen M,Parker DA,et al.Femoral nerve blocks for acute postoperative pain after knee replacement surgery.Cochrane Database Syst Rev,2014,(5):CD009941.
[14]Moucha CS,Weiser MC,Levin EJ.Current strategies in anesthesia and analgesia for total knee arthroplasty.J Am Acad Orthop Surg,2016,24(2):60-73.
[15]Lavie LG,Fox MP,Dasa V.Overview of total knee arthroplasty and modern pain control strategies.Curr Pain Headache Rep,2016 20(11):59.
[16]Kim DH,Lin Y,Goytizolo EA,et al.Adductor canal block versus femoral nerve block for total knee arthroplasty:a prospective,randomized,controlled trial.Anesthesiology,2014,120(3):540-550.

