GC法测定用于生脉注射液中五味子药材挥发性成分指纹图谱的建立*
吴建国 董 礼 李 梅 徐小平
[1.四川大学华西药学院,四川 成都 610041;2.华润三九(雅安)药业有限公司,四川 雅安625000]
生脉注射液是根据古验方“生脉散”研制成的中药注射剂,由红参、麦冬、五味子3味药组成[1]。现代药理学研究证明,生脉注射液在扩张血管、增进冠状动脉血流量方面有较好的疗效,临床上可用于治疗心肌梗死、心源性休克、感染性休克、其他微循环障碍[2]。2011年国家食品药品监督管理局颁布正式执行生脉注射液新质量标准[3]。该标准明确了生脉注射液制备工艺,其中五味子蒸馏液是生脉注射液的重要组分之一,但是质量标准中并未对生脉注射液中挥发性成分进行质量控制,因此在控制五味子挥发性成分质量上存在一定缺陷。五味子是生脉注射液中处方之一,具有益气生津、收敛固涩、补肾宁心的功效,用于久嗽虚喘、梦遗滑精、遗尿尿频、久泻不止等症[4]。研究发现,五味子中含有挥发油、有机酸、维生素、木脂素、三萜、倍半萜及多糖等多种化学成分[5]。其中,五味子挥发油主要成分为萜类化合物[6],其对中枢神经系统有调节作用,能增强机体对非特异性刺激的防御能力[7]。因此,基于对五味子药材中挥发性成分进行质量控制,可有效保证生脉注射液中五味子挥发性成分质量稳定,为临床疗效提供保障。本研究试图建立五味子药材挥发性成分指纹图谱,为五味子标准的提高以及生脉注射液企业内控质量标准的建立提供依据。现报告如下。
1 仪器与材料
1.1 仪器 Agilent 6890型气相色谱仪(美国安捷伦科技公司)、Agilent 6890N/5973N型气质联用仪(美国安捷伦科技公司)、XA205DU型电子天平(瑞士梅特勒-托利多公司)。中药色谱指纹图谱相似度评价系统(2.0版)软件(国家药典委员会颁布)。
1.2 材料 五味子药材 10批(A150601、A150801、A151001、A151101、A151202、A160501、A160601、A160801、A161001、A161101),购于集安市宏兴参业有限公司;生脉注射液3批(16030802002、16080502003、16121205001),由雅安三九药业有限公司生产。
1.3 试药 4-萜品醇(批号111967-201501)、α-松油醇(批号:111859-201503)均购于中国食品药品检定研究院。 色谱乙腈(Merck)、色谱乙醇(Merck)。
2 方法与结果
2.1 检测条件 1)色谱条件。采用Agilent DB-1(30 m×250 μm,0.25 μm) 毛细管色谱柱(100%甲基聚硅氧烷);进样口温度230℃;恒流模式,流量(FID为N2,质谱为He)1.1 mL/min;程序升温,初始温度50℃,保持2 min,以10℃/min升温速率升温至110℃,保持22min,再以40℃/min升温速率升温至230℃保持3min;分流比 5∶1;进样量 1 μL。 FID 检测器检测,检测器温度250℃;2)质谱条件。EI离子源温度为230℃;MS四极杆温度150℃;电子能量为70 eV;接口温度为280℃;溶剂延迟4.0 min。
2.2 溶液的制备 1)参照物溶液的制备。取4-萜品醇对照品、α-松油醇对照品适量,精密称定,用色谱级乙腈溶解制成质量浓度分别约为100、200、50、50 μg/mL的混合溶液,即得。2)供试品溶液的制备。(1)五味子供试品溶液制备。取五味子果实10 g于蒸馏瓶中,加入100 mL纯化水,煮沸蒸馏,收集蒸馏液25 mL,冷藏(2~5 ℃)过夜;趁冷滤纸过滤;取滤液于固相萃取柱(C18,200 mg/mL)吸附,以 5 mL 纯化水洗涤;将吸附后的小柱离心去除残留水;再用乙腈洗脱至2 mL,即得。(2)注射液供试品溶液制备。取生脉注射液 20 mL,于固相萃取柱(C18,500 mg/mL)吸附富集,以5 mL纯化水洗涤;将吸附后的小柱离心去除残留水;再用乙腈洗脱至2 mL,即得。(3)阴性样品溶液的制备。实验室按生脉注射液标准[3]制得缺五味子蒸馏液生脉液,按上述注射液供试品溶液制备方法制备,即得。
2.3 参照物成分的确定 取参照物溶液、五味子供试品溶液,以“2.1”项下GC条件进行检测。见图1。从图中可以看出,与参照物溶液图谱相应的保留时间位置,供试品溶液图谱中出现两个显著的特征峰。取五味子供试品溶液,以“2.1”项下GC-MS条件进行检测,图谱见图2。质谱片段与对比数据库,确定与参照物相应的峰分别为4-萜品醇、α-松油醇,见图3。

图1 五味子挥发性成分指纹图谱(A)和参照物溶液图谱(B)
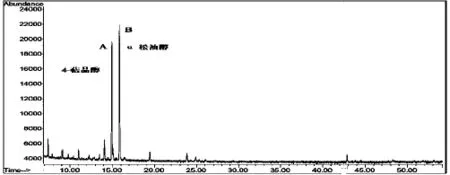
图2 五味子供试品溶液GC-MS的TIC图谱

图3 五味子供试品溶液GC-MS A、B峰质谱图
2.4 方法学考察 1)精密度试验。取同1份五味子供试品溶液,以“2.1”项下色谱条件连续进样5次,记录色谱指纹图谱,计算各共有色谱峰(9个)与参照峰(α-松油醇)的相对保留时间和相对峰面积,结果RSD均小于4.5%,表明仪器精明度良好。2)重复性试验。取同一批五味子药材5份,按照“2.2”项下五味子供试品溶液制备方法进行制样,并以“2.1”项下色谱条件进行检测,记录色谱指纹图谱,计算各共有色谱峰(9个)与参照峰(α-松油醇)的相对保留时间和相对峰面积,结果RSD均小于5.2%,表明该方法重复性良好。2)稳定性试验。取同一份五味子供试品溶液,以“2.1”项下色谱条件分别于 0、2、4、8、12、24 h 进行检测, 记录色谱指纹图谱,计算各共有色谱峰(9个)与参照峰(α-松油醇)的相对保留时间和相对峰面积,结果RSD均小于4.5%,表明供试品溶液在24 h内稳定性良好。
2.5 对照指纹图谱的建立 取10批五味子药材,照“2.2”项下五味子供试品溶液制备方法进行制样,并以“2.1”项下色谱条件进行检测,记录色谱指纹图谱,见图4。利用中药色谱指纹图谱相似度评价系统(2.0版)软件,对色谱图中特征峰(9个)进行匹配,并以平均值生成对照图谱,见图5。
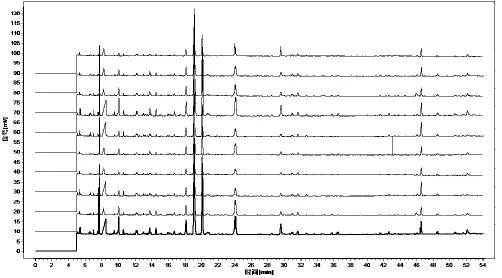
图4 五味子药材挥发性成分指纹图谱
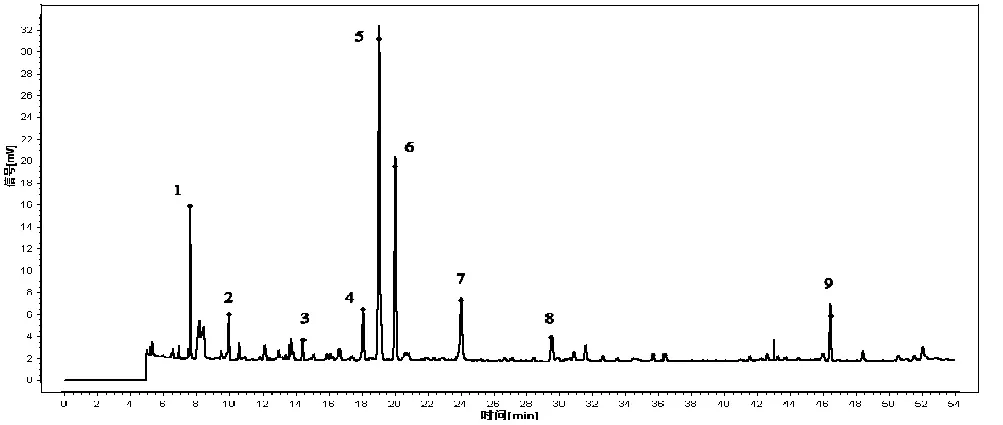
图5 五味子药材挥发性成分对照指纹图谱
2.6 专属性验证 取注射液供试品溶液、阴性样品溶液,以“2.1”项下色谱条件进行检测,色谱图见图。对比分析阴性样品溶液、注射液供试品溶液的指纹图谱和五味子对照指纹图谱。见图6。从图中可知,注射液供试品溶液存在五味子对照指纹图谱中的色谱峰,其中4-萜品醇、α-松油醇峰显著;阴性样品中无五味子供试品色谱峰,提示利用五味子药材挥发性成分指纹图谱控制生脉注射液中五味子挥发性成分专属性强。
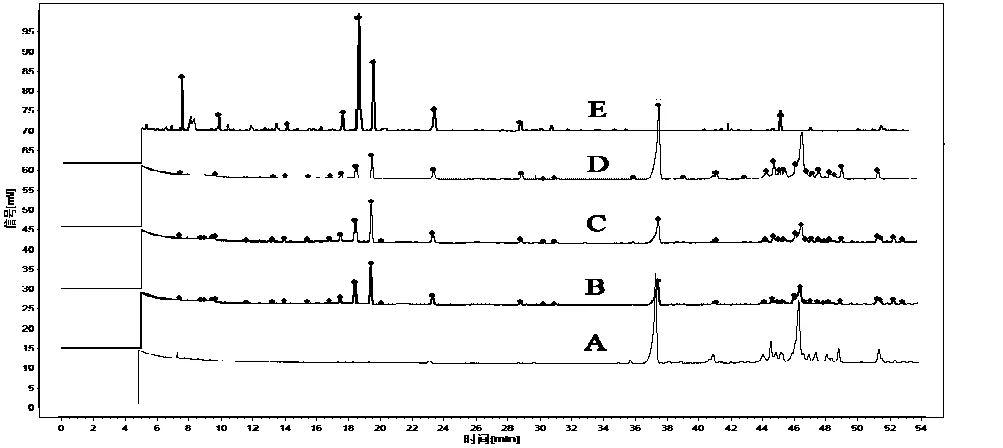
图6 阴性样品溶液(A)、注射液供试品溶液(B:16030802002,C:16080502003,D:16121205001)的指纹图谱和五味子对照指纹图谱(E)
3 讨 论
五味子挥发性成分的研究较多[8-10],多采用水蒸气蒸馏提取。生脉注射液制法中五味子挥发性成分采用水蒸气蒸馏法提取[3],因此本研究采用水蒸气蒸馏法提取五味子挥发性成分,与生产工艺保持一致。固相萃取技术以其高效、高选择性、高度自动化的特点被广泛用于各种生物样品的分离和纯化[11],已有文献报道采用固相萃取法富集挥发性成分[12]。本研究采用固相萃取法富集五味子蒸馏液和生脉注射液挥发性成分,能快速有效地在GC分析中避免水蒸气对色谱柱的影响。
文献报道在北五味子中发现50种挥发性成分[13],4-萜品醇和α-松油醇为其主要成分。本研究采用GCMS对五味子挥发性指纹图谱特征峰进行定性分析,得出图谱中最大的2个峰分别为4-萜品醇和α-松油醇。研究报道4-萜品醇和α-松油醇,具有良好的抑菌[14-15]、杀虫[16]活性,对人体皮肤无影响[17]。 因此以该两种成分作为五味子药材挥发性指纹图谱中的特征峰,质量控制方向明确。
采用固相萃取法富集生脉注射液挥发性成分,气相色谱图中存在4-萜品醇、α-松油醇以及其他色谱信息,说明基于生脉注射液工艺制法建立的五味子药材挥发性成分指纹图,能从源头上控制生脉注射液产品质量,具有较好的质量控制意义。
[1]汪祺,郑笑为,于健东,等.生脉注射液中皂苷类化学成分的研究[J].中国中药杂志,2013,38(11):1731-1734.
[2]夏晶,王钢力,季申,等.HPLC测定生脉注射液中4种成分的含量[J].中成药,2006,28(1):27-30.
[3]国家食品药品监督管理局.WS3-B-2865-98-2011生脉注射液[S].2011.
[4]国家药典委员会.中国药典(一部)[M].北京:中国医药科技出版社,2015:66-67.
[5]李昕,聂晶,高正德,等.超声微波协同水蒸气蒸馏-GCMS分析南、北五味子挥发油化学成分[J].食品科学,2014,35(8):269-274.
[6]汤臣康.五味子的化学和药理研究的新进展[J].西北药学杂志,1994,9(6):278-282.
[7]张胜娜,吴素香.南北五味子挥发油化学成分及药理作用研究进展[J].中药材,2007,30(1):118-120.
[8]徐思思,徐惠芳.GC法测定不同产地五味子藤茎中挥发油含量[J].山西中医学院学报,2015,16(4):31-33.
[9]李慧,娄利峰,李秀歌.北五味子挥发油分离提纯及成分分析[J].食品科学,2014,35(14):73-75.
[10]毛日文,张敏,徐佐旗,等.超临界流体CO2提取法与水蒸汽蒸馏法提取南五味子挥发油的成分比较[J].食品与药品,2011,13(3):189-191.
[11]王洪允,江骥,胡蓓,等.固相萃取技术进展及在生物药物分析中的应用[J].药物分析杂志,2003,23(3):236-241.
[12]高申蓉,吕翼,卢金清.固相萃取-气质联用分析菊花挥发性化学成分 [J].中国医院药学杂志,2014,34(5):380-383.
[13]戴好富,谭宁华,周俊,等.北五味子挥发性化学成分研究[J].中草药,2005,36(9):1309-1310.
[14]陈根强,冯俊涛,陈安良,等.植物精油组分松油烯-4-醇研究进展[J].西北农林科技大学学报,2004,32(8):130-134.
[15]Soon-Nang P,Yun Kyong L,Marcelo OF,et al.Antimicrobial effect of linalool and α-terpineol against periodontopathic and cariogenic bacteria[J].Anaerobe,2012,18(3):369-372.
[16]Matheus DB,Thirssa HG,Carine FS,et al.In vitro and in vivo action of terpinen-4-ol, γ-terpinene, and α-terpinene against Trypanosoma evansi[J].Experimental Parasitology,2016,162(3):43-48.
[17]Lan AS,Susanne F,Diana R.Skin irritancy of tea tree oil[J].Journal of Essential Oil Research,1997,9(1):47-52.

