苯酚加氢制取环己酮的Pd基催化剂研究
张鲁阳, 樊丽辉, 刘东斌, 申延明
(沈阳化工大学 化学工程学院, 辽宁 沈阳 110142)
环己酮是一种无色油状的饱和环酮,是生产尼龙、己内酰胺、己二胺和己二酸的重要有机化工原料,同时也是油漆、油墨、农药、合成树脂、合成橡胶的优良溶剂和稀释剂,在医药、涂料、染料等精细化工领域中应用广泛[1].在工业上,环己酮的合成工艺主要有苯酚加氢法、环己烷氧化法及环己烯水合法[2].伴随着我国石油和焦化工业的发展,苯酚的产量逐年上升,苯酚的价格趋于平稳,采用苯酚加氢法制取环己酮有利于实现苯酚的综合利用[3].
苯酚法是最早应用于工业化生产环己酮的工艺,可以分为两步法和一步法[4-5].两步法是使苯酚先加氢生成环己醇,再脱氢生成环已酮.一步法直接合成环己酮可以更加有效地节约成本和降低能耗.然而,环己酮是一个活泼的反应中间体,可以被进一步加氢生成环己醇等副产物.苯酚一步法又可以分为气相加氢和液相加氢,气相加氢由于反应温度高,副产物较多,且过程中需要汽化原料苯酚和甲醇溶剂,能耗较高;液相加氢反应温度压力较低,环己酮质量较好,能耗较小[6].Pd基催化剂在苯酚液相加氢制环己酮中表现出优良的性能而被广泛使用,已报道的Pd基催化剂有Pd/Al2O3、Pd/SiO2、Pd/MgO、Pd/C等[7-9].研究结果表明载体的性质诸如酸碱性[10]、活性金属Pd的晶粒大小、分散度[11]等对催化剂的性能影响较大.本文以SiO2为载体,制备Pd质量分数为0.5 % 的负载型Pd/SiO2催化剂,考察液相催化苯酚加氢制取环己酮反应的性能.
1 实验部分
1.1 催化剂制备
酸性硅溶胶(SiO2质量分数约为25 %)、Pd(NO3)2·2H2O 购于国药集团化学试剂有限公司.称取25 g酸性硅溶胶,加入62.5 mg Pd(NO3)2·2H2O,超声处理10 min后,常温搅拌下浸渍12 h.之后85 ℃水浴中至溶液蒸干,所得固体80 ℃下干燥12 h,再在550 ℃焙烧4 h,制得Pd/SiO2催化剂.采用水合肼还原催化剂,将制得的催化剂加入烧杯中,加适量蒸馏水并搅拌均匀,逐滴加入过量的水合肼(水合肼与Pd的摩尔比为1.5),常温下搅拌还原4 h,洗涤抽滤后,80 ℃干燥12 h,压片研磨至60~80目备用.
1.2 催化剂表征
催化剂物相结构采用Bruker公司D8 Advance型X光衍射仪进行分析,测试条件:Cu靶,Ka辐射,电流80 mA,电压40 kV,扫描范围2°~70°;比表面积分析采用V-sorb 2800P型全自动氮吸附比表面仪,测试条件:样品在150 ℃下真空预处理5 h后,在液氮温度(-196 ℃)下测定样品的N2吸附-脱附等温线;NH3/CO2-TPD表征采用自制装置,200 mg催化剂N2气氛下在450 ℃活化4 h,待温度降至室温后通NH3/CO2吸附0.5 h,重复吸氨2次.之后N2气氛下100 ℃吹扫1 h,脱除物理吸附的NH3/CO2,降温至室温后,通入He(流量40 mL/min),以10 ℃/min程序升温至800 ℃,记录TCD信号;H2-TPR分析采用自制装置,催化剂装填量50 mg,在N2气氛下450 ℃恒温吹扫30 min,冷却至室温后,通入体积分数分别为95 %和5 %的N2和H2混合气,流量40 mL/min,以10 ℃/min由室温程序升温至800 ℃,记录TCD信号值.
1.3 催化剂的活性评价
催化剂的活性评价在100 mL高压釜(ZNCL-TS型滨海县正信仪器厂)中进行.将1 g还原后的催化剂及20 mL原料[m(苯酚)∶m(乙醇)=1∶4]加入高压釜中,先用N2置换出釜内空气,再用H2置换数次.调节釜内压力达到反应所需值,关闭进口阀并保证高压釜的气密性.升温至所需反应温度,开始搅拌并记录反应时间.反应产物采用SP-2100型气相色谱仪(北分瑞利)进行分析,色谱柱为AT FFAP 30 m×0.32 mm×0.5 μm型毛细管柱,氢火焰离子化检测器(FID).
2 结果与讨论
2.1 Pd/SiO2催化剂的表征结果
图1、图2分别为Pd/SiO2催化剂的吸附-脱附等温线和孔径分布图.从图1可以看出:吸附-脱附等温线属于Ⅳ型,具有滞后环,属于介孔的特征.在低压阶段吸附量平缓增加,此时N2分子以单层到多层吸附在介孔的内表面.在p/p0=0.7~0.9左右吸附量有一突增,源于N2分子在孔道内的冷凝积聚.由图2可以看出:Pd/SiO2在2~20 nm范围内具有较宽泛的孔径分布,计算得出平均孔径为8.37 nm.采用BET(Brunauer-Emmett-Teller)及BJH(Barrett-Joiner-Halenda)模型分别计算比表面积及孔容为237.93 m2/g和0.53 cm3/g.
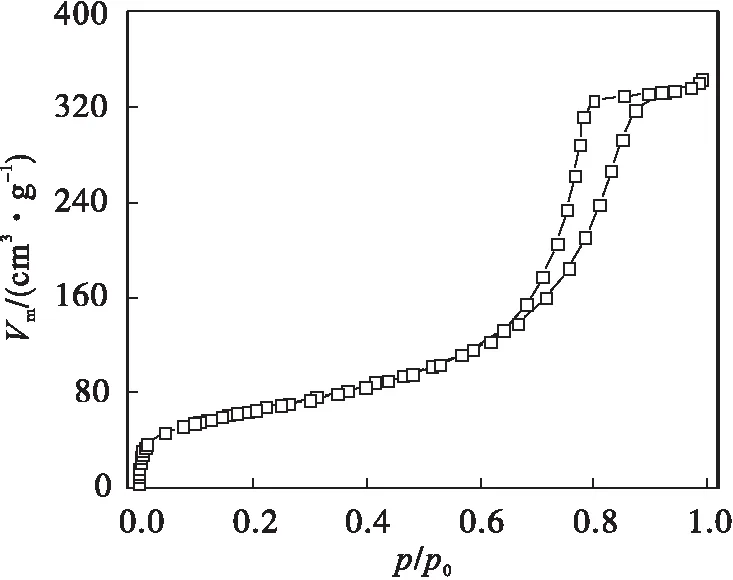
图1 Pd/SiO2的吸附-脱附等温线Fig.1 Adsorption-desorption isotherm of Pd/SiO2

图2 Pd/SiO2的孔径分离Fig.2 Pore distribution curver of Pd/SiO2
由图3可以看出:还原后的Pd/SiO2在2θ=21.2°处出现了弥散的衍射峰,归属于SiO2特征衍射峰(PDF 01-0378)[8],说明SiO2以无定型状态出现.XRD图谱中未发现明显的Pd或者PdO的特征衍射峰,这可能是由于Pd负载量较低而无法检出[12].
图4为Pd/SiO2的H2-TPR图,可发现在低温 (tmax低于 105 ℃)时出现较强的负峰,此负峰是由于Pd0表面吸附氢所致,这也证明SiO2载体上Pd0的存在[13],而第2个负峰应为Pd0表面氢溢流所致[14].TPR图中未出现明显的正峰,表明负载的Pd颗粒度较小,Pd在SiO2载体表面分散较好,导致Pd2+在较低温度下即可被H2还原.
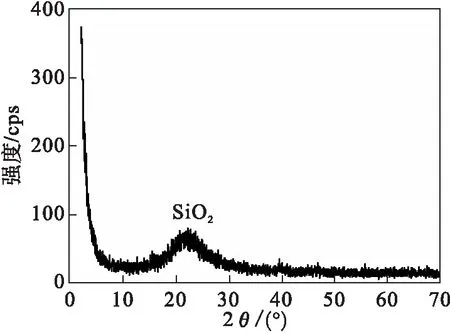
图3 Pd/SiO2催化剂的XRD图Fig.3 XRD patterns of Pd/SiO2 catalyst
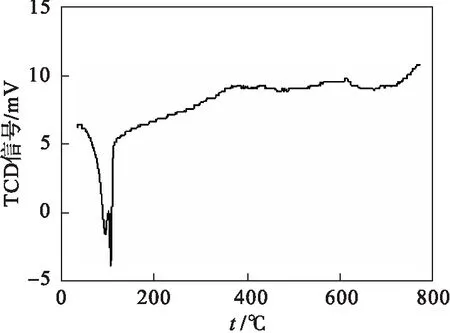
图4 Pd/SiO2催化剂的H2-TPR图Fig.4 TPR profile of Pd/SiO2 catalyst
图5为Pd/SiO2催化剂的NH3-TPD及CO2-TPD图.催化剂的酸(碱)性中心可以根据脱附温度的高低划分为弱酸(碱)中心(150~250 ℃),中强酸(碱)中心(250~350 ℃),强酸(碱)中心(350~450 ℃)[15-16].NH3-TPD图可以看出在150~250 ℃有一强的脱除峰,表明Pd/SiO2具有弱酸性[17-18],而CO2-TPD图中没有明显的脱除峰,只是在350~700 ℃有一宽泛的弱峰,应归属于中强碱中心上CO2的脱除峰,比较NH3-TPD和CO2-TPD图可知Pd/SiO2催化剂主要以弱酸性为主.

图5 Pd/SiO2催化剂的NH3-TPD和CO2-TPD图Fig.5 NH3-TPD and CO2-TPD profiles of Pd/SiO2
2.2 催化剂活性评价结果
据报道苯酚加氢制环己酮的反应历程可以描述为[8,19]:首先苯酚吸附在催化剂载体表面,氢气吸附在Pd表面,之后吸附的苯酚与吸附的氢反应生成1-羟基环己烯,1-羟基环己烯很活泼,迅速重排生成环己酮.环己酮可以继续反应生成环己醇、环己烷等副产物,反应历程如图6所示.

图6 苯酚加氢反应历程Fig.6 Process of phenol hydrogenation reaction
2.2.1 反应温度对催化活性的影响
由表1反应温度对催化剂活性的影响可以看出:随着反应温度的升高,转化率不断上升,从40.99 %增加到94.42 %,这说明升高温度可以有效提高催化剂的活性;另一方面苯酚加氢制环己酮的反应为放热反应[6],温度过高加剧了副反应的发生,导致苯酚过度加氢,副产物增多,环己酮的选择性随之下降.苯酚加氢制取环己酮的反应在135 ℃进行时,具有较高的转化率71.62 %,环己酮的选择性达到90.77 %.
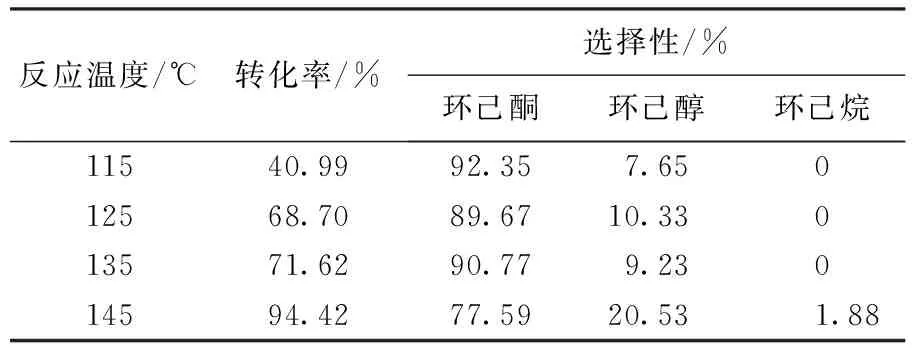
表1 反应温度对Pd/SiO2催化活性的影响Table 1 Catalytic activity on Pd/SiO2 obtained at different reaction temperature
注:反应压力1 MPa,反应时间3.5 h.
2.2.2 反应时间对催化活性的影响
反应时间对催化活性的影响如表2所示.Pd/SiO2催化苯酚加氢反应时,随着反应时间的延长,苯酚有充裕的时间与H2反应,从而催化剂的转化率不断上升.但是环己酮的选择性先增高后下降,这是因为反应时间过长会导致反应产物环己酮继续加氢生成环己醇等副产物,适宜的反应时间为3.5 h.
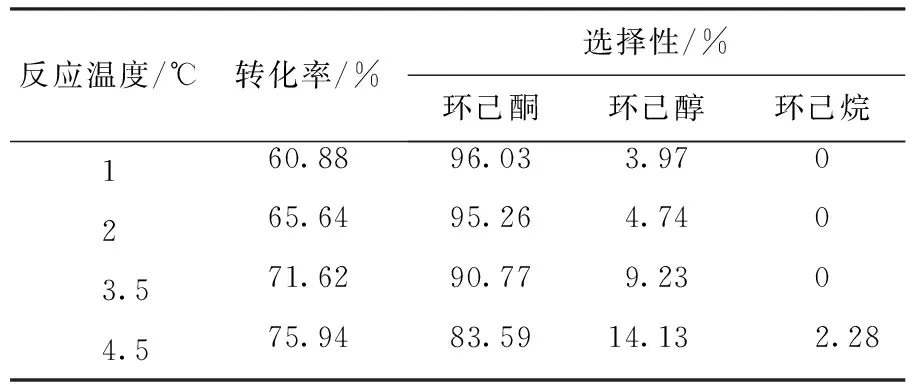
表2 反应时间对Pd/SiO2催化活性的影响Table 2 Catalytic activity on Pd/SiO2 obtained at different reaction time
注:反应压力1 MPa,反应温度135 ℃.
2.2.3 H2压力对催化活性的影响
由表3可以看出:随着H2压力的提高,苯酚的转化率不断上升,但达到1.0 MPa后,增加H2压力,转化率基本不变.但是环己酮的选择性却随着H2压力的增加而降低,表明低压有利于避免苯酚过度加氢生成环己醇等副产物.考虑到苯酚的转化率以及设备耐压性及安全性的问题,选择反应压力为1.0 MPa为宜.
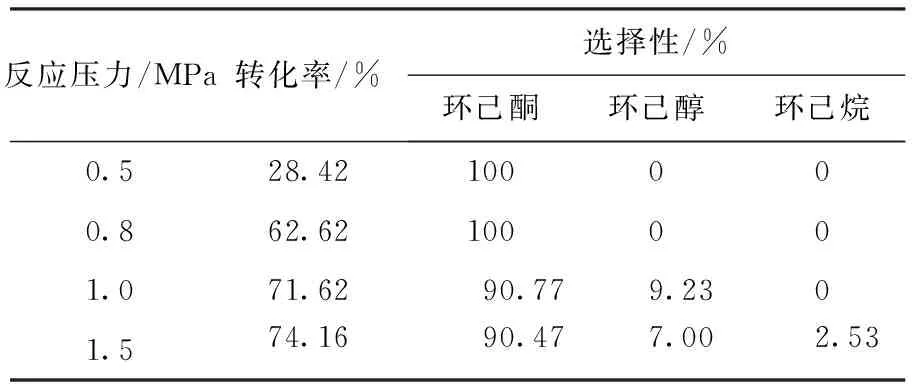
表3 H2压力对Pd/SiO2催化活性的影响Table 3 Catalytic activity on Pd/SiO2 obtained at different H2 pressure
注:反应温度135 ℃,反应时间3.5 h.
2.3 反应机理
按照上述反应路线,苯酚在催化剂上的吸附能力、吸附方式对反应活性起到很重要的作用,而苯酚在催化剂表面的吸附与催化剂载体的酸碱性、表面Pd的分散程度等因素有关[20].在酸性载体上苯酚以“共平面”方式吸附,利于生成环己醇及环己烷[21].Pd/SiO2催化剂主要以弱酸性为主,苯酚主要以“共平面”方式吸附在催化剂表面,但是,高度分散的Pd能与苯环形成“π-配合物”,利于苯酚加氢生成环己酮[19].反应机理如图7所示.
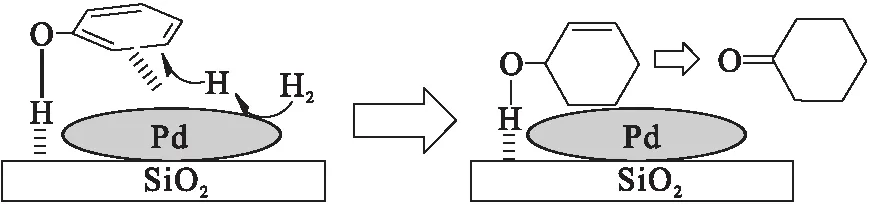
图7 苯酚加氢反应机理Fig.7 Mechanism of phenol hydrogenation reaction
3 结 论
Pd/SiO2催化剂具有良好的苯酚液相加氢制备环己酮性能,在反应温度135 ℃,反应压力1 MPa,反应时间3.5 h的反应条件下,苯酚的转化率为71.62 %,环己酮的选择性达到90.77 %.良好的催化性能源于Pd/SiO2催化剂较大的比表面积、高度分散的Pd以及适宜的酸碱性.
:
[1] BELLUSSI G,PEREGO C.Industrial Catalytic Aspects of the Synthesis of Monomers for Nylon Production[J].Cattech,2000,4(1):4-16.
[2] 刘小秦.环己酮生产工艺的发展及研究进展[J].化工进展,2003,22(3):306-309.
[3] YANG P,WANG B.Review of Treatment of Coking Wastewater by Biological Methods[J].Environmental Protection of Chemical Industry,2001,21(3):4.
[4] 任培兵,任雁,张妍,等.环己酮生产技术分析[J].化学工业,2010,28(1):20-21.[5] MAHATA N,RAGHAVAN K V,VISHWANATHAN V,et al.Phenol Hydrogenation over Palladium Supported on Magnesia:Relationship between Catalyst Structure and Performance[J].Phys.Chem.Chem.Phys,2001,3(13):2712-2719.
[6] ZHONG J W,CHEN J Z,CHEN L M.Selective Hydrogenation of Phenol and Related Derivatives[J].Catalysis Science & Technology,2014,4(10):3555-3569.
[7] 朱俊华,丁洁莲,曾崇余.载体对钯催化剂催化苯酚加氢制环己酮性能的影响[J].催化学报,2007,28(5):441-445.
[8] LI H,LIU J L,LI H X.Liquid-Phase Selective Hydrogenation of Phenol to Cyclohexanone over the Ce-doped Pd-B Amorphous Alloy Catalyst[J].Materials Letters,2008,62(2):297-300.
[9] 姬生菲,申延明,刘东斌,等.Pd/CNTs苯酚气相加氢制环己酮催化剂[J].沈阳化工大学学报,2012,26(1):26-30.
[10] WATANABE S,ARUNAJATESAN V.Influence of Acid Modification on Selective Phenol Hydrogenation over Pd/Activated Carbon Catalysts[J].Topics in Catalysis,2010,53(15):1150-1152.
[11] 王鸿静,项益智,徐铁勇,等.Ba修饰的Pd/Al2O3对苯酚液相原位加氢制环己酮反应的催化性能[J].催化学报,2009,30(9):933-938.
[12] 唐博合金,吕仁庆,项寿鹤.纳米Pd/Al2O3催化剂的表征及其选择性加氢反应性能[J].石油学报(石油加工),2007,3(3):13-19.
[13] CLAUS P,BERNDT H,MOHR C,et al.Pd/MgO:Catalyst Characterization and Phenol Hydrogenation Activity[J].Journal of Catalysis,2000,192(1):88-97.
[14] AMORIM C,KEANE M A.Catalytic Hydrodechlorination of Chloroaromatic Gas Streams Promoted by Pd and Ni:The Role of Hydrogen Spillover[J].Journal of Hazardous Materials,2012,211-212:208-217.
[15] DIXIT M,MISHRA M,JOSHI P A,et al.Physico-Chemical and Catalytic Properties of Mg-Al Hydrotalcite and Mg-Al Mixed Oxide Supported Copper Catalysts[J].Journal of Industrial and Engineering Chemistry,2013,19(2):458-468.
[16] CHEN J,TIAN S H,LU J,et al.Catalytic Performance of MgO with Different Exposed Crystal Facets Towards the Ozonation of 4-chlorophenol[J].Applied Catalysis A:General,2015,506:118-125.
[20] NERI G,VISCO A M,DONATO A,et al.Hydrogenation of Phenol to Cyclohexanone over Palladium and Alkali-doped Palladium Catalysts[J].Applied Catalysis A:General,1994,110(1):49-59.
[21] VELU S,KAPOOR M P,INAGAKI S,et al.Vapor phase Hydrogenation of Phenol over Palladium Supported on Mesoporous CeO2and ZrO2[J].Applied Catalysis A:General,2003,245(2):317-331.

