二维层状谷氨酸-Gd配合物的合成、结构及磁性研究
陈小玲, 由立新, 熊 刚, 孙亚光
(沈阳化工大学 应用化学学院, 辽宁 沈阳 110142)
随着配位化学的飞速发展,稀土氨基酸配合物被大量报道,其在微肥、饲料添加剂、荧光材料、生物医学和分子磁性材料等方面的应用[1-3]也被广泛研究.稀土氨基酸配合物可作为植物的生长调节剂,具有增加产量和改善品质等多种功能[1,4];稀土氨基酸配合物还可用作畜、禽、鱼饲料的添加剂,显著提高动物对营养物质的利用和吸收,具有提高产量和质量、抵制疾病的作用[1,5-6];稀土氨基酸配合物大多具有较强的荧光性能,主要用于生物荧光探针领域[7];在生物医药方面,稀土氨基酸配合物具有杀菌、消炎、降血糖等作用[8-9];部分稀土氨基酸配合物表现出慢磁弛豫行为或高的磁熵变[3,10].因此合成新颖的稀土氨基酸配合物具有重要意义和实用价值.本文以L-谷氨酸为配体,合成二维层状结构的{[Gd4(L-HGlu)4(H2O)16](ClO4)8·5H2O}n稀土配位聚合物,并对其结构进行了详细表征.另外,使用等温磁化率研究了配合物中的磁超交换行为.
1 实验部分
1.1 试剂及仪器
所有试剂均为市售分析纯,使用过程中未做任何纯化处理,实验中所用水为蒸馏水.红外光谱是将待测样品与光谱纯KBr的圆形压片在Bruker Tensor27 FTIR型红外光谱仪中测试得到.C、H、N的含量分析测试使用Perkin-Elemer 240型元素分析仪.X-射线粉末衍射PXRD在D/Max-2500 X-射线衍射仪中进行测试.磁性测试是使用Quantum Design MPMS-7 Micro-SQUID型磁强计测试,实验数据均用Pacal’s常数进行抗磁校正.
1.2 配合物的合成
将1.0 mmol Gd(ClO4)3·6H2O、1.0 mmolL-谷氨酸H2Glu溶解于10 mL H2O中,得到无色透明溶液.将0.1 mol/L的NaOH水溶液逐滴加入到透明溶液,将pH值调至4.7左右,此时溶液无明显变化.将溶液加热至80 ℃,恒温反应4 h.冷却过滤,自然挥发.十几天后,只剩少量的溶液,此时有大量的无色透明片状晶体析出.用乙醇洗涤、35 ℃干燥,得到0.423 0 g产物,产率为70.76 %.
1.3 晶体结构测试


表1 配合物的晶学参数Table 1 Crystal parameters of the complex
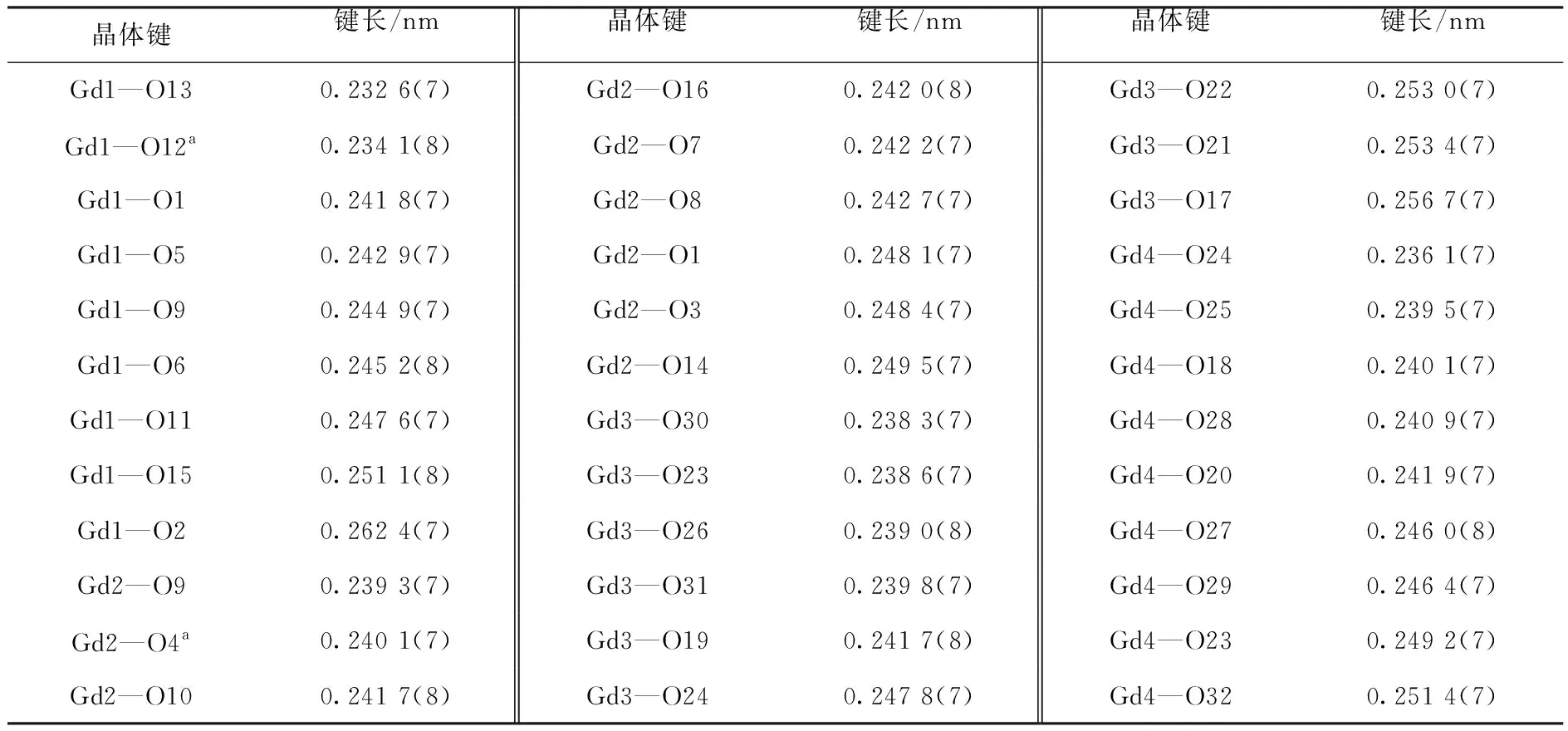
表2 配合物主要的键长Table 2 The bond length for complex
注:a1-x,1/2+y,1-z.
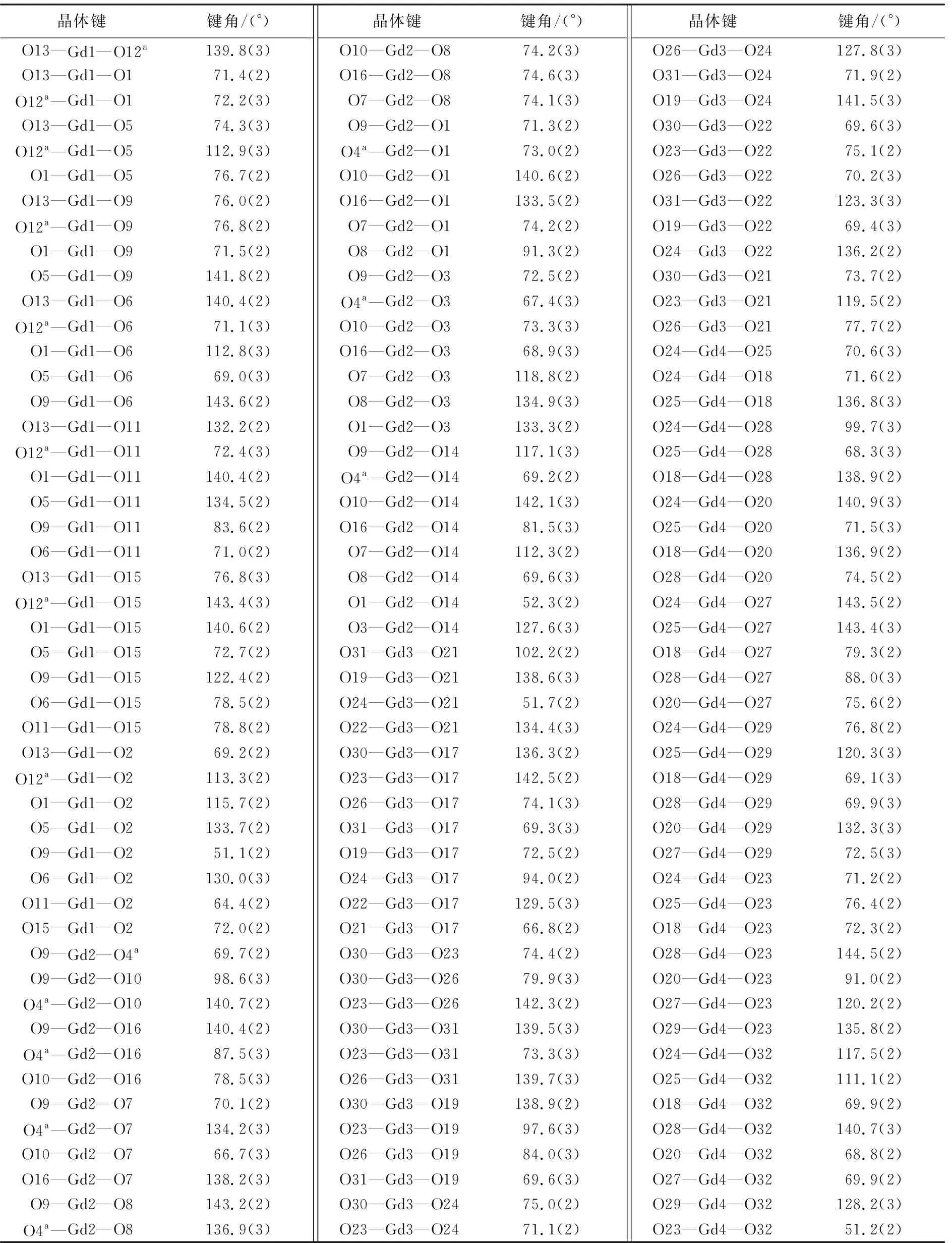
表3 配合物主要的键角Table 3 The bond angle for complex
注:a1-x,1/2+y,1-z.
2 结果与讨论
2.1 配合物的元素分析和IR
分子式为C20H58O69N4Gd4Cl8,相对分子质量为2 371.28,元素分析理论值(实验值),w/%:C,10.12(9.24);N,2.36(2.43),H,2.45(2.48).配合物的红外光谱如图1所示, 3 401 cm-1(s)为 O—H和N—H的伸缩振动吸收峰,1 618 cm-1(m)为羰基中C==O的伸缩振动吸收峰,1 341 cm-1(s)为C-H的面内弯曲吸收峰,1 001 cm-1(s) 为羰基C—O单键的伸缩振动吸收峰,627 cm-1(m)为N—H的扭曲振动吸收峰.
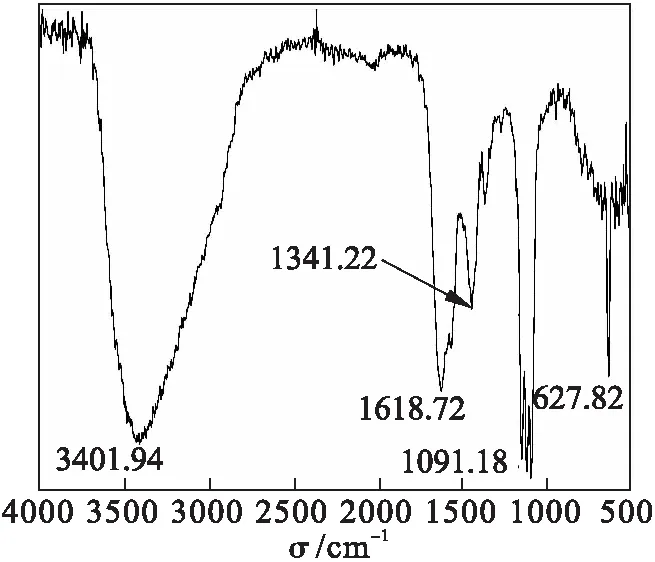
图1 配合物的红外光谱Fig.1 The IR spectrum of the complex
2.2 配合物的单晶结构描述
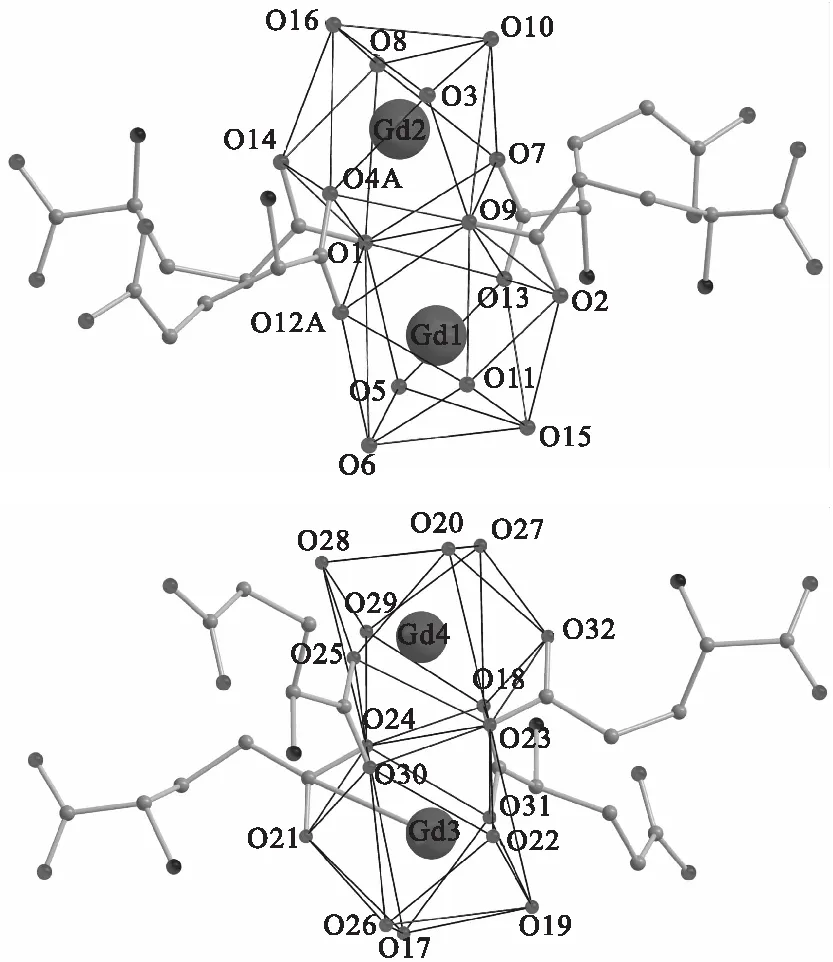
图2 配合物中Gd离子的配位环境Fig.2 The coordination environment of Gd ions in the complex
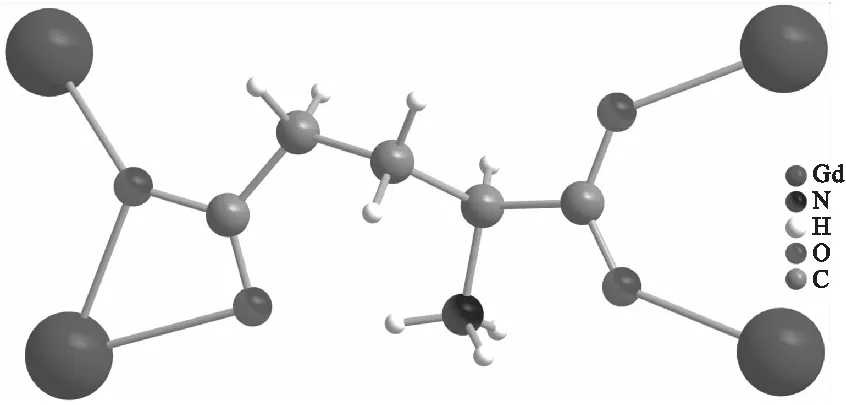
图3 L-谷氨酸的配位环境Fig 3 The coordination mode of L-Glutamic acid
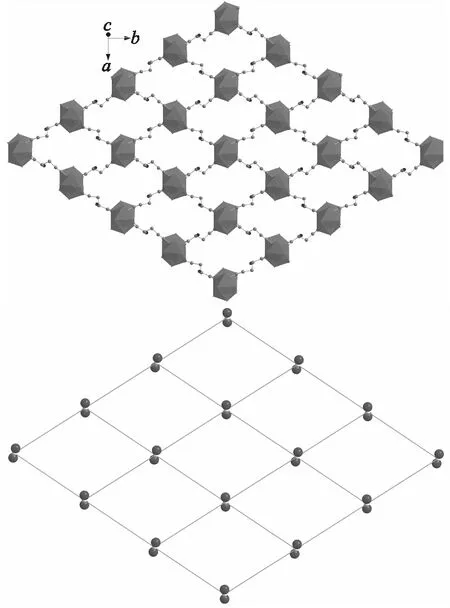
图4 配合物的二维网状结构及其拓扑图Fig 4 The two dimensional structure and topology of the complex
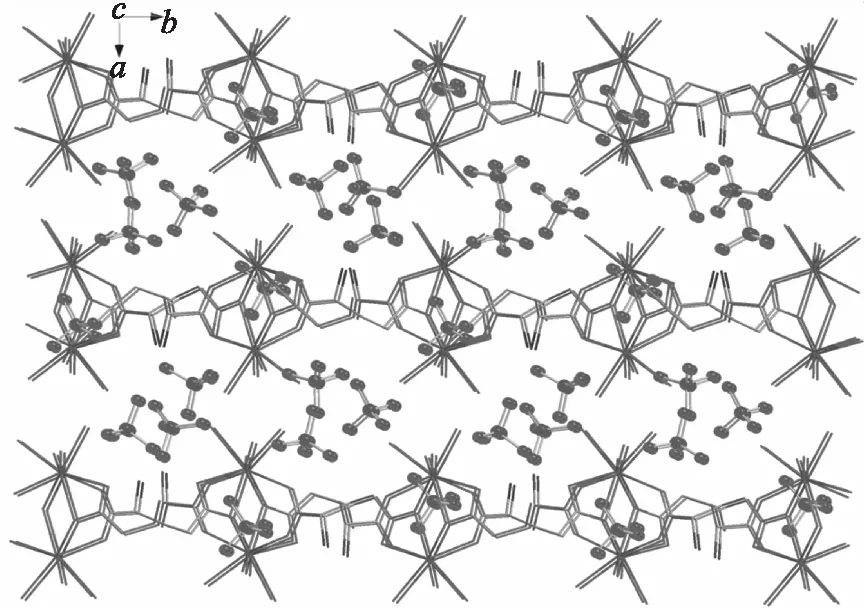
图5 配合物的超分子三维结构Fig 5 The supermolecule structure of the complex
2.3 配合物的PXRD
在室温下,2θ为3°~60°之间,采用X-射线粉末衍射法对配合物进行粉末衍射测试.配合物的PXRD谱图如图6所示,通过对比样品粉末衍射谱图与单晶结构数据模拟谱图,发现它们很好地吻合,证明配合物具有较高的相纯度.
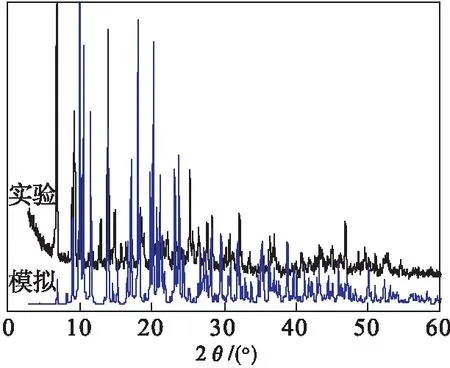
图6 配合物的粉末衍射谱图以及单晶结构数据模拟谱图Fig.6 The experimental PXRD patterns and the simulated XRD patterns from single-crystal data of the complex
2.4 配合物的磁学性质
配合物的变温磁化率在温度2~300 K,外加磁场0.1 T条件下进行测定,结果见图7.室温条件下,χmT的实验值为30.9 cm3mol-1K,接近理论值31.5 cm3mol-1K.当温度在80~300 K时,随着温度的降低,χmT值基本维持不变.当温度在2~80 K时,χmT值随着温度的降低而减小,在2 K时达到χmT的最小值为26.32 cm3mol-1K,这种χmT的下降趋势显示了配合物中不同GdⅢ之间存在弱的反铁磁相互作用.利用χm=C/(T-θ)对实验数据进行最小二乘法拟合,得出的直线如图7中的实线所示.
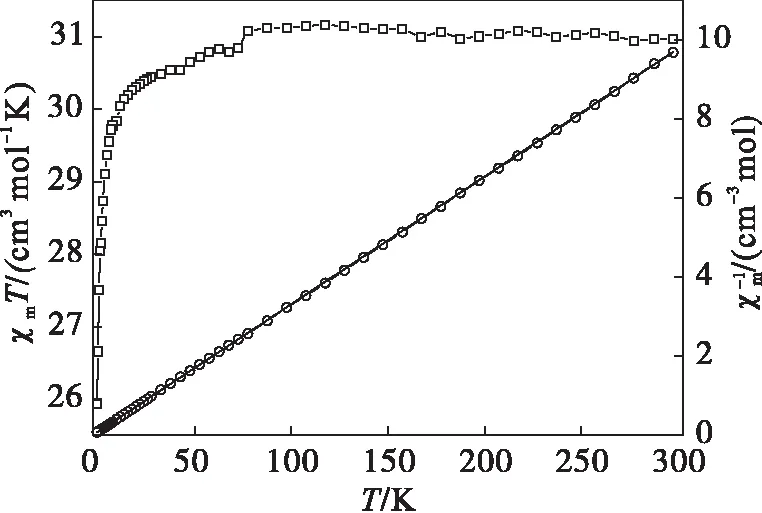
图7 配合物的χmT对T(□)和对T(○)的曲线Fig.7 χmT vs.T and vs.T plots of complex
最佳拟合参数Weiss常数θ=-0.24 K,Curie常数C=30.97 cm3mol-1K,由拟合得到的Weiss常数可以进一步说明在配合物中存在着GdⅢ之间的反铁磁相互作用[3,10].
3 结 论
通过调节pH值的方法合成了配合物,并对其进行X-射线单晶衍射、PXRD和红外光谱等方法的测试,结果表明配合物是二维网格的层状结构,是通过谷氨酸的羧基氧桥连双核Gd单元进而构筑而成.在此基础上,不同的层与层之间通过氢键相互作用与游离在外界的高氯酸根相连进一步扩展成类似“夹心三明治”的三维超分子结构.通过对配合物的变温磁化率的研究,发现在配合物中的双核Gd单元中Gd离子之间存在弱的反铁磁作用.
:
[1] 林木雄,向华,唐晖然,等.稀土氨基酸配合物应用研究综述[J].广东微量元素科学,2016,23(1):9-16.
[2] 周秋明.稀土与氨基酸固体配合物的合成及性质探讨[J].山东工业技术,2014(12):222.
[3] XIONG G,XU H,CUI J Z,et al.The Multiple Core-Shell Structure in Cu24Ln6Cluster with Magnetocaloric Effect and Slow Magnetization Relaxation[J].Dalton Trans.,2014,43(15):5639-5642.
[4] 申凤善,李熙英.氨基酸稀土配合物对植物病原菌及辣椒幼苗生长的影响[J].延边大学农学学报,2008,30(3):181-184.
[5] 张义,周定刚,刘宏伟.稀土及其螯合物在鸡上的研究应用[J].饲料工业,2007,28(22):6-8.
[6] 许甲平,鲍宏云,邓志刚,等.稀土元素氨基酸螯合物对保育期仔猪生长性能的影响[J].饲料工业,2012,33(8):60-62.
[7] GENG J,QU X G.Recent Progress Report on DNA B-Z Transition Modulated by Rare Earth-Amino Acid Complex and Alzheimer′s Disease Amyloid Beta[J].Journal of Rare Earths,2010,28(6):820-823.
[8] 何水样,宋迪生,郭爱莲.稀土与氨基酸固体配合物的合成及生物活性的研究[J].中国稀土学报,1995,13(4):368-370.
[9] 刘杰凤,韩寒冰,周天.镝氨基酸(Tyr,Trp) 咪唑配合物的合成与抗菌性能研究[J].湖北农业科学,2011,50(16):3310-3313.
[10] XIONG G,QIN X Y,SHI P F,et al.New Strategy to Construct Single-Ion Magnets:a Unique Dy@Zn6Cluster Exhibiting Slow Magnetic Relaxation[J].Chem.Commun.,2014,50(32):4255-4257.
[11] SHELDRICK G M.A Short History ofSHELX[J].Acta Crystallographica,2008,64(1):112-122.

