比较单纯与结合椎体内射频消融的椎体成形术的临床效果
陈祥铠,郑丰裕
(北京王府中西医结合医院骨伤科,北京 102209)
目前骨质疏松性椎体压缩骨折(osteoporotic vertebral compression fracture,OVCF)的发生率不断增高,经皮椎体成形术(percutaneous vertebroplasty,PVP)作为一项治疗此种骨折的新型微创脊柱外科技术被广泛应用于临床[1],随着在临床的广泛开展,PVP相关骨水泥渗漏等并发症的报道逐渐增多[2-4]。如何在保证手术治疗效果的情况下减少骨水泥渗漏等并发症已成为越来越多学者们的研究目标。我院应用PVP联合射频消融(radiofrequency ablation,FRA)治疗OVCF在恢复椎体高度上有一定疗效,在缓解患者疼痛症状及减少骨水泥渗漏等并发症上有良好的效果,现报告如下。
1 资料与方法
1.1 一般资料 回顾性研究分析2016年1月至2017年7月我院骨科收治的109例行PVP治疗的OVCF患者。根据手术方法不同,分组如下:单纯椎体成形术组,即对照组;椎体成形术结合椎体内射频消融组,即联合组。所有手术均由同一个手术医师完成。
在109例患者中,男性32例,女性77例;年龄60~95岁,平均77.0岁。对照组57例患者,共69个伤椎;其中T7椎体1个,T9椎体1个,T10椎体1个,T11椎体5个,T12椎体19个,L1椎体23个,L2椎体7个,L3椎体5个,L4椎体4个,L5椎体3个。联合组52例患者,共66个伤椎;其中T6椎体1个,T7椎体2个,T8椎体3个,T9椎体2个,T10椎体1个,T11椎体8个,T12椎体13个,L1椎体15个,L2椎体6个,L3椎体8个,L4椎体6个,L5椎体1个。两组患者在年龄、性别、受伤时间方面比较差异无统计学意义(P>0.05),具有可比性(见表1)。

表1 两组一般资料比较
1.2 纳入标准 a)诊断符合WHO组织制定的骨质疏松性椎体压缩骨折诊断标准[5];b)影像学显示为新鲜骨折;c)受伤时间≤3周。
1.3 排除标准 a)术后病理结果为骨肿瘤;b)影像学资料不全;c)受伤时间>3周。
1.4 手术方法
1.4.1 术前准备 两组患者均进行常规的肝肾功能、心电图、胸片、凝血功能、血常规、尿常规、便常规以及脊柱X线、MRI或CT检查,指导患者俯卧位训练。
1.4.2 手术操作 常规心电、血氧饱和度及血压监测,建立静脉通道,让患者俯卧位并将胸腹部悬空,C型臂透视下定位伤椎,常规确定双侧椎弓根穿刺点并标记。对术区做好常规的消毒、铺巾工作。使用浓度为1%的利多卡因对患者进行局麻,用尖刀以椎体两处穿刺标记点切开2个3 mm左右切口,分别用一次性专用PVP骨穿刺针,经切口标记点循椎弓根入路穿入。在C型臂正侧位透视监视下,侧位片发现进针至椎体前1/3处,正位片显示穿刺针尖越过椎弓根内缘。
对照组操作如下:调制骨水泥并装入骨水泥推进器,待到拉丝期将其接入已经穿刺到位的PVP针管,逐渐旋转推注器,并间断进行X线透视,观察骨水泥在伤椎内弥散情况,并旋转针管直到椎体内骨水泥有良好的弥散状态,等待骨水泥凝固之后取出穿刺针,做好无菌包扎。手术过程密切监测生命体征变化情况。
联合组操作如下:先用20 mL注射器注入生理盐水进行灌洗,再选用SYSTEMS 2000型等离子射频消融仪,将一次性射频刀头经穿刺针置入椎体内部,以高频(50HZ)进行电流刺激。根据穿刺椎体内压力和出血情况,对椎体前中部进行多点、多次,从低温等离子消融到高温气化的不同操作,时间持续3~5 min。在射频消融中不定时透视针尖位置,并反复用生理盐水从另一侧穿刺针注入进行灌洗,操作后用注射器抽吸至出血明显减少。骨水泥注入过程同对照组。
1.4.3 术后处理 患者术后返回病房,即能够翻身,必要时给予心电监测并行X线检查。术后指导患者进行功能锻炼,以主动活动为主。
1.5 观察指标 X线测量患者治疗前和治疗后的椎体前后缘高度比,观察是否出现骨水泥渗漏,并详细记录外渗具体位置,分为骨水泥总体外渗和椎旁血管渗漏。收集患者基本资料,记录术前及术后第1天的视觉模拟评分(visual analogue scale,VAS)。

2 结 果
2.1 两组单椎体骨水泥注入量及手术时间比较 联合组在单椎体骨水泥注入量及单椎体手术时间上均略高于对照组,但无差异无统计学意义(见表2)。
2.2 两组VAS评分比较 两组患者治疗后VAS均低于治疗前,差异有统计学意义(P<0.001);两组术前VAS组间比较,差异无统计学意义(P>0.05)。联合组术后VAS低于PVP组,但两组比较差异无统计学意义(P>0.05,见表3)。

表2 两组单椎体骨水泥注入量及手术时间比较
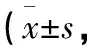
表3 两组术前及术后VAS评分比较分)
2.3 两组椎体高度恢复情况 两组患者治疗后伤椎前后缘高度比均高于治疗前,但差异无统计学意义(P>0.05);两组术前及术后组间相比较,椎体前后缘比较差异无统计学意义(P>0.05,见表4)。

表4 两组术前及术后椎体前后缘高度比恢复情况
2.4 两组骨水泥渗漏情况 两组伤椎骨水泥渗漏发生率为28.9%,对照组26个椎体(37.7%),联合组13个椎体(19.7%),两组比较差异有统计学意义(P<0.05);两组血管渗漏发生率8.9%,对照组10个椎体(14.5%),联合组2个椎体(3.0%),两组比较差异有统计学意义(P<0.05)。
2.5 典型病例 82岁男性患者,摔伤后腰背部疼痛伴活动受限1 d入院。入院时患者四肢肌力和感觉正常,诊断为T12椎体压缩性骨折。入院后第6天行单纯PVP治疗,术后第1天患者腰背部疼痛明显缓解,四肢肌力和感觉正常。复查X线片示T12椎体骨水泥弥散良好,椎体高度有所恢复,但骨水泥椎旁血管渗漏。手术前后影像学资料见图1~3。
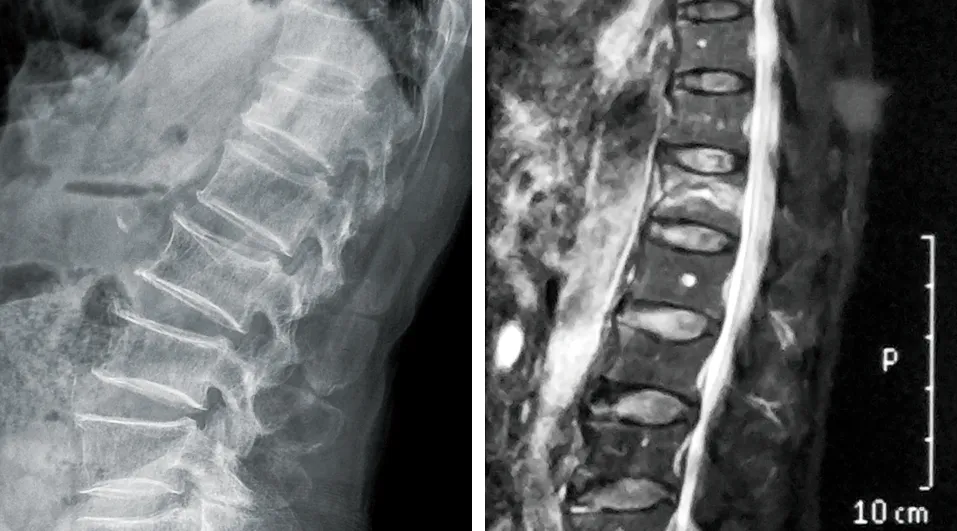
图1 术前侧位X线片示T12楔形变 图2 术前MRI矢状位脂肪抑制像示T12椎体高信号
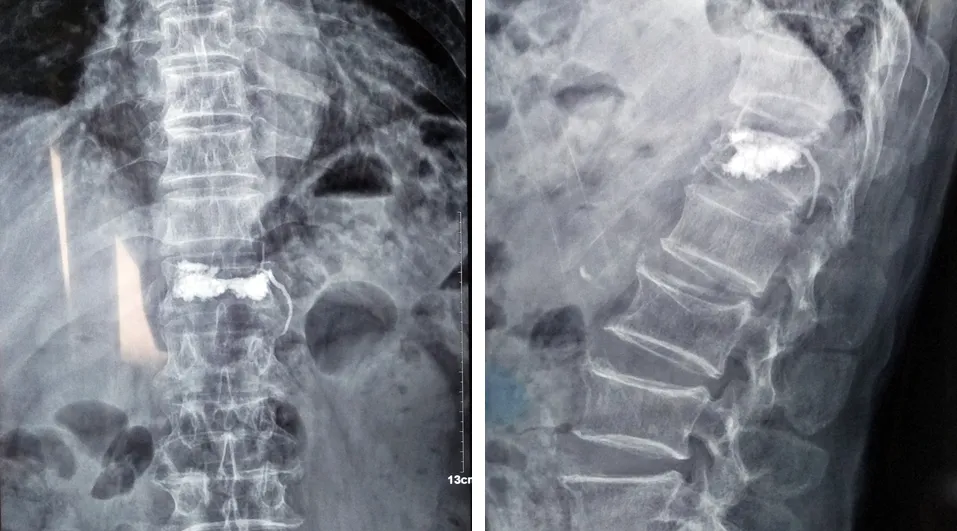
图3 术后正侧位X线片示T12椎体骨水泥血管渗漏
3 讨 论
3.1 椎体成形术止痛机制 经皮椎体成形术作为治疗胸腰椎骨质疏松性骨折的一种新型微创技术,可以达到固定椎体、防止塌陷、缓解疼痛、甚至恢复部分椎体高度的目的[6]。PVP的止痛机制目前尚不完全清楚,一般认为是[7-9]:a)骨水泥注入后,其机械作用使局部血管截断,化学毒性作用和聚合时产生的热效应可使周围组织神经末梢坏死;b)骨水泥的注入加强了椎体强度,并稳定了压缩椎体内的微骨折,减少了骨折断端的微运动,从而减少了对痛觉神经末梢的刺激。
3.2 椎体成形术骨水泥渗漏原因 虽然PVP止痛效果令人满意,但也存在一些风险,其中骨水泥渗漏是椎体成形术中的关键性问题[10]。按渗漏部位分类有硬膜外渗漏、椎间神经孔渗漏、椎间盘渗漏、脊椎旁软组织渗漏、椎旁静脉渗漏、穿刺针道渗漏[11]。虽然大部分骨水泥渗漏无临床症状,但是骨水泥经椎基底静脉或后缘皮质裂缝渗漏进入椎管区域,极有可能对硬膜及脊髓神经造成压迫;经椎体间静脉丛渗漏一旦脱落随血液回心返流,则有可能直接造成致命性的肺部栓塞[12-13]。椎体成形术中骨水泥渗漏仍存在较高概率,Garfin等[14]文献回顾,骨水泥渗漏在椎体成形术中发生率达30%~67%。而本次研究中,我们发现对照组骨水泥渗漏率为37.7%,与既往文献报道相近,而联合组的骨水泥渗漏率为19.7%,低于既往文献报道,在椎旁血管渗漏上后者也明显低于前者。目前临床上普遍认为骨水泥渗漏除了椎体骨皮质损伤破损因素外,跟骨水泥注射时的压力也呈正相关性[15]。注射骨水泥时椎体内压力增高,高于椎体内静脉压,容易导致骨水泥向椎体静脉系统渗漏[16]。杨铁军等[17]通过球囊二次扩张能够降低伤椎注射骨水泥时的压力而降低骨水泥渗漏率。
3.3 射频消融在椎体成形术中的作用机制 射频消融作为一种新型的微创技术,采用低温等离子冷融切割技术,利用射频电场产生的等离子薄层,获得足够动能的离子具有切割和消融的效果[18]。冷融切过程是在低温(40~70°C)状态下使细胞分子链断裂,形成切割、紧缩、止血、焊接作用[19]。近年来射频消融联合椎体成形术广泛应用于脊柱转移肿瘤的治疗,研究报道[20-21]在椎体成形术之前进行射频消融可以减少骨水泥渗漏率以及椎旁和椎体内血管栓塞率。Georgy等[21]认为应用射频消融能够在病变椎体组织形成一个空隙,这个空隙有助于骨水泥的注入并且使骨水泥远离椎体后皮质,在减少骨水泥渗漏的基础上也降低了术中并发症的发生。Schaefer等[22]认为射频消融的热损伤可使血供丰富的椎体内静脉丛形成血栓,防止骨水泥的渗漏。因此,我们认为射频消融在减少椎体成形术中骨水泥渗漏上起到了以下两点作用:a)椎体内射频消融通过毁损椎体内静脉窦及闭塞部分损伤血管,而达到减少椎体成形时骨水泥向血管内渗漏的概率;b)椎体内射频消融可以起到对椎体内组织进行气化减压,使骨水泥注入时压力减小从而降低骨水泥渗漏的概率。在缓解疼痛方面,Mannion等[23]认为射频消融能阻断毁损进入骨膜和骨皮质的邻近传感神经纤维,阻止了疼痛的传导。从VAS评分看术后联合组比对照组低,尽管没有统计学意义,但也说明射频消融后患者疼痛得到一定缓解。因此,我们认为射频消融联合PVP在缓解骨质疏松导致的胸腰椎压缩性骨折疼痛上具有协同作用。
综上所述,结合椎体内射频消融的椎体成形术治疗骨质疏松性椎体压缩骨折,尽管在恢复椎体高度上改善不明显,但其可缓解疼痛,能够降低常规椎体成形术中骨水泥渗漏,特别是椎旁血管渗漏。本研究是回顾性研究,确切的临床疗效还需要进一步前瞻性、多中心、大样本量研究。
参考文献:
[1]吴耀,王峰,周建强,等.经皮椎体成形术和经皮椎体后凸成形术治疗骨质疏松性椎体骨折的临床疗效分析[J].中国骨伤,2014,27(5):385-389.
[2]李自强,杜科伟,杜夏铭,等.椎体成形术与椎体后凸成形术治疗骨质疏松性椎体压缩性骨折发生骨水泥渗漏的相关临床评价[J].解放军医药杂志,2016,28(5):54-58.
[3]余俊喜,吴少坚,鲁培荣,等.椎体成形术和椎体后凸成形术术后骨水泥渗漏的临床观察及分析[J].中国现代药物应用,2017,11(16):66-68.
[4]苏祥正,毛克亚,刘郑生,等.椎体成形术后骨水泥渗漏分析[J].解放军医学院学报,2014,35(10):987-989.
[5]Rapadeo A.General management of vertebralfractures[J].Bone,1996,18(3):191-196.
[6]牛广续,刘振峰,王振斌,等.经皮椎体成形高黏度骨水泥注入修复老年椎体压缩骨折:椎体高度恢复评价[J].中国组织工程研究,2015,19(38):6126-6132.
[7]商澜镨,田耘,刘晓光.聚甲基丙烯酸甲酯与可吸收骨水泥治疗骨质疏松椎体压缩骨折的临床疗效对照研究[J].北京大学学报(医学版),2017,49(2):267-273.
[8]穆小平,易伟林,韦建勋,等.高黏度与普通黏度骨水泥椎体成形系统修复骨质疏松性椎体压缩性骨折的荟萃分析[J].中国组织工程研究,2017,21(2):322-328.
[9]吴先红,丁学铭,刘家素.70例经皮椎体成形术治疗骨质疏松性椎体压缩性骨折的临床体会[J].医学前沿,2015,5(20):49-50.
[10]Habib M,Serhan H,Marchek C,et al.Cement leakage and filling pattern study of low viscous vertebroplastic versus high viscous confidence cement[J].SAS J,2010,4(1):26-33.
[11]罗鹏明,王新虎,左春光.椎体成形和椎体后凸成形术术后骨水泥渗漏的临床观察及分析[J].实用骨科杂志,2014,20(5):398-400.
[12]金桥,沈文.经皮椎体成形、经皮椎体后凸成形灌注骨水泥相关临床应用的再评价[J].中国组织工程研究,2015,19(3):465-471.
[13]章恺,王鸥,荚龙.椎体成形和椎体后凸成形术术后骨水泥渗漏的临床观察及分析[J].实用骨科杂志,2015,21(8):679-682.
[14]Garfin SR,Yuan HA,Reiley MA.New technologies in spine:kyphoplasty and vertebroplastyfor thetreatment of painful osteoporotic compression fractures[J].Spine,2001,26(14):1511-1515.
[15]Mathis JM,Ortiz AO,Zoarski GH.Verlebroplasty versus kyphoplasty:a comparison and contrast[J].AJNR Am J Neuroradiol,2004,25(5):840-845.
[16]Gravius S,Kraska N,Maus U,et al.Intravertebral pressureduring vertebroplasty-an in-vitro study[J].Z Orthop Unfall,2009,147(1):43-47.
[17]杨铁军,周君琳,田庆显,等.球囊二次扩张椎体后凸成形术治疗脊柱压缩性骨折[J].中华骨科杂志,2016,36(2):88-95.
[18]Chen YC,Lee SH,Saenz Y,et al.Histologic findingsof disc,end palate and neural elements after coblation ofnucleus pulposus:an experimental nucleoplasty study[J].Spine J,2003,3(6):466-470.
[19]彭志华,张胜,蔡迎峰,等.等离子射频消融髓核成形术治疗腰椎间盘突出症32例[J].广州医药,2012,43(1):12-14.
[20]张超,王国文,韩秀鑫,等.椎板减压联合射频消融辅助椎体成形术治疗高度恶性肿瘤脊柱转移的临床研究[J].中国肿瘤临床,2014,49(9):585-588.
[21]Georgy BA,Wong W.Plasma-mediated radiofrequency ablation assisted percutaneous cement injection for treating advanced malignant vertebral compression fractures[J].AJNR Am J Neuroradiol,2007,28(4):700-705.
[22]Schaefer O,Lohrmann C,Markmiller M,et al.Technical innovation.Combined treatment of a spinal metastasis with radiofrequency heat ablation and vertebroplasty[J].AJR Am J Roentgenol,2003,180(4):1075-1077.
[23]Mannion RJ,Woolf CJ.Pain mechanisms and management:A central perspective[J].Clin J Pain,2000,16(3):S144-S156.

