MgO用量对其改性ZSM-5结构及其催化甲醇转化制丙烯、丁烯反应性能的影响
桑 宇 ,缪 平 ,邢爱华 *,张妮妮 ,袁德林 ,孙 琦 ,吴玉龙
(1.北京低碳清洁能源研究所,北京 102209;2.北京石油化工学院,北京 102617;3.清华大学,北京 100084)
丙烯、丁烯等低碳烯烃是重要的化工原料,目前主要通过石脑油裂解和炼油厂的副产物得到[1]。石油资源的需求量增长与其资源量储量减少的矛盾突显。在我国以相对丰富的煤炭资源制备低碳烯烃以及在煤制烯烃技术领域取得的突破是缓解石油路线生产烯烃资源短缺的有效途径。甲醇为原料制烯烃,目前工业化了的技术路线主要有MTO工艺(主要生产乙烯和丙烯)和MTP工艺(主要生产丙烯)[2-4]。
ZSM-5分子筛特殊孔道结构 (0.53×0.56nm的10元环直孔道及0.51×0.55nm的10元环Zigzag形孔道)和适宜的酸性能,使其在MTP过程中展现出高的催化活性、产品选择性及较好的稳定性[5]。以ZSM-5分子筛为催化剂在MTP反应中,存在双循环反应机理:烯烃循环,烯烃进行甲基化/裂解反应,丙烯和丁烯主要是按照该路径生成;芳香烃循环,乙烯和芳烃是按照此路径生成。芳烃路线易导致催化剂失活[6]。因此,有效抑制芳香烃循环进行可延长催化剂寿命,提高丙烯与丁烯选择性。ZSM-5分子筛的酸分布不均、较多的强酸性位点等因素都导致ZSM-5分子筛在催化剂甲醇转化反应时芳烃循环比例增加,导致积炭速度加快,降低烯烃选择性,催化剂寿命缩短[7]。因此,适宜的酸强度与酸分布可获得较好的催化性能。
ZSM-5分子筛酸性能与骨架四配位Al的数量、表面和体相分布及在直孔道、正弦孔道或是交叉孔道的落位、水热环境下使用时骨架Al脱除等因素有关。通过分子筛合成直接调节酸性、后处理改性,对催化剂酸性进行调节,从而改善催化性能[8,9]。直接调节法包含调变硅铝比、改变硅源及铝源种类、改变模板剂类型、制备过程中是否加入钠离子、制备过程中直接引入杂原子、或是异晶导向法引入稀土离子(通过采用含稀土的Y分子筛异晶导向作用,引入 Re3+、La3+和 Ce4+);后处理调节包含焙烧,水热处理,化学处理,向分子筛中引入杂原子,晶体外表面外延生长,化学硅沉积,外表面毒化,选择性外表面化学脱铝[10]。采用P元素对ZSM-5分子筛进行改性时,含磷物种通过多种形式与骨架Al相互作用:减少B酸性位点;抑制脱Al、提高骨架Al的水热稳定性[11]。 采用 Ca,Mg 元素改性时,Ca,Mg 主要是通过选择性毒化强酸性位点来调节酸性能;此外,Ca2+,Mg2+形成的水合离子作为平衡骨架负电荷的阳离子出现在骨架Al周围,可抑制脱铝,提高骨架Al的水热稳定性[6,12]。Long等[12]通过等体积浸渍法制备了负载MgO质量分数为0.61%~8.16%的ZSM-5分子筛,发现负载MgO质量分数为0.61%时,强酸性位显著减少;随负载量增加,强酸性位点量持续减少。当负载MgO质量分数达到1.41%~2.92%时,弱酸性位点量达到最大。此外,无论MgO负载量为多少,弱酸与强酸位的强度几乎不变。在蒸气重整二甲醚制H2的反应中,最佳的Mg改性催化剂,具有93%的H2产率,产生碳氢化合物的副反应被明显抑制。因此,通过改变MgO的负载量可有效地调节酸性能,使其适应不同催化反应的需要。
本文采用低温水热晶化法,制备了纳米ZSM-5分子筛团聚体,并改变MgO量,对其进行改性,考察了不同MgO量对ZSM-5分子筛结构、酸性能的影响,并考察了物化性能变化对其催化甲醇转化制丙烯与丁烯(MTPB)反应的影响。
1 实验部分
1.1 纳米ZSM-5分子筛团聚体制备
将质量分数为25%的TPAOH水溶液,氢氧化钠,铝酸钠,30%硅溶胶和水按一定顺序混合,搅拌24h形成凝胶,凝胶中各物质的物质的量比为:100SiO2:Al2O3:10TPAOH:3.8Na2O:1350H2O。 将 老 化24h后的凝胶转移到水热晶化釜中,在125℃及自身压力下动态晶化72h。晶化完成后,将固体产物进行抽滤洗涤,干燥,在空气气氛下以5℃/min升温至300℃焙烧4h,再以5℃/min继续升温至550℃焙烧8h,得到钠型纳米ZSM-5分子筛团聚体。采用0.5M的硝酸铵溶液在80℃下3次离子交换,80℃干燥12h,在空气气氛下400℃焙烧10h,得到氢型纳米ZSM-5分子筛团聚体。样品在530℃下、100%水蒸汽气氛下水热处理17h。样品命名为ZSM-5。
1.2 不同MgO量改性纳米ZSM-5分子筛团聚体制备
将不同量的溶解在10mL水中,将5g氢型纳米ZSM-5分子筛团聚体加入到上述溶液,混合物在80℃搅拌2h。 滴加NH3·H2O,调节pH值到9。MgO改性后的样品在80℃下干燥12h,空气气氛下以5℃/min的速率升温至300℃并保持4h,再以5℃/min的速率升温至550℃,焙烧8h。焙烧后的样品在530℃下、100%水蒸汽气氛下水热处理17h。Mg与Al的物质的量比分别为0.05,0.1和0.2,样品分别命名为5%Mg/Al-ZSM-5,10%Mg/Al-ZSM-5和20%Mg/Al-ZSM-5。
1.3 表征
XRD测试在Bruker公司D8 ADVANCE型X射线衍射仪上进行,Cu Kα射线,工作电压为40kV,工作电流为40mA。
SEM测试在FEI公司Nova NanoSEM 450型扫描电镜仪上进行。
XRF测试在Rigaku公司ZSX PrimusⅡ型X射线荧光仪上进行。
N2物理吸附测试在Micromeritics公司3-FLEX型物理吸附仪上进行。样品在300℃及真空下处理3h。在相对压力为0.007~0.02的范围内使用BET模型计算得到总比表面积(Stotal),使用t-plot方法计算得到微孔体积(Vmicro)和外比表面积(Sexter),采用相对压力为0.99的单点脱附孔体积得到总孔体积(Vtotal),微孔比表面积(Smicro)通过总比表面积减去外比表面积得到,介孔体积(Vmeso)通过总孔体积减去微孔体积得到,使用NLDFT模型计算得到孔径分布(D)。
NH3-TPD测试在Micromeritics公司AutoChemⅡ2920/AutoChem HP 2950型化学吸附仪上进行。0.2g样品在He气氛中550℃下热处理0.5h,然后,降温到100℃,随后,通入φ(NH3)为10%的 NH3-He混合气,样品进行80min的NH3吸附,再用He吹扫20min以去除物理吸附的NH3,最后,在He气氛中以10℃/min速率从100℃升温到600℃进行程序升温NH3脱附。
吡啶吸附的傅里叶转换红外光谱测试在Bruker公司的VERTEX 70型傅里叶转换红外光谱仪及厦门拓斯仪器装备开发有限公司的高真空测试系统上进行。首先,样品在500℃下热处理0.5h。之后,降到室温,吡啶吸附1h,随后,抽真空0.5h。最后,样品在真空环境下分别在100℃、200℃和350℃保持0.5h,图谱在每个温度点都被采集。
1.4 催化性能评价
采用固定床反应器进行MTPB反应,焙烧活化后的分子筛经压片、筛分为20~40目样品,1g分子筛与5g、20~40目的石英砂均匀混合后装入反应器中。反应原料为质量分数80%的甲醇,反应压力为常压,反应温度为480℃,甲醇质量空速为3h-1。
样品在150mL/min的N2气氛中加热到480℃并稳定0.5h,通入甲醇原料。反应产物由Agilent公司7890A型气相色谱进行分析,色谱柱分别为HPPLOT Al2O3/KCl柱 (50m×0.53mm×15μm) 以分离C1-C6碳氢化合物,HP-PLOT Q 柱 (30m×320μm×20μm)以分离醇类和醚类,6'×1/8"Hayesep Q 柱和10'×1/8"13X 分子筛柱以分离 CO,CO2,H2,N2等永久性气体,检测器分别为2台FID检测器和1台TCD检测器。
2 结果与讨论
2.1 XRD表征分子筛物相结构

图1 不同MgO量改性的纳米ZSM-5分子筛团聚体XRD图谱
从XRD图中可以看出,未改性的ZSM-5分别在 7.9o,8.9o,23.1o,23.3o和 23.9o处有五个最强的特征峰,与JCPDS卡No.44-0003相对应,表明生成了MFI结构的ZSM-5。不同MgO量改性后的样品,ZSM-5特征峰的强度依然很高,表明ZSM-5的骨架结构被很好地保留。所有改性的样品,没有MgO的特征峰(42.5o)出现,也没有MgAl2O4等混合氧化物的特征峰存在[12]。毋庸置疑,在550℃的焙烧温度下,镁物种会以MgO的形式存在[13,14]。Mg用量占分子筛中Al原子的5%~20%之间时,MgO高度分散在ZSM-5分子筛中。
2.2 SEM表征分子筛形貌

图2 纳米ZSM-5分子筛团聚体SEM图
从SEM图(图2)中可以看出,ZSM-5颗粒形貌呈现为类球形,是由平均晶粒尺寸约为90nm的小晶粒堆积成的大颗粒,大颗粒尺寸不均匀,平均尺寸约为1.3μm。由于MgO改性量较少,不会影响ZSM-5颗粒的形貌及尺寸特征。
2.3 XRF表征分子筛体相元素
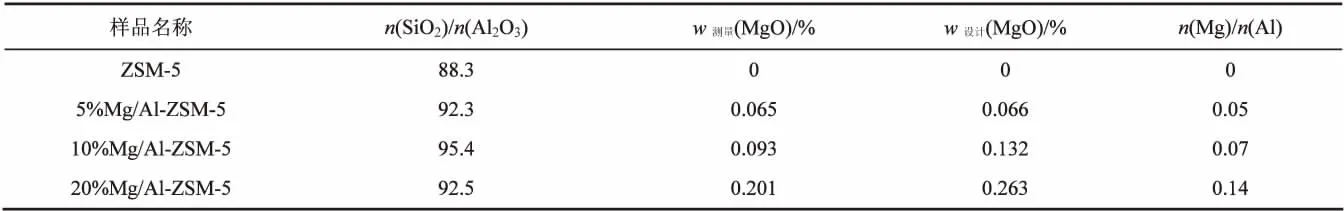
表1 不同MgO量改性样品SiO2/Al2O3物质的量比及MgO含量(XRF)
采用XRF对Mg改性前后的分子筛进行元素组成分析,结果如表所示。Mg改性后分子筛的n(SiO2)/n(Al2O3)略有增加,这可能是由于镁改性的过程中加入Mg(NO3)2溶液后产生酸性环境使分子筛发生轻微脱铝所致。不同镁量改性的样品 (5%Mg/Al-ZSM-5,10%Mg/Al-ZSM-5 和 20%Mg/Al-ZSM-5),w(MgO)分别为0.065%,0.093%和0.201%,比相应的设计值0.066%,0.132%和0.263%都有所减少,且随着镁改性量的增加,测量值与设计值差距越大。此外,n(Mg)/n(Al)分别为 0.05,0.07 和 0.14,比相应的设计值0.05,0.10和0.20随着镁改性量的增加差距增加。这可能是由于随着改性的镁量增加,未进入分子筛微孔孔道、介孔孔道的镁量增加,可能与分子筛没有任何作用的游离Mg2+与氨水作用,生成氢氧化镁,焙烧后形成独立于分子筛的MgO,由于其量较低,XRD检测不到MgO的特征峰。
2.4 N2物理吸附表征分子筛结构参数
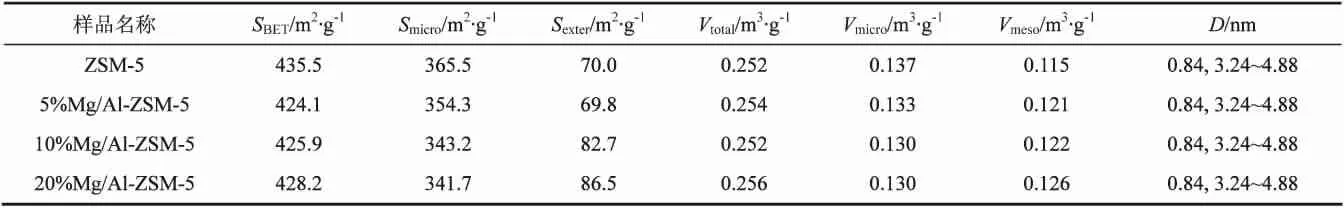
表2 不同MgO量改性ZSM-5分子筛样品的结构参数
从表2给出的结构参数可知,在n(Mg)/n(Al)分别为0.05,0.1和0.2的范围内,镁改性样品的结构参数变化不大,SBET从435.5m2/g减小至424.1m2/g,Vtotal从 0.252cm3/g 增加至 0.256cm3/g;Smicro从365.5m2/g减小至 341.7m2/g,Vmicro从 0.137cm3/g减少至0.130cm3/g,这可能是由于随着Mg(NO3)2溶液浓度的增加,进入分子筛微孔孔道中的Mg2+几率增加,Mg2+形成水合离子在微孔占据的孔体积比H+的水合离子大,导致微孔体积和表面积下降;Smeso从70.0m2/g增加至86.5m2/g,Vmeso从 0.115cm3/g增加至0.126cm3/g,这可能是由于随着Mg(NO3)2溶液浓度的增加,进入ZSM-5分子筛颗粒中由90nm晶粒堆积形成的介孔的镁物种增加,焙烧后生成MgO物种导致介孔孔体积和表面积降低。
2.5 NH3-TPD表征分子筛酸性

图3 不同MgO量改性的纳米ZSM-5分子筛团聚体NH3-TPD图
未改性及不同镁量改性ZSM-5分子筛的酸性表征结果如图3所示。所有样品都具有两个NH3脱附峰,其中158~167℃的低温峰对应的是从弱酸性位点脱附的NH3,312~354℃的高温峰对应的是从强酸性位点脱附的NH3[15]。除5%Mg/Al-ZSM-5的弱酸和强酸中心的强度有所降低外,10%Mg/Al-ZSM-5和20%Mg/Al-ZSM-5的弱酸中心和强酸中心强度与未改性分子筛接近。
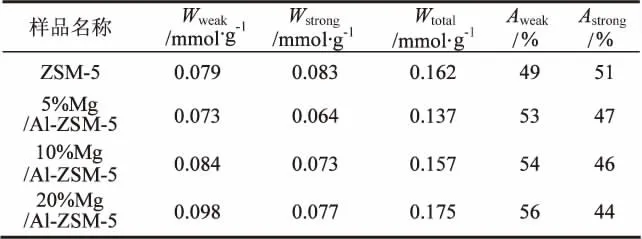
表3 不同MgO量改性样品NH3-TPD酸性
从表3可知,未改性ZSM-5的弱酸及强酸比例都接近50%。镁改性后,随着镁量增加弱酸性位点所占比例增加,而强酸性位点所占比例减少。这与之前的一些关于MgO改性ZSM-5分子筛是减少其强酸性位点的有效方法相一致[16,17]。镁改性样品中弱酸性位点的增加是由于Mg2+取代硅铝桥羟基中的H+形成Mg(OH)+的L酸性位点造成的[18]。
2.6 吡啶红外表征分子筛酸性
在不同温度下,随改性镁用量的变化,分子筛的B酸和L酸量变化规律如图4所示,其中,1540cm-1左右的特征峰归属于吡啶与B酸性位点作用形成的峰,1450cm-1左右的特征峰归属于吡啶与L酸性位点作用形成的峰[19]。100℃时所得的酸量分别是总B酸量及总L酸量,200℃时所得的酸量分别是中强和强B酸量及中强和强L酸量,350℃时所得的酸量分别是强B酸量及强L酸量。
镁改性后ZSM-5分子筛的弱、中等、强L酸量均增加。20%Mg/Al-ZSM-5的弱L酸和强L酸增加最多,且其总L酸量最多。对于中等强度L酸性位增加最多的是10%Mg/Al-ZSM-5。与未改性ZSM-5相比,10%Mg/Al-ZSM-5的总B酸量略有增加,5%Mg/Al-ZSM-5和20%Mg/Al-ZSM-5的总B酸均降低。5%Mg/Al-ZSM-5和10%Mg/Al-ZSM-5的弱B酸和中等B酸位比未改性分子筛略有增加,但强B酸位均少于未改性样品。

图4 不同MgO量改性的纳米ZSM-5分子筛团聚体在(A)100℃,(B)200℃和(C)350℃下的吡啶红外图
2.7 MTPB反应表征分子筛催化性能

图5 甲醇转化率随反应时间的变化规律
甲醇转化率随反应时间的变化规律如图5所示。从图中可以看出,所有样品的初始甲醇转化率都为100%,随着反应的进行甲醇转化率呈下降趋势。未改性的ZSM-5分子筛具有最长的寿命,转化率为99%以上的时间为160h;对于镁改性的样品,随着镁量的增加,寿命先增加后减少,5%Mg/Al-ZSM-5、10%Mg/Al-ZSM-5和 20%Mg/Al-ZSM-5的寿命分别为67h,96h和55h。
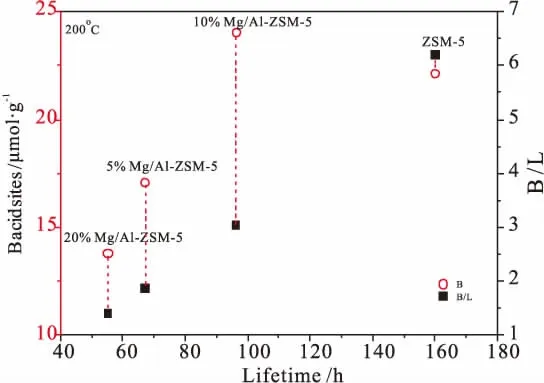
图6 寿命与中等强度以上酸性的对应关系
寿命与200℃吡啶脱附定量的中等以上强度的B酸、B/L酸性关系如图6所示。图中结果表明,与未改性样品相比,除10%Mg/Al-ZSM-5中等以上强度B酸性位增加外,其余两个样品的B酸性均有降低。对MgO改性的样品而言,与5%Mg/Al-ZSM-5与20%Mg/Al-ZSM-5相比,10%Mg/Al-ZSM-5的B酸位最多,故其寿命最长。
与未改性样品相比,尽管10%Mg/Al-ZSM-5的B酸中心高于前者,但其寿命不如前者长。图6中的结果表明,影响分子筛寿命的除了B酸性位的多少外,L酸中心也发挥着作用。当B酸活性位数量接近时,中等强度以上L酸量越少的分子筛寿命越长,即B/L值越高,分子筛寿命越长。

图7 丙烯与丁烯总选择性随反应时间的变化规律
丙烯与丁烯总选择性随反应时间的变化规律如图7所示。从图中可以看出,10%Mg/Al-ZSM-5在转化率为99%以上的时间里都具有最高的丙烯与丁烯总选择性。在反应进行50h之前,5%Mg/Al-ZSM-5与ZSM-5的丙烯与丁烯总选择性接近,但前者在50h以后逐渐降低,而未改性分子筛的产品选择性在相当长的时间内维持稳定。20%Mg/Al-ZSM-5的丙烯与丁烯总选择性随时间延长快速降低。
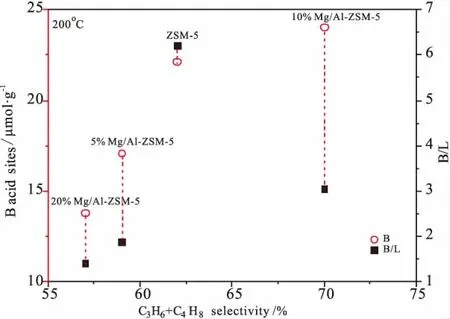
图8 反应进行48h时的丙烯与丁烯总选择性与中等强度以上酸性的对应关系
反应进行48h时,所有样品的转化率都在99%以上,且48h以前丙烯与丁烯总选择性相对平稳,所以选48h的丙烯与丁烯总选择性与中等强度以上酸性进行关联。反应进行48h时,丙烯与丁烯总选择性与200℃吡啶脱附定量的中等强度以上B酸量和B/L的对应关系如图8所示。从图中可以看出,随中强和强B酸量增加,丙烯与丁烯总选择性增加。图8中的结果表明,随着B/L值增加,产品选择性逐渐增加,这是由于其B酸活性中心也同时增加所致;B酸中心进一步增加,B/L值降低,丙烯、丁烯选择性之和进一步增加,结合图4(B)和(C)可知,提高中等强度B酸中心数量有利于提高目标产品选择性。

图9 丙烷选择性随反应时间的变化规律
丙烷选择性随反应时间的变化规律如图9所示。从图中可以看出,镁改性后,样品的丙烷选择性减少,随着镁量的增加,丙烷选择性先增加后减少,20%Mg/Al-ZSM-5的丙烷选择性最低。

表4 在200℃脱附温度下不同MgO量改性样品吡啶红外酸性
从表4中可以看出,镁改性后,L酸量增加。随着分子筛的B/L值增加,丙烷选择性提高。B酸量增加,且B/L值越高,越易于丙烯发生氢转移反应生成丙烷。
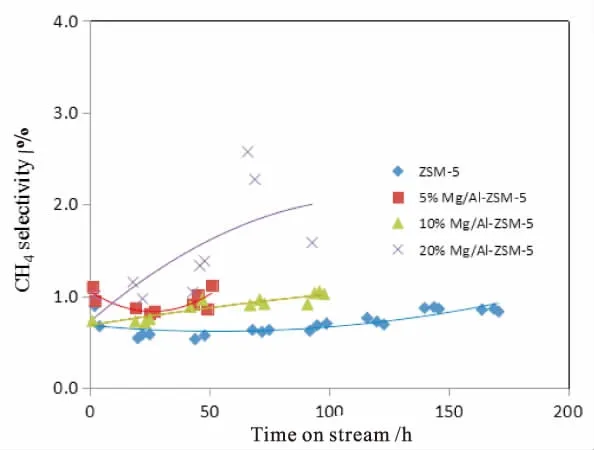
图10 甲烷选择性随反应时间的变化规律
甲烷选择性随反应时间的变化规律如图10所示。从图中可以看出,镁改性后,样品的甲烷选择性增加,甲烷选择性顺序为20%Mg/Al-ZSM-5>5%Mg/Al-ZSM-5>10%Mg/Al-ZSM-5>ZSM-5。 甲烷通过以下三种途径逐渐生成:一是表面甲氧基与甲醇或二甲醚的反应,二是甲醇的甲烷化反应,三是某些芳烃的脱甲基反应[20]。随着反应的进行,催化剂积炭量逐渐增加,芳烃脱甲烷反应趋势增强。

图11 乙烷选择性随反应时间的变化规律
乙烷选择性随反应时间的变化规律如图11所示。从图中可以看出,镁改性后,样品的乙烷选择性增加,乙烷选择性顺序为20%Mg/Al-ZSM-5>5%Mg/Al-ZSM-5>10%Mg/Al-ZSM-5>ZSM-5。 乙烷主要是通过稠环芳香烃等积炭前驱体侧链断裂生成[20],稠环芳烃物种增加会使乙烷选择性提高。

图12 氢气选择性随反应时间的变化规律
氢气选择性随反应时间的变化规律如图12所示。从图中可以看出,镁改性后,样品的氢气选择性增加,氢气选择性顺序为20%Mg/Al-ZSM-5>5%Mg/Al-ZSM-5>10%Mg/Al-ZSM-5>ZSM-5。 氢气主要来源于芳构化反应,芳构化反应增加有利于氢气选择性提高。

表5 改性前后分子筛的B酸和L酸量(吡啶红外表征结果)
从表5中可以看出,吡啶脱附温度为200~350℃对应的是中等强度酸中心,L/B值越大,甲烷,乙烷及氢气的选择性越高。吡啶脱附温度为350℃对应的是强酸中心,L/B越大,甲烷,乙烷及氢气的选择性越高。表明中等强度以上的L酸越多,越有利于脱氢芳构化、甲醇或二甲醚热裂解、芳烃侧链断裂生成甲烷,乙烷等反应。
3 结论
制备了一系列不同镁量改性的纳米ZSM-5分子筛团聚体,探讨了其对结构,酸性能与MTPB催化性能的影响,得到以下结论:
(1)在产品中体相n(Mg)/n(Al)为 0.05~0.14的镁改性量范围内,MgO高度分散在晶型结构较好的由90nm的小晶粒堆积成的平均尺寸约为1.3μm大颗粒的ZSM-5中。
(2)未改性的ZSM-5,弱酸及强酸所占的比例都接近50%。镁改性后,弱酸性位点所占比例增加,而强酸性位点所占比例减少。与未改性ZSM-5相比,镁改性使各个强度的L酸量都有所增加,5%Mg/Al-ZSM-5和10%Mg/Al-ZSM-5的弱B酸和中等强度B酸有所增加,三个Mg改性样品的强B酸量均有所下降。
(3)未改性ZSM-5分子筛同时具有较多中等以上强度B酸位及高B/L特性,其寿命最长;10%Mg/Al-ZSM-5的中等强度B酸中心数量最多,丙烯和丁烯选择性之和最高;中等强度以上L/B酸增加,导致甲烷,乙烷及氢气的选择性增加。
参考文献
[1] Ahmadpour J,Taghizadeh M.Selective production of propylene from methanol over high-silica mesoporous ZSM-5 zeolites treated with NaOH and NaOH/tetrapropylammonium hydroxide [J].Comptes Rendus Chimie,2015,18:834-847.
[2] Losch P,Boltz M,Louis B,et al.Catalyst optimization for enhanced propylene formation in the methanol-to-olefins reaction[J].Comptes Rendus Chimie,2015,18:330-335.
[3] Barros Z S,Zotin F M Z,Henriques C A.Conversion of natural gas to higher valued products:light olefins production from methanol over ZSM-5 zeolites[J].Stud Surf Sci Catal,2007,167(7):255-260.
[4] Yaripour F,Shariatinia Z,Sahebdelfar S,et al.Conventional hydrothermal synthesis of nanostructured H-ZSM-5 catalysts using various templates for light olefins production from methanol[J].JNat Gas Sci Eng,2015,22:260-269.
[5] Yong X J,Du Z P,Li Y,et al.Application status of Lurgi methanol to propylene technology and development of key catalyst[J].Technol Dev Chem Ind,2013,42(9):18-21.
[6] Yarulina I,Bailleul S,Pustovarenko A,et al.Suppression of the aromatic cycle in methanol-to-olefins reaction over ZSM-5 by post-synthetic modification using calcium[J].ChemCatChem,2016,8:3057-3063.
[7] Li H S,He SC,Ma K,et al.Micro-mesoporous composite molecular sieves H-ZSM-5/MCM-41 for methanol dehydration to dimethyl ether:Effect of SiO2/Al2O3 ratio in H-ZSM-5[J].Appl Catal A,2013,450:152-159.
[8] Yokoi T,Mochizuki H,Namba S,et al.Control of the Al distribution in the framework of ZSM-5 zeolite and its evaluation by solid-state NMR technique and catalytic properties[J].JPhys Chem C,2015,119:15303-15315.
[9] Sang Y,Jiao Q Z,Li H S,et al.HZSM-5/MCM-41 composite molecular sieves for the catalytic cracking of endothermic hydrocarbon fuels:nano-ZSM-5 zeolites as the source[J].JNanopart Res,2014,16(12):1-11.
[10] Zhang S L,Gong Y J,Zhang L L,et al.Hydrothermal treatment on ZSM-5 extrudates catalyst for methanol to propylene reaction:Finely tuning the acidic property[J].Fuel Process Technol,2015,129:130-138.
[11] Blasco T,Corma A,Martinez-Triguero J.Hydrothermal stabilization of ZSM-5 catalytic-cracking additives by phosphorus addition[J].JCatal,2006,237:267-277.
[12]Long X,Zhang QJ,Liu Z T,et al.Magnesia modified HZSM-5 as an efficient acidic catalyst for steam reforming of dimethyl ether[J].Appl Catal B,2013,134-135:381-388.
[13] Mao D,Yang W,Xia J,et al.Highly effective hybrid catalyst for the direct synthesis of dimethyl ether from syngas with magnesium oxide-modified HZSM-5 as a dehydration component[J].JCatal,2015,230:140-149.
[14] Mitra B,Kunzru D.Disproportionation of toluene on monoliths washcoated with metal oxide modified ZSM5[J].Catal Lett,2011,141:1569-1579.
[15] Arena F,Dario R,Pamalina A.A characterization study of the surface acidity of solid catalysts by temperature programmed methods[J].Appl Catal A,1998,170:127-137.
[16] Xue B,Li Y,Deng L.Selective synthesis of p-xylene by alkylation of toluene with dimethyl carbonate over MgO-modified MCM-22[J].Catal Commun,2009,10:1609-1614.
[17] Li H,Li M,Chu Y,et al.Influence of different modified βzeolite on skeletal isomerization of n-hexene in the presence of hydrogen[J].Micropor Mesopor Mater,2009,117:635-639.
[18] Li Y G,Xie W H,Yong S.The acidity and catalytic behavior of Mg-ZSM-5 prepared via a solid-state reaction[J].Appl Catal A,1997,150:231-242.
[19]Sang Y,Li H S,Zhu M H,et al.Catalytic performance of metal ion doped MCM-41 for methanol dehydration to dimethyl ether[J].JPorous Mater,2013,20:1509-1518.
[20] 齐国祯,谢在库,钟思青,等.甲醇制烯烃反应副产物的生成规律分析[J].石油与天然气化工,2006,35(1):5-9.

