石英砂介质中CO2水合物形成影响研究
张金华,张 郁,魏 伟
(1.中国石油勘探开发研究院新能源研究所,河北 廊坊 065007;2.中国科学院广州能源研究所,广东 广州 510640)
作为一种温室气体,CO2是全球气候变暖的重要影响因素之一[1]。据统计,与20世纪90年代相比,21世纪初全球CO2排放速率增长了2倍[2],中国的CO2排放也呈现逐年增长的趋势[3],为此,CO2的减排和处理受到了广泛的关注,CO2的分离、捕捉与封存被认为是一种缓解气候变化的重要技术选择[4,5],以固态CO2气体水合物形式储存CO2于深海底部被认为是一种比较安全的方法,对环境保护和经济社会的可持续发展具有重大的现实意义[6]。
CO2气体的地层埋藏是将CO2气体以水合物的形式封存于一定深度的地层沉积物中。海底沉积物和冻土区的土壤都属于多孔介质,因此,需要开展多孔介质中CO2气体水合物的生成影响因素研究。然而,现有的研究主要集中在纯水及盐水体系[7,8],而对多孔介质中CO2水合物生成特性的研究还较少。Brewer等[9]通过现场实地试验,在深海现场观测了液态CO2生成水合物的过程。Komai等[10]研究了CO2及其混合气体水合物在沙质沉积层中晶体生长和生成反应的动力学,并进行了沉积层CO2海洋封存性能的风险评估,认为以水合物形式将CO2大量封存在海洋沉积层中的方案是可行的。Seo等[11]利用热力学测量法与核磁共振(NMR)技术研究了多孔硅胶中CO2水合物的生成过程,结果表明:分散于硅胶中的水与CO2气体非常迅速地发生反应。Kang等[12]实验研究了不同的温压条件下在孔径为100nm的硅胶中CO2水合物生成过程,研究发现CO2气体水合物的生成速率随驱动力的增大而快速增加。Kumar等[13]通过实验研究了多孔介质中CO2水合物的形成和降压分解过程,测定了水合物生成过程中多孔介质的渗透率变化,并通过测定累积气体生成量和时间的关系计算了水合物在降压分解过程中分解速率。张学民等[14]与李金平等[15]主要针对不同孔径与不同粒径的石英砂,开展了CO2水合物储气量等生成特性的研究。此外,国外已经开展了CO2置换甲烷水合物的研究和实践[16-18],利用CO2水合物形成过程产生的热量,促使甲烷水合物发生分解,一方面实现了CO2的地下封存并维持水合物层地质结构的稳定,另一方面又实现了甲烷水合物的开采,为人类提供丰富的天然气能源。
为了进一步了解CO2水合物生成过程中相变特性、生成速率、生成量等方面特征,本文开展了不同粒径石英砂中、不同温度条件下和不同压力条件下的CO2水合物生成动力学研究,分析了CO2水合物在石英砂体系中相态变化、生成速度及诱导时间等特性以及相关影响因素,以期能更深入认识CO2地下固态封存和CO2置换甲烷水合物。
1 实验部分
1.1 实验装置
水合物实验装置主要由供气部分、水合物反应釜、温度控制部分(水浴控温)和数据采集等部分组成(图1)。材质为不锈钢的水合物反应釜为圆柱型,内径4cm,高度6cm,有效容积约50mL,最高工作压力为30MPa。反应釜内布置有温度传感器和压力传感器,分别实时记录反应釜内温度、压力随时间的变化。温度传感器为Pt100铂电阻,测量精度±0.1℃。压力传感器的量程25MPa,精度范围±0.25%。反应釜放置于恒温水浴中,控温范围-10~30℃,控温精度±0.1℃。实验过程中反应釜内的压力以及温度等数据通过数据采集仪采集并由电脑实时记录。

图1 水合物生成实验装置示意图Fig.1 Schematic diagram of hydrate experiment device
1.2 实验样品
二氧化碳气体:佛山华特气体有限公司提供,纯度为99.9%。
石英砂:三种粒径石英砂。粒径为2μm和5μm的石英砂由阿拉丁公司提供;粒径为200μm是石英砂由天津市福晨化学试剂厂提供。
去离子水:自制,由南京超纯水技术有限公司提供的超纯水设备制备,电导率为18.25mΩ/cm。
1.3 实验方法
针对不同初始压力、水合物生成温度以及不同石英砂粒径共开展了11组实验(表1)。
实验步骤:(1)将石英砂样品置于100℃的干燥箱内干燥10h;(2)将干燥后的一定质量的石英砂与去离子水置于烧杯中,石英砂与水的质量比为5:1,充分搅拌,使石英砂和去离子水混合均匀,然后填充到反应釜中,并且压实,所填充的含水石英砂质量为60g;(3)向反应釜内注入1MPa CO2气体,然后放空,反复操作3次,以排出反应釜中的残余空气;(4)将水浴温度设置为15℃,向反应釜内注入CO2气体至反应预设的压力,并关闭阀门;(5)根据实验需要,调节水浴温度,随着温度降低,反应釜压力也随之降低,当温度降到一定值时,反应釜压力急剧下降,表示有水合物生成。通过采集系统采集实验过程中温度和压力的变化;(6)当反应釜压力保持3h不变时,可视为反应结束,停止数据采集。
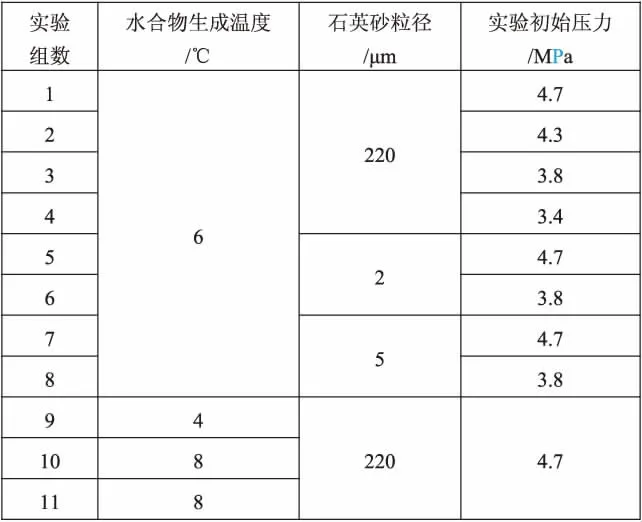
表1 开展的实验组合情况Table 1 Combinations of experiments
2 结果与分析
2.1 初始压力的影响
针对实验初始压力分别为 4.7MPa,4.3MPa,3.8MPa与3.4MPa的4组实验,4组实验的水合物生成温度均为6℃、实验所用石英砂粒径均为220μm,根据实验数据,绘制了不同初始压力下反应釜温度和压力随时间变化趋势(图2)。从图2中可以看出,在实验过程中,随着体系温度的下降,反应釜中压力随之降低。4组实验的体系温度都快速下降至6℃并维持稳定,随着实验的继续,四组实验都出现了反应釜温度急速上升再回落的现象(图2-a),并最终维持在约6℃,同时反应釜压力在降低过程中有一个稳定不变的阶段,并最终都维持在2.5MPa左右(图2-b)。此外,从图2中还可以看出,除初始压力为4.7MPa的实验外,总体表现为初始压力越高,反应釜温度出现急速上升再回落的现象越早,反应釜达到最终压力的耗时也越短。
通过分析,认为出现上述现象的原因及内涵主要体现在以下几个方面:(1)在水合物为生成之前,封闭的反应釜可视为一个定容过程。根据定容过程气体状态方程:P/T=常数,可知,在定容过程中,气体的压力与温度成正比,因此,随着体系温度的降低,反应釜中的压力也将随之降低;(2)在降低过程中压力有一个稳定不变的阶段,这表明水合物在生成过程中有一个明显的诱导时间,并且诱导时间随着初始压力的降低而明显变长(图2-b);(3)伴随压力加速下降出现的反应釜温度急速上升再回落是由于水合物反应放热引起反应釜的温度上升,而随后反应釜的温度在外界水浴控温的作用下开始逐渐的下降并达到稳定;(4)在 4.3MPa,3.8MPa与3.4MPa的实验中,压降幅度越大,对应的温度上升幅度也越大。压力的下降幅度对应了水合物生成量的大小,初始压力越大,压降幅度越大,水合物生成量也越大,因此生成放热越多,温度的上升幅度也越大;(5)对于 4.3MPa,3.8MPa 与 3.4MPa 的实验,当水合物开始生成之后,反应迅速完成,而对于4.7MPa的实验,反应过程较长,压力下降速度呈现多个阶段,并且其温度上升幅度也较小,这是由于该实验中水合物生成速度较慢引起的。

图2 不同初始压力下生成温度为6℃时反应釜温度和压力随时间变化Fig.2 Temperature and pressure changes of reactor with time at forming temperature of 6℃under different initial pressure
针对初始压力为4.7MPa实验中的温度和压力曲线与其它三组实验存在明显差异的现象,进一步分析了反应釜压力随温度变化,及其与CO2液化压力曲线与CO2水合物平衡生成压力曲线的关系(图3)。
在初始压力4.7MPa的实验中,随着温度的下降,压力开始逐渐降低,从A点开始(约15min),压力下降的速度有所增加,究其原因可能是反应釜中从A点开始,CO2气体产生了液化。由于实验中温度测点位于反应釜的正中心,在通过外部水浴降温过程中,反应釜中存在一定的温度滞后性及差异,中心点的温度最高,靠近反应釜釜壁及水浴槽一侧温度较低。从图3中可以看出,A点对应的压力略低于该温度下CO2的液化压力,而此时周围区域的温度可能已经低于对应压力下的液化压力,导致CO2气体发生液化。随着温度与压力的进一步降低,在C点温度开始上升,但升幅度较小,并且随后开始下降到设定的水浴温度,此后压力继续下降,水合物也继续生成。而在初始压力为3.8MPa的实验中,温度在降低到设定温度一段时间后开始上升,温度最大上升到接近相平衡曲线附近,随后压力温度的下降基本上压力相平衡去曲线进行。这表明水合物的生成速度较快,反应生成热量来不及释放,因而反应的速度受到平衡生成压力的限制。此外,从图3中也可以看出,当温度压力降低相平衡点(如B点)时,CO2并不是马上形成水合物,显示出需要一个诱导作用和时间的过程。

图3 不同初始压力下生成温度为6℃时反应釜压力随温度变化曲线Fig.3 Pressure change of reactor with temperature at forming temperature of 6℃under different initial pressure
综合认为,对于4.7MPa下温度压力曲线差异及水合物生成速度较慢可能有以下几个原因:(1)在较高的初始压力下,水合物生成的诱导时间较短,水合物生成时的过冷度较低,因而开始时生成速度也较低;(2)在较高的初始生成压力下,水合物总的生成量较多,可能会影响后期生成过程气体的扩散过程并降低气-液反应面积;(3)CO2的液化可能会影响水合物的生成反应速度,这需要进一步的进行研究。
2.2 温度的影响
针对水合物生成温度分别为8℃,6℃与4℃的4组实验(其中8℃的实验进行了两次;四组实验初始压力均为4.7MPa;实验所用石英砂粒径均为220μm),进行了生成温度对CO2水合物形成的影响分析。根据实验数据,绘制了不同生成温度下的压力和反应釜温度随时间的变化趋势(图4)。从图4-a中可以看出,水合物生成温度越低,反应釜中最终压力也越低,压降幅度也越大,总生成时间也明显变长。这是因为水合物的最终生成量受到平衡生成压力的限制,在较低的温度下,水合物的生成压力也较低,压降幅度也越大,总生成量也越大。在较低的温度下,总体生成速度较慢,可能是由于相对多的水合物生成后,降低了气体扩散到生成界面的速度引起的。此外,从图4-a和图4-b中可以看出,两次生成温度均为8℃的实验,其压力和反应釜温度随时间的变化曲线都具有较好的重合性,这表明CO2水合物在多孔介质中的生成过程具有较好的可重复性。
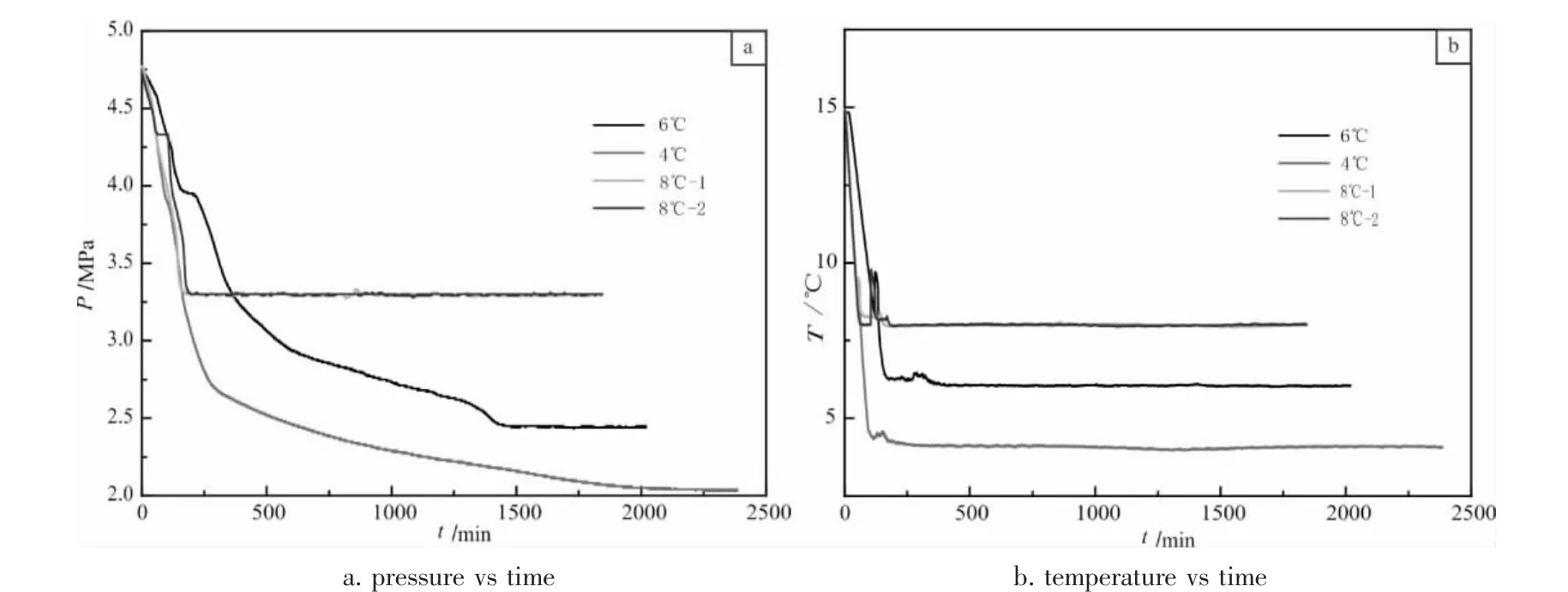
图4 初始压力4.7MPa时不同生成温度下反应釜压力和温度随时间的变化曲线图Fig.4 Temperature and pressure changes of reactor with time under 4.7MPa and different forming temperature
2.3 粒径的影响
针对水合物生成温度为6℃时,实验初始压力分别为4.7MPa和3.8MPa,石英砂粒径分别为220μm、5μm和2μm的6组实验,进行了石英砂粒径对CO2水合物形成的影响分析。根据实验数据,绘制了生成温度6℃时,各自初始压力下,不同粒径下反应釜内的压力和温度随时间变化的趋势 (图5)。
从图5-a中可以看出,在初始压力为4.7MPa时,不同粒径的石英砂体系下,CO2水合物的生成诱导时间均不明显。在2μm与5μm的石英砂中,水合物生成速度很快,压力与温度的变化趋势较为接近;而在220μm的石英砂中,水合物的生成速度明显变慢,体系温度上升幅度也较小。此外,不同粒径下的最终稳定压力基本相同,显示最终水合物生成量相同,这表明水合物的最终生成量不受石英砂粒径大小的影响。
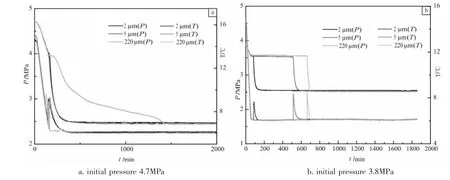
图5 生成温度6℃时不同粒径下反应釜压力随时间变化Fig.5 Pressure changes of reactor with time at forming temperature of 6℃under different particle sizes
对比图5-a和图5-b可以看出,随着初始压力的减小,不同石英砂粒径下的实验诱导时间均明显变长;同时从图5-b中可以看出,诱导时间随着粒径的增大也呈现出明显的增加。造成这种现象的原因可能是由于随着石英砂粒径的减小,总的比表面积增大,水合物更容易成核,从而更易形成水合物。此外,在初始压力3.8MPa时,不同石英砂粒径下的实验最终稳定压力也基本相同,显示出最终水合物生成量基本相同,这也进一步表明了水合物的最终生成量不受石英砂粒径大小的影响。
3 结论
通过实验研究石英砂粒径分别为220μm、5μm和 2μm,实验初始压力范围为 3.4MPa、3.8MPa、4.3MPa和4.7MPa,以及水合物生成温度分别为4℃、6℃和8℃体系中CO2水合物的生成特性,得出以下结论:
(1)除了在较高的实验初始压力(如4.7MPa)下,CO2在生成水合物前存在液化现象,并可能是造成较高的实验初始压力下水合物平均生成速度较慢的原因之一。通常,随着初始实验压力降低、水合物生成温度降低和石英砂粒径增大,水合物平均生成速度变慢。
(2)水合物的生成量主要受到水合物平衡压力大小的制约,随着实验初始压力的增大与生成温度的降低而增大,基本不受石英砂粒径的影响。
(3)除了在较高的初始压力下水合物生成诱导时间不明显外,水合物在生成过程中的诱导时间均较为明显,并且诱导时间随着初始压力的降低和石英砂粒径的增加而明显变长,而生成温度对诱导时间的影响不是很明显。
参考文献
[1] Hasrelmann K,Latif M,Hooss G,et al.The challenge of long-term climate change [J].Science,2003,302:1923-1925.
[2] Vries G J,Ferrarini B.What accounts for the growth of carbon dioxide emissions in advanced and emerging economies:The role of consumption,technology and global supply chain participation[J].Ecological Economics,2017,132:213-223.
[3] Du K R,Xie C P,Ouyang X L.A comparison of carbon dioxide (CO2)emission trends among provinces in China[J].Renewable Sustainable Energy Rev,2017,73:19-25.
[4] Ramos A D,Singh B,Zhang X,et al.Global warming footprint of the electrochemical reduction of carbon dioxide to formate [J].J Cleaner Prod,2015,104:148-155.
[5] 孙始财,魏伟,丛晓春,等.水合物法分离回收烟气二氧化碳研究进展 [J].天然气化工—C1化学与化工,2010,35(2):71-74.
[6] Austvik T,Loken K P.Deposition of CO2on the seabed in the form of hydrates [J].Energy Convers Manage,1992,33:659-666.
[7] 轩小波,刘妮,李菊,等.影响二氧化碳水合物生成特性的实验研究[J].天然气化工—C1化学与化工,2011,36(2):10-13.
[8] 叶鹏,刘道平,时竞竞.二氧化碳水合物生成驱动力的研究[J].天然气化工—C1化学与化工,2013,38(2):38-41.
[9] Brewer P G,Friederich G,Peltzer E T,et al.Direct experiments on the ocean disposal of fossil fuel CO2[J].Science,1999,284:943-945.
[10]Komai T,Sakamoto Y,Kawamura T,et al.Formation kinetics of CO2gas hydrates in sandy sediment and change in permeability during crystal growth[C]//Proc 6th International Conference on Gas Hydrates,Vancouver,2008.
[11]Seo Y T,Moudrakovski I L,Ripmmeester J A,et al.Efficient recovery of CO2from flue gas by clathrate hydrate formation in porous silica gel [J].Environ Sci Technol,2005,39:2315-2319.
[12]Kang S P,Lee J W.Kinetic behavior of CO2hydrates in porous media and effect of kinetic promoter on the formation kinetics [J].Chem Eng Sci,2010,65:1840-1845.
[13]Kumar A,Maini B,Bishnoi P R,et al.Experimental determination of permeability in the presence of hydrates and its effect on the dissociation characteristics of gas hydrates in porous media [J].JPetrol Sci Eng,2010,70:114-122.
[14]张学民,李金平,吴青柏,等.孔隙介质中二氧化碳水合物生成过程实验研究 [J].应用基础与工程科学学报,2016,24(1):168-175.
[15]李金平,焦亮,张学民,等.石英砂孔径介质中二氧化碳水合物生成过程研究[J].甘肃科学学报,2015,27(1):82-85.
[16]The Ignik Sikumi Gas Hydrate Exchange Trial Project Team.Ignik Sikumi gas hydrate field trial completed[J].Fire in the Ice,2012,12(1):1-3.
[17]Ota M,Abe Y,Morohashi K,et al.Methane recovery from methane hydrate using pressurized CO2[J].Fluid Phase Equilibria,2005,228-229:553-559.
[18]Ota M,Morohashi K,Abe Y,et al.Replacement of CH4in the hydrate by use of liquid CO2[J].Energy Convers Manage,2005,46:1680-1691.

