急性缺血性脑卒中阿替普酶静脉溶栓相关并发症的临床研究进展
石宝洋, 靳 航综述, 杨 弋审校
脑卒中已跃升至人类的第二大死亡原因,其高发病率、高致残率、高死亡率以及高复发率给家庭、社会及国家带来了沉重的负担。70%~80%的脑卒中为缺血性脑卒中。“时间就是大脑”的治疗观念已得到大多数学者的认可,因此早期治疗、尽早开通梗死相关血管是缺血性脑卒中超急性期的最重要治疗原则,阿替普酶静脉溶栓治疗是临床上治疗急性缺血性脑卒中的里程碑,它为早期开通梗死相关血管提供了可能,在其被批准用于急性缺血性脑卒中临床治疗20余年里,在急性缺血性脑卒中治疗中发挥了不可替代的作用。被国内外众多临床指南高级别推荐。但随着其长期、广泛运用,不可避免地带来了带来了一些并发症,个别并发症甚至影响患者的康复及预后。熟知各种并发症及其危险因素、临床表现、预防与治疗等对预防并发症的发生、尽早识别并及时处理、降低并发症给患者带来的危害等至关重要。因此本文将急性缺血性脑卒中阿替普酶静脉溶栓相关并发症综述如下。
1 过敏反应
阿替普酶治疗急性心肌梗死的过敏反应发生率约为0.02%,然而,在急性脑梗死阿替普酶静脉溶栓中,过敏反应相对更为常见,其发生率为0.89%~5.88%[1~4]。1997年,Pancioli等[5]第一次报道了1例急性脑梗死患者阿替普酶静脉溶栓后瘫痪侧口咽及舌部水肿的病例,病情迅速进展,1 h后双侧舌咽部水肿,口舌部水肿甚至占据整个口腔,造成上呼吸道梗阻。有学者回顾性分析了105例接受阿替普酶静脉溶栓的患者,其中有2例患者(1.9%)出现了过敏反应。除舌咽部血管性水肿之外,尚有文献报道过敏患者表现为皮疹、荨麻疹、窦性心动过速、支气管痉挛、低血压、休克等。
Hill等[3]前瞻性地研究了1996~2001年期间176例接受阿替普酶静脉溶栓的患者,分别于给药后45 min、60 min、75 min及24 h仔细检查患者口、唇及咽部,结果显示,9例患者(5.1%)发生舌咽部血管性水肿,溶栓前服用ACEI类药物史可增加舌咽部血管性水肿的发生风险(相对风险13.6),CT上显示岛叶或额叶梗死灶也是舌咽部血管性水肿的危险因素(相对风险 9.1)。然而,Pinho等的研究表明女性及既往服用ACEI类药物是舌咽部血管性水肿的独立危险因素,而溶栓前CT上显示的岛叶早期梗死征象与舌咽部血管性水肿无显著关系。
一旦发现过敏现象,特别是出现致命性过敏反应如喉头水肿、低血压、休克等,应立即终止阿替普酶输注,监测生命体征及过敏症状的动态变化,并可根据病情适当运用抗组胺药物、糖皮质激素、肾上腺素等,必要时采取相应生命支持技术。
2 出 血
2.1 颅内出血 溶栓后出血转化(hemorrhage transformation,HT)一般指缺血性脑卒中经溶栓治疗后出现的颅内出血性病变。根据出血转化在CT上位置及占位效应的不同将其分为如下类型:如图1所示:(1)出血性梗死1型(hemorrhagic infraction 1,HI1):梗死边缘的小斑点状出血灶;(2)出血性梗死2型(hemorrhagic infraction 2,HI2):梗死区域内部融合成片的出血,但无占位效应;(3)脑实质出血1型(parenchymal hemorrhage 1,PH1):血肿体积≤梗死体积30%,伴轻微占位效应;(4)脑实质出血2型(parenchymal hemorrhage 2,PH2):血肿体积>梗死体积30%,伴明显占位效应。根据有无神经功能减退可分为症状性颅内出血(symptomatic intracranial hemorrhage,sICH)和非症状性颅内出血(asymptomatic intracranial hemorrhage,aICH)。sICH是指伴有神经功能减退的HT,其在不同临床研究中的具体定义见表1。一项研究分别分析了脑实质型颅内出血,NINDS、 ECASSⅡ和SITS-MOST研究定义的sICH,结果表明,ECASSⅡ和SITS-MOST这两个研究中定义的sICH能更好地识别与不良预后相关的sICH。
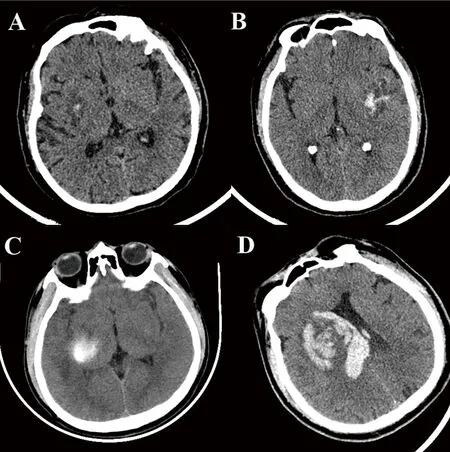
A:HI1;B:HI2;C:PH1;D:PH2
不同的定义、特定的研究人群及研究方案的差异等,使不同研究中sICH的发生率差异很大,数据显示,其发生率波动在1.7%~8.8%之间[6~9],是导致患者神经功能恶化甚至死亡的主要原因。在NINDS研究[6]中,阿替普酶静脉溶栓后sICH的发生率为6.4%,而对照组为0.6%;与对照组相比,阿替普酶组能提高患者约30%的良好预后率,且3 m后的死亡率低于对照组(17% vs 21%,但无统计学差异)。这一研究结果促成了美国食品与药物管理局批准阿替普酶用于治疗急性缺血性脑卒中。ECASSⅡ研究[7]发现,阿替普酶组与对照组相比,两组3 m后mRS评分在0~2分的比例分别为54.3%、46%(P=0.024),两组sICH的发生率分别为8.8%和3.4%,两组之间的死亡率无显著差异。关于溶栓后sICH发生率及死亡率的研究结果见表2。

表1 不同临床研究中sICH的定义
*PH2型脑出血即脑实质出血2型:血肿体积>梗死体积30%,伴明显占位效应

表2 不同临床研究的基本信息、sICH率、死亡率
a:NINDS中sICH的诊断标准,即36 h内的伴有临床上任何可疑的脑出血症状或任何程度的神经功能减退的CT提示的脑出血;b:ECASSⅡ中sICH的诊断标准,即静脉溶栓7 d内出现的伴有NIHSS评分增加≥4分的CT显示的颅内出血;c:ATLANTIS中sICH的诊断标准未明确给出;d:DEFUSE中sICH的诊断标准,即静脉溶栓36 h内出现的且同时NIHSS评分增加≥2分的CT/MR显示的颅内出血;e:STARS中sICH的诊断标准未明确给出;f:CASES中sICH的诊断标准,即24 h之内出现的伴有任何程度神经功能减退的颅内出血;g:EPITHET中sICH采用SITS-MOST的诊断标准,即36 h内出现的且同时NIHSS评分增加≥4分的PH2型颅内出血;h:GWTG中sICH的诊断标准未明确给出;i:90 d后的死亡率;j:30 d后的死亡率;k:住院期间的死亡率
Mokin等[17]回顾性分析了接受静脉溶栓的267例患者,发现17例(6.3%)患者出现了sICH,从注射阿替普酶至诊断sICH的中位数时间是5 h 28 min(最短1 h 26 min,最长23 h 24 min);另有一项研究[18]表明大部分sICH发生在静脉溶栓后24 h之内,10%~15%的sICH可发生于24 h之后。因此,静脉溶栓后,特别是24 h内应密切监测患者神经功能及生命体征的变化。
识别sICH的危险因素能为评估患者溶栓风险提供科学的依据,有助于探索sICH发生的潜在机制,能为降低sICH发生提供相应治疗措施,还可以为后续相关试验设计提供思路。Whiteley等[19]分析了55个研究共计65264例急性脑梗死患者的43个变量,结果表明高龄、卒中严重程度、高血糖是sICH的独立危险因素,其中心房纤颤病史、心力衰竭病史、肾功能不全病史、既往服用抗血小板药物、脑白质疏松、溶栓前CT显示早期梗死征象增加约1倍的sICH发生率。多个研究表明年龄是sICH的预测因子[20,21]。在NINDS研究[21]中,基线NIHSS评分>20分的患者出现sICH的概率是NIHSS评分≤5分患者的11倍。既往有糖尿病病史或基线较高的血糖水平是sICH的独立危险因素[22~24]。Gilligan等研究认为基线高收缩压是sICH的独立危险因素,但另外一项研究表明高血压仅在单因素分析中与sICH相关[23]。既往心脏病病史,尤其是心房纤颤及心力衰竭,是sICH的危险因素[20,22,23]。有研究表明发病3~4.5 h接受静脉溶栓的患者sICH的发生率显著高于发病3 h之内用药者[25]。血小板计数偏低可能是sICH的独立危险因素[23,24]。关于抗血小板药物的应用仅在单因素分析中与sICH相关[23]。多个研究发现,头部CT平扫显示早期梗死征象增加溶栓后出血转化的风险。Tsivgoulis等[26]发现溶栓前核磁显示脑微出血是sICH的独立危险因素。基于sICH 危险因素的研究,临床上有很多预测sICH的量表,量表主要内容及其对sICH的预测价值见表3。

表3 各种预测sICH量表的内容及预测价值
溶栓后出血转化的治疗原则大致同自发性脑出血,包括必要时的呼吸和循环支持,监测生命体征及神经功能缺损的动态变化,卧床休息,避免剧烈运动及情绪激动,控制血压及颅内压,预防血肿扩大以及并发症的处理等。如患者有潜在的出血转化风险,则应立即停止溶栓治疗并行头CT检查,如头CT证实发生了颅内出血,因阿替普酶的半衰期短,对凝血系统的影响较小,故大多数颅内出血可经停止溶栓、抗凝、抗血小板药物等保守措施控制出血,少数未能得到有效控制者可输注血制品,包括冷沉淀、新鲜冰冻血浆和血小板等,必要时采取外科手术治疗。
2.2 其他部位出血 常见的其他部位出血包括口腔、鼻粘膜、胃肠道、泌尿道、注射部位等的出血,浅表部位的出血多在压迫止血后即可得到控制;尚有文献报道一些少见部位的出血,如硬膜外出血、脾脏破裂出血、甲状腺出血、腹壁肌肉层血肿。因此静脉溶栓后应密切关注患者病情变化,监测生命体征,定期复查血常规、凝血常规,早期发现、早期干预治疗出血并发症。
3 血栓栓塞性事件
急性心肌梗死后静脉溶栓治疗可造成潜在的血栓破碎并继发其他系统或器官的栓塞,据此推测,急性脑梗死患者静脉溶栓后也可出现类似现象。Garg等[27]报道了1例患者,在阿替普酶静脉溶栓结束之后出现瘫痪对侧肢体的无力,CTA发现相关责任血管闭塞,复查心脏彩超发现在溶栓过程中发现的左心室血栓消失;另外有文献报道2例患者静脉溶栓后发生包括肾脏血管和脑血管在内的多系统栓塞[28]。目前关于血栓栓塞的研究较少,有研究表明静脉溶栓后血栓栓塞事件的发生与原有心脏血栓的破碎移位有关[29],但Derex等的研究未证实两者之间的关系[30]。
4 癫 痫
Rodan等[31]报道了3例既往无癫痫病史的重症卒中患者在阿替普酶静脉溶栓过程中出现癫痫发作,Hafeez等[32]报道了1例患者在静脉滴注阿替普酶20 min时出现癫痫的病例,同时,有研究表明缺血性卒中48 h内约有2%的患者出现癫痫发作。静脉溶栓后癫痫的发生与阿替普酶的关系尚不明确。卒中静脉溶栓后癫痫的可能机制有:(1)再灌注癫痫;(2)阿替普酶的某些特性所致;(3)溶栓过程中继发皮质梗死;(4)、卒中后癫痫,正巧发生在溶栓之后[31]。
5 小结与展望
虽然多数与阿替普酶静脉溶栓的过敏反应是轻微的,但仍有过敏性休克、舌咽部血管性水肿致上呼吸道梗阻等可能威胁生命安全的过敏反应,因此应给予高度重视,据以往的观察研究,发生过敏反应的患者中有相当比例的患者同时服用ACEI类药物,其发生机制及治疗措施仍需大样本的研究;症状性颅内出血是阿替普酶静脉溶栓治疗的严重并发症之一,其机制尚不明确,目前推测可能与凝血功能紊乱、再灌注损伤及血脑屏障的破坏等相关;关于sICH的危险因素及预测量表的研究有很多,但目前的量表预测价值有限;在治疗方面,纠正应用阿替普酶后紊乱的凝血功能是主要的措施,但仍然缺乏特异的治疗方法。目前只有很少的个案报道与阿替普酶静脉溶栓相关的血栓栓塞及癫痫的发生,其发生率、发生机制及治疗等需要进一步深入的研究。
[参考文献]
[1]Yayan J. Lingual angioedema with macroglossia during the treatment of acute ischemic stroke with alteplase[J]. Int J Gen Med,2012,5(7):183-186.
[2]Ottomeyer C,Sick C,Hennerici MG,et al. Orolingual angioedema under systemic thrombolysis with rt-PA:an underestimated side effect[J]. Der Nervenarzt,2009,80(4):459-463.
[3]Hill M,Lye T,Moss H,et al. Hemi-orolingual angioedema and ACE inhibition after alteplase treatment of stroke[J]. Neurology,2003,60(9):1525-1527.
[4]Lin S,Tang S,Tsai L,et al. Orolingual angioedema after alteplase therapy of acute ischaemic stroke:incidence and risk of prior angiotensin-converting enzyme inhibitor use[J]. Eur J Neurol,2014,21(10):1285-1291.
[5]Pancioli A,Brott T,Donaldson V,et al. Asymmetric angioneurotic edema associated with thrombolysis for acute stroke[J]. Ann Emerg Med,1997,30(2):227-229.
[6]The national institute of neurological disorders and stroke t-PA stroke study group. Tissue plasminogen activator for acute ischemic stroke[J]. N Engl J Med,1995,333(24):1581-1587.
[7]Hacke W,Kaste M,Fieschi C,et al. Randomised double-blind placebo-controlled trial of thrombolytic therapy with intravenous alteplase in acute ischaemic stroke (ECASS Ⅱ)[J]. Lancet,1998,352(9136):1245-1251.
[8]Wahlgren N,Ahmed N,Dávalos A,et al. Thrombolysis with alteplase for acute ischaemic stroke in the Safe Implementation of Thrombolysis in Stroke-Monitoring Study (SITS-MOST):an observational study[J]. Lancet,2007,369(9558):275-282.
[9]Albers GW,Thijs VN,Wechsler L,et al. Magnetic resonance imaging profiles predict clinical response to early reperfusion:the diffusion and perfusion imaging evaluation for understanding stroke evolution (DEFUSE) study[J]. Ann Neurol,2006,60(5):508-517.
[10]Sandercock P,Lindley R,Wardlaw J,et al. The third international stroke trial (IST-3) of thrombolysis for acute ischaemic stroke[J]. Trials,2008,18(9):17-37.
[11]Clark WM,Wissman S,Albers GW,et al. Recombinant tissue-type plasminogen activator (alteplase) for ischemic stroke 3 to 5 hours after symptom onset. The ATLANTIS Study:a randomized controlled trial[J]. JAMA,1999,282(21):2019-2026.
[12]Albers GW,Bates VE,Clark WM,et al. Intravenous tissue type plasminogen activator for treatment of acute stroke:the Standard Treatment with Alteplase to Reverse Stroke (STARS) Study[J]. JAMA,2000,283(9):1145-1150.
[13]Hill MD,Buchan AM. Thrombolysis for acute ischemic stroke:results of the Canadian Alteplase for Stroke Effectiveness Study[J]. CMAJ,2005,172(10):1307-1312.
[14]Davis SM,Donnan GA,Parsons MW,et al. Effects of alteplase beyond 3 h after stroke in the Echoplanar Imaging Thrombolytic Evaluation Trial (EPITHET):a placebo-controlled randomised trial[J]. Lancet Neurol,2008,7(4):299-309.
[15]Ahmed N,Grond M,Hennerici M,et al. Implementation and outcome of thrombolysis with alteplase 3~4.5 h after an acute stroke:an updated analysis from SITS-ISTR[J]. Lancet Neurol,2010,9(9):866-874.
[16]Fonarow GC,Smith EE,Saver JL,et al. Timeliness of tissue-type plasminogen activator therapy in acute ischemic stroke:patient characteristics,hospital factors,and outcomes associated with door-to-needle times within 60 minutes[J]. Circulation,2011,123(7):750-758.
[17]Mokin M,Kass-Hout T,Kass-Hout O,et al. Blood pressure management and evolution of thrombolysis-associated intracerebral hemorrhage in acute ischemic stroke[J]. J Stroke Cerebrovasc Dis,2012,21(8):852-859.
[18]Strbian D,Sairanen T,Meretoja A,et al. Patient outcomes from symptomatic intracerebral hemorrhage after stroke thrombolysis[J]. Neurology,2011,77(4):341-348.
[19]Whiteley WN,Slot KB,Fernandes P,et al. Risk factors for intracranial hemorrhage in acute ischemic stroke patients treated with recombinant tissue plasminogen activator:a systematic review and meta-analysis of 55 studies[J]. Stroke,2012,43(11):2904-2909.
[20]Larrue V,Kummer R,Müller A,et al. Risk Factors for severe hemorrhagic transformation in ischemic stroke patients treated with recombinant tissue plasminogen activator:a secondary analysis of the European-Australasian Acute Stroke Study(ECASS Ⅱ)[J]. Stroke,2001,32(2):438-441.
[21]The National Institute of Neurological Disorders and Stroke rt-PA Stroke Study Group. Intracerebral hemorrhage after intravenous t-PA therapy for ischemic stroke[J]. Stroke,1997,28(11):2109-2118.
[22]Jaillard A,Cornu C,Durieux A,et al. Hemorrhagic transformation in acute ischemic stroke:the MAST-E study[J]. Stroke,1999,30(7):1326-1332.
[23]Tanne D,Kasner SE,Demchuk AM,et al. Markers of increased risk of intracerebral hemorrhage after intravenous recombinant tissue plasminogen activator therapy for acute ischemic stroke in clinical practice:the multicenter rt-PA acute stroke survey[J]. Circulation,2002,105(14):1679-1685.
[24]Kase CS,Furlan AJ,Wechsler LR,et al. Cerebral hemorrhage after intra-arterial thrombolysis for ischemic stroke:The PROACT Ⅱ trial[J]. Neurology,2001,57(9):1603-1610.
[25]Hacke W,Kaste M,Bluhmki E,et al. Thrombolysis with Alteplase 3 to 4.5 Hours After Acute Ischemic Stroke[J]. J Vasc Surg,2008,48(6):1634-1635.
[26]Tsivgoulis G,Zand R,Katsanos AH,et al. Risk of symptomatic intracerebral hemorrhage after intravenous thrombolysis in patients with acute ischemic stroke and high cerebral microbleed burden:a meta-analysis[J]. JAMA Neurol,2016,73(6):675-683.
[27]Garg A,Yaduvanshi A,Mohindra KD. Cardioembolic stroke on unaffected side during thrombolysis for acute ischemic stroke[J]. Neurol India,2010,58(1):112-114.
[28]Georgiadis D,Engelter S,Tettenborn B,et al. Early recurrent ischemic stroke in stroke patients undergoing intravenous thrombolysis[J]. Circulation,2006,114(3):237-241.
[29]Stafford P,Strachan C,Vincent R,et al. Multiple microemboli after disintegration of clot during thrombolysis for acute myocardial infarction[J]. BMJ,1989,299(6711):1310-1312.
[30]Derex L,Nighoghossian N,Perinetti M,et al. Thrombolytic therapy in acute ischemic stroke patients with cardiac thrombus[J]. Neurology,2001,57(12):2122-2127.
[31]Rodan LH,Aviv R,Sahlas M,et al. Seizures during stroke thrombolysis heralding dramatic neurologic recovery[J]. Neurology,2006,67(4):2048-2049.
[32]Hafeez F,Razzaq MA,Levine RL,et al. Reperfusion seizures:a manifestation of cerebral reperfusion injury after administration of recombinant tissue plasminogen activator for acute ischemic stroke[J]. J Stroke Cerebrovasc Diseases,2007,16(6):273-277.

