死腔分数对急性呼吸窘迫综合征预后的评估价值*
徐 冕,杨德兴,颜悦新,刘桠名,周凤高,许 成,刘 荣△
(1.昆明医科大学第一附属医院急诊重症监护室,昆明 650032;2.云南省第一人民医院急诊科,昆明 650034)
急性呼吸窘迫综合征(ARDS)是多器官功能障碍综合征发生时最早受累或最易出现的脏器功能障碍表现。ARDS起病隐匿,进展迅速,病死率高达40%~50%[1-3],弥漫性肺泡损伤是其特征性病理改变。目前尚无有效的指标可用来判断ARDS患者的预后[4]。研究发现,ARDS后期死腔率高达60%,明显增高的死腔分数(VD/VT)为ARDS患者病死率的独立预测因子,应常规监测死腔VD/VT以便进行亚组分析[5]。本研究对ARDS患者VD/VT的动态变化及其预后评估的作用进行分析,现报道如下。
1 资料与方法
1.1一般资料 选择2015年1月至2016年8月昆明医科大学第一附属医院急诊重症监护室(EICU)的ARDS患者32例纳入研究。纳入标准:年龄大于或等于18岁,符合柏林定义诊断标准[6]的有创机械通气患者。排除标准:年龄小于18岁;有急性心力衰竭、妊娠、肺栓塞、慢性阻塞性肺疾病、肺叶切除;不接受机械通气及积极药物治疗。根据28 d生存情况分存活组和死亡组。
1.2方法
1.2.1基本情况收集 收集两组患者年龄、性别、ARDS病因、急性生理和慢性健康评分(APACHEⅡ)和肺损伤预测评分(LIPS)等,随访患者入EICU 28 d病死率。
1.2.2VD/VT的监测 患者镇痛镇静状态下,利用飞利浦MP20多参数监护仪监测呼吸末CO2分压(ETCO2),并抽取动静脉血气分析,依据公式VD/VT=0.320 0+0.010 6[动脉血二氧化碳分压(PaCO2)-ETCO2]+0.003 0呼吸频率(RR)+0.001 5年龄(Age)[7]计算VD/VT。自入EICU起连续监测6 d,同时记录并比较两组氧合指数(PaO2/FiO2)、呼气未正压(PEEP)、平台压、乳酸等。
2 结 果
2.1存活组和死亡组基本情况 共32例ARDS患者纳入研究,死亡10例,病死率31.25%。死亡组和存活组LIPS和APACHEⅡ比较差异有统计学意义(P<0.05),其余指标比较差异均无统计学意义(P>0.05),见表1。
2.2VD/VT不同时相点比较 1~6 d VD/VT死亡组逐渐增高,存活组变化趋势比较差异无统计学意义(P>0.05)。1~3 d VD/VT两组间比较差异无统计学意义,而4~6 d死亡组明显高于存活组(P<0.01),见表2。
2.3单因素分析比较 死亡组和存活组动静脉二氧化碳分压差(△PCO2)、PaO2/PiO2和pH比较差异有统计学意义(P<0.05),其余指标比较差异均无统计学意义(P>0.05),见表3。
2.4多因素Logistic回归分析 将VD/VT、APACHEⅡ、PaO2/PiO2、pH、△PCO2、LIPS带入二分类Logistic回归分析最后得出,APACHEⅡ、LIPS、△PCO2、VD/VT均是预后的危险因素,见表4。
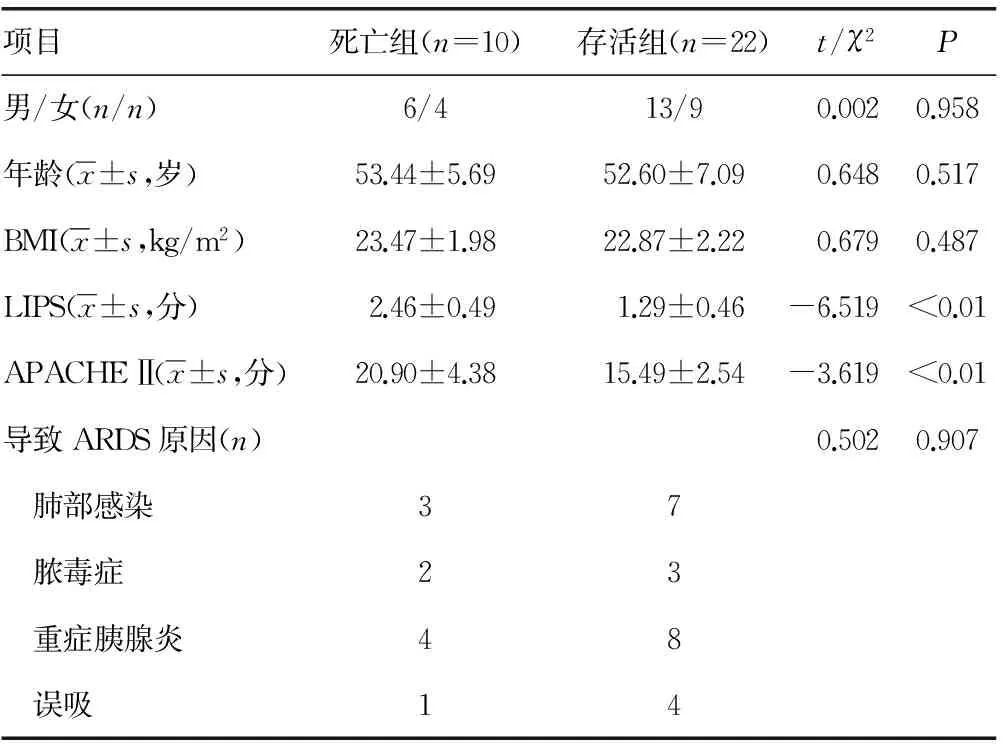
表1 患者一般资料比较

表2 两组患者VD/VT比较
a:P<0.01,与存活组比较
MV:通气量;CVP:中心静脉压
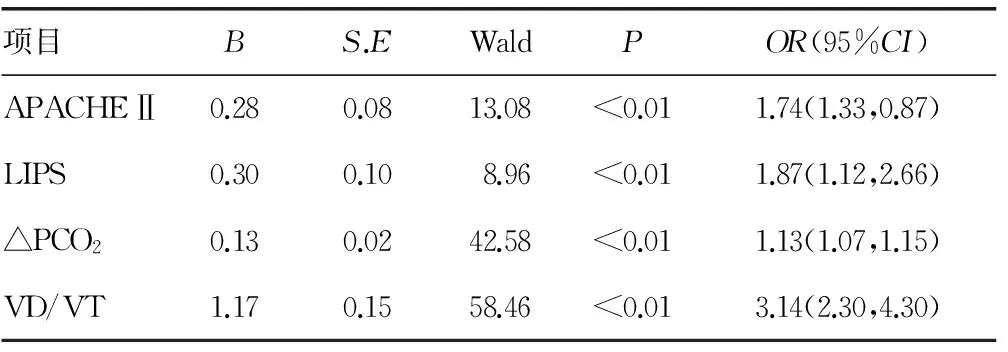
表4 影响ARDS患者预后的Logistic回归分析
2.5预后评价的受试者工作特征(ROC)曲线分析 将患者按照预后结局分成存活组和死亡组,其中存活组为对照组,死亡组为试验组,把1、4、5、6 d VD/VT绘制ROC曲线,ROC曲线下面积分别为0.564、0.961、0.759、0.814。其中4 d VD/VT ROC曲线下面积最大,故4 d VD/VT诊断意义最大,其临界值为0.620,灵敏度90.0%,特异度95.5%,具有较高诊断价值,见图1。
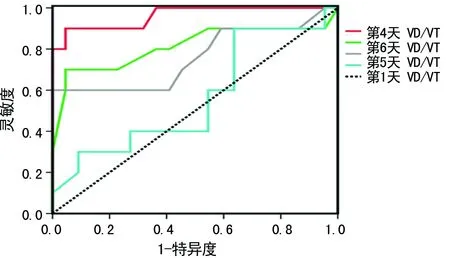
图1 不同时相预测ARDS患者预后的ROC曲线
3 讨 论
ARDS是多器官功能障碍综合征(MODS)在肺部的表现,机体失控的炎性反应使肺泡大量塌陷,出现通气不足、真性分流和死腔增加。VD/VT可反映肺通气功能和血流分布异常[8]。自1967年提出ARDS概念以来,最广泛应用的也仅仅是PaO2/FiO2[9]其总体病死率仍居高不下,特别是早期,常因预判不足而延误病情,急需更多精准、简便的指标,以便提供及时有效的治疗[10]。基于病理生理改变及临床相关研究,VD/VT逐渐成为研究的热点,探讨VD/VT对ARDS患者预后评估的可行性和应用前景显得尤为重要。
先前已有研究证实,ARDS早期VD/VT明显升高,VD/VT居高不下超过1周的患者,预后多不佳,且死亡风险度随着VD/VT的升高而明显增加[11-14]。越来越多的学者认为VD/VT能有效地区别ARDS的严重程度,并较为准确的判断预后,有望与PaO2/FiO2一起纳入柏林定义,成为ARDS诊断的辅助标准[15-17]。但迄今为止,VD/VT在ARDS患者不同时相及整体变化趋势的研究仍较少。因此本研究通过对上述研究的进一步整合,动态监测ARDS患者1~6 d VD/VT的变化,阐述VD/VT在ARDS患者不同预后的总体变化规律及各时相特征。结果显示1~6 d存活组和死亡组VD/VT均升高,且随着病程延长死亡组VD/VT有逐渐升高趋势,而存活组VD/VT波动不大;1~3 d两组VD/VT无明显差异,而4~6 d死亡组VD/VT明显高于存活组。ROC曲线分析4 d VD/VT面积最大,以0.62为截断值拥有较高的灵敏度和特异度,上述研究与VENDER等[18]结果基本符合。
VD/VT在ARDS患者第4天出现明显差异可能与ARDS临床分期有关。起病1~3 d,多相对稳定,患者呼吸平稳,胸片大致正常,病变以渗出为主,病情迅速进展至72 h后,逐渐出现呼吸窘迫和紫绀,胸片有非对称的斑片状阴影。此期为ARDS增生期,坏死的细胞和残余的纤维素形成透明膜,导致肺泡大面积塌陷,引起死腔增加。第4天VD/VT对ARDS患者预后的诊断价值最大,若能利用第4天VD/VT在ARDS机械通气患者中尽早的识别高危,尽快地实施体外膜肺氧合保证气体交换减少肺损伤[19-20],可为患者呼吸功能的修复赢得时间。
本研究中死亡组LIPS和APACHEⅡ较存活组高,说明LIPS和APACHEⅡ可能对ARDS患者预后具有相关性和一定的预测价值,但是这样的结论仍需要后续进一步研究证实。另外本研究发现△PCO2也是影响ARDS患者预后的危险因素,而乳酸差异不大,可能与ARDS时组织缺氧、微循环灌注不足,△PCO2反应得更早、更快,受其他影响更小有关[21]。
综上所述,本研究证实VD/VT能有效地评估ARDS患者的预后,第4天VD/VT可以辅助识别高危患者,动态连续的监测更有临床指导价值。
参考文献
[1]SUD S,SUD M,FRIEDRICH J O,et al.High frequency oscillation in patients with acute lung injury and acute respiratory distress syndrome (ARDS):systematic review and meta-analysis[J].BMJ,2010,340(7759):1290.
[2]DIAZ J V,BROWER R,CALFEE C S,et al.Therapeutic strategies for severe acute lung injury[J].Crit Care Med,2010,38(8):1644-1650.
[3]杨军辉,李佳,李宁,等.影响急性呼吸窘迫综合征患者预后的危险性因素分析及治疗研究[J].陕西医学杂志,2016,45(4):404-405.
[4]COOKE C R,KAHN J M,CALDWELL E,et al.Predictors of hospital mortality in a population-based cohort of patients with acute lung injury[J].Crit Care Med,2008,36(5):1412-1420.
[5]BEITLER J R,THOMPSON B T,MATTHAY M A,et al.Estimating dead-space fraction for secondary analyses of acute respiratory distress syndrome clinical trials[J].Crit Care Med,2015,43(5):1026-1035.
[6]RANIERI V M,RUBENFELD G D,THOMPSON B T,et al.Acute respiratory distress syndrome:the Berlin definition ARDS definition task force[J].JAMA,2012,307(23):2526-2533.
[7]SUE D Y.Predicting dead space ventilation in critically ill patients using clinically available data[J].Cri Care Med,2010,38(1):288-291.
[8]FOWLER W S.Lung function studies:the respiratory dead space.[J].Am J Physiol,1948,154(3):405-416.
[9]FERGUSON N D,FAN E,CAMPOROTA L,et al.The Berlin definition of ARDS:an expanded rationale,justification and supplementary material[J].Int Care Med,2012,38(10):1573-1582.
[10]刘松桥,陈菁,郭凤梅,等.死腔分数与早期急性呼吸窘迫综合征患者预后的关系[J].中华急诊医学杂志,2012,21(6):597-601.
[11]KALLET R H,ALONSO J A,PITTET J F,et al.Prognostic value of the pulmonary dead-space fraction during the first 6 days of acute respiratory distress syndrome[J].Res Care,2004,49(9):1008-1014.
[12]FERGUSON N D,FAN E,CAMPOROTA L,et al.The Berlin definition of ARDS:an expanded rationale,justification,and supplementary material[J].Int Care Med,2012,38(10):1573-1582.
[14]VILLAR J,PREZMNDEZ L,BASALDA S,et al.A risk tertiles model for predicting mortality in patients with acute respiratory distress syndrome:age,plateau pressure,and PaO2/FiO2at ARDS onset can predict mortality[J].Respir Care,2011,56(4):420-428.
[15]KALLET R H,ZHUO H,LIU K D,et al.The association between physiologic dead-space fraction and mortality in subjects with ARDS enrolled in a prospective multi-center clinical trial[J].Respir Care,2014,59(11):1611-1618.
[16]ZHANG Y J,GAO X J,LI Z B,et al.Comparison of the pulmonary dead-space fraction derived from ventilator volumetric capnography and a validated equation in the survival prediction of patients with acute respiratory distress syndrome[J].Chinese J Traumat,2016,19(3):141-145.
[17]RAURICH J M,VILAR M,COLOMAR A,et al.Prognostic value of the pulmonary dead-space fraction during the early and intermediate phases of acute respratory distress syndrome[J].Resp Care,2010,55(3):282-287.
[18]VENDER R L,BETANCOURT M F,LEHMAN E B,et al.Prediction equation to estimate dead space to tidal volume fraction correlates with mortality in critically ill patients[J].J Criti Care,2014,29(2):e1-317.
[19]NOAH M A,PEEK G J,FINNEY S J,et al.Referral to an extracorporeal membrane oxygenation center and mortality among patients with severe 2009 influenza A(H1N1)[J].Jama,2016,306(15):1659-1668.
[20]LEE J J,HWANG S M,KO J H,et al.Efficacy of veno-venous extracorporeal membrane oxygenation in severe acute respiratory failure[J].Yonsei Med J,2015,56(1):212-219.
[21]MONNET X,JULIEN F,AIT-HAMOU N,et al.Lactate and venoarterial carbon dioxide difference/arterial-venous oxygen difference ratio,but not central venous oxygen saturation,predict increase in oxygen consumption in fluid responders[J].Crit Care Med,2013,41(6):1412-1420.

