聚偏氟乙烯/氧化硅复合电解质在电致变色器件中的应用
刘学龙,王宏志,张青红,李耀刚,陈 培
东华大学 材料科学与工程学院 先进玻璃制造技术教育工程研究中心,上海201620
电致变色是指材料在外加电场作用下发生稳定、可逆颜色变化的现象。用电致变色材料所组装成的器件称为电致变色器件。一般电致变色器件在很小的电压下就可实现光学性质的可逆变化[1]。这种光学性质的可逆变化以及所需电压较小的独特优势,使其在智能窗、显示器以及可视化超级电容器等领域展现出了广泛的应用前景[2-5]。
电致变色器件结构中最重要的组成部分是电致变色材料和电解质层。
电致变色材料可以分为有机电致变色材料和无机电致变色材料两大类。有机电致变色材料主要有聚苯胺[6]、聚噻吩[7]以及紫罗精[8]等。大多数有机电致变色材料在太阳光照射下都会出现降解。导致性能下降现象,因此有机电致变色材料很少应用在智能窗等相关领域[9]。无机电致变色材料则不会出现以上情况。WO3是研究最为充分的无机电致变色材料,已经被广泛应用于智能窗领域[10-13]。
关于电致变色用电解质的研究起步较晚,但是其对电致变色器件却至关重要。电解质的性能直接影响到整个器件的性能。所以,电解质层的选择是电致变色器件能否满足实际应用的关键。
目前,电致变色器件中使用较多的电解质是聚合物电解质,但单纯的聚合物电解质普遍存在电导率不高以及机械性能不好等缺点[14],因此迫切需要采取一些方法来提高其性能。提高聚合物电解质性能的方法一般有交联法[15]、共聚法[16]以及无机陶瓷填料法[17]等。通过有机/无机复合 (也就是在聚合物电解质中引入无机陶瓷颗粒) 能够有效地提高电解质的机械性能和和化学性能[18]。此外,无机陶瓷填料的表面极性基团和聚合物中的路易斯酸碱之间会形成络合作用,可以降低聚合物的结晶性,从而提高聚合物电解质的电导率[19]。常用的无机粒子有SiO2[20]、二氧化钛 (TiO2)[21]和氧化铝(Al2O3)[22]等。通常,使用无机陶瓷填料法改善聚合物电解质性能最主要的是控制无机粒子在聚合物中的添加量以及控制成膜工艺。
本文讨论了不同质量比无机陶瓷粒子对聚合物电解质性能的影响规律,并将复合电解质组装成电致变色器件,研究了其电致变色性能。
1 实 验
1.1 PVDF/SiO2复合凝胶态电解质的制备
室温下,称取干燥后的高氯酸锂10.96 g与100 mL N,N-二甲基甲酰胺 (DMF) 配制成1 mol/L高氯酸锂的N,N-二甲基甲酰胺溶液。将PVDF和SiO2(粒径7 nm) 按照质量比为100:0、96:4、92:8、88:12分别加入到上述溶液中,制备成有机/无机复合浆料。然后,将浆料置于两片玻璃基板间,使用热压机在115°C下热压10 min,制备出透明复合凝胶态电解质膜。
1.2 WO3电致变色薄膜的制备
将5 g钨酸和1.44 g氧化钼在95°C下溶于60 mL双氧水,冷却至室温后,用等体积的乙醇和去离子水将其稀释至200 mL,得到浓度为0.1 mol/L的前驱体溶液。然后,将100 mL前驱体溶液和100 mL蒸馏水装入烧瓶中,于110°C下冷凝回流12 h,得到蓝色溶液。将蓝色溶液离心洗涤,将离心沉淀物分散在去离子水中配制成2 g/L的WO3墨水。取出20 mL所制备的墨水,采用喷涂的方法在导电玻璃基底上制备出电致变色薄膜。
1.3 电致变色器件的封装
将所制备好的复合凝胶态电解质膜贴合在喷涂有墨水的导电玻璃以及另一块干净的导电玻璃表面,然后压合,再使用紫外固化胶将边缘密封,以避免接触空气。最终制备出面积为2.5 cm × 2.5 cm的电致变变色器件。
1.4 样品品表征
采用用日本 Hitachhi公司的 MModelS-48000型场发射扫扫描电子显微微镜 (FE-SEMM) 观察钼掺掺杂WO3薄膜的微微观形貌以及及有机/无机复复合凝胶态电电解质薄膜。采采用日本Riggaku公司的D/max-25500型X射线衍射仪仪 (XRD) 对对钼掺杂WO33电致变色薄薄膜进行物相相分析 (Cu-KKα,λ = 1.54005 Å 管压400 KV,电流300 mmA),扫描范范围为 20° ~80°,扫描速速度为 0.02°/ss。测试电致致变色器件性能的主要仪器器是上海辰华CHHI760D型电化化学工作站,,器件的光学学性能则使用用美国 Perkinn Elmer 公司司的Lambda 9950 型紫外-可见见分光光度计进进行表征。
2 结果与与讨论
2.1 WO33薄膜的结构构和形态表征征
图11 (a) 示出了了喷涂法制备备的钼掺杂WWO3电致变色色薄膜扫描电电子显微镜照片,可以看出出该薄膜呈现出了了多孔的纳米米颗粒形貌,这种多孔结结构可以增加加薄膜的比表面积,进而增增加与电解质质的接触面积,从从而缩小电解解质层和电致致变色层的界界面阻抗[23]。图1 (b) 是喷喷涂法所制备备的钼掺杂WWO3薄膜的XRD图谱。可以看看出,喷涂法制制备的钼掺杂杂WO3电致变变色薄膜XRRD图谱与标标准卡片 (JCPPDS Card no. 01-0776-1279) 相对对应,为单斜斜相W0.71Moo0.29O3的衍射射峰。

图1 钼掺掺杂WO3薄膜膜的 (a) SEMM照片和 (b) XXRD图谱Figure1 (a) FE--SEM imagess and (b) XRDD pattern of as-prepared tunggsten molybdenum oxide fii lm

图2 不同PVDFF/SiO2质量比条件下制备的的复合凝胶态态电解质FE-SSEM照片Figure2 FE-SEM immages of the ccomposite gell-state electrollyte through diferent PVDFF/SiO2 weight ratios
2.2 PVDF/SiO2复合凝胶态电解质的形貌表征
图2 为在不同PVDF/SiO2质量比条件下制备得到的复合凝胶态电解质扫描电镜照片。由图中可以看出,当不添加无机陶瓷颗粒SiO2时,复合凝胶态电解质的表面较平整,当添加SiO2时,复合凝胶态电解质的表面出现多孔的结构,这说明无机填料的加入使得电解质出现了多孔结构。这种多孔结构一方面可以增加液相电解质的存储能力,使活性离子能够在液相介质中迁移,有益于复合凝胶电解质的离子电导率,另一方面也为离子提供了通道,有利于离子的迁移[24,25]。
智媛并不是唯一的醒悟者,现在越来越多的女生剪短发、抛弃化妆品。对她们来说,漂亮不是唯一重要的事,获得更多的知识,开拓更多的技能,让自己成为一个更优秀的人,才是更加重要的事情。
2.3 PVDF/SiO2复合凝胶态电解质的电导率
离子电导率是电解质的重要性能之一,表征了离子在电场作用下的迁移快慢,关系到所组装电致变色器件的性能优劣。
电解质的离子电导率可由下式给出:

式中,l为电解质样品的厚度 (cm),A为电解质样品与电极接触的有效面积 (cm2),Rb为电解质的本体电阻 (Ω),代表了交流阻抗谱与X轴的截距[26]。
图3示出了不同PVDF/SiO2质量比条件下制备得到的复合凝胶态电解质的交流阻抗谱以及离子电导率随SiO2添加量的变化关系曲线。可以看出,当SiO2与PVDF的质量比从0 wt% 增加到8 wt%时,电解质的本体阻抗Rb降低,体系离子电导率提高,从1.6 mS·cm-1增加至最大2.4 mS·cm-1。其间的主要原因是:一方面,随着SiO2含量的增加,体系的活性粒子显著增加,从而使复合凝胶态电解质的离子电导率提高;另一方面,由电解质的扫描电镜照片分析可知,随着SiO2的添加,电解质的微观结构呈多孔形态,这种多孔结构有利于液相的存储,有助于离子的迁移,从而使电解质电导率提高。但是,当SiO2与PVDF的质量比超过8 wt% 时,复合凝胶态电解质的离子电导率出现下降趋势。造成这种现象的原因可能在于:当体系的无机填料增多后,小尺寸效应将导致无机纳米粒子发生团聚,从而使无机粒子在复合电解质中的分散性降低,造成体系的电导率降低[27]。
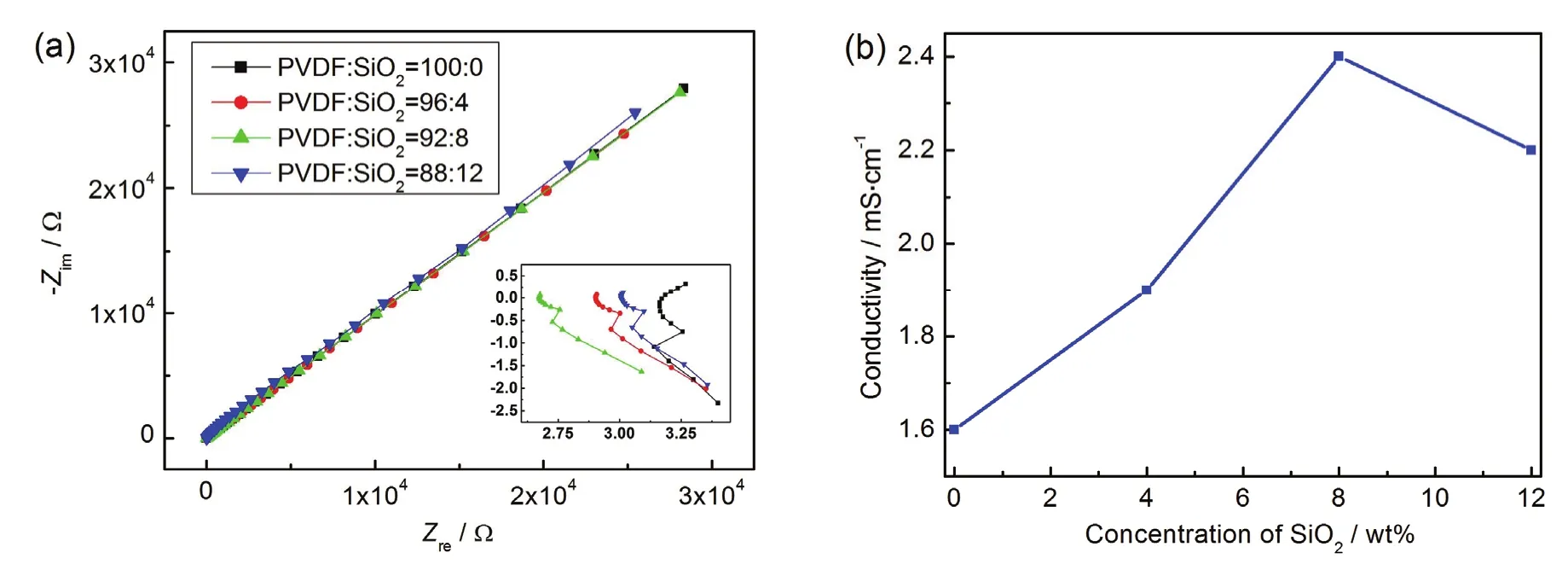
图3 复合凝胶态电解质的 (a) 交流阻抗图谱以及 (b) 离子电导率随SiO2添加量的变化曲线Figure3 (a) Electrochemical impedance spectroscopy and (b) conductivity of the composite gel-state electrolytes
2.4 电致变色性能
光调制范围是指电致变色器件在褪色态与着色态的光学透过率在某一波长下的差值,是衡量电致变色器件性能好坏的重要参数之一。
从光调制范围可以看出,不同SiO2含量会影响到电致变色器件的光调制能力。当氧化硅和PVDF质量比从0 wt% 增加到8 wt%时,电致变色器件的光调制范围持续上升,当氧化硅和PVDF的质量比超过8 wt%时,电致变色器件光调制范围发生下降的现象。可以发现光调制范围的变化趋势与复合凝胶态电解质电导率变化趋势相吻合,这说明电解质的离子电导率是影响整体电致变色器件性能的一个重要参数。在PVDF和SiO2质量比为92:8时,所制备的电致变色器件光调制范围达到最大,这得益于在该质量比下所制备得到的复合凝胶态电解质具有较高的电导率,从而在相同时间下会有更多的离子在该电解质层内发生迁移,于是就会引起较多的离子在电致变色层发生嵌入和脱出,最终使器件的光调制范围高于其它器件。
响应时间和着色效率也是衡量电致变色器件性能的重要指标。通过以上分析可以发现,在PVDF和SiO2质量比为92:8时,所制备出的电致变色器件光调制范围达到最大。因此,本研究对该器件的响应时间和着色效率进行了测试。
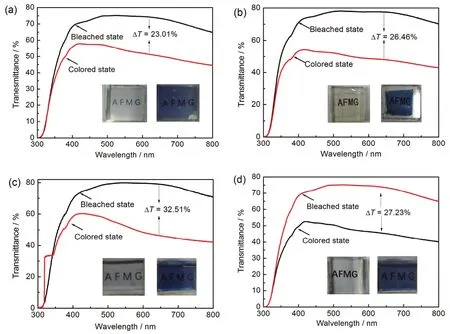
图4 电致变色器件在着色态和褪色态的透过率光谱 (插图为相对应器件的数码照片)Figure4 UV-vis transmittance spectrum of the electrochromic devices (ECDs). The insert shows the digital photographs of the ECDs.(a) PVDF:SiO2 = 100:0; (b) PVDF:SiO2 = 96:4; (c) PVDF:SiO2 = 92:8; (d) PVDF:SiO2 = 88:12.
图5 (a) 给出了PVDF和SiO2质量比为92:8的复合凝胶态电解质所组装的电致变色器件在着色和褪色态的原位归一化透过率变化曲线和光密度变化随注入电荷密度的变化曲线图。采用计时电流法的发波电压为-2.5 V/1.5 V,以在632.8 nm处的透过率实现90% 变化所需时间为响应时间[28],结合图5所示数据可以计算出器件的响应时间。可以发现,在PVDF和SiO2质量比为92:8时,电致变色器件的着色时间和褪色时间分别是40 s和29 s。这比以往所报道的凝胶态电解质基的电致变色玻璃时间要短[29],主要原因有两个:第一,这种有机/无机复合凝胶态电解质具有优异的离子导电性能,离子能够在电场的作用下快速地发生迁移;第二,所制备的变色层具有多孔的纳米结构,使得离子能够更好地从电解质层嵌入与脱出,且多孔的结构能够与电解质层之间更好地匹配。这两点原因使得所制备的电致变色器件能够拥有较好的着色与褪色性能。
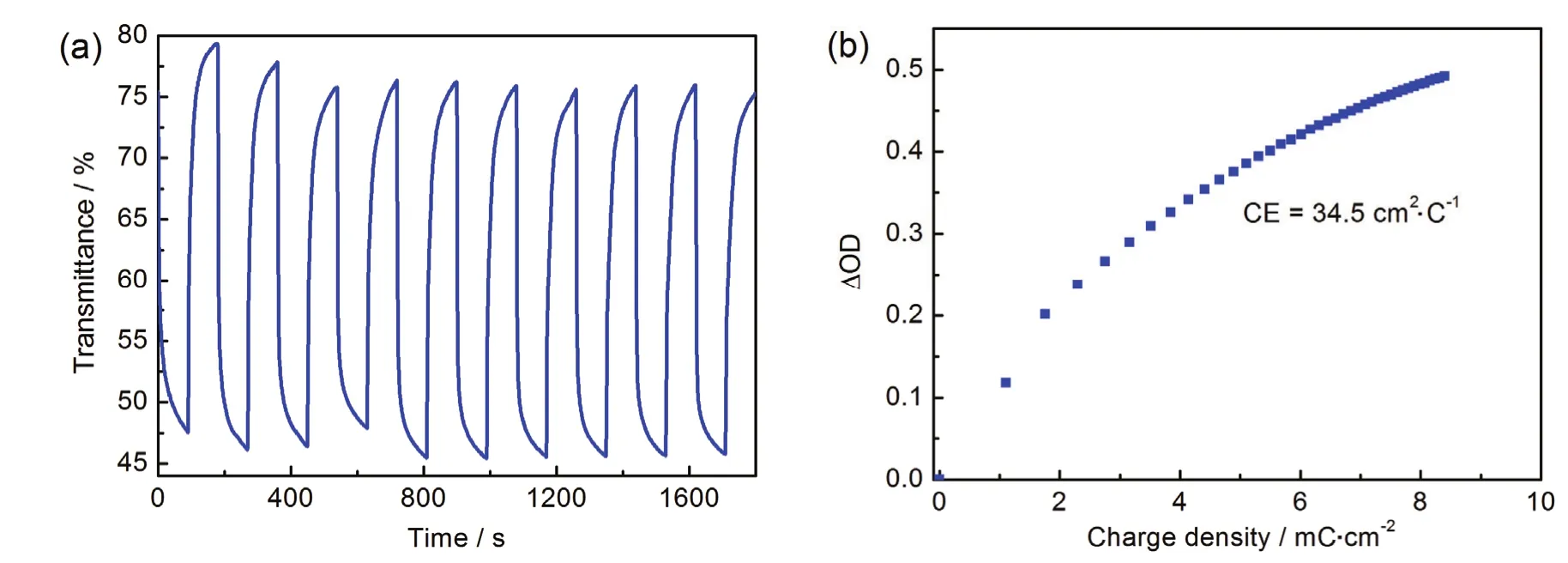
图5 由PVDF:SiO2 = 92:8复合凝胶态电解质组装的电致变色器件在着色和褪色态的 (a) 原位归一化透过率变化曲线图; (b) 光密度变化随注入电荷密度的变化曲线图Figure5 In situ normalized transmittance for electrochromic devices assembled by composite gel-state electrolyte with PVDF:SiO2 = 92:8
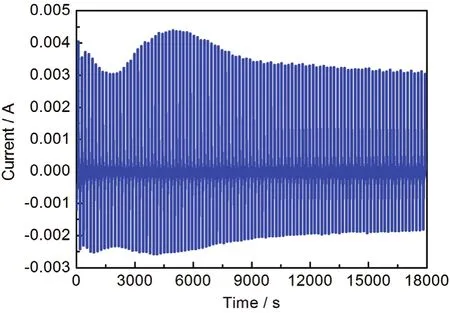
图6 电致变色器件电流大小随变色时间的变化关系曲线Figure6 Relationship between times and current for electrochromic
着色效率是单位面积所注入一定量电荷所获得的光学吸光度变化,是评估电致变色器件性能优劣的一个综合参数,它主要由器件的光调制范围和光响应时间所决定。着色效率CE可以由以下计算公式得出[30]:
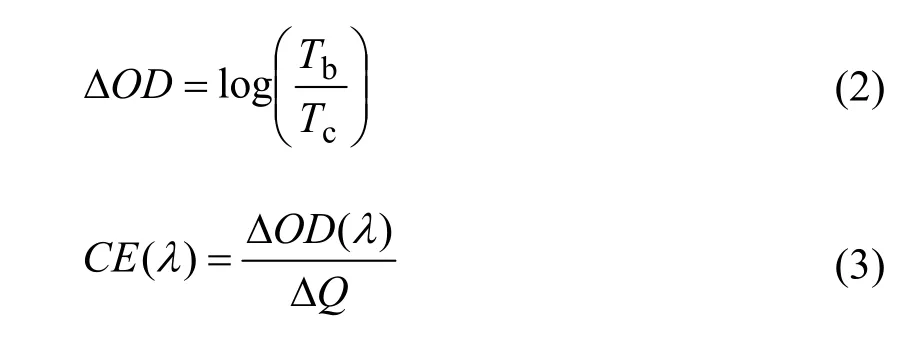
式中,Tb和Tc分别对应于电致变色器件着色和褪色态的光学透过率,Q为电荷密度。
图5 (b) 示出了PVDF和SiO2质量比为92:8时的电致变色器件光密度变化值随注入电荷密度的变化曲线,由图中数据可以计算出器件的着色效率为34.5 cm2/C,这说明得益于复合电解质优异的离子电导率,器件拥有较好的电致变色性能。
衡量电致变色玻璃能否真正应用于智能窗领域,循环稳定性是重要指标。采用计时电流法测试了器件的100次循环稳定性,结果如图6所示。由电流峰值大小可以看出,在循环100次后,器件的电流峰值依然保持在最初的90% 以内,说明器件拥有较好的循环稳定性,且仍有提升的空间。
3 结 论
通过控制PVDF和无机粒子SiO2的比例,采用热压法制备了不同的复合凝胶态电解质膜。研究表明,当PVDF与SiO2的质量比为92:8时,所制备的复合凝胶态电解质膜结构较好,电导率最大,为2.4 mS·cm-1。采用喷涂法制备钼掺杂WO3电致变色薄膜,并与复合凝胶态电解质组装成电致变色器件,对其性能进行了研究。结果表明,当PVDF:SiO2= 92:8时,复合凝胶态电解质所组装的电致变色器件展现出优异的电致变色性能,光调制范围为32.51%,褪色和着色时间分别40 s和29 s,着色效率34.5 cm2/C,并且循环100次之后,器件的电流峰值依然保持在最初的90%。因此,适当控制无机填料的比例,能够获得性能优异的有机/无机复合电解质膜,从而制备出性能较好的电致变色器件,该器件具有在智能窗领域的广阔应用前景。
[1] CAI G, CUI M, KUMAR V, et al. Ultra large optical modulation of electrochromic porous WO3film and the local monitoring of redox activity [J]. Chemical Science, 2016, 7 (2): 1373-1382.
[2] LI H, LI J, HOU C, et al. Solution-processed porous tungsten molybdenum oxide electrodes for energy storage smart windows [J]. Advanced Materials Technologies, 2017, DOI: 10.1002/admt.201700047.
[3] GRANQVIST CG. Handbook of Inorganic Electrochromic Materials [M]. The Netherlands, Amsterdam:Elsevier, 1995.
[4] HONG CM, LODGE TP, FRISBIE C D. Solution processable, electrochromic ion gels for sub-1V, flexible displays on plastic [J]. Chemistry of Materials, 2015, 27 (4): 1420-1425.
[5] ZHU M, HUANG Y, HUANG Y, et al. An electrochromic supercapacitor and its hybrid derivatives:quantifiably determining their electrical energy storage by an optical measurement [J]. Journal of Materials Chemistry A, 2015, 3 (42): 21321-21327.
[6] ZHAO L, ZHAO L, XU Y, et al. Polyaniline electrochromic devices with transparent graphene electrodes[J]. Electrochimica Acta, 2009, 55 (2): 491-497.
[7] KIM TH, PARK SH, KIM DH, et al. Roll-to-roll sputtered ITO/Ag/ITO multilayers for highly transparent and flexible electrochromic applications [J]. Solar Energy Materials & Solar Cells, 2017, 160: 203-210.
[8] HONG CM, KIM CH, LODGE TP, et al. Multicolored, low power, flexible electrochromic devices based on ion gels [J]. ACS Applied Materials & Interfaces, 2016, 8 (9): 6252-6260.
[9] BAETENS R, JELLE BP, GUSTAVSEN A. Properties, requirements and possibilities of smart windows for dynamic daylight and solar energy control in buildings: a state-of-the-art review [J]. Solar Energy Materials & Solar Cells, 2010, 94 (2): 87-105.
[10] MA D, SHI G, WANG H, et al. Hierarchical NiO microflake films with high coloration efficiency, cyclic stability and low power consumption for applications in a complementary electrochromic device [J].Nanoscale, 2013, 5 (11): 4808-4815.
[11] WANG J, ZHANG L, YU L, et al. A bi-functional device for self-powered electrochromic window and self-rechargeable transparent battery applications [J]. Nature Communications, 2014, DOI:10.1038/ncomms5921.
[12] GRANQVIST CG. Electrochromics for smart windows: oxide-based thin films and devices [J]. Thin Solid Films, 2014, 564 (8): 1-38.
[13] LI H, SHI G, WANG H, et al. Self-seeded growth of nest-like hydrated tungsten trioxide film directly on FTO substrate for highly enhanced electrochromic performance [J]. Journal of Materials Chemistry A,2014, 2 (29): 11305-11310.
[14] FAN L, NAN CW, ZHAO S. Effect of modified SiO2on the properties of PEO-based polymer electrolytes[J]. Solid State Ionics, 2003, 164 (1): 81-86.
[15] IZUCHI S, OCHIAI S, TAKEUCHI KI. Solid polymer electrolytes for lithium cells [J]. Journal of Power Sources, 1997, 68 (1): 37-42.
[16] CHOI SW, JO SM, LEE WS, et al. An electrospun poly(vinylidene fluoride) nanofibrous membrane and its battery applications [J]. Advanced Materials, 2003, 15 (23): 2027-2032.
[17] CAPIHLIA C, MUSTARELLI P, QUARTARONE E, et al. Effects of nanoscale SiO2on the thermal and transport properties of solvent-free, poly(ethylene oxide) (PEO)-based polymer electrolytes [J]. Solid State Ionics, 1999, 118 (1–2): 73-79.
[18] RAGHAVAN P, ZHAO X, KIM JK, et al. Ionic conductivity and electrochemical properties of nanocomposite polymer electrolytes based on electrospun poly(vinylidene fluoride-co-hexafluoropropylene)with nano-sized ceramic fillers [J]. Electrochimica Acta, 2009, 54 (2): 228-234.
[19] JEONG KU, CHAE HD, LIM CI, et al. Fabrication and characterization of electrolyte membranes based on organoclay/tripropyleneglycol diacrylate/poly(vinylidene fluoride) electrospun nanofiber composites [J].Polymer International, 2010, 59 (2): 249-255.
[20] ZACCARIA M, FABIANI D, CANNUCCIARI G, et al. Effect of silica and tin oxide nanoparticles on properties of nanofibrous electrospun separators [J]. Journal of the Electrochemical Society, 2014, 162 (6):A915-A920.
[21] JUANG RS, HSIEH CT, CHEN PA, et al. Microwave-assisted synthesis of titania coating onto polymeric separators for improved lithium-ion battery performance [J]. Journal of Power Sources, 2015, 286:526-533.
[22] LIANG B, TANG S, JIANG Q, et al. Preparation and characterization of PEO-PMMA polymer composite electrolytes doped with nano-Al2O3[J]. Electrochimica Acta, 2015, 169: 334-341.
[23] KHOO E, LEE PS, MA J. Electrophoretic deposition (EPD) of WO nanorods for electrochromic application [J]. Journal of the European Ceramic Society, 2010, 30 (5): 1139-1144.
[24] LIU W, LIU N, SUN J, et al. Ionic conductivity enhancement of polymer electrolytes with ceramic nanowires fillers [J]. Nano Letters, 2015, 15 (4): 2740-2745.
[25] SEKHON SS, SINGH HP. Ionic conductivity of PVdF-based polymer gel electrolytes [J]. Solid State Ionics, 2002, 152–153: 169-174.
[26] PUGUAN JMC, CHUNG WJ, KIM H. Ion-conductive and transparent PVdF-HFP/silane-functionalized ZrO2nanocomposite electrolyte for electrochromic applications [J]. Electrochimica Acta, 2016, 196:236-244.
[27] ILJNUR BP, GRANQVIST CG, MARSAL R, et al. [PEI–SiO2]:[LiTFSI] nanocomposite polymer electrolytes:Ion conduction and optical properties [J]. Solar Energy Materials & Solar Cells, 2012, 98 (98):465-471.
[28] LI HZ, WANG JM, SHI QW, et al. Constructing three-dimensional quasi-vertical nanosheet architectures from self-assemble two-dimensional WO3·2H2O for efficient electrochromic devices [J]. Applied Surface Science, 2016, 380: 281-287.
[29] TANG Q, LI H, YUE Y, et al. 1-Ethyl-3-methylimidazolium tetrafluoroborate-doped high ionic conductivity gel electrolytes with reduced anodic reaction potentials for electrochromic devices [J].Materials & Design, 2017, 118: 279-285.
[30] CHEN LC, HO KC. Design equations for complementary electrochromic devices: application to the tungsten oxide–Prussian blue system [J]. Electrochimica Acta, 2001, 46 (13): 2151-2158.

