我国转基因动物及其安全性评价发展现状
卢军锋,李 晓,杨公社,史新娥
(西北农林科技大学动物科技学院 动物脂肪沉积与肌肉发育实验室,陕西 杨凌 712100)
转基因动物(transgenic animal)是指利用基因工程手段将外源基因有目的、有计划地导入受体动物的受精卵或胚胎,使之稳定整合于动物基因组并能遗传给后代的一类动物,包括畜禽、水生动物、节肢动物等。1980年,Gordon等[1]将重组DNA导入小鼠受精卵,这是人类首次对哺乳动物进行人工改造,距今已有37年。
转基因动物具有广阔的应用前景,如培育动物新品种(高产、优质、抗病)、探究人类疾病机理、作为生物反应器生产药用蛋白等。但是转基因动物也存在诸多问题,如畸形、生长迟缓、不育、抗病力差等。自转基因技术问世以来,公众对其安全性一直存有争议,因此转基因动物的安全性评价尤为重要。发达国家在不断发展转基因技术的过程中逐渐形成了一系列世界公认的转基因动物安全评价标准和共识性文件。我国在参考这些标准与共识的同时,结合自身国情和发展现状,陆续颁布了一系列转基因动物相关安全法律法规,并根据转基因技术的发展不断进行修改完善。
1 转基因动物国内外研究进展
转基因动物研究起源于20世纪80年代,Palmiter等[2](1982)采用显微注射法将大鼠的生长激素基因成功导入到小鼠基因组中,这被公认为世界上第一例真正意义上的转基因动物。此后,科学家先后获得转基因非洲爪蟾[3]、转基因果蝇[4-5]、转基因绵羊和转基因猪[6]等。1997年,Wilmut等[7]通过体细胞核移植技术率先制作出世界上第一头转基因克隆羊“多莉”,这是人类首次对哺乳动物体细胞核进行移植,同时也改善了转基因效率低下的问题。2006年6月,世界首个利用转基因动物乳腺生物反应器生产的基因工程蛋白药物—重组人抗凝血酶Ⅲ(商品名:ATryn)获得欧洲医药评价署人用医药产品委员会的上市许可,标志着通过转基因动物进行药物生产进入产业化阶段。2015年11月,世界上首例导入外源基因使生长速度变快的转基因三文鱼(商品名:AquAdvanage三文鱼)获得美国食品和药品管理局(Food and Drug Administration,FDA)批准进入市场销售,标志着转基因动物供人类食用迈出了关键一步。
我国是世界上较早开展转基因动物研究的国家。1983年由中国科学研究院朱作言院士联合中国科学院发育生物学研究所、广西水产研究所和中国水产科学院长江水产研究所沙市分所的课题组将重组人生长激素基因导入鲫鱼受精卵,获得快速生长的转基因鱼[8]。魏庆信等[9](1992)以湖北白猪为实验材料,通过显微注射法和精子载体法导入OMT/PGH基因获得了转基因猪。罗军等[10](1993)用显微注射法获得了4只健康转基因仔兔。国内其他课题组也先后获得了转基因小鼠、转基因克隆牛、转基因免、转基因山羊、转基因猪等。2008年,中国农业大学李宁课题组历时7年多,成功培育出一批人乳铁蛋白转基因奶牛,所产牛奶中的重组人乳铁蛋白含量为国际最高水平,并具有与天然蛋白相同的转运铁、抗菌等生物活性[11]。2011年,内蒙古农业大学李光鹏课题组联合吉林大学、南京大学、中国科学院动物所的研究团队成功获得Fat-1转基因牛,Fat-1是动物产生n-3多不饱和脂肪酸的关键基因,Fat-1转基因牛的动物产品对于预防人的心脑血管病具有重要价值[12]。2015年,西北农林科技大学陈玉林课题组联合榆林学院屈雷课题组和南京大学黄行许课题组利用CRISPR/Cas 9基因编辑技术,获得敲除成纤维细胞生长因子5(fibroblast growth factor 5,FGF5)和肌肉生长抑制素(myostatin,MSTN)基因的羔羊[13],这是世界上第一例家养动物多基因多位点一次性操作敲除基因,对于推动我国乃至世界绒山羊种质资源的创新和产业发展具有重要意义。2017年,华南农业大学吴珍芳课题组将转基因小鼠的唾液腺作为生物反应器[14],生产出具有良好生物活性的人神经生长因子蛋白(human nerve growth factor,hNGF),该蛋白可用于治疗人类小儿脑瘫和老年痴呆等神经损伤或退化性疾病,标志着转基因动物的唾液腺作为生物反应器制备人类蛋白药物成为现实。
转基因技术发展的30余年,培育出的转基因动物不计其数,目前的转基因动物培育工作主要出于改善动物自身生存、提高动物源性产品的品质和产量、减少动物排泄物对环境的污染和用于生物制药工程。
2 转基因动物安全性评价内容
目前世界上转基因动物安全性评价主要是按照国际食品法典委员会(CAC)、联合国粮农组织(FAO)、世界卫生组织(WHO)、经济合作与发展组织(OECD)制定的一系列转基因生物安全评价标准和共识性文件等全球公认的评价准则来进行。参考全球公认的评价准则,结合我国自身国情和发展现状,我国颁布的转基因生物相关安全法律法规有:科技部《中国生物安全框架》和《基因工程安全管理办法》,农业部《农业生物技术基因工程安全管理实施办法》和《农业转基因生物标识管理办法》,国务院《农业转基因生物安全条例》和卫生部《转基因食品卫生管理办法》等。转基因动物与其他农业转基因生物一样,需要纳入生物安全管理,进行安全性评价。
目前我国转基因动物安全性评价主要内容包括分子特征、遗传稳定性、健康状况、功能效率评价、环境适应性、转基因动物逃逸(释放)及其对环境的影响以及食用安全(图1)(中华人民共和国农业部,2017《转基因动物安全评价指南》)。
动物经过转基因后,表型及基因型的改变都可能带来潜在的风险[15]。目前科学技术的发展研究还不可能完全精确地预测某个基因在一个新的环境中会产生什么样的相互作用,而转基因动物基因的表达受环境等诸多因素影响,因此分子特征的测定尤为重要[16]。要完全精确地预测转基因动物的后代遗传稳定性尚有困难,因此要用适宜的观察手段考察目标性状对转基因动物一生及其所产生后代的情况,研究后代与父代母代在遗传上的差异,至少连续追踪不少于2代。另外按照个案分析的原则,对转基因动物可能导致的兽药残留、重金属、毒素等主要污染物的蓄积进行评价。
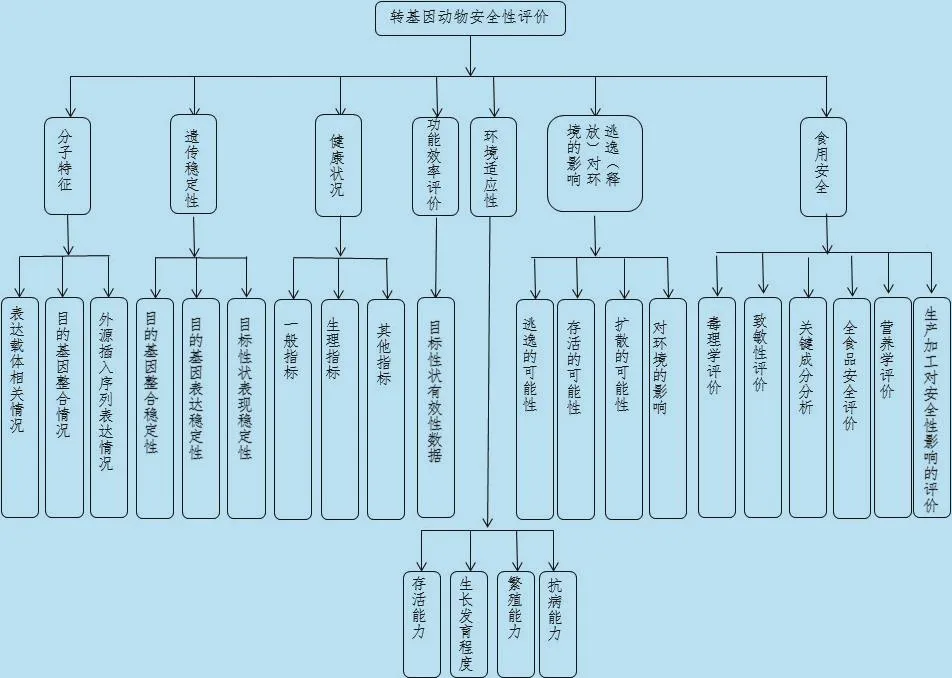
图1 转基因动物安全性评价内容
3 我国转基因动物安全性评价现状
2008年,国家开始实施 “转基因生物新品种培育重大专项”,这大大促进了我国农业转基因生物新品种的培育工作。转基因动物方面是以猪、牛、羊三类动物为重点,以培育抗病、高产、优质、高效的转基因新品种为中心,重点突破功能基因克隆与验证、规模化转基因操作和生物安全评价三大核心技术。2009年,生物育种列入“战略性新兴产业规划”。最近十年的中央一号文件8次提到转基因,强调应该加强农业转基因技术研发和监管,在确保安全的基础上慎重推广。
2002年1月5日农业部令第8号公布《农业转基因生物安全评价管理办法》,2004年7月1日农业部令第38号进行了修订,2016年7月25日农业部第7号令再次进行修订。两次修订,优化了管理机制,规范了评价程序,同时提升评价水平,涉及的内容包括明确研究试验单位第一责任人,要求制定试验操作规程,将转基因生物安全委员会委员任期由3年改为5年,同时规定安委会每年至少开展两次农业转基因生物安全评审,完善了实验监管制度等。2016年第五届安委会成立,共有来自国务院各有关部门推荐的农业、医药、卫生、食品、环境、检测检验等相关领域的75名专家学者(包含14名两院院士),具有广泛的专业代表性和政府权威性(中华人民共和国农业部,2016《农业转基因生物安全评价管理办法》)。这标志着我国转基因安全评价步入了正轨。
目前,我国转基因安全评价本着科学合理、个案审查和逐步的原则,将转基因动物评价等级分为:(1)对人健康和生态环境尚不存在危险,对人健康和生态环境未曾发生过不良影响,或演化成有害生物的可能性极小,或仅用于特殊研究,存活期短,自然环境中仍难以存活;(2)对人健康和生态环境具有低度危险,但通过采取安全控制措施避免其危害;(3)对人健康和生态环境具有中度危险,但通过采取安全控制措施基本上可以避免其危害;(4)对人健康和生态环境具有高度危险,而且尚无适当的安全控制措施来避免其危害。
4 展望
随着科学技术和社会的进步,越来越多的国家开始重视社会、经济和环境的可持续发展,开展以现代生物技术为核心的农业技术革命。美国、日本、澳大利亚等发达国家加强了生物育种领域功能基因的挖掘和利用,跨国公司纷纷抢滩登陆,在我国陆续建立研发机构,关注产业核心技术和产品研发的同时积极向基础研究领域以及产业的上下游延伸。巴西、阿根廷、印度等发展中国家对转基因研发投入成倍增加,势头强劲。我国在取得一系列重大研究进展的同时,也需要时刻保持危机意识和紧迫感。
当前,转基因动物安全性评价主要集中于动物健康、食品安全、环境安全等方面。而转基因动物还不可避免地要面对社会公众的接受认可和伦理道德等问题。获得社会公众的认可,使公众对转基因有一个更为客观公正的评价并传递生物技术安全信息,我们既要通过严谨、准确的科学实验结果予以证明,更需要注重安全评价性中的非科学因素,冷静地去分析和面对[17]。另外,动物福利问题也不容忽视,转基因动物在研究过程中往往很难同时兑现动物福利概念所阐述的5个基本要素(生理、环境、卫生、行为和心理福利),损害它们的健康往往是研究的必经过程[18]。相信随着现代生物技术研究的深入,转基因动物安全性评价将朝着便捷、安全、自动化的方向发展。
参考文献:
[1] Gordon J W,Scangos G A,Plotkin D J,et al.Genetic transformation of mouse embryos by microinjection of purified DNA[J].Proceedings of the National Academy of Sciences,1980,77(12):7 380-7 384.
[2] Palmiter R D,Brinster R L,Hammer R E,et al.Dramatic growth of mice that develop from eggs microinjected with metallothionein-growth hormone fusion genes[J].Nature,1982,300(5893):611-615.
[3] Rusconi S,Schaffner W.Transformation of frog embryos with a rabbit beta-globin gene[J].Proceedings of the National Academy of Sciences,1981,78(8):5 051-5 055.
[4] Rubin G M,Spradling A C.Genetic transformation of Drosophila with transposable element vectors[J].Science,1982,218(4570):348-353.
[5] Spradling A C,Rubin G M.Transposition of cloned P elements into Drosophila germ line chromosomes[J].Science,1982,218(4570):341-347.
[6] Hammer R E,Pursel V G,Rexroad C E,et al.Production of transgenic rabbits,sheep and pigs by microinjection[J].Nature,1985,315(6021):680-683.
[7] Wilmut I,Schnieke A E,McWhir J,et al.Viable offspring derived from fetal and adult mammalian cells[J].Nature,1997,385(6619):810-813.
[8] 严绍颐,陆德裕,杜淼,等.硬骨鱼类的细胞核移植——鲫鱼细胞核和鲤鱼细胞质配合的杂种鱼[J].中国科学(B辑 化学生物学农学医学地学),1984,31(08):729-732.
[9] 魏庆信,樊俊华,李绍章,等.OMT/PGH基因导入湖北白猪后的整合与表达[J].湖北农业科学,1992,31(01):29-32.
[10] 罗军,范必勤.家兔显微受精研究[J].江苏农业学报,1993(02):1-5.
[11] Yang P,Wang J,Gong G,et al.Cattle Mammary Bioreactor Generated by a Novel Procedure of Transgenic Cloning for Large-Scale Production of Functional Human Lactoferrin[J].Plos One,2008,3(10):e3 453.
[12] Wu X,Ouyang H,Duan B,et al.Production of cloned transgenic cow expressing omega-3 fatty acids[J].Transgenic Research,2012,21(3):537-543.
[13] Wang X,Yu H,Lei A,et al.Generation of gene-modified goats targeting MSTN and FGF5 via zygote injection of CRISPR/Cas9 system[J].Scientific Reports,2015,5:13 878.
[14] Zeng F,Li Z,Zhu Q,et al.Production of functional human nerve growth factor from the saliva of transgenic mice by using salivary glands as bioreactors[J].Scientific Reports,2017,7:41 270.
[15] Kochhar H P,Evans B R.Current status of regulating biotechnology-derived animals in Canada-animal health and food safety considerations[J].Theriogenology,2007,67(1):188-197.
[16] 汪亮,崔文涛,刘娣,等.可遗传与非可遗传构件应用与转基因动物食品安全评价介绍[J].中国畜牧兽医,2009,36(1):151-154.
[17] 贺月静.转基因生物安全评价中的非科学因素探究[D].郑州:河南师范大学,2013.
[18] 栗景蕊,贺争鸣.转基因动物应用的福利问题及欧盟的相关对策[J].实验动物科学,2014,31(6):56-61.

