索非布韦对治疗慢性丙肝及缓解肝脏纤维化的临床研究
陈 安,杨振宇,杜锡林,代柏树,鲁建国
(空军军医大学唐都医院普通外科,西安 710038;*通讯作者,E-mail:lujguo@hotmail.com)
丙型肝炎病毒(hepatitis C virus,HCV)是引起慢性丙型病毒性肝炎(chronic hepatitis C,CHC)的病原体。其中约80%的患者能够自愈,但是约有20%的患者体内持续存在HCV而成为慢性感染[1,2]。据报道,WHO统计全球约有1.95亿人感染HCV,全球发病率约为3%,而国内感染率大致在3.2%,且呈全球性流行[3]。发生慢性丙型肝炎的特点是症状隐匿,有些丙肝患者可能在患病后的20年内不发生任何症状,容易让人忽略[4]。并且人们对其认知程度低,诊断率低,接受抗病毒治疗的比例也低,统计仅不到2%的患者进行过抗病毒治疗[5]。慢性肝炎一旦形成,很难治愈,且极易发展为肝硬化或肝癌[6]。CHC患者预后差,生存率低,已经是全球性的公共卫生问题[7]。
目前,针对慢性丙肝患者的管理以及治疗,标准的治疗方案即为干扰素α(interferon alfa,IFN-α)或者为聚乙二醇干扰素α(peginterferon alfa,PEG-IFN α)两种药物分别联合利巴韦林(RBV)进行干预治疗[8]。但是无论哪种方案,都存在价格昂贵、药品不良反应(ADRs)几率大的问题[9],与此同时上述方案用于治疗基因2型和3型HCV感染者,持久病毒学应答(sustained virological response,SVR)仅仅为80%。而对基因1型HCV感染者的SVR只有约50%。并且在所有的治疗中,干扰素或者聚乙二醇干扰素都禁忌用于已发生肝脏纤维化的患者中,所以对所有已发生肝硬化的患者并没有统一有效的治疗方案[10]。综上所述,急需一种新的治疗方案,降低不良反应发生的同时可以应用于肝脏纤维化的人群中,使得所有患者均可获益[11]。
索非布韦(sofosbuvir,SOF)是新上市治疗丙肝的药物[12],是一种不需要与干扰素联合即可产生作用的新型药物。HCV病毒中NS5B RNA聚合酶负责HCV的RNA链的复制,是HCV病毒增殖的关键酶[13],SOF能够有效针对此聚合酶。本研究目的为探讨索非布韦对慢性丙肝患者血清病毒学应答率以及安全性的研究。
1 资料与方法
1.1 一般资料
本研究选取2016-11~2017-09初诊于唐都医院普外科的未合并肝硬化的慢性丙肝患者80例,采用随机数字表法,分为对照组及观察组,两组各40例。组间性别、年龄、BMI、谷草转氨酶(AST)、谷丙转氨酶(ALT)、总胆红素(TB)、总胆固醇(TC)、谷氨酰转移酶(GGT)等基线资料水平差异无统计学意义(P>0.05,见表1),具有可比性;同时选取同期合并发生肝硬化的丙肝患者40例。本研究经医院伦理委员会批准执行,患者或其家属均知情同意并签订知情同意书。
表1观察组与对照组一般资料的比较
Table1Comparisonofclinicaldatabetweenobservationgroupandcontrolgroup
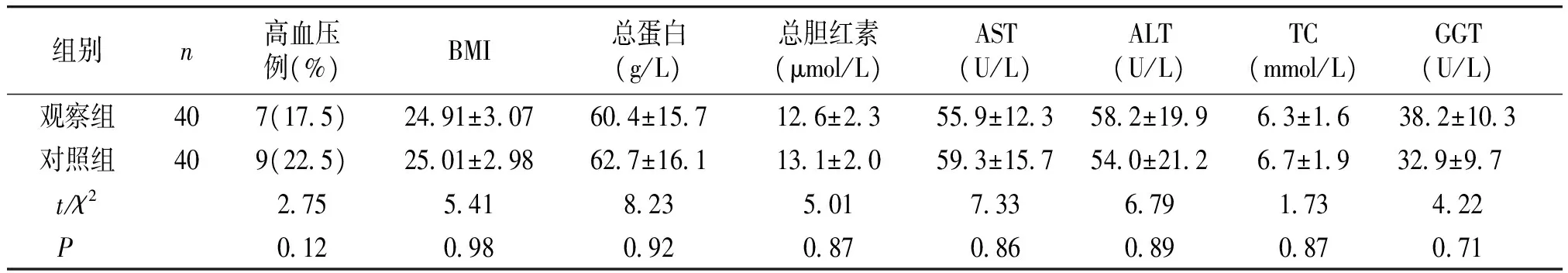
组别n高血压例(%)BMI总蛋白(g/L)总胆红素(μmol/L)AST(U/L)ALT(U/L)TC(mmol/L)GGT(U/L)观察组407(175)2491±307604±157126±23559±123582±19963±16382±103对照组409(225)2501±298627±161131±20593±157540±21267±19329±97 t/χ2275541823501733679173422P 012098092087086089087071
两组间相同指标比较,均P>0.05
1.2 纳入及排除标准
诊断符合中华医学会肝病学会2004年制定的《丙型肝炎防治指南》标准。同时根据要求所有纳入研究的患者需满足:血清HCV抗体阳性>6个月;HCV-RNA≥80 IU/ml;无妊娠期女性;无严重的肝、肾及其他疾病;排除其他肝炎病毒重叠感染、重症肝炎、自身免疫性肝病、药物性肝炎、寄生虫肝病、酒精性肝病等患者。
1.3 治疗方法
将非合并肝硬化的慢性丙肝患者随机数字法分为观察组及对照组,对照组患者采用皮下注射聚乙二醇干扰素α-2a 180 μg/周,口服利巴韦林1 000 mg/d;观察组采用口服索非布韦400 mg/d,口服利巴韦林1 000 mg/d;两组联合应用12周。同时选取合并肝硬化代偿期的慢性丙肝患者40例,均采用口服索非布韦400 mg/d,口服利巴韦林1 000 mg/d方案连续12周[14]。
1.4 观察指标
对所有患者进行血生化检查,均清晨空腹采血,对比分析用药前后患者血清中HCV-RNA定量水平;治疗结束时病毒学应答(end-treatment virus response,ETVR)情况,即治疗结束时血清HCV-RNA含量小于80 IU/ml的人数;持续病毒学应答(sustained virological response,SVR),即治疗结束后至少继续随访12周查血清HCV-RNA定量检测小于80 IU/ml;同时统计服药期间患者出现的不良反应,如发热、胃肠道不良反应、头痛、乏力、白细胞及红细胞的减少;提取合并肝硬化患者空腹静脉血,离心机3 000 r/min,5 min提取血清,用电化学发光免疫分析仪(美国拜耳)检测HA(郑州安图绿科生物公司试剂)水平,利用放射免疫试剂盒(北京福润康生物公司)检测血清PCⅢ水平,判断肝脏纤维化水平,同时判断血清病毒学应答情况。
1.5 统计学方法
2 结果
2.1 非合并肝硬化患者服药前后血生化指标比较
患者在服药12周后检测血清中HCV-RNA水平统计病毒学应答情况,对照组转阴率为82.5%,观察组为95.0%,观察组明显高于对照组,差异具有统计学意义(P<0.01);在停药12周后第一个周六复查病毒水平,统计持续应答水平,对照组为72.5%,观察组为90.0%,观察组优于对照组(P<0.01)。
2.2 两组间不良反应发生率比较
服药期间,观察组有21例出现不良反应,发生率为67.5%。而对照组40例均有不同程度的不良反应发生,发生率达100%,观察组发生不良反应明显少于对照组(见表3)。
2.3 合并肝硬化患者服药前后肝脏纤维化指标水平变化
给予合并肝硬化患者服用索非布韦联合利巴韦林治疗24周,检测患者血清中Ⅲ型前胶原(PCⅢ)和透明质酸(HA)水平,发现治疗后PCⅢ及HA水平均显著低于治疗前,差异有统计学意义(P<0.01,见表4)。检测患者血清病毒应答水平,有37例血清病毒呈阴性,转阴率达到92.5%。
表2观察组与对照组服药前后指标比较
Table2Comparisonofclinicalindexesbeforeandaftertreatmentbetweentwogroups

组别n病毒转阴率[例(%)]AST(U/L)ALT(U/L)治疗前治疗后治疗前治疗后持续转阴率[例(%)]观察组4038(950)#559±123376±176∗582±199407±153∗36(900)#对照组4033(825)593±157395±164∗540±212412±175∗29(725)
同组与治疗前比较,*P<0.01;与对照组比较,#P<0.05
表3观察组与对照组服药后出现不良反应比较例(%)
Table3Comparisonofadverseeffectsaftertreatmentbetweentwogroupscases(%)

组别发热 寒战 乏力 头痛 白细胞减低 血小板减少 总发生率 对照组33(825)21(525)26(650)5(125)5(125)11(275)40(1000)观察组17(425)∗13(325)∗15(375)∗7(175)∗6(150)∗5(150)∗ 21(675)∗
与对照组比较,*P<0.05
表4合并肝硬化患者服药后指标变化
Table4ChangesofclinicalindexesinHCVpatientswithliverfibrosisbeforeandaftertreatment

组别PCⅢ(μg/L)HA(mg/L)服药前1124±1023165±492服药后 512±79∗1292±614∗
与服药前比较,*P<0.05
3 讨论
随着医疗水平的提高以及检出率的升高,我国患有慢性丙型肝炎的患者高达3%,根据大型临床研究结果显示[15],丙肝病毒有一套特殊的生物学特性,往往可以逃避人体生理性的免疫功能,从而不会清除,形成慢性感染。慢性丙肝患者中,有将近30%的患者存在进展为肝硬化以致肝癌的潜在风险。病毒性肝炎之后发展为病毒性肝硬化,最终导致为肝癌,这病情三步走的传统观念被人们熟知。据报道,所有病毒性肝硬化患者中,每年有超过3%的患者出现癌变,也有超过10%的患者出现肝功能的急剧恶化,经统计,出现肝硬化的患者中,10年的死亡率高达80%[16,17]。
慢性丙肝患者的治疗目标是清除丙肝病毒,控制相关炎症损伤,抑制肝硬化的发生发展,提升患者的生活质量以及生存期。目前公认的是,若在发生肝脏纤维化这一环节甚至之前,能够清除患者慢性丙肝病毒,可以有效控制病情发展,阻断肝脏纤维化的程度加深以及恶性肿瘤的发生几率[18]。目前针对慢性丙肝的治疗,主要生物制剂:如干扰素(IFN)、重组人干扰素(rIFN)、聚乙二醇干扰素等;还有一种是以利巴韦林为代表的小分子药物,作为清除丙肝病毒的一线用药,是鸟苷类的抗病毒药物,常用于呼吸道病毒感染。利巴韦林具有针对DNA、RNA病毒广泛的抗病毒活性。其对肝功的改善以及病毒的抑制有着很好的效果,但是具有病毒转阴率较低、稳定性差、反弹率较高等问题。
目前临床治疗丙肝病毒的关注点仍聚焦于病毒的RNA非结构蛋白编码区域。聚乙二醇干扰素是聚乙二醇蛋白修饰剂与干扰素α-2b结合而成。特点是皮下注射后可延长吸收时间,使机体代谢缓慢,血清半衰期延长,是普通干扰素的10倍[19]。临床研究表明,聚乙二醇干扰素联合应用可以有效地将患者血清病毒水平转阴,并且产生持续性病毒学应答,重新转阳率低。但此种方案仍存在多种问题,报道发现聚乙二醇干扰素的副作用与普通干扰素类似,发生不良反应率以及严重程度也未有改观。常见的有发热、类感冒症状、白细胞及红细胞降低、肝脏纤维化等[20,21],因聚乙二醇干扰素有诱发肝脏纤维化的可能,所以是病毒性肝硬化患者的禁忌。
索非布韦(sofosbuvir,SOF)是一种核苷聚合酶抑制剂,是已上市针对HCV NS5B RNA聚合酶的第一种药物[22]。这个聚合酶是HCV在RNA链复制过程中的关键酶。SOF正是能够通过抑制NS5B聚合酶的合成,从而有效控制了HCV的复制。相比传统干扰素联合利巴韦林治疗方案,首先SOF联合利巴韦林的治疗周期明显缩短[23],传统方案中治疗周期为48周,但SOF将治疗周期缩短至12周,并且在病毒清除率较传统方案更有效,在服药12周后,SOF方案患者病毒清除率为95.0%,略高于传统方案的82.5%。并且在持久血清应答水平上优于传统方案。SOF是一种可以不用联合干扰素就可发挥重大病毒清除作用的口服用药,可以有效地简化抗病毒治疗方案,并且对初次治疗或既往治疗失败的患者均有效。相比传统干扰素治疗方案,SOF方案最明显的即为相对较少的不良反应发生率。在干扰素治疗方案中,最常见的包括了疲劳、头疼、恶心以及失眠,几乎所有的治疗中患者都或多或少存在不同症状,不良反应发生率几乎达到100%。而SOF方案中这类不良反应发生率明显较少,所有治疗患者发生不良反应21例(67.5%)。慢性肝炎症状少,表现隐匿,大多数患者发现时已不是早期。有的患者甚至于出现肝脏纤维化才发现病情,肝硬化的发生、发展是慢性丙肝患者重要的阶段,严重威胁患者的生活质量。肝硬化伴随肝功能失代偿,造成的腹水、肝性脑病、电解质紊乱等,严重地影响着患者的生命安全。但干扰素方案最大的禁忌证即为肝硬化,这意味着出现肝硬化的患者面临无药可用。但是SOF可安全用于肝脏纤维化的患者,并且用药12周后,患者血清转阴率高达92.5%,通过PCⅢ以及HA的评估,也证实患者的肝脏纤维化症状得以明显改善。
本次研究,将慢性肝炎的治疗药物SOF联合利巴韦林与传统聚乙二醇干扰素联合利巴韦林进行全方位的比较,包括病毒清除率、持久应答率、安全性、肝功指标以及对肝脏纤维化患者的意义等。在服药12周后SOF在血清病毒转阴率以及持久应答率上明显优于干扰素,但也有可能是因为SOF的治疗周期为12周,而干扰素治疗周期仅12周并不达标。与此同时,在肝硬化患者中,SOF同样有效,不仅使得患者血清病毒转阴率极高,并且通过肝脏纤维化评价指标发现SOF对患者肝脏纤维化的发生发展有着重要的作用,为肝脏纤维化的患者带来了诊疗思路。但是本文仍有许多不足之处,譬如患者均来自我院,病源存在一定地域限制,有一定的局限性。纳入人数较少等。同时,在患者筛选以及分组上,存在一定的选择性偏倚。对此,需要设计一种前瞻性研究,利用双盲,避免混杂与偏倚,同时扩大样本量采用多中心研究。
参考文献:
[1] Saez-Gonzalez E, Vinaixa C, San JF,etal. Impact of hepatitis C virus(HCV) antiviral treatment on the need for liver transplantation(LT)[J]. Liver Int,2017,27:1-6.
[2] Teitzel G. Timeline: targeted treatment of hepatitis C virus[J]. Cell,2016,167(1):288.
[3] Esmaeili A, Mirzazadeh A, Morris MD,etal. The effect of female sex on hepatitis C incidence among people who inject drugs: results from the international multi-cohort InC3 collaborative[J]. Clin Infect Dis,2017,66(1):20-28.
[4] Ichikawa T, Miyaaki H, Miuma S,etal. Hepatitis C virus-related symptoms, but not quality of life, were improved by treatment with direct-acting antivirals[J].Hepatol Res,2017,24(13):1-8.
[5] Liu X, Shen JJ, Lee JL,etal. Cost-Effective but Unaffordable and Unequal Hepatitis C Treatment in the US[J]. Am J Gastroenterol,2017,112(11):1749-1760.
[6] 张玲荣,郝彦琴,任姣龙,等.慢性乙肝患者肝纤维化与肝硬度、超声量化指标、血清肝纤维化指标的相关性[J].山西医科大学学报,2015,46(1):45-48.
[7] Marot A, Henrion J, Knebel JF,etal. Alcoholic liver disease confers a worse prognosis than HCV infection and non-alcoholic fatty liver disease among patients with cirrhosis: An observational study[J]. PLoS One,2017,12(10):e186715.
[8] Piekarska A, Koslinska-Berkan E, Wojcik K,etal. Efficacy and direct costs of chronic hepatitis C treatment with first generation NS3/4A protease inhibitors in a real life population[J]. Clin Exp Hepatol,2016,2(4):133-137.
[9] Nakamura Y, Imamura M, Kawakami Y,etal. Efficacy and safety of daclatasvir plus asunaprevir therapy for chronic hepatitis C patients with renal dysfunction[J]. J Med Virol,2017,89(4):665-671.
[10] Maan R, van der Meer AJ, Hansen BE,etal. Risk of infections during interferon-based treatment in patients with chronic hepatitis C virus infection and advanced hepatic fibrosis[J]. J Gastroenterol Hepatol,2015,30(6):1057-1064.
[11] 张美霞,徐细明.乙肝病毒感染与B淋巴瘤患者利妥昔单抗联合CHOP化疗后的临床观察[J].山西医科大学学报,2015,46(7):613-616.
[12] Buggisch P, Vermehren J, Mauss S,etal. Real-world effectiveness of 8 weeks treatment with ledipasvir/sofosbuvir in chronic hepatitis C[J].J Hepatol,2017,11(19):456-464.
[13] Brancaccio G, Sorbo MC, Frigeri F,etal. Treatment of Acute Hepatitis C With Ledipasvir and Sofosbuvir in Patients with Hematological Malignancies Allows Early Re-start of Chemotherapy[J]. Clin Gastroenterol Hepatol,2017,28(35):689-696.
[14] He X, Hopkins L, Everett G,etal. Safety and efficacy of ledipasvir/sofosbuvir on hepatitis C eradication in hepatitis C virus/human immunodeficiency virus co-infected patients[J]. World J Hepatol,2017,9(30):1190-1196.
[15] Whiteley D, Whittaker A, Elliott L,etal. Hepatitis C in a new therapeutic era: Recontextualising the lived experience[J]. J Clin Nurs,2017,27(14):68-77.
[16] Majumdar A, Kitson MT, Roberts SK. Systematic review: current concepts and challenges for the direct-acting antiviral era in hepatitis C cirrhosis[J]. Aliment Pharmacol Ther,2016,43(12):1276-1292.
[17] Obolonczyk L, Siekierska-Hellmann M, Wisniewski P,etal. Epidemiology, risk factors and prognosis of Interferon alpha induced thyroid disorders. A Prospective Clinical Study[J]. Postepy Hig Med Dosw (Online),2017,71:842-849.
[18] Marot A, Henrion J, Knebel JF,etal. Alcoholic liver disease confers a worse prognosis than HCV infection and non-alcoholic fatty liver disease among patients with cirrhosis: An observational study[J]. PLoS One,2017,12(10):e186715.
[19] Seo K, Kim SK, Kim SR,etal. Comparison of Sofosbuvir Plus Ribavirin Treatment with Pegylated Interferon Plus Ribavirin Treatment for Chronic Hepatitis C Genotype 2[J]. Dig Dis,2017,35(6):541-547.
[20] Hameed MA, Mehmood A, Farooq MA,etal. Hypothyroidism In Hepatitis C Patients On Pegylated Interferon Therapy[J]. J Ayub Med Coll Abbottabad,2016,28(4):706-708.
[21] Kawase K, Kondo K, Saito T,etal. Risk factors and clinical characteristics of the depressive state induced by pegylated interferon therapy in patients with hepatitis C virus infection: A prospective study[J].Psychiatry Clin Neurosci,2016,70(11):489-497.
[22] Backus LI, Belperio PS, Shahoumian TA,etal. Comparative effectiveness of ledipasvir/sofosbuvir+/-ribavirin vs. ombitasvir/paritaprevir/ritonavir+dasabuvir+/-ribavirin in 6961 genotype 1 patients treated in routine medical practice[J]. Aliment Pharmacol Ther,2016,44(4):400-410.
[23] Ciesek S, Proske V, Otto B,etal. Efficacy and safety of sofosbuvir/ledipasvir for the treatment of patients with hepatitis C virus re-infection after liver transplantation[J]. Transpl Infect Dis,2016,18(3):326-332.

