一种桔小实蝇Minus-C气味结合蛋白的分子克隆和结合特征分析
吴 健,张贺贺,杨燕川,陈 湜,杨建全,王 波,陈家骅
(福建农林大学 益虫研究所,福建 福州 350002)
桔小实蝇(Bactroceradorsalis)可危害40多个科的多种水果和蔬菜,是一种世界危害性害虫。目前,桔小实蝇的防治采取综合防治的方法,主要包括引诱剂、蛋白饵剂、生物防治和不育雄虫等手段[1-2],以达到控制桔小实蝇数量的目的。其中行为调控技术的开发和利用在桔小实蝇综合防治中起着重要的作用[3],而对其气味结合蛋白基因的研究,将有助于我们对桔小实蝇的防控。
气味结合蛋白(odorent binding proteins,OBPs)在昆虫的生理和行为方面起着重要的作用[4],是昆虫识别外界环境的第一步生化反应[5]。大部分OBP的保守结构域都具有6个高度保守的半胱氨酸位点,但还有一类非典型的OBP,其拥有多于或少于6个的半胱氨酸位点。因此,根据保守的半胱氨酸位点个数,可以将OBP分为“Classic”、“Dimer”、“Minus-C”、“Plus-C”、“Atypical”五大类[7]。其中“Minus-C”OBP缺少C2和C5两个半胱氨酸[8-9]。
近年来,随着分子生物学技术的发展,OBP基因的研究逐渐增多,OBP蛋白可以选择性结合配基气味分子的研究已经在很多昆虫中完成。如鳞翅目中的小菜蛾Plutellaxylostella[7]、膜翅目中的中华蜜蜂ApisceranaceranaFabricius[10]、半翅目中的绿盲蝽Apolyguslucorum[11]、双翅目中的冈比亚按蚊Anophelesgambiae[12]等。在双翅目昆虫中,OBP基因的研究虽然比较多,但大量的研究仅仅停留在基因的鉴定和表达分析上,关于蛋白结构、结合特征和功能上的研究却很少,特别是“Minus-C”OBP的研究甚少,目前已报道的有枣实蝇CarpomyavesuvianaCosta CvcoOBP2和CvcoOBP5[13],二化螟ChilosuppressalisCsupOBP1[14],棉铃虫HelicoverpaarmigeraHubner HarmOBP17和HarmOBP18[15]等。据报道,“Minus-C”OBP氨基酸序列排列方式通常是Xn-C1-X30-C2-X39-C3-X16-C4-Xn(X可代表任意氨基酸)[16],在其三维结构的研究中,最先被报道的是西方蜜蜂ApismelliferaLinnaeus AmelOBP14[17],随后其他昆虫的“Minus-C”OBP的三维结构也有报道,如云斑天牛BhorOBPm2[18]。
桔小实蝇OBP的研究同样比较少,其中大部分也仅对桔小实蝇OBP基因进行了鉴定和表达谱分析[19-22],共发现7种Minus-COBP基因,根据其组织表达分析可知“Minus-C”OBP在腹部大量表达或在所有组织中微量表达。而Chen等[23]只对一个普通气味结合蛋白进行了功能分析,“Minus-C” OBP的结合特征和功能研究在桔小实蝇中没有被报道。而OBP的结合特征有助于桔小实蝇引诱物的筛选,从而配制出具有良好引诱作用的诱剂。因此,在前人的基础上对桔小实蝇的一个“Minus-C”OBP基因进行了克隆、体外原核表达和不同寄主植物挥发物的结合能力测定,对其结合能力进行了分析。
1 材料与方法
1.1 实验虫源
实验昆虫为福建农林大学益虫研究所所饲养的桔小实蝇(敏感品系)。幼虫与成虫都用实验室研制的人工饲料喂养。饲养温度(22±1)℃,光周期14L∶10D,湿度60%~70%。
1.2 主要试剂
RNA提取试剂盒RNAprep Pure Tissue Kit,DNA胶回收试剂盒EasyPure®Quick Gel Extraction Kit,质粒提取试剂盒TransTaq®HiFi DNA polymerase,pEASY®-T1 Clone Vector,BL21(DE3)均购自北京全式金;限制性内切酶NcoI和XhoI购自TaKaRa;引物由铂尚生物技术(上海)有限公司合成;荧光探针N-phenyl-1-naphthylamine(简称1-NPN)购自福州都拜特生物技术有限公司;寄主植物挥发物如表1所示,均购自上海麦克林生化科技有限公司。
1.3 引物的设计及合成
根据GenBank上桔小实蝇OBP1序列(登录号为KC559112),利用Primer Premire 5.0设计引物OBP1-F、OBP1-R(表2),并送自到铂尚生物技术(上海)有限公司合成。
1.4 总RNA的提取及cDNA第一链的合成
取桔小实蝇雌雄虫各一只(羽化15 d,不考虑其交配情况),在液氮中用研磨棒反复研磨后,用RNAprep Pure Tissue Kit提取总RNA。cDNA的合成参照cDNA Synthesis SuperMix说明书进行。第一链cDNA合成后分管保存于-20 ℃冰箱或用于下一步实验。

表1 候选配基
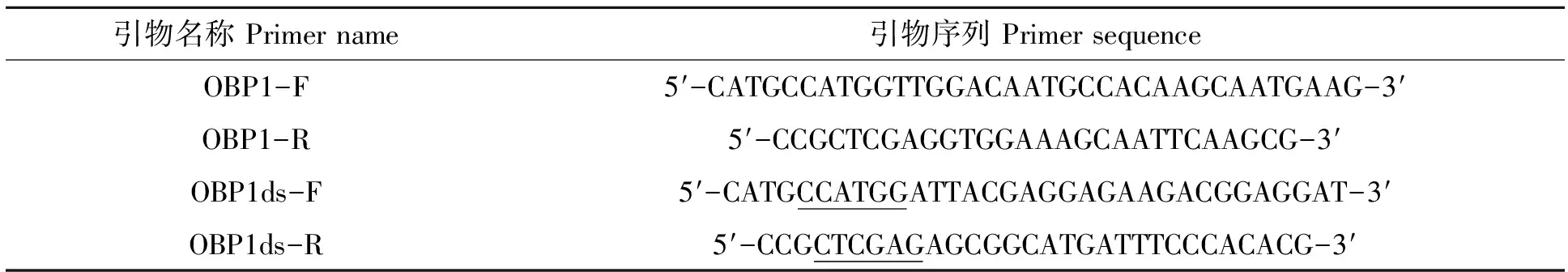
表2 实验所用引物
1.5 桔小实蝇气味结合蛋白的克隆、序列分析和进化树构建
以cDNA为模板,PCR扩增获得桔小实蝇OBP1a基因序列。PCR反应条件:95 ℃预变性4 min,95 ℃变性30 s,59 ℃退火30 s,72 ℃延伸30 s,30个循环,72 ℃延伸5 min,12 ℃保存。电泳胶回收后连接至pEASY®-T1 载体上,并转化到Trans1-T1感受态细胞中,经培养后,挑单克隆菌进行菌液PCR检验,最后将验证正确的菌液送至铂尚生物公司测序。
利用在线软件Expasy(http://web.expasy.org/translate/)和(http://web.expasy.org/protparam/)进行蛋白翻译、ORF预测和理化性质分析;利用SignalP 4.1在线软件(http://www.cbs.dtu.dk/services/SignalP/)进行信号肽预测;利用BLAST(http://blast.ncbi.nlm.nih.gov/BLAST/)工具进行序列相似性搜索,并利用MEGA5.0软件中的最小进化法(1 000次抽样分析)构建基于氨基酸序列的系统进化树。
1.6 重组质粒的构建
根据序列分析结果设计去信号肽引物OBP1ds-F、OBP1ds-R(表2),并在引物上下游加上酶切位点NcoI和XhoI(下划线表示),利用PCR扩增获得去信号肽序列,PCR反应条件:95 ℃预变性4 min,95 ℃变性30 s,62 ℃退火30 s,72 ℃延伸30 s,30个循环,72 ℃延伸5 min,12 ℃保存。电泳胶回收,测浓度后连接至pEASY®-T1 载体上,并转化到Trans1-T1感受态细胞中,经培养后挑取单克隆菌进行菌液PCR检验,最后将检验正确的菌液送至铂尚生物公司测序,并返还质粒。将测序正确的质粒与pET28a载体分别经NcoI和XhoI酶切,之后用T4DNA连接酶连接。最后将连接产物转化到大肠杆菌BL21(DE3)感受态细胞中。过夜培养后,挑取阳性克隆菌落,经菌液PCR验证成功后用于原核表达。
1.7 重组蛋白表达条件的优化和纯化
将克隆菌接种到含卡那霉素(kanamycin)的LB液体培养基(工作浓度为50 μg/mL)中,37 ℃过夜培养。次日,按1∶100的比例,将活化菌接种到10 mL LB液体培养基中,37 ℃ 200 r/min震荡培养2~3 h至OD600=0.6时,添加IPTG至终浓度0.1,0.3,0.5,0.7,0.9 mmol/L,8 h后收集菌体;0.5 mmol/L IPTG浓度下接种活化菌,于0,2,4,6,8 h收集1 mL菌体,共5管;0.5 mmol/L IPTG浓度下接种活化菌,在30 ℃条件下诱导6 h。将收集的菌液用PBS溶液悬浮,加溶菌酶(工作浓度为250 mg/mL)过夜溶解,再经超声波(200 W,持续5 s,间隔5 s)破碎20 min。12 000 r/min离心20 min分别收集包涵体和上清。最后,利用聚丙烯酰胺凝胶电泳确定其表达形式,若目的蛋白在上清中,可直接用于纯化,反之则需要对包涵体进行变性和复性处理。纯化:将蛋白液离心后,过镍柱,使目的蛋白吸附到柱子上,用不同浓度的咪唑(20,40,80,150,200,300,400 mmol/L)洗脱缓冲液进行洗脱,经SDS检测后,用透析袋对含有目的蛋白的洗脱液进行过夜透析。
1.8 桔小实蝇OBP1重组蛋白的配基结合实验
BdorOBP1a蛋白与1-NPN的结合曲线测定:取2 mL(用50 mmol/L Tris缓冲液稀释至2 μmol/L)蛋白溶液于荧光比色皿中,依次添加1-NPN溶液(甲醇溶解),使其浓度从2~20 μmol/L依次递增,每次反应时间为2 min,记录在337 nm激发波长下的荧光值,重复3次,并计算出该蛋白与1-NPN的结合常数。
本实验共选取了21种寄主植物挥发物,用甲醇溶液将其稀释到2 mmol/L。在配基结合实验中,向比色皿中加入蛋白与1-NPN的混合溶液(终浓度均为2 μmol/L),静止2 min,使其充分反应,测定其在337 nm激发波长下的荧光值,然后挥发物依次添加到比色皿中,使其浓度从2~16 μmol/L依次递增,每次反应时间为2 min,记录荧光值,对于荧光值有明显下降趋势的气味标样,再进行2次重复测定。根据公式计算配基的解离常数Ki(Ki=IC50/[1+(1-NPN)/K1-NPN]),其中IC50为配基替换50%探针时的浓度,(1-NPN)为未结合1-NPN浓度,K1-NPN为OBP与1-NPN复合物的结合常数[24]。
1.9 桔小实蝇对挥发物的行为反应
实验选取结合能力较好的挥发物进行测试,用甲醇将其稀释到100 μmol/L。测试小笼(30 cm×30 cm×30 cm不锈钢骨架加100目尼龙网)中放入40头性成熟的成虫(已饥饿处理、雌雄比为1∶1),其上放一含水的海绵,每笼放置两个诱集瓶,分别添加样品和对照(甲醇溶液)各1 mL,测试时间为24 h,统计诱集瓶中实蝇的数量,重复3次。
1.10 数据处理
所得数据采用SPSS软件中的单因数方差分析。
2 结果与分析
2.1 桔小实蝇气味结合蛋白基因的cDNA克隆及序列分析
以第一链cDNA为模板,扩增得到一条特异性条带,测序结果表明该片段大小为480 bp。通过序列对比发现与GenBank上的基因序列(登录号:KC559112)相似性为98%。蛋白序列相似性为99%,有两个氨基酸不同。
BdorOBP1a开放阅读框(open reading frame,ORF)长480 bp,编码159个氨基酸,具有4个保守的半胱氨酸残基(图1),是一个Minus-COBP基因,缺少C2、C5两个保守的半胱氨酸。BdorOBP1a的预测分子量为18.77 ku,等电点为5.68,成熟肽的分子量为16.9 ku。

下划线表示为信号肽序列,方框内表示为保守的半胱氨酸,星号表示为终止密码子,着重号表示为变异的氨基酸 The predicted signal peptide sequence is underlined,conserved cysteines are boxed,stop codon is indicated with an asteriskand mutant amino acids are indicated with bullets.图1 桔小实蝇BdorOBP1a基因的核酸及氨基酸序列Fig.1 Nucleotide and amino acid sequences of the BdorOBP1a gene of Bactrocera dorsalis

图2 BdorOBP1a与其它昆虫Minus-C OBPs序列对比Fig.2 Alignment of BdorOBP1a with Minus-C OBPs from other insects

OBPs序列来源,BdorOBP1:桔小实蝇,双翅目;BlatOBP99a:辣椒实蝇,双翅目;BoleOBP99a:橄榄果蝇,双翅目;ZcucOBP99a:瓜实蝇,双翅目;ZtauOBP99a:南亚实蝇,双翅目;CcapOBP99a:地中海实蝇,双翅目;CvesOBP2:枣实蝇,双翅目;RzepOBP99ax1:苹果实蝇,双翅目;RzepOBP99ax2:苹果实蝇,双翅目;AfraOBP8a:按实蝇,双翅目;AoblOBP8a:西印度按实蝇,双翅目;ScalOBP99b:厩螫蝇,双翅目;MdomOBP99b:家蝇,双翅目;GmorOBP22:刺舌蝇,双翅目;CstyOBP:幽暗丽蝇,双翅目;DplaOBP20:灰地种蝇,双翅目;DwilOBP8a:魏氏果蝇,双翅目;DpseOBP8a:拟暗果蝇,双翅目;DyakOBP8a:亚库巴果蝇,双翅目;DsimOBP8a:拟果蝇,双翅目。各序列名称后为序列的GenBank登陆号,本实验克隆OBP用实心三角标出The origin of OBPs sequence,BdorOBP1:Bactrocera dorsalis,Dpitera;BlatOBP99a:Bactrocera latifrons,Dpitera;BoleOBP99a:Bactrocera oleae,Dpitera;ZcucOBP99a:Bactrocera cucurbitae,Dpitera;ZtauOBP99a:Zeugodacus tau,Dpitera;CcapOBP99a:Ceratitis capitata,Dpitera;CvesOBP2:Carpomay vesuviana,Dpitera;RzepOBP99ax1:Rhagoletis zephyria,Dpitera;RzepOBP99ax2:Rhagoletis zephyria,Dpitera;AfraOBP8a:Anastrepha fraterculus,Dpitera;AoblOBP8a:Anastrepha obliqua,Dpitera;ScalOBP99b:Stomoxys calcitrans,Dpitera;MdomOBP99b:Musca domestica,Dpitera;GmorOBP22:Glossina morsitans,Dpitera;CstyOBP:Calliphora stygia,Dpitera;DplaOBP20:Delia platura,Dpitera;DwilOBP8a:Drosophila willistoni,Dpitera;DpseOBP8a:Drosophila pseudoobscura,Dpitera;DyakOBP8a:Drosophila yakuba,Dpitera;DsimOBP8a:Drosophila simulans,Dpitera.The GenBank accession numbers are listed after the sequence names,the cloned OBP in this table is highlighted with a solid triangle图3 基于氨基酸序列构建的Minus-C OBPs的进化树(最小进化法)Fig.3 Minmum-Evolution Tree of Minus-C OBPs based on amino acid sequences
2.2 BdorOBP1a氨基酸序列的比对及系统进化树的分析
对BdorOBP1a序列进行序列相似性搜索,与其他21个氨基酸序列进行对比(图2)表明,所有序列都具有4个保守的半胱氨酸位点,氨基酸序列一致性在33%~96%。序列一致性最高的是辣椒实蝇BactroceralatifronsBlatOBP99a(GenBank登录号:LOC108972842),最低的是拟果蝇DrosophilasimulansDsimOBP8a(GenBank登录号:KMZ08930)和亚库巴果蝇DrosophilayakubaDyakOBP8a(GenBank登录号:XM_002101474)。
采用MEGA的最小进化法对双翅目2个科20种昆虫的20个Minus-C OBP构建的进化树表明(图3),桔小实蝇与同科的15种昆虫聚为一类,分别为辣椒实蝇、橄榄果蝇、瓜实蝇、南亚实蝇、地中海实蝇、枣实蝇、苹果实蝇、按实蝇、西印度按实蝇、厩螫蝇、家蝇、刺舌蝇、幽暗丽蝇、灰地种蝇,剩余4中昆虫聚为另一类,分别为魏氏果蝇、拟暗果蝇、亚库巴果蝇、拟果蝇。
2.3 pET-OBP1重组蛋白的表达及纯化
不同IPTG浓度的诱导结果[图4(A):1-6泳道]表明,BdorOBP1a的表达不随IPTG浓度的变化而改变;不同时间的诱导结果[图4(B):7-11泳道]表明,4 h或6 h的诱导表达量最高;不同温度的表达结果[图4(C):12-14泳道]显示,30 ℃条件下的表达量高于37 ℃。重组蛋白表达模式结果[图5(A):1-2泳道]显示,目的蛋白主要集中在包涵体中。蛋白纯化结果[图5(B):3-11泳道]显示,目的蛋白在120 mmol/L咪唑洗液下,洗脱情况最佳。
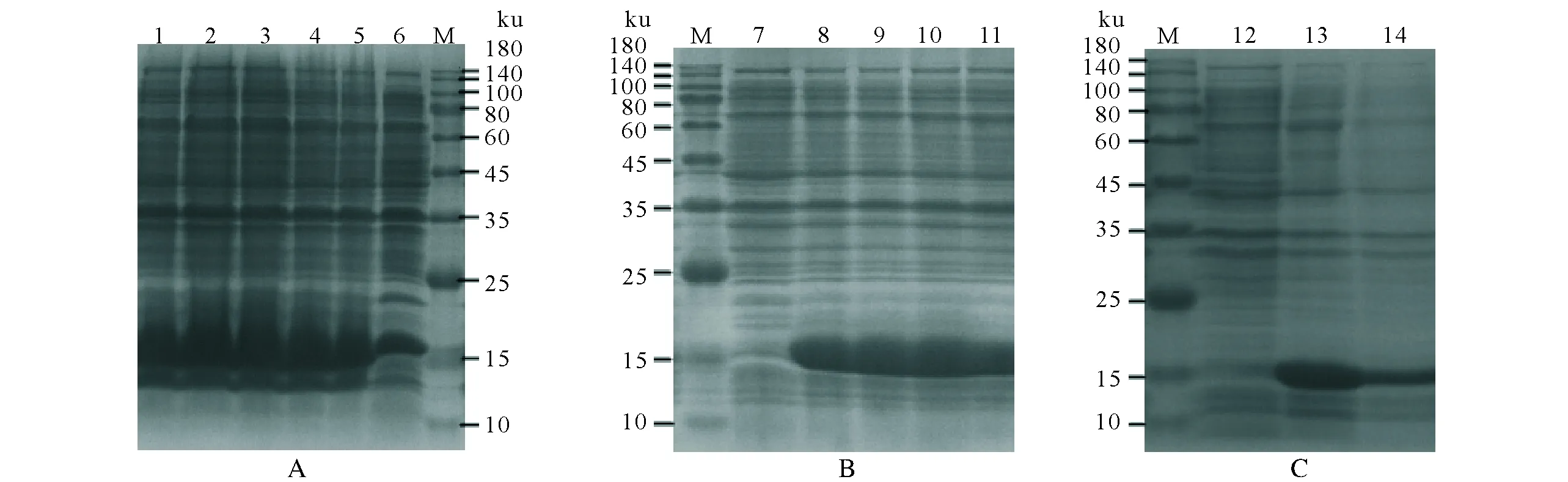
M:蛋白分子量标准;1~6:IPTG浓度分别为0.9,0.7,0.5,0.3,0.1,0 mmol/L的表达产物;7~11:分别为IPTG诱导0,2,4,6和8h的表达产物;12:未经IPTG诱导的表达产物;13~14:分别为30和37 ℃下的表达产物M:Protein molecular weight marker;1-6:Expression products included by 0.9,0.7,0.5,0.3,0.1and 0 mmol/L of IPTG,respectively;7-11:Expression products included by IPTG for 0,2,4,6 and 8h,respectively;12:Expression products non-induced by IPTG;13-14:Expression products included by IPTG at 30 and 37℃,respectively图4 重组桔小实蝇气味结合蛋白BdorOBP1a诱导表达IPTG浓度(A)、诱导时间(B)和诱导温度(C)的优化Fig.4 Optimization of IPTG concentration(A),induction time(B)and induction temperature(C)in induced expression of the recombinant BdorOBP1a
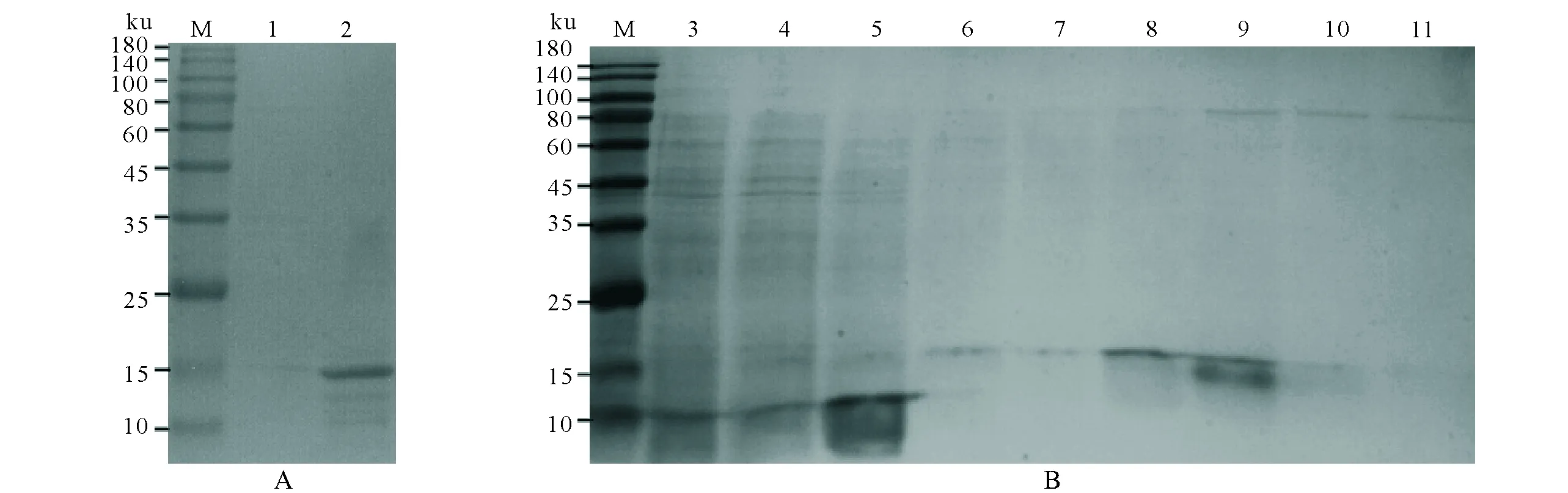
M:蛋白分子量标准;1~2:分别为pET-BdorOBP1a的上清与包涵体;3~5:分别为样品原液,流出液和洗涤液;6~11:分别为40,80,120,160,200,300 mmol/L咪唑梯度洗脱目的蛋白M:Protein molecular weight marker;1-2:supernatant and sediment of pET-BdorOBP1a;3-5:original sample liquid,effluent and wash buffer of pET-BdorOBP1a;6-11:Taget protein eluted with 40,80,120,160,200,300 mmol/L图5 重组桔小实蝇气味结合蛋白BdorOBP1a表达形式的确定及纯化Fig.5 Determination the forms of expression and purification of the recombinant BdorOBP1a
2.4 BdorOBP1a与不同气味分子结合能力分析
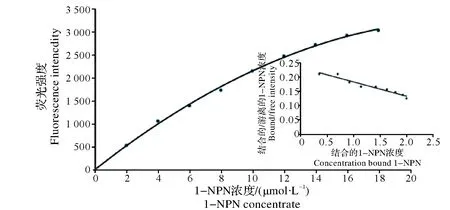
图6 1-NPN与BdorOBP1a的结合曲线Fig.6 Bound curve of 1-NPN to BdorOBP1a
根据Scachard方程将1-NPN与BdorOBP1a的结合曲线线性化,得到1-NPN与BdorOBP1a的结合常数为19.8μmol/L(图6)。荧光竞争结合实验测定了BdorOBP1a与21种挥发性气味的结合能力,结果显示(图7和表3),在所测的挥发物中,有15种挥发物与BdorOBP1a有结合能力,其中β-紫罗兰酮和苯甲醛的结合能力最强,解离常数分别为31.1和31.8 μmol/L;其次是己酸乙酯和乙酸异戊酯,解离常数分别为45.3和47 μmol/L;与其他挥发物结合的解离常数均高于50 μmol/L。
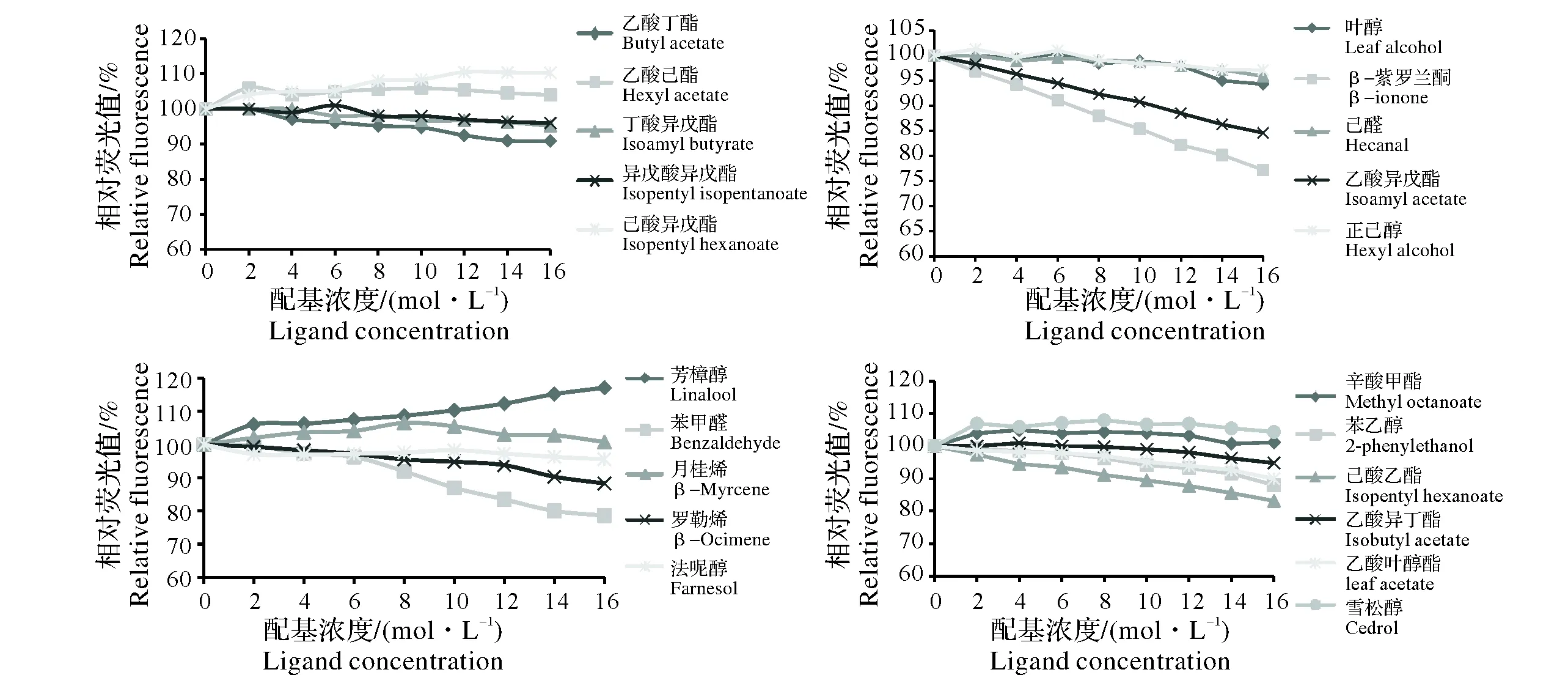
图7 配基与1-NPN竞争结合重组蛋白BdorOBP1aFig.7 Competitive binding of candidate ligands with 1-NPN to recombinant BdorOBP1a
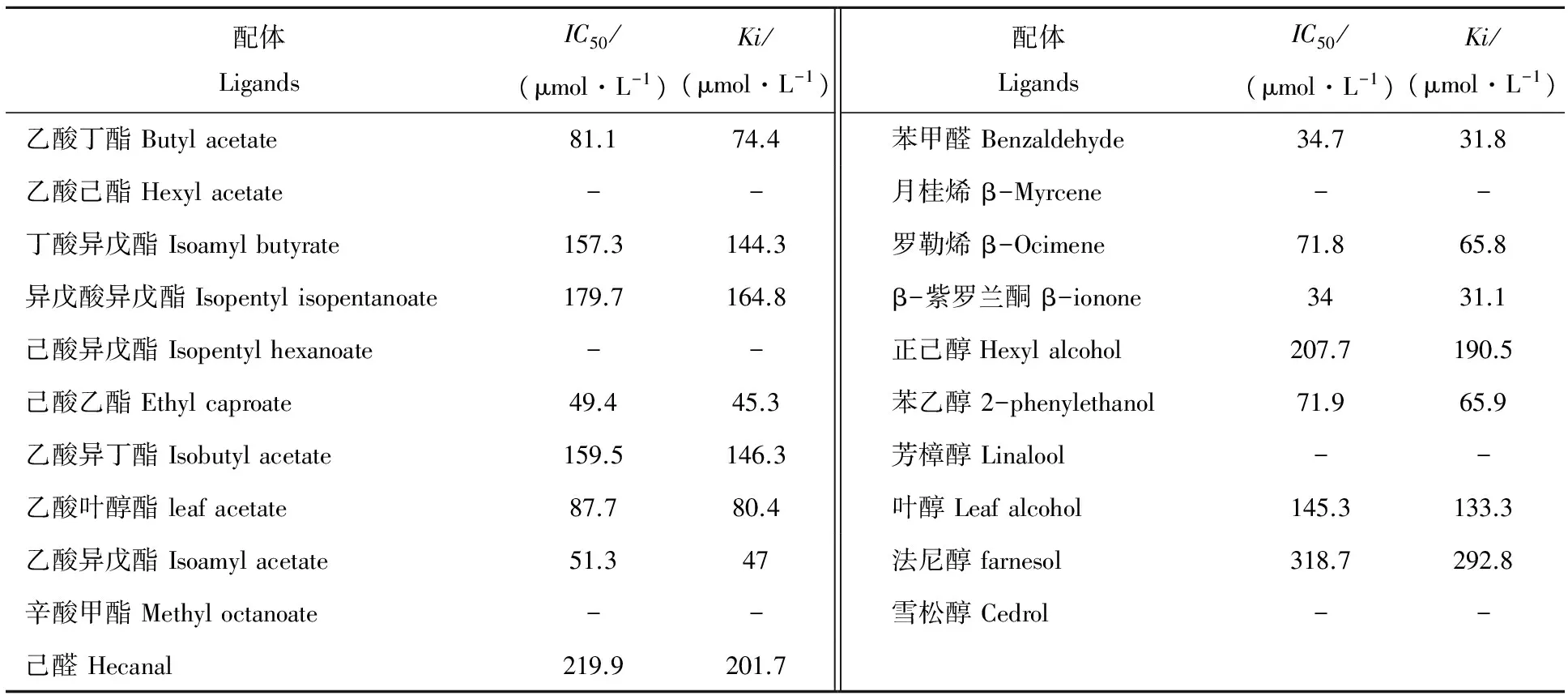
配体LigandsIC50/(μmol·L-1)Ki/(μmol·L-1)配体LigandsIC50/(μmol·L-1)Ki/(μmol·L-1)乙酸丁酯Butylacetate81.174.4苯甲醛Benzaldehyde34.731.8乙酸己酯Hexylacetate--月桂烯β-Myrcene--丁酸异戊酯Isoamylbutyrate157.3144.3罗勒烯β-Ocimene71.865.8异戊酸异戊酯Isopentylisopentanoate179.7164.8β-紫罗兰酮β-ionone3431.1己酸异戊酯Isopentylhexanoate--正己醇Hexylalcohol207.7190.5己酸乙酯Ethylcaproate49.445.3苯乙醇2-phenylethanol71.965.9乙酸异丁酯Isobutylacetate159.5146.3芳樟醇Linalool--乙酸叶醇酯leafacetate87.780.4叶醇Leafalcohol145.3133.3乙酸异戊酯Isoamylacetate51.347法尼醇farnesol318.7292.8辛酸甲酯Methyloctanoate--雪松醇Cedrol--己醛Hecanal219.9201.7
2.5 桔小实蝇行为反应测定
桔小实蝇对4种挥发物的行为反应(图8)显示:桔小实蝇雌虫(A)对4种挥发物都表现出显著差异,其中己酸乙酯、乙酸异戊酯和β-紫罗兰酮对桔小实蝇有显著的引诱作用,而苯甲醛对桔小实蝇有显著的趋避作用;桔小实蝇雄虫(B)对其中两种挥发物表现出显著差异,分别是己酸乙酯和乙酸异戊酯,对桔小实蝇有显著的引诱作用。

A:桔小实蝇雌虫;B:桔小实蝇雄虫;*样品与对照间的选择性显著差异(P<0.05)A:Bactrocera dorsalis female adults;B:Bactrocera dorsalis male adults;*significant different of choose in samples and control samples(P<0.05)图8 桔小实蝇对4种挥发物的行为反应Fig.8 Behavioral responses of Bactrocera dorsalis tofourvolatiles
3 结论与讨论
本研究从桔小实蝇克隆了一个非典型的OBP基因BdorOBP1a,其分子特性和氨基酸序列符合OBPs家族的共有特征:分子量小,亲水性强和等电点低[25],表明本实验克隆的桔小实蝇BdorOBP1a基因属于昆虫OBPs家族成员之一。其编码的蛋白序列含有26个氨基酸的信号肽,与NCBI上的蛋白序列有两个氨基酸的差异,分别在信号肽和蛋白序列末端,蛋白序列相似性为99%;此外,该基因只含有4个保守的半胱氨酸位点,这与报道的大多数昆虫气味结合蛋白特征不一致,属于“Minus-C”OBP,这类OBP报道的比较少,如二化螟Chilo suppressalis CsupOBP1[14]。BdorOBP1a与其他昆虫气味结合蛋白序列对比和进化树结果显示,本实验克隆得到的桔小实蝇BdorOBP1a与GenBank上的BdorOBP1序列位于同一分支上,因此可知这两个序列为同源序列,碱基的差异可能是不同的地理环境或饲料的不同而造成。
为了了解BdorOBP1a的结合特性,我们利用了原核表达系统大量表达了目的蛋白,经纯化柱纯化后,用于测定BdorOBP1a与21种挥发物的结合能力。测定结果显示,有15种寄主植物挥发物与BdorOBP1a具有一定的结合能力,如具有较强结合能力的乙酸异戊酯——成熟香蕉释放的主要挥发物,这与桔小实蝇对成熟香蕉具有较高的趋性而对未成熟的香蕉趋性一般相一致[26],同时,乙酸异戊酯在成熟香蕉中的含量是未成熟香蕉的2.2倍,是所有挥发物中差异最大的[27],因此推测乙酸异戊酯可能是香蕉引诱桔小实蝇的特异性物质;而乙酸己酯——成熟苹果的主要挥发物[28]却与BdorOBP1a不结合,这也与桔小实蝇对苹果的趋性较差[29]相一致,这表明BdorOBP1a在寻找寄主的过程中起着感受挥发物和寄主定位的作用。
BdorOBP1a与醇类的结合能力较弱,而与酯类,醛类和酮类的结合能力较强,这可能是配基与蛋白的结合过程受氢键,疏水作用,不饱和键以及碳原子个数[30]影响而造成的。醇类含有羟基,可与水形成氢键,从而影响了醇类与气味结合蛋白的结合,而酯类,醛类和酮类都不易溶于水(低级酮除外),是亲酯类化合物,这使其与疏水区中的疏水性氨基酸结合位点有较好的结合能力;此外,蛋白空腔的形状,位置及氨基酸序列等同样也会影响配基与蛋白的结合。据报道,在“Minus-C”OBP中,分子体积和疏水性相互作用在结合中更重要,氢键的影响相对较弱些[16]。这从21种挥发物的结合特性来看,也有着相似的结果。
所有挥发物中结合能力最强的是β-紫罗兰酮和苯甲醛,解离常数分别为31.1、31.8 μmol/L;其次是己酸乙酯和乙酸异戊酯,解离常数分别为45.3、47 μmol/L。前人的研究表明,配基与蛋白的结合常数(Ki值)小于10 μmol/L时说明具有较强的结合能力[31-32],从表2的Ki值可知,BdorOBP1a与15种挥发物的结合常数都大于30 μmol/L这与GmolOBP3[33]的结合特性相似,表明所选的配基结合能力一般,选择的挥发物还不够广泛,好的配基没有筛选到。为了弄清它的功能,我们进行了行为反应测定,表明桔小实蝇对β-紫罗兰酮,乙酸异戊酯,苯甲醛和己酸乙酯都具有趋性,这一结果与配基结合特性间接说明BdorOBP1a在桔小实蝇对寄主植物气味的定位过程中起着重要的作用。
参考文献:
[1] 陈景芸,蔡平,张国彪,等.橘小实蝇发生与综合防治研究进展[J].安徽农业科学,2011,39(5):17324-17326.
Chen J Y,Cai P,Zhang G B,et al.Research progress of occurrence and comprehensive control of oriental fruit fly[J].Journal of AnhuiAgricultural Sciences,2011,39(5):17324-17326.
[2] 梁帆,梁广勤,赵菊鹏,等.广州地区桔小实蝇的发生与综合防治关键措施[J].广东农业科学,2008(3):58-61.
Liang F,Liang G Q,Zhao J P,et al.Key methods of occur and comprehensive control to oriental fruit fly in Guangzhou area[J].Guangdong Agricultural Sciences,2008(3):58-61.
[3] 魏佳宁,王宪辉,孙玉诚,等.害虫的遗传与行为调控[J].应用昆虫学报,2012,49(2):299-308.
Wei J N,Wang X H,Xun Y C,et al.Mechanisms for controlling insects by manipulating their genetics and behavior from gene to ecosystem[J].Chinese Journal of Applied Entomology,2012,49(2):299-308.
[4] Liu N Y,Yang K,Liu Y,et al.Two general-odorant binding proteins inSpodopteralituraare differentially tuned to sex pheromones and plant odorants[J].Comparative Biochemistry & Physiology Part A Molecular & Integrative Physiology,2015,180:23-31.
[5] Feng L,Prestwich G D.Expression and characterization of a lepidopteran general odorant binding protein[J].Insect Biochem Mol Biol,1997,27(5):405-412.
[6] Vogt R G,Callahan F E,Rogers M E,et al.Odorant binding protein diversity and distribution among the insect orders,as indicatedby LAP,an OBP-related protein of the true bugLyguslineolaris(Hemiptera,Heteroptera)[J].Chemical Senses,1999,24(5):481-495.
[7] 程小娟,蔡立君,郑丽双,等.小菜蛾气味结合蛋白OBP2基因的克隆、表达谱及其结合特性分析[J].昆虫学报,2016,59(4):365-376.
Cheng X J,Cai L J,Zheng L S,et al.Cloning,expression profiling and binding characterization of the OBP2 gene in the diamondback moth,Plutellaxylostella( Lepidoptera: Plutellidae)[J].Acta Entomologica Sinica,2016,59(4):365-376.
[8] Spinelli S,Lagarde A,Iovinella I,et al.Crystal structure ofApismelliferaOBP14,a C-minus odorant-binding protein,and its complexes with odorant molecules[J].Insect Biochemistry & Molecular Biology,2012,42(1):41.
[9] Li Z Q,Zhang S,Luo J Y,et al.Two Minus-C odorant binding proteins fromHelicoverpaarmigera,display higher ligand binding affinity at acidic pH than neutral pH[J].Journal of Insect Physiology,2013,59(3):263-272.
[10] 吴帆,黄君君,谭静,等.中华蜜蜂信息素结合蛋白OBP10的基因克隆、原核表达和配基结合特性分析[J].昆虫学报,2016,59(1):25-32.
Wu F,Huang J J,Tan J,et al.Molecular cloning,prokaryotic expression and lignand-binding characterization of a novel pheromone binding protein OBP10 inApisceranacerana(Hymenoptera: Apidae)[J].Acta Entomologica Sinica,2016,59(1):25-32.
[11] 朱晓强,丁玉骁,刘航玮,等.绿盲蝽气味结合蛋白AlucOBP8的结合特性分析[J].中国生物防治学报,2015,31(6):821-829.
Zhu X Q,Din Y X,Liu H W,et al.Binding characterization of the odorant binding proteinsAlucOBP8 inApolyguslucorum[J].Chinese Journal of Biological Control,2015,31(6):821-829.
[12] Biessmann H,Andronopoulou E,Biessmann M R,et al.TheAnophelesgambiaeodorant binding protein 1 (AgamOBP1) mediates indole recognition in the antennae of female mosquitoes[J].Plos One,2010,5(3):e9471.
[13] 李亚伟,张小菊,王科珂,等.枣实蝇气味结合蛋白基因的克隆及表达谱分析[J].新疆农业科学,2017,54(2):313-319.
Li Y W,Zhang X J,Wang K K,et al.Clone and expression profiling of odorant-binding proteins inCarpomyavesuvianaCosta[J].Xinjiang Agricultural Sciences,2017,54(2):313-319.
[14] Wei D,Ye Z F,Gao J Q,et al.Molecular cloning and functional identification of a Minus-C odorant binding protein from the rice striped stem borer,Chilosuppressalis(Lepidoptera: Pyralidae).[J].Acta Entomologica Sinica,2013,56(7):754-764.
[15] Li Z Q,Zhang S,Luo J Y,et al.Two Minus-C odorant binding proteins fromHelicoverpaarmigera,display higher ligand binding affinity at acidic pH than neutral pH[J].Journal of Insect Physiology,2013,59(3):263-272.
[16] Li D Z,Yu G Q,Yi S C,et al.Structure-based analysis of the ligand-binding mechanism for DhelOBP21,a C-minus odorant binding protein,fromDastarcushelophoroides(Fairmaire; Coleoptera: Bothrideridae)[J].International Journal of Biological Sciences,2015,11(11):1281-95.
[17] Spinelli S,Lagarde A,Iovinella I,et al.Crystal structure ofApismelliferaOBP14,a C-minus odorant-binding protein,and its complexes with odorant molecules[J].Insect Biochemistry & Molecular Biology,2012,42(1):41-50.
[18] Zheng Z C,Li D Z,Zhou A,et al.Predicted structure of a Minus-C OBP fromBatocerahorsfieldi(Hope) suggests an intermediate structure in evolution of OBPs[J].Scientific Reports,2016,6:33981.
[19] 龚妃良.桔小实蝇气味结合蛋白基因的鉴定与表达分析[D].广州:仲恺农业工程学院,2014.
Gong F L.Identification and expression profiling of odorant-binding proteins inBactroceradorsalis[D].Guangzhou:Zhongkai University of Agriculture and Engineering,2014.
[20] Zheng W,Peng W,Zhu C,et al.Identification and expression profile analysis of odorant binding proteins in the oriental fruit fly Bactrocera dorsalis[J].International Journal of Molecular Sciences,2013,14(7):14936-14949.
[21] Liu Z,Smagghe G,Lei Z,et al.Identification of male- and female- specific olfaction genes in antennae of the oriental fruit fly (Bactroceradorsalis)[J].Plos One,2016,11(2):e0147783.
[22] Wu Z,Zhang H,Wang Z,et al.Discovery of chemosensory genes in theoriental fruit fly,Bactroceradorsalis[J].Plos One,2015,10(6):e0129794.
[23] Chen L,Li H L,Zhou Y X,et al.cDNA cloning,tissue expression and ligand binding characteristics of odorant-binding protein 2 from the oriental fruit fly,Bactroceradorsalis(Diptera: Tephritidae)[J].Acta Entomologica Sinica,2013,56(6):612-621.
[24] Zhou J,Zhang N,Wang P,et al.Identification of host-plant volatiles and characterization of two novel general odorant-binding proteins from the legume pod borer,MarucavitrataFabricius (Lepidoptera: Crambidae)[J].Plos One,2015,10(10): e141208.
[25] Pelosi P,Zhou J J,Ban L P,et al.Soluble proteins in insect chemical communication[J].Cellular & Molecular Life Sciences Cmls,2006,63(14):1658-1676.
[26] Armstrong J W.Quarantine security of bananas at harvest maturity against mediterranean and oriental fruit flies (Diptera: Tephritidae) in Hawaii[J].Journal of Economic Entomology,2001,94(1):302.
[27] Shen J M,Zeng L,Hu L M,et al.Comparative analysis of volatile components of banana[J].Journal of Environmental Entomology,2011,33(2):277-281.
[28] Bengtsson M,Bäckman A C,Liblikas I,et al.Plant odor analysis of apple: antennal response of codling moth females to apple volatiles during phenological development[J].J Agric Food Chem,2001,49(8):3736-3741.
[29] 于文惠.桔小实蝇对几种寄主果实的选择和嗅觉学习行为[D].重庆:西南大学,2013.
Yu W H.Host selection and olfactory learning behavior ofBactroceradorsalisto several host fruit[D].Chongqing:Southwest University,2013.
[30] Zhang T,Liu N Y,Dong S L.cDNA cloning,tissue distribution and ligand binding characteristics of antennal binding protein 2 from the beet army worm,Spodopteraexigua(Lepidoptera: Noctuidae)[J].Acta Entomologica Sinica,2012,55(5):499-509.
[31] Guo H,Huang L Q,Pelosi P,et al.Three pheromone-binding proteins help segregation between two Helicoverpa species utilizing the same pheromone components[J].Insect Biochem Mol Biol,2012,42(9):708-16.
[32] Liu N Y,Peng H,Dong S L.Binding properties of pheromone-binding protein 1 from the common cutwormSpodopteralitura[J].Comparative Biochemistry & Physiology Part B Biochemistry & Molecular Biology,2012,161(4):295.
[33] 宋月芹,解幸承,董钧锋,等.梨小食心虫气味结合蛋白GmolOBP3的cDNA克隆、表达谱及结合特性分析[J].昆虫学报,2014,57(3):274-285.
Song Y Q,Xie X C,Dong J F,et al.cDNA cloning,expression profiling and binding properties of odorant-binding protein GmolOBP3 in the oriental fruit moth,Grapholitamolesta(Lepidoptara: Tortricidae)[J].Acta Entomologica Sinica,2014,57(3):274-285.

