间歇式静电纺丝制备纳米纤维药物控释系统
母朝静, 吴庆生
(1. 同济大学 化学科学与工程学院, 上海 200092; 2. 上海市化学品分析、风险评估与控制重点实验室, 上海 200092)
近年来,随着药物研究的深入、制剂工艺的进步,药物控制释放越来越受到关注.药物疗效的发挥都有其有效的作用位置(一般称为病灶部位),然而一般情况下在实际用药的过程中并不能保证药物一开始就被送到病灶部位发生作用.但是,经过设计的药物制剂,可以通过一定的手段控制其在病灶部位释放,即实现靶向给药,成为“药物导弹”[1-2].
一般方剂中,血药浓度在服药后都会上升至峰值,随后下降并最终衰减至零.每种药物都有其治疗浓度范围,浓度过低达不到疗效,过高则会产生毒性.有的药物作用于全身,目标区域浓度较低;有的药物虽然需要即时见效,但是药物可能还没有到达有效病灶部位已经与其他部位的组织细胞发生作用了,如抗菌药[3-5];还有的药物可能需要到达病灶部位后立即见效,但是还需要持续用药并保持恒定的药量才能确保控制疾病,而仅仅靶向持续给药会造成血药浓度过高产生毒性,如降压药[6-7];有的药物则需要到达病灶部位后缓慢发生作用以避免剧烈反应引起的副作用,药效持续上升达到一定效果后并长时间保持恒定,而实际药物往往在病灶部位的血药浓度很快就下降了,如抗癌药[2,8];诸如此类药物不仅疗效欠佳,往往还有副作用.如果使用适当的药物控释技术,在用药时就可以有针对性地控制药物释放的方式,以“对症用药”,发挥疗效.这种以药物使用剂量小、副作用降至最低、疗效发挥最大为目的的药物传递系统(drug delivery system)[9-10]近年来已经得到了快速发展.
由于纳米尺度下材料表现出的多种特性,将药物制备成纳米药物或者用纳米材料担载药物制备成纳米药物传递系统[11-13],可以在用药剂量、降低副作用、发挥最大疗效等方面发挥明显的作用.而作为需要保持活性的药物在制备成药剂时,需要选择不会影响药效的制备方法,条件温和、简单方便、成本低廉是需要考虑的因素.静电纺丝法因其设备简单、成本低廉、操作便捷以及高效可行,已经被视为制备纳米药物载体最有效的方法之一[14-16].这种方法可以将大多数常规药物混合到电纺丝液中,而纺丝液一旦配制完成后,药物一般不损失,也不会失去生物活性.纳米纤维的特性使得所含药物与周围环境的接触面积大大增加,许多原来难以被人体吸收的药物,吸收效率大大提高.静电纺丝虽然已经比较成熟,但传统方法制备的纳米纤维很容易黏连成膜.本课题组经过探索[17-18],提出了间歇式静电纺丝法,即通过控制纺丝过程,让纤维一层一层平铺,防止了黏连成膜的现象,这更有利于将其用作药物载体.
一些具有较好控制释放效果的合成高分子多具有生物毒性,许多药剂的制备还要使用各种有毒的有机溶剂或经历有损生物活性的制药过程.而作为“二次加工”制备药物复合纳米纤维控释系统,以无毒的、具有很好的生物相容性和完全可生物降解的高分子作为载体材料无疑是上佳选择.十多年来的研究表明,可生物降解的人工合成高分子在药物控释系统中有着广阔的应用前景,比如聚乳酸(PLLA)[19-20]、聚己内酯(PCL)[21-23]、聚乙烯吡咯烷酮(PVP)[24-25]、聚乙二醇(PEG)[26-27]等高分子化合物都是具有良好的生物降解性、生物相容性、无毒性或低毒性,可以作为重要的药物载体或者添加剂使用,并且可溶于水或某种有机溶剂中,通过静电纺丝制备纳米纤维.PAN虽然具有生物毒性,但与其他聚合物通过混纺的方式可以达到改性的目的,有效地克服这一缺陷,具有较好的生物相容性,也常常用作生物医用材料[28].
要达到“对症下药”的目的,就需要控制纳米载药体系的药物释放速度,而这个速度跟体系的降解方式和速度[29-30]有直接的关系.本文旨在通过间歇式静电纺丝制备纳米纤维,进一步探讨其性能,探索不同降解特征的载体体系,以期未来可以有选择地应用于不同给药需求的药物控释系统.为验证制备的纳米纤维的控释效果,选取了一种常见降压药硝苯地平进行了相关的实验.
1 实验方法
1.1 实验材料
PCL,相对分子质量为50 000; PVP,相对分子质量为130 000;PEG,相对分子质量为10 000; PAN,相对分子质量为150 000;PLLA,相对分子质量为150 000;N,N-二甲基甲酰胺(DMF),分析纯;二氯甲烷,分析纯;无水乙醇,分析纯;NaCl,分析纯;硝苯地平(Nifedipine,BR)、Ca(NO3)2,购自上海国药集团有限公司;硝苯地平控释片,药店购买,用于参比对照;透析袋(MD31,CE膜),购自斯百全(上海)有限公司;PBS缓冲溶液,实验室自制;去离子水.
1.2 实验仪器
磁性搅拌器;注射器;8号针头(外径8 mm);高压静电发生器;静电纺丝自动进样装置;静电纺丝接收屏;S-4800高分辨场发射扫描电子显微镜(FE-SEM,Hitachi公司,日本);紫外可见分光光度计(Agilent8453,美国安捷伦);D8 X-射线衍射仪(XRD,Bruker公司,德国);Nicolet6700傅里叶变换红外光谱仪(FT-IR,赛默飞世尔公司,美国);TG -DSC差热分析仪STA409 PC(德国耐茨);原子吸收光谱仪AAS3510(安捷伦).
1.3 实验内容
1.3.1药物载体高分子纳米纤维制备
纺丝溶液的制备.将一定量的高分子材料(PCL、PAN-PEG、PVP、PLLA)在水浴加热下,加入到一定量的溶剂(DMF、CH2Cl2、无水乙醇或去离子水)中,搅拌3~4 h后,制成均匀分散的高分子溶胶(质量分数范围5%~20%,视不同高分子,范围有所不同).
高压静电纺丝.将上一步分散均匀的高分子溶胶转移到注射器中,注射器固定在自动进样装置上,并通过细导管与8号针头连接,调节针头到接收屏的距离(范围为10~25 cm);将高压静电发生器的两极分别与针头和接收屏连接(接地),开启自动进样装置,设置好进样流量(范围为0.5~3.0 mL·h-1);接通高压静电发生器电源,调节合适的电压(范围为10~25 kV),开始观察接收屏上纤维的沉积情况.所有实验均在室温下进行.接收样品一定时间后结束实验,对收集到的纳米纤维真空干燥48 h,以备后用.
1.3.2高分子纳米纤维制备的条件参数
本文所制备的纳米纤维涉及到的高分子材料包括PCL、PAN-PEG、PVP、PLLA,静电纺丝过程中除了外界环境因素(包括室温、湿度等)外,高分子溶液的质量分数、外加电压、溶液流量、接收距离以及多组分溶液中不同组分的配比都会对所制备的产品的形貌、结构和性质产生影响.实验过程中,对不同条件参数的影响进行了考察.条件参数设置见表1~4.
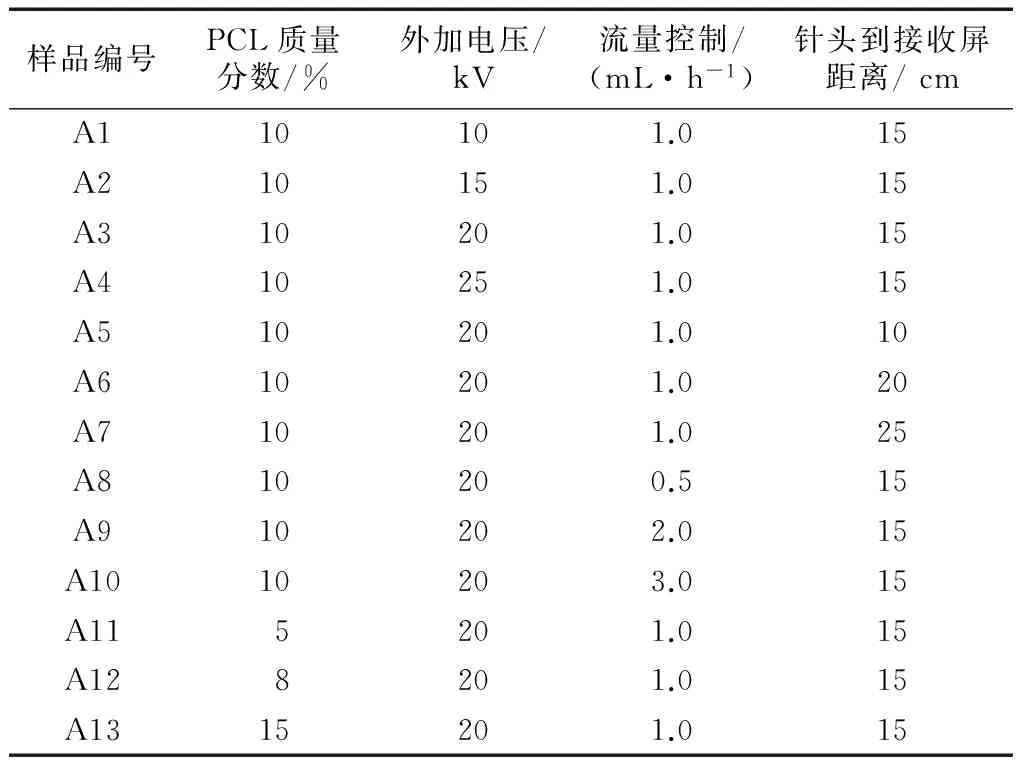
表1 静电纺丝制备PCL纳米纤维的不同条件参数Tab.1 Different conditions for PCL nanofiberpreparation by electrospun
注:溶剂为DMF;高分子占纺丝液总质量分数为10%.
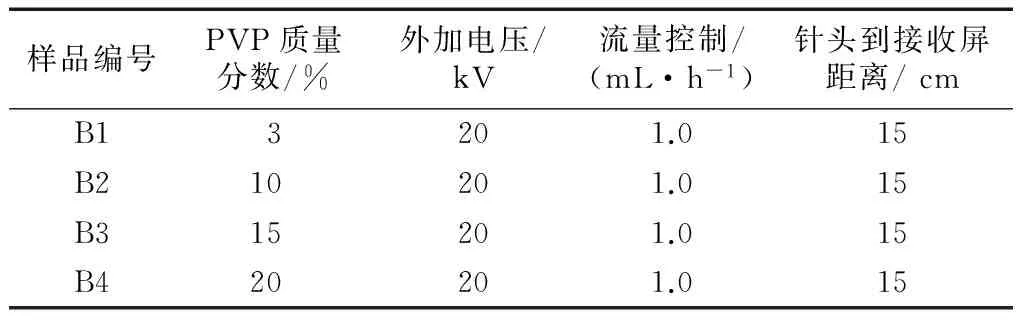
表2 静电纺丝制备PVP纳米纤维的不同条件参数Tab.2 Different conditions for PVP nanofiberpreparation by electrospun
注:溶剂为DMF;高分子占纺丝液总质量分数为10%.
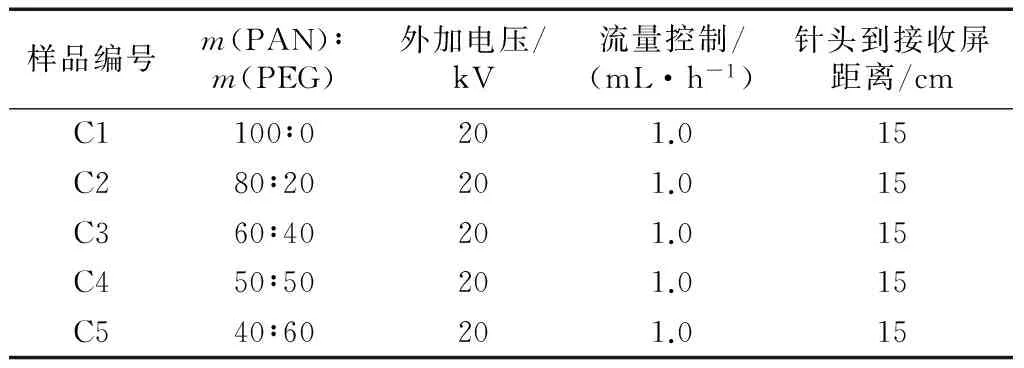
表3 混纺制备PAN-PEG纳米纤维的不同条件参数Tab.3 Different conditions for PAN-PEG nanofiberpreparation by electrospun
注:溶剂为DMF/无水乙醇(体积比为1∶1); 高分子占纺丝液总质量分数为10%.
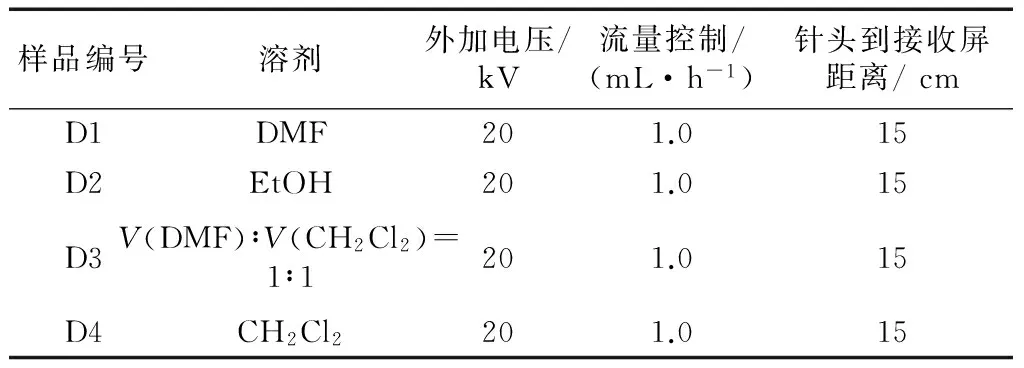
表4 静电纺丝制备PLLA纳米纤维的不同条件参数Tab.4 Different conditions for PLLA nanofiberpreparation by electrospun
注:高分子占纺丝液总质量分数为10%.
1.3.3高分子纳米纤维的表征
在S-4800高分辨场发射扫描电子显微镜下观察所收集到的纳米纤维的形态.所有样品扫描前通过喷金处理.标尺测量后,计算纳米纤维的平均直径,并测算平均直径的分布情况.
用X-射线衍射仪D8分析高分子材料粉末、空白高分子纳米纤维的结构.X-射线衍射仪参数设置为:Cu/Ka辐射靶(λ=1.540 56×10-10m,40 kV,40mA),2θ= 10°~70°,扫描速度0.2 s-1.
通过Nicolet6700傅里叶变换红外光谱表征高分子材料和空白高分子纳米纤维的分子结构.将高分子粉末与溴化钾(KBr)混合压片,纳米纤维则剪碎后与KBr混合压片,红外扫描范围波数为4 000~400 cm-1.
用TG-DSC差热分析仪STA409PC对所制备的纳米纤维进行吸热放热的分析,升温速率20 ℃·min-1,从20 ℃升温至500 ℃,保温2 min,再以10 ℃·min-1降至20 ℃.
1.3.4高分子纳米纤维在不同溶液中的降解行为
前述4种高分子纳米纤维(高分子总质量分数10%,外加电压20 kV,流量1.0 mL·h-1,接收距离15 cm,其中PAN-PEG选取质量比为80∶20)各剪取6份1 cm×1 cm的纤维产品(质量计为W0),每小块纤维毡用尼龙纱布(100~150目)包裹,以防止降解碎片分散到缓冲液中影响失重计算的准确性.在每个样品上坠上一个短玻璃棒,以防止样品由于比表面积较大而漂浮到缓冲液面上.将每种纤维6份样品放在一个装有250 mL自制PBS缓冲液(pH = 7.4)的广口瓶中,共分3组.将上述样品放在一振荡培养箱中,温度保持在(37±0.1)℃,转速为90 r·min-1.每隔一定时间,分别从3个广口瓶中各取出一个样品,用蒸馏水冲洗3次,然后用滤纸将样品表面的水吸干,称重(质量计为Ww).待样品在室温条件下干燥至恒重后再称重(质量计为Wd).实验数据取3个样品的平均值.样品的吸水率和失重率分别为
吸水率 = (Ww-Wd)/Wd×100%
(1)
失重率 = (W0-Wd)/W0×100%
(2)
1.3.5硝苯地平控释体系的构建及体外释放以及体外钙离子拮抗效果模拟测定
通过前面的方法制备负载硝苯地平的纳米载药体系—Nifedipine@PAN-PEG纳米纤维.
用UV-Vis分光光度计测定硝苯地平的标准曲线.取一定量硝苯地平配成PBS的标准溶液,质量浓度分别为10、100、250、500、1 000 μg·mL-1,用UV-Vis分光光度计检测吸光度.取所制备的Nifedipine@PAN-PEG纳米纤维100 mg放置在缓释溶液中,每隔一段时间取样1 mL,用UV-Vis分光光度计检测,同时向溶液中补入等体积的缓释溶液PBS(pH=7.4).通过取样测定,得到了Nifedipine@PAN-PEG纳米纤维的释放曲线.以空白PAN-PEG纳米纤维作为对照组,进行3次实验取平均值.
用Ca(NO3)2配制0.1 mol·L-1(16.4 mg·mL-1)的溶液250 mL.以透析袋模拟细胞膜,准备4个透析袋,分别标记为a、b、c、d,各取上述Ca(NO3)2溶液20 mL装入透析袋中.样品a直接密封放入盛有100 mL PBS缓冲溶液中,样品b、c、d分别加入硝苯地平30 mg、硝苯地平控释片一片(含硝苯地平30 mg)、前面实验中制备的Nifedipine@PAN-PEG一定量(其中含硝苯地平30 mg);密封后分别放入盛有100 mL PBS缓冲溶液的烧杯中.每隔一段时间分别从4个烧杯中取样1 mL(同时各补入PBS溶液1 mL),加入1 mL的LaCl3,稀释100倍,通过原子吸收光谱仪测定溶液中Ca2+的浓度,换算出每个烧杯溶液中的Ca2+的浓度.
2 结果与讨论
2.1 高分子纳米纤维的SEM形貌
图1~4分别表示在不同条件参数调控下所制备的PCL纳米纤维的SEM形貌.
图1是调节外加电压下所得的纤维产品.外加电压较小时(10 kV),因电压对溶胶的拉伸力不够,致使大部分没有形成纤维,而是溶胶直接垂滴到接收屏上,形成一层高分子溶胶膜(图1a);随着外加电压的增加(15 kV),纳米纤维生成得还不够稳定,纤维的形貌也不规则,有些部分会累积团聚(图1b);在外加电压达到20 kV时,纤维稳定沉积,纤维截面直径比较均匀,整体形貌也较规则(图1c);当继续增大外加电压时,由于拉伸力过大,使得外加电场中的部分溶胶在到达接收屏时,溶剂挥发不完全,虽然还是能够看到大量的纤维存在,但纤维表面很快就被一层溶胶液滴覆盖.
接收距离对纤维形貌的影响与外加电压的影响趋势比较相似:在接收距离过小时(10 cm),由于大量液滴在电场力的作用下直接滴到接收屏上,形成一层膜,几乎看不到成型的纤维(图2a);在接收距离为15 cm时,纤维沉积稳定、形貌规则、直径均匀(图2b);随着接收距离的继续增加,由于外加电压不变,电场作用力减弱,纤维沉积逐渐不稳定,平均直径也渐趋增大(图2c、2d).

a外加电压为10kVb外加电压为15kV

c外加电压为20kVd外加电压为25kV

图1 不同外加电压下得到的PCL纳米纤维Fig.1 PCL nanofibers fabricated by electrospun atdifferent voltages

c接收距离为20cmd接收距离为25cm
图2不同接收距离下得到的PCL纳米纤维
Fig.2PCLnanofibersfabricatedbyelectrospunatdifferentdistances
从图3中可以看出,通过调控纺丝溶液的流量,接收屏上沉积的纤维平均直径逐渐增大,流量增加一倍后,由于液滴太大,溶剂挥发不完全,接收屏上的纤维出现严重的黏结现象.通过间歇式控制纺丝过程一定程度上可以缓解此现象.

a流量为0.5mL·h-1b流量为1.0mL·h-1

c流量为1.5mL·h-1d流量为2.0mL·h-1
图3不同流量下静电纺丝得到的PCL纳米纤维
Fig.3PCLnanofibersfabricatedbyelectrospunatdifferentflowrates
从图4中可以看出,随着纺丝溶液中PCL的质量分数增大,纳米纤维平均直径逐渐变大,沉积纤维的量逐渐变多.PCL质量分数较小时,虽整体纤维平均直径较小,但分布不均匀;PCL质量分数为10%左右时,纤维直径分布均匀,纺丝过程稳定;但PCL质量分数达到15%以上后,纺丝液溶胶流动性减小,除了增大了拉伸成纤维的难度,还会经常发生针头堵塞现象,静电纺丝过程不连续,通过间歇式纺丝主动控制,则可以避免这种情况的出现.
从理论上说,纺丝溶液中高分子的质量分数对静电纺丝成型和效率的影响应该是在一个合适的范围内,高分子的质量分数太低和太高都会导致纤维不成形或者电纺丝设备发生故障的情况.为此,又对PVP质量分数对纺丝过程的影响进行了考察,见图5.从图5中可以看出,PVP质量分数太小时,因为纺丝溶液黏度太小,在电场力尚未将其拉伸成纤维时,液滴已经直接滴到接收屏上了,几乎没有得到纤维(图5a);而PVP质量分数过大时(20%),就会出现“过犹不及”的情况,纺丝溶液流动性不够,难以拉伸成纤维,接收屏上的纤维几乎完全黏结,经常导致静电纺丝设备的故障.间歇式控制纺丝过程在这里也有一定效果.

aw(PCL)为5%bw(PCL)为8%

cw(PCL)为10%dw(PCL)为15%

图4 不同PCL质量分数下得到的PCL纳米纤维Fig.4 PCL nanofibers with different mass fractionsfabricated by electrospun

cw(PVP)为10%dw(PVP)为15%
图5不同PVP质量分数下得到的PVP纳米纤维
Fig.5PVPnanofiberswithdifferentmassfractionsfabricatedbyelectrospun
将两种或两种以上溶解性质有别的高分子材料混纺制备纳米纤维,预期可以有多种用途.通过调节混纺溶液中不同高分子的质量比例,可以达到调控纺丝过程、调节纤维形貌并控制降解速率等目的.本文将PAN和PEG混合进行静电纺丝,探讨PAN-PEG复合纤维的性质和功能.从图6可以看出,在高分子总质量分数不变的情况下,随着易溶的PEG的比例增大,所得纤维在一定范围内平均直径渐小.但当PEG比例继续增大,混纺溶液黏度下降,纺丝不能成型,得不到纤维产品.

am(PAN)∶m(PEG)=100∶0bm(PAN)∶m(PEG)=80∶20

cm(PAN)∶m(PEG)=60∶40dm(PAN)∶m(PEG)=50∶50

e m(PAN)∶m(PEG)=40∶60图6 不同配比下得到的PAN-PEG复合纳米纤维
Fig.6PAN-PEGcompositenanofibersfabricatedbyelectrospunatdifferentratiosofPAN/PEG
在静电纺丝过程中,溶剂的挥发速度对于纤维的成型有着重要影响,本文也就不同溶剂中高分子材料静电纺丝得到纳米纤维的情况进行了考察,见图7.从图7中可以看出,随着溶剂挥发性变佳,PLLA纤维成型容易,且形貌规整,但是纤维截面平均直径也逐渐增大.随着溶剂挥发速度的增加,PLLA纤维表面出现明显的孔隙,PLLA纤维的这一特性使得其可以在需要靶向给药后快速释放.
2.2 高分子纳米纤维的XRD图谱解析
实验过程中,对原料高分子材料和每种静电纺丝制备的纳米(复合)纤维进行了XRD表征.从图8中可以看出,静电纺丝制备的PCL纤维(a)保持了较好的晶体结构,在2θ= 21.6°、24.0°处有明显的结晶峰;PAN-PEG复合纤维(b)与原来的PAN粉末(c)相比较,其中PAN的XRD衍射峰较好地保持了原来的结晶构型;PVP纤维(d)的结晶度有明显的减弱,衍射峰明显变宽;而PLLA纤维(e)呈比较明显的弥散峰,为典型的无定形态.

aDMFbEtOH

cV(DMF)∶V(CH2Cl2)=1∶1dCH2Cl2
图7不同的溶剂下得到的表面带孔隙的PLLA纳米纤维
Fig.7PLLAnanofiberswithporesonthesurfacefabricatedbyelectrospunindifferentsolvents

a PCL纤维; b PAN-PEG复合纤维; c PAN粉末; d PVP纤维;e PLLA纤维
图8高分子原料及纳米纤维的XRD图谱
Fig.8XRDspectraofpolymerandnanofibers
在常温常压下进行静电纺丝制备的纳米纤维,晶型的变化不受过程影响,而是由高分子自身溶解或分散在纺丝液中所决定的.从结果推断,PLLA和PVP是以大分子的形式溶解在溶剂中,在达到一定浓度后形成溶胶,在随后的静电纺丝过程中,液滴在静电作用下被拉伸后,高分子以无定形分布在纤维中;而PAN和PCL则可能不是溶解在溶剂中,而是在外界条件作用下,分散到了溶剂中形成溶胶,所以在静电拉伸作用下得到的纳米纤维仍然较好地保持原来的晶体结构.这从侧面反映了静电纺丝过程对纺丝溶液中的成分影响甚微,也证明了静电纺丝法制备纳米纤维用作药物控释体系的优势所在.
2.3 高分子纳米纤维的红外光谱分析
图9是静电纺丝制备的纳米纤维膜的红外光谱图.通过比对红外标准谱图,发现纯物质的高分子纳米纤维与各自粉末、膜或者液体的红外峰基本一致,说明在静电纺丝过程中,高分子的分子结构没有发生明显的变化.其中PAN-PEG(c)复合纤维与PAN(b)标准红外谱图对比,在指纹区吸收峰有比较大的变化,说明PEG的加入对PAN的分子结构有影响.

a PCL纤维; b PAN粉末; c PAN-PEG复合纤维; d PEG -10000粉末; e PVP纤维; f PLLA纤维
图9高分子原料及纳米纤维的FT-IR光谱图
Fig.9FT-IRspectraofpolymerandnanofibers
2.4 高分子纳米纤维的DSC分析
图10是前述几种高分子纳米纤维和粉末的DSC曲线.除PAN与PEG混纺制备了两种高分子的复合纳米纤维,其他高分子均为纯物质纺丝,所得
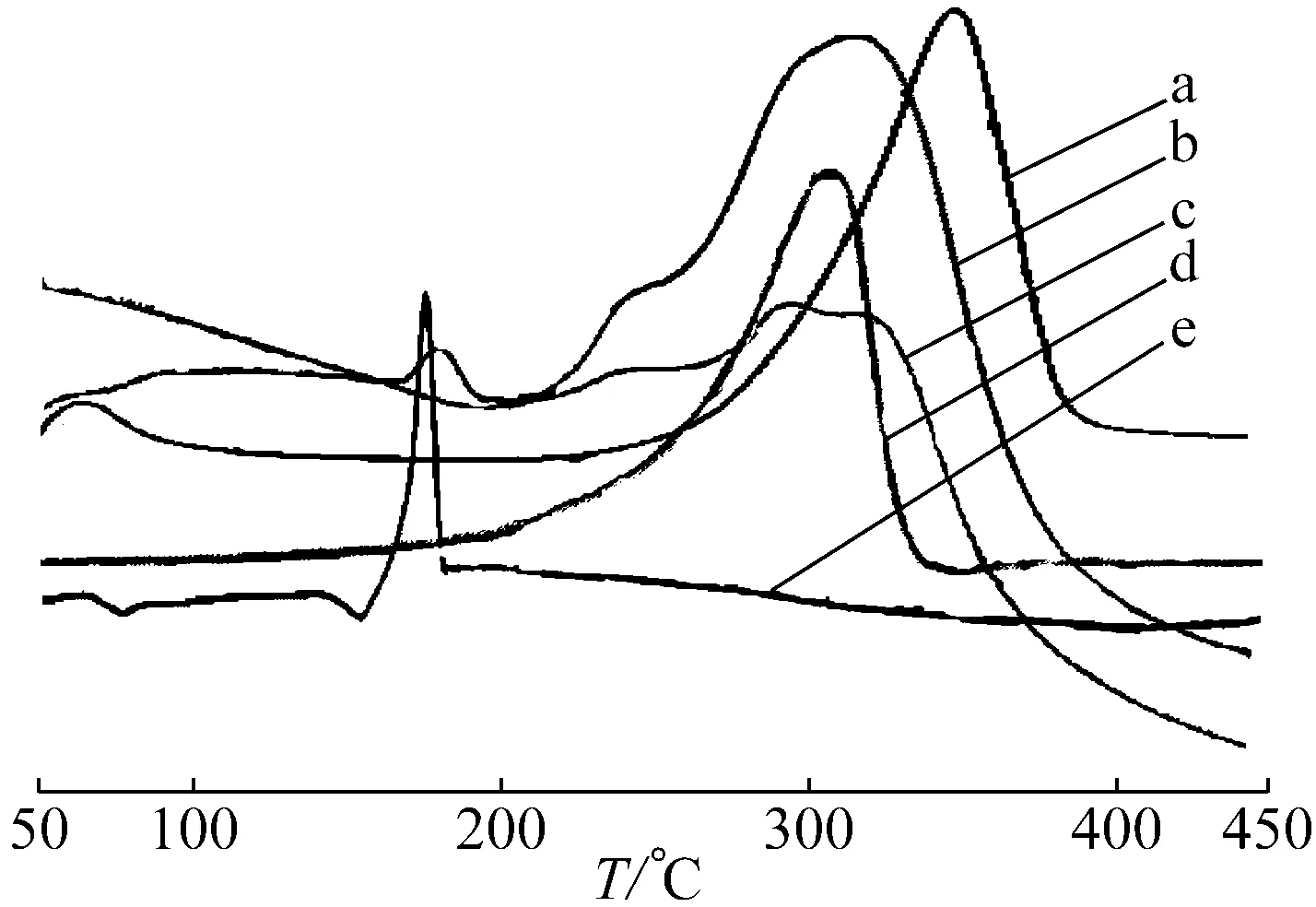
a PCL纤维; b PAN-PEG复合纤维; c PAN粉末; d PVP纤维;e PLLA纤维
图10高分子原料及纳米纤维的DSC曲线
Fig.10DSCcurveofpolymerandnanofibers
的纳米纤维的热学性能与高分子原料相近.与PAN相比较,PAN-PEG复合纤维在187 ℃左右有一个明显的吸热峰,说明PEG在其中影响了复合纤维的吸热过程.
2.5 高分子纳米纤维在不同溶液中的降解行为
图11为PCL、PAN-PEG(80∶20)、PVP、PLLA静电纺丝(复合)纳米纤维在自制PBS溶液(pH=7.4)中降解的吸水率.
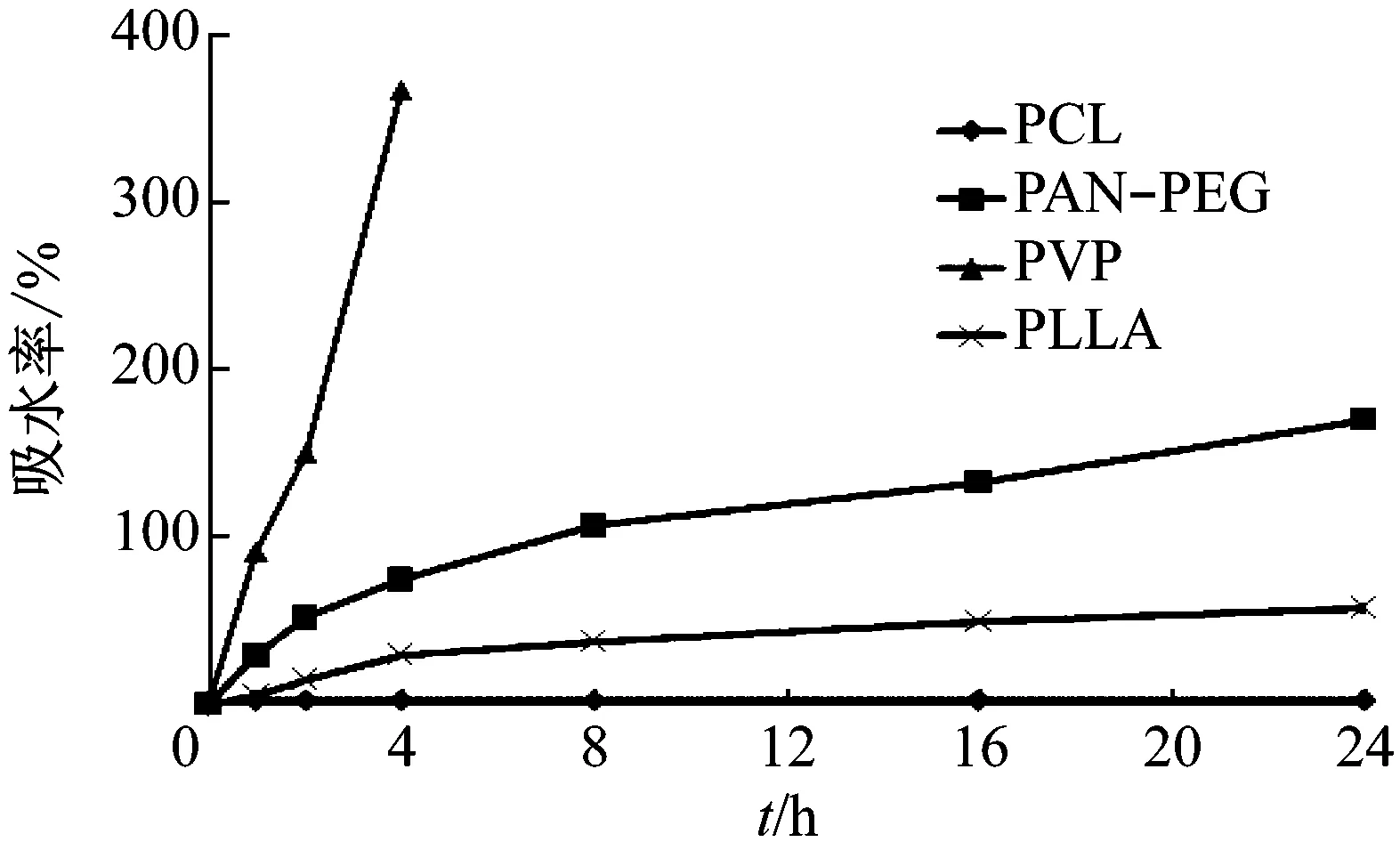
图11 PBS溶液中纳米纤维吸水率Fig.11 Water-absorption of nanofibers in PBS solution
从图11可以看出,几种高分子纳米纤维在PBS溶液中的吸水率差别较大,印证了各自的分子结构情况.PCL纤维吸水很少,说明PCL结晶性较好,不易水解;PAN-PEG(80∶20)复合纤维吸水率随时间逐渐增大,尽管PAN在纤维中也有很好的结晶性,但由于复合纤维中PEG易溶于水,对水的吸附增大,又因为PEG质量分数仅为20%,纤维并没有快速水解;在纺丝过程中结晶性不好的PVP纳米纤维,因其极易水解,所以在PBS溶液中,PVP纤维一开始吸水率快速上升,仅4 h后,PVP纤维就完全水解;在静电纺丝成纳米纤维的过程中,PLLA结晶性下降,呈无定形状态,虽然在PBS溶液中,PLLA不易溶于水,但吸水率随时间增加也逐渐增大,这可以从PLLA纤维的形貌特征给出解释:PLLA纳米纤维有很大的比表面积,表面分布着大量多孔结构,能够吸入水分子,PLLA纤维浸入PBS溶液后,水分子被大量吸入,表现为吸水率渐趋增大.
图12为PCL、PAN-PEG(80∶20)、PVP、PLLA静电纺丝(复合)纳米纤维在自制PBS溶液(pH=7.4)中降解的失重率.
从图12可以看出,随着时间的延长,纤维的失重率也逐渐增加,也即是纤维在PBS溶液中降解的量逐渐增加,两者基本上呈线性关系;但不同的高分子纳米纤维的失重速率差异很大,对应了不同纤维在PBS溶液中的降解速度的差异.图12显示PCL纤维在PBS溶液中失重曲线的斜率一开始较小,PCL纤维缓慢而稳定地降解;随着时间推移,斜率有渐增的趋势;随着在溶液中浸泡的时间增长,PCL的降解会逐渐加快.PAN-PEG复合纤维在PBS溶液中的失重曲线斜率一开始较大,但随着时间增长渐渐减小,这是由于复合纤维中PEG易溶于水,PEG的快速溶解导致了纤维的失重率增加较快;随着时间推进,纤维中PEG的量下降,水解缓慢的PAN起到了主导作用,纤维的失重率增速较小.极易溶于水的PVP,因其大量吸水,逐渐变为溶胶,在溶液的量较大时,溶胶很快就溶解在外界溶剂中,导致PVP纤维膜快速失重,大概4~5 h左右,PVP纤维膜完全溶解“消失”.而PLLA纤维虽然不易溶于水,由于高比表面积,大大增加了纤维与缓冲液的接触面积,吸水率较大,从而加快了它的降解速度,相对于PCL纤维,降解较快,失重率增速稳定.这说明PLLA在PBS溶液中降解稳定.

图12 纳米纤维在PBS溶液中浸泡后的失重率Fig.12 Weight-loss of nanofibers after soaking inPBS solution
2.6 Nifedipine@PANPEG体外释放和载药效率
测量Nifedipine在PBS缓冲溶液中配成的不同质量浓度的溶液随时间变化的吸光度,得到Nifedipine在PBS溶液中的紫外吸收标准曲线,如图13所示.标准曲线方程为
y= 0.000 8x+ 0.002 6
(3)
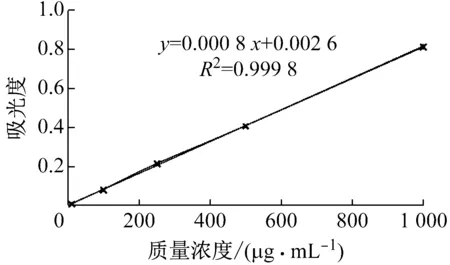
图13 硝苯地平在PBS缓冲液中的UV-Vis吸收标准曲线Fig.13 UV-Vis absorption standard curve ofnifedipine in PBS
剪取Nifedipine@PAN-PEG复合纳米纤维一定量(100 mg)放入100 mL的PBS缓冲溶液中,记录随时间变化的紫外吸光度.根据标准曲线得到的方程(3),可以计算得到不同时间PBS溶液中Nifedipine的浓度,从而得到复合纳米纤维Nifedipine@PAN-PEG的释放曲线,见图14,其中每个数据点代表3次实验的平均值.
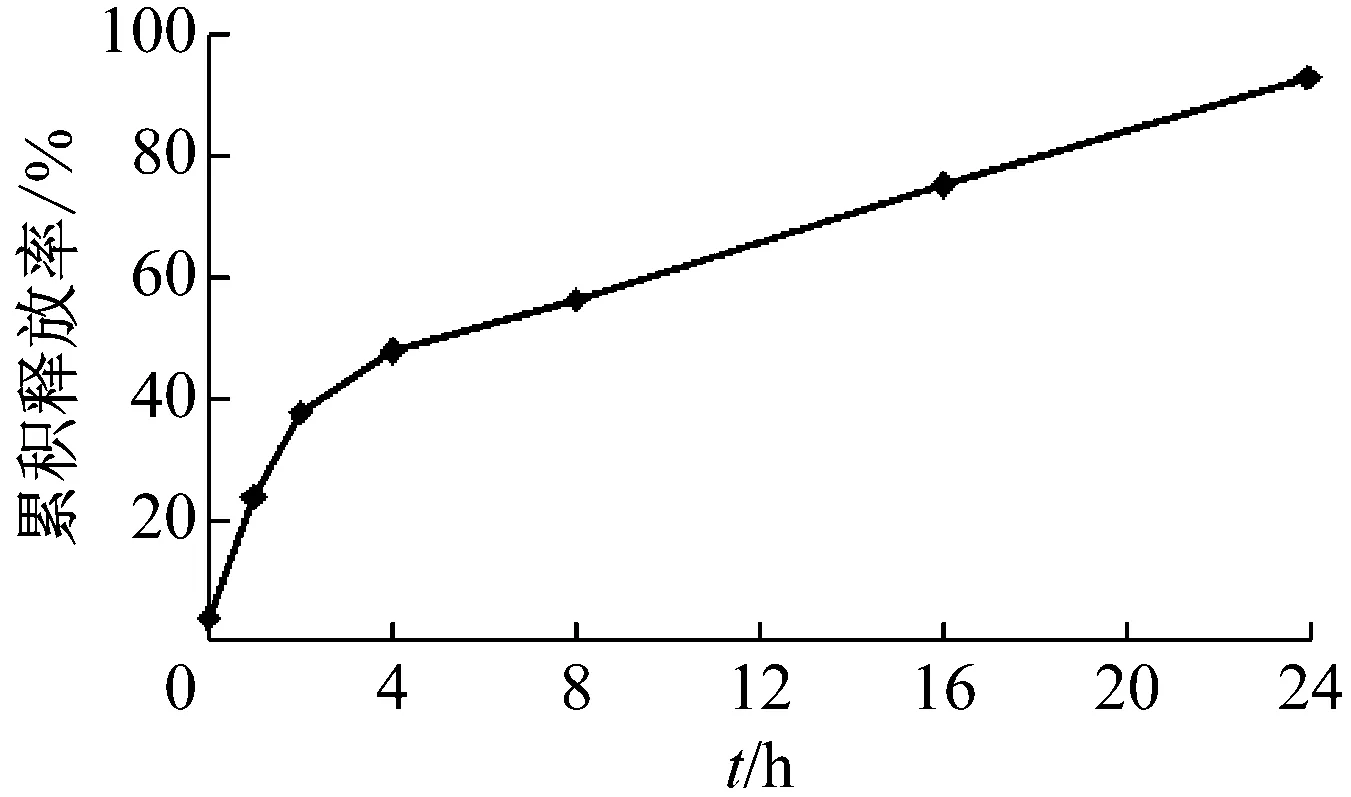
图14 Nifedipine@PANPEG在PBS缓冲液中的释放曲线Fig.14 Release curve of Nifedipine@PAN-PEG in PBS
从图14可以看出,Nifedipine@PAN-PEG复合纳米纤维在PBS中的释放没有出现“突释”现象,但一开始就有部分硝苯地平被检测到,说明硝苯地平在复合纤维表面也有分布,通过扩散直接进入溶液中.随着时间推移,刚开始的数小时内,释放曲线斜率较大,说明释放速率较快.PAN-PEG复合纤维由于PEG易溶于水,随着PEG的快速水解,硝苯地平随着PEG水解快速释放.当PEG水解完全后,硝苯地平释放速率有所下降并保持恒定地释放,持续24 h以上.这对于硝苯地平在抗高血压临床应用上有积极意义,可以持续较长时间稳定地保持血压平衡.继续检测硝苯地平释放情况直到累积释放量不变时,可以计算出产品的包封率达到96.27%.
2.7 Nifedipine@PANPEG体外钙离子拮抗效果
以透析袋模拟细胞膜,在体外模拟表征Nifedipine@PAN-PEG复合纳米纤维钙离子拮抗效应的效果,尽管这与体内环境有很大差异,但仍有一定的实验意义.体外模拟钙离子拮抗实验结果如图15所示.从模拟实验看到,在没有加入硝苯地平时,钙离子从透析袋中通过渗透通过半透膜进入袋外溶液中,大约2 h后,袋内外钙离子就达到平衡,即钙离子透过率达到50%.直接将硝苯地平粉末加入透析袋中,一开始对抑制钙离子的通过作用明显(1 h后钙离子透过率为12.5%);而加入硝苯地平控释片的组,1 h后钙离子透过率为18.9%,这是因为控释片外层糖衣溶解需要一定时间,一开始释放硝苯地平的量较少;而Nifedipine@PAN-PEG加入后1 h时,钙离子的透过率为14.6%,与原药接近,这与前述Nifedipine@PAN-PEG复合纳米纤维的药物释放结果一致,因为PEG的溶解,硝苯地平一开始就能释放出来一定的量,对钙离子的透过有抑制.接着,原药组的钙离子透过率迅速上升,很快(约再过2 h)就达到最大,这可能是因为在抑制钙离子通过的同时,原药也有通过半透膜进入透析袋外溶液中或者原药在溶液中分解,使得抑制钙离子的作用下降.而对应的控释片组,随着外层糖衣的溶解,钙离子拮抗效果明显增强,并且可以达到一定时间的持续,约可以保持8 h,但如果糖衣溶解完后,硝苯地平控释片的药效也会达到极限;而载药复合纳米纤维由于可以长效稳定释放硝苯地平,对钙离子透过率的抑制作用持续更长时间,长达1 d,这对于抗高血压药的用药有着十分重要的意义.
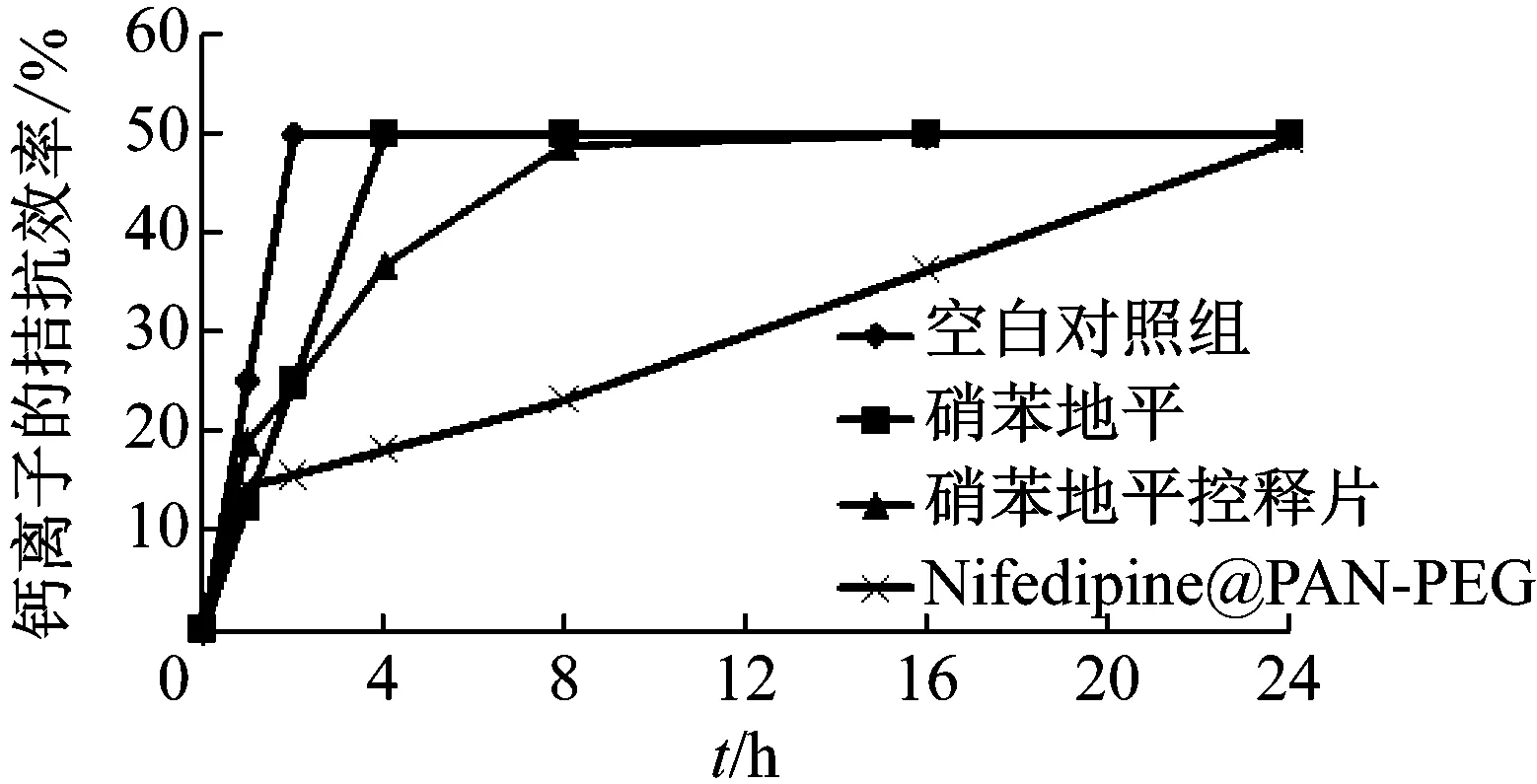
图15 钙离子拮抗体外模拟效果Fig.15 Calcium ion antagonism in vitro
3 结论
对几种高分子材料纳米纤维的降解性能研究仅仅是考察了体外PBS缓冲液中的模拟情况,如果应用于临床时,药物载体进入体内后还会由相应的蛋白酶控制着这些材料的降解,所以高分子材料在体内的降解情况要复杂得多,有的高分子的降解与体外模拟情况不尽相同.近些年,大量的研究者都致力于将纳米纤维作为医用材料,包括人工组织、药物载体、伤护材料等.而作为药物载体的纳米纤维,其生物可降解性是必须考虑的,所以需要选择可降解、易降解的材料.通过体外模拟实验考察各种高分子纳米纤维的降解行为,发现降解的过程和方式形式多样,千差万别.
纳米材料医用主要方向是靶向治疗技术和药物载体,而药物载体也致力于各种靶向控制和控制释放.而很多药物因其在实际用药过程中,常常发生尚未达到病灶部位就已经与其他细胞发生反应,药物失效、产生副作用或者用药低效等问题,所以对药物载体有着较高的要求.不同的药物,其发生作用的方式、用药发生药效的需求等不同,对载体的要求也就不同,也就是要通过对载体控制来达到控制药效的目的.由于不同的高分子材料有不同的降解方式,合理利用这一特性,通过制备可控降解的高分子纳米纤维作为药物载体,用以担载不同释药需求的药物.
本文利用静电纺丝技术,分别以几种高分子材料(PLLA、PCL、PVP、PAN、PEG)单独或其中两种不同配比来构建纳米纤维.特别针对纺丝过程中容易出现的黏连现象,通过间歇式对过程进行控制,有效避免了这种现象.对构建的纳米纤维进行形貌、结构、性质等表征,初步探讨不同纳米纤维的降解行为,分析如何利用不同降解行为,通过“对症下药”,以选择合适的体系作为可控降解的载体担载不同的药物,构建载药复合纳米纤维.
考虑到抗高血压药需要到达病灶部位后立即见效,又需要持续用药并保持恒定的药量才能确保控制疾病,文中还以常见降压药硝苯地平为例,采用PAN-PEG作为载体材料,担载硝苯地平制备了Nifedipine@PAN-PEG,对其体外释药性能进行了考察,并模拟考察了其钙离子拮抗效果,达到了预期的可控降解,进而可以对症用药.
参考文献:
[1] KAWATA H, UESUGI Y, SOEDA T,etal. A new drug delivery system for intravenous coronary thrombolysis with thrombus targeting and stealth activity recoverable by ultrasound [J]. J Am Coll Cardiol, 2012,60(24):2550.
[2] 董士阳, 胡春弟. 靶向制剂在抗癌药物中的应用研究进展[J]. 山东化工, 2016(11):42.
DONG Shiyang, HU Chundi. Targeted applications in anticancer drug preparations [J]. Shandong Chemical Industry, 2016(11):42.
[3] 吴庆生, 罗志辉, 吴昌柱, 等. 无机纳米晶对抗菌药物的协同增效作用:1+1>2[C/CD]∥第十二届固态化学与无机合成学术会议,青岛:中国化学会,2012.
WU Qingsheng, LUO Zhihui, WU Changzhu,etal. Synergistic synergism of inorganic nanocrystalline to antimicrobial agents: 1+1>2 [C/CD]∥12th Conference on Solid State Chemistry and Inorganic Synthesis. Qingdao: Chinese Chemical Society, 2012.
[4] SUCHY T, SUPOVA M, KLAPKOVA E,etal. The release kinetics, antimicrobial activity and cytocompatibility of differently prepared collagen/hydroxyapatite/vancomycin layers: microstructure vs. nanostructure[J]. Eur J Pharm Sci, 2017,100:219.
[5] CHEN D W, LIU S J. Nanofibers used for delivery of antimicrobial agents [J]. Nanomedicine (Lond), 2015,10(12):1959.
[6] 谢建刚. 抗高血压药物合成及其电纺载药纳米纤维膜的制备研究[D]. 上海:东华大学, 2011.
XIE Jiangang. Study of synthesisi of antihypertensive drugs and preraration of drug-losded nanofiber membranes via electrospinning [D]. Shanghai: Donghua University, 2011.
[7] SHEN X, XU Q, XU S,etal. Preparation and transdermal diffusion evaluation of the prazosin hydrochloride-loaded electrospun poly(vinyl alcohol) fiber mats [J]. J Nanosci Nanotechnol, 2014,14(7):5258.
[8] WU H, LIU S, XIAO L,etal. Injectable and pH-responsive silk nanofiber hydrogels for sustained anticancer drug delivery [J]. ACS Appl Mater Interfaces, 2016,8(27):17118.
[9] 兰静, 赵健, 张馨文. 智能药物传输系统的研究进展[J]. 现代药物与临床, 2012(5):488.
LAN Jing, ZHAO Jian, ZHANG Xinwen. Advances in studies on intelligent drug delivery system [J]. Drugs & Clinic, 2015(5):488.
[10] MEI L, WANG Y, TONG A,etal. Facile electrospinning of an efficient drug delivery system [J]. Expert Opin Drug Deliv, 2016,13(5):741.
[11] GENCTURK A, KAHRAMAN E, GUNGOR S,etal. Polyurethane/hydroxypropyl cellulose electrospun nanofiber mats as potential transdermal drug delivery system: characterization studies and in vitro assays [J]. Artif Cells Nanomed Biotechnol, 2017,45(3):655.
[12] TORT S, ACARTURK F. Preparation and characterization of electrospun nanofibers containing glutamine [J]. Carbohydr Polym, 2016,152:802.
[13] GARG T, RATH G, GOYAL A K. Biomaterials-based nanofiber scaffold: targeted and controlled carrier for cell and drug delivery [J]. J Drug Target, 2015,23(3):202.
[14] AKDUMAN C, OZGUNEY I, KUMBASAR E P. Preparation and characterization of naproxen-loaded electrospun thermoplastic polyurethane nanofibers as a drug delivery system [J]. Mater Sci Eng C Mater Biol Appl, 2016,64:383.
[15] 赵治锋, 杨之洵, 李峰, 等. 载药系统中的静电纺丝材料及其应用[J]. 中国组织工程研究, 2017(2):303.
ZHAO Zhifeng, YANG Zhixun, LI Feng,etal. Electrospun materials applied in drug delivery system [J]. Chinese Journal of Tissue Engineering Research, 2017(2):303.
[16] 李玉洁, 姚军燕, 陈明河, 等. 聚乳酸静电纺丝纳米纤维及其药物缓释体系[J]. 高分子材料科学与工程, 2014(6):147.
LI Yujie, YAO Junyan, CHEN Minghe,etal. Electrospun poly(lactic acid) nanofibers and application in drug delivery system [J]. Polymer Materials Science & Engineering, 2014(6):147.
[17] CHAI J H, WU Q S. Electrospinning preparation and electrical and biological properties of ferrocene/poly(vinylpyrrolidone) composite nanofibers [J]. Beilstein J Nanotechnol, 2013,4:189.
[18] CHEN P, WU Q S, DING Y P,etal. A controlled release system of titanocene dichloride by electrospun fiber and its antitumor activity in vitro [J]. Eur J Pharm Biopharm, 2010,76(3):413.
[19] MALIK R, GARG T, GOYAL A K,etal. Diacerein-loaded novel gastroretentive nanofiber system using PLLA: development and in vitro characterization [J]. Artif Cells Nanomed Biotechnol, 2016,44(3):928.
[20] 杜智, 姚军燕, 李玉洁, 等. 聚乳酸/杆菌肽静电纺丝纤维的体外释药研究 [J]. 材料科学与工艺, 2015(5):52.
DU Zhi, YAO Junyan, LI Yujie,etal. Drug controlling release behavior of electrospun poly(lactic acid)/bacitracin drug delivery system [J]. Materials Science and Technology, 2015(5):52
[21] JUNG S M, YOON G H, LEE H C,etal. Chitosan nanoparticle/PCL nanofiber composite for wound dressing and drug delivery [J]. J Biomater Sci Polym Ed, 2015,26(4):252.
[22] HAN J, CHEN T X, BRANFORD-WHITE C J,etal. Electrospun shikonin-loaded PCL/PTMC composite fiber mats with potential biomedical applications [J]. Int J Pharm, 2009,382(1/2):215.
[23] 董常明, 孙琳, 刘威, 等. 扇型聚己内酯共聚物的点击合成及其光敏靶向药物控释体系[C/CD]∥2011年全国高分子学术论文报告会. 大连:中国化学会高分子学科委员会, 2011.
DONG Changming, SUN Lin, LIU Wei,etal. Clicking synthesis of fan type polyhexyl ester copolymer and its photosensitive targeting drug controlled release system [C/CD]∥2011 National High Polymer Paper Report. Dalian: Polymer Division,Chinese Chemical Socierty, 2011.
[24] 朱振舒. 聚乙烯吡咯烷酮纳米药物传输系统研究[D]. 南京:南京大学, 2011.
ZHU Zhenshu. Study of poly(N-vinyl pyrrolidone) based nanodrug delivery systems [D]. Nanjing: Nanjing University, 2011
[25] RASEKH M, KARAVASILI C, SOONG Y L,etal. Electrospun PVP-indomethacin constituents for transdermal dressings and drug delivery devices [J]. Int J Pharm, 2014,473(1/2):95.
[26] PIRES L R, GUARINO V, OLIVEIRA M J,etal. Ibuprofen-loaded poly(trimethylene carbonate-co-epsilon-caprolactone) electrospun fibres for nerve regeneration [J]. J Tissue Eng Regen Med, 2016,10(3):E154.
[27] 潘晶晶. 基于PEG修饰的GO@Au肿瘤靶向药物控释系统的构建及基础研究[D]. 郑州:郑州大学, 2016.
PAN Jingjing. The contruction and evaluation of a tumor-targeting contrrolled drug delivery system based on PEG modified GO@Au nanoparticles [D]. Zhengzhou: Zhengzhou University, 2016.
[28] 刘海洋.PAN基碳纳米纤维杂化复合材料及其生物特性研究[D]. 北京:北京化工大学, 2010.
LIU Haiyang. PAN-based hybrid carbon nanofibers and its biological characteristics [D]. Beijing: Beijing University of Chemical Technology, 2010.
[29] KELNER A, SCHACHT E H. Tailor-made polymers for local drug delivery: release of macromolecular model drugs from biodegradable hydrogels based on poly(ethylene oxide) [J]. J Control Release, 2005,101(1/2/3):13.
[30] 王浩, 温梦, 刘俊鹏, 等. 厚朴酚聚乳酸珠串纤维毡的制备及酶降解药物释放[J]. 辽宁医学院学报, 2013(3):78.
WANG Hao, WEN Meng, LIU Junpeng,etal. The preparation of magnolol entrapped poly(lactic acid) rosary-like fiber mats and the release of enzyme degradation drug [J]. J Liaoning Medical University, 2013(3):78.

