超小剂量地西他滨治疗骨髓增生异常综合征和急性髓系白血病11例疗效观察
陆佳,姚福生,徐海涛
(安徽医科大学附属安庆医院血液科,安徽 安庆 246003)
骨髓增生异常综合征(MDS)是一组起源于造血干细胞的髓系克隆性疾病,其根本病变是克隆性造血干细胞发育异常。临床上表现为骨髓病态造血,外周血中各系血细胞显著减少,容易演变为急性髓系白血病(AML)。近年来,随着对MDS生物学研究的深入,国内外多采用地西他滨等去甲基化药物治疗MDS,降低中高危MDS患者向 AML 进展的风险,改善生活质量,减少输血依赖。但是,由于MDS多发于60岁以上老年人群,这部分人群在接受常规剂量地西他滨治疗时,常因发生出血、感染等严重不良反应,导致预定疗程无法完成,对治疗效果产生严重影响。因此,我们探究能否在保证疗效的基础上,通过减少地西他滨剂量、改进给药方式,尽量减少不良反应,提高患者的耐受性和依从性[1]。
1 资料与方法
1.1 一般资料
研究对象入选标准为安徽医科大学附属安庆医院2015年1月至2016年12月确诊及治疗的中高危MDS和AML患者 。根据WHO2008标准进行分型诊断,11例患者中,男性8例,女性3例,中位年龄59(14~81)岁;MDS-RA 1例,MDS-RCMD 4例,MDS-RAEBI 1例,MDS-RAEBⅡ 3例,MDS-RARS 1例,AML 1例。11例骨髓染色体核型中7例正常核型,1例+8 ,1例-Y+X,2例复杂核型。见表1。
1.2 治疗方法
11例患者中我们采取中危-Ⅰ组选用单药地西他滨(江苏豪森药业集团有限公司,批号:150902、160515)治疗,中危-Ⅱ组和高危组患者及AML患者采取地西他滨联合化疗方案。具体为6例中危-Ⅰ组MDS患者接受地西他滨5~7 mg·m-2·d-1,皮下,每天1次,连用5~6 d为一个疗程的治疗方案;2例中危-Ⅱ组和1例高危组MDS接受地西他滨联合半程CAG方案,具体为地西他滨5~7 mg·m-2·d-1,d1~5,阿克拉霉素20 mg·d-1,隔天1次,d3~6,阿糖胞苷30 mg·d-1,d3~9,粒细胞集落刺激因子300 μg·d-1,d3~9(当外周血白细胞>20×109L-1时暂停注射);1例高危患者采用地西他滨联合HA方案,具体为地西他滨5~7 mg·m-2·d-1,d1~6,高三尖杉酯碱 1 mg·d-1,d6~11,阿糖胞苷30 mg·d-1,d6~11;1例AML患者接受地西他滨联合DA方案,具体为地西他滨5~7 mg·m-2·d-1,d1~5,柔红霉素60 mg·d-1,d1~3,阿糖胞苷150 mg·d-1,d1~7。1个月后重复1周期,2周期后评价疗效。根据患者治疗期间血常规变化情况,适当输注单采血小板及悬浮红细胞,如果中性粒细胞小于0.5×109L-1,就给予重组人粒细胞集落刺激因子(G-CSF)治疗。每2个疗程结束后评价疗效,通过电话及患者返院复查对11例进行随访。截止2016年12月,中位随访时间6个月,10例存活,1例死亡。
2 结果
2.1 临床疗效
MDS疗效评估参考国际工作组(IWG)疗效标准[2]将完全缓解(CR)、部分缓解(PR)和血液学改善(HI)作为有效病例。总有效率(DRR)=(CR+PR+HI)/总例数×100%。11例患者中,CR 3例,PR 4例,HI 1例,无进展(SD)2例,死亡1例。ORR为72.7%,缓解率为27.3%。
2.2 不良反应
2.2.1血液学毒性 11例患者在治疗过程中有6例出现不同程度的血液学毒性。其中,3例出现Ⅱ级血液学不良反应,3例出现Ⅲ级血液学不良反应。血液学不良反应发生率54.5%。
2.2.2感染 11例患者中肺部感染3例,其中2例予以抗感染、皮下注射G-CSF,输注红细胞及血小板等治疗后好转,1例因肺部感染死亡。感染发生率27.3%。
2.2.3其他不良反应 本研究所有患者均未出现过敏反应,1例患者出现消化道出血,予以输注血小板,抑酸对症治疗后好转。1例出现治疗相关死亡。出血发生率18.1%。
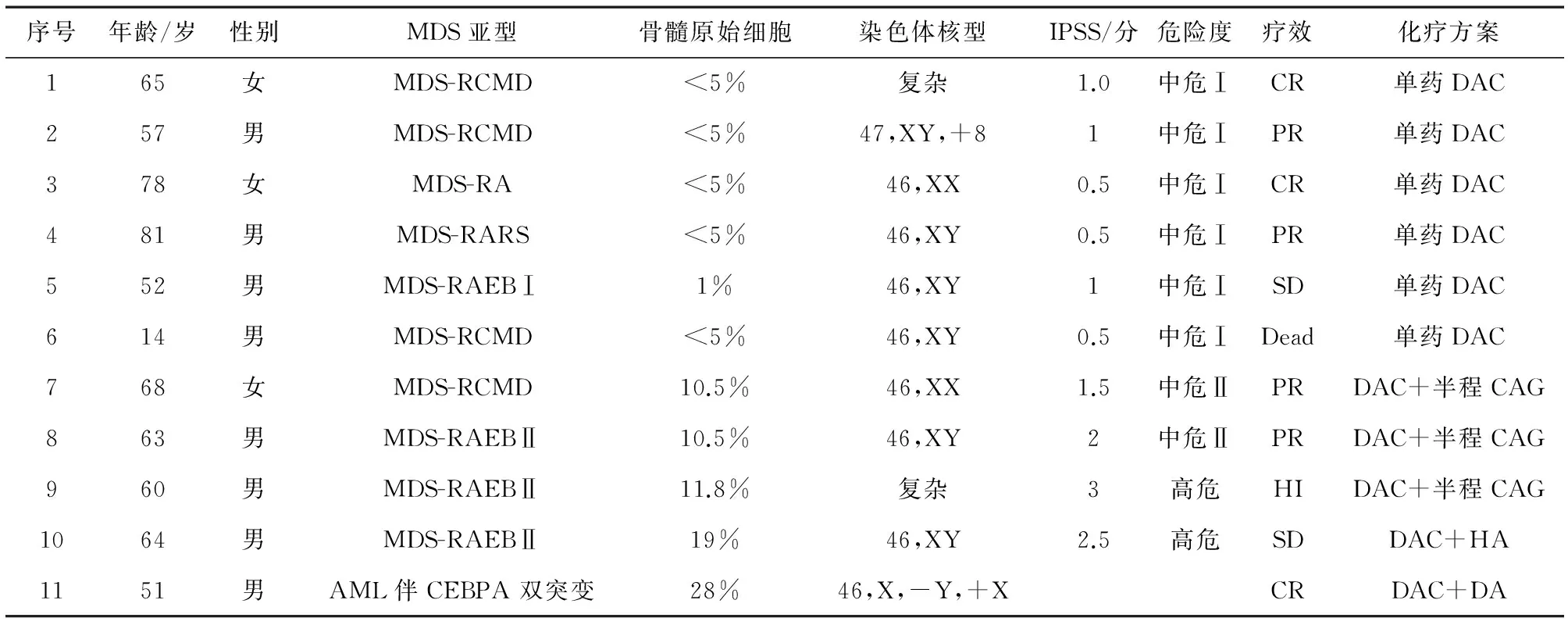
表1 11例MDS的临床资料
注:MDS为骨髓增生异常综合征;IPSS为国际预后积分系统;CR为完全缓解;PR为部分缓解;HI为血液学改善;SD为疾病进展;Dead为死亡。DAC为地西他滨,MDS-RA为难治性贫血,MDS-RARS难治性贫血伴环状铁粒幼细胞,MDS-RCMD为难治性贫血伴多系发育异常,MDS-RAEBⅠ为难治性贫血伴原始细胞过多Ⅰ,MDS-RAEBⅡ为难治性贫血伴原始细胞过多Ⅱ。
3 讨论
MDS是一种克隆性疾病,具有异质性,是因造血髓系干细胞、祖细胞或者多功能干细胞发生损伤而致的[3]。MDS患者一般以中老年人居多,因年龄偏高、免疫力低下、脏器功能不全等因素,难以承受标准计量化疗或造血干细胞移植[4-5]。如今MDS患者的治疗还没有标准的方案,我们需要寻找一种能够改善造血、提高患者生活质量而且安全有效的治疗方法[6-7]。
地西他滨属于DNA抗甲基化药物[8],使用超小剂量能使抑癌基因的正常去甲基化状态恢复,激活失活的抑癌基因的活性,促进细胞的正常分化和凋亡,但是如果高剂量使用时则会对细胞产生毒性作用[9]。CAG方案中阿糖胞苷属于嘧啶类抗代谢药物,能够干扰细胞增殖,有效抑制DNA的合成,其主要用于治疗急性粒细胞白血病[9]。G-CSF能促进白血病细胞的增殖,增加其对细胞周期依赖性药物的敏感性[10]。
地西他滨适宜用于国际预后评分系统(IPSS)评分为中高危的MDS、复发难治性白血病、MDS转化的AML及老年白血病患者[11-12],有研究结果表明,使用地西他滨治疗在低中危MDS患者中也获得了较好的疗效[13],运用地西他滨可延长MDS患者向白血病转化及死亡的中位时间,改善预后[14]。特别对于那些不能耐受高强度化疗的中高危老年患者,这些治疗方法能够降低输血依赖,促进病情稳定。
2006年美国食品药品监督管理局(FDA)批准地西他滨可用于治疗MDS,推荐剂量15 mg·m-2,每18 h一次,持续3 d,治疗病死率高。Steensma等[11]在ADOPT研究中采用20 mg·m-2,持续5 d,总有效率67.1%,血液学不良反应率70.9%,99例患者中有6例因为使用地西他滨死亡,死亡率6%,结果仍不满意。国内临床推荐剂量20 mg·m-2,持续5 d,为了能降低药物不良反应,我国某些学者如刘真真等[15]使用地西他滨20 mg·m-2,持续3 d,通过减低剂量来治疗MDS,取得一定效果,但不良反应发生率65%,仍然较高。因此,至今仍未找到地西他滨的最佳治疗方案。我们在本次11例中高危MDS患者及AML患者治疗中,改良地西他滨使用方法,减少地西他滨的剂量,即地西他滨5~7 mg·m-2·d-1,联合或不联合化疗方案,结果显示总有效率72.7%,缓解率27.5%,11例患者中,6例出现血液学不良反应,血液学不良反应发生率54.5%。3例出现肺部感染,感染发生率27.3%。1例出现消化道出血,出血发生率18.1%。也就是说超小剂量地西他滨皮下治疗中高危MDS及AML总有效率高(72.7%vs67.1%),血液学不良反应少(54.5%vs70.9%),安全性好[11]。为不能耐受强化疗和造血干细胞移植的患者提供了新的治疗方法。但由于我们所观察的病例数少,观察时间短,其有效性和安全性还需扩充病例数及随访,进一步证实上述结论[1]。
[1] 李迎伟,沈元元,李萨萨,等.超小剂量地西他滨治疗老年骨髓增生异常综合征[J].临床荟萃,2015,30(7):773-776.
[2] 张之南,沈悌.血液病诊断及疗效标准[M].北京:科学出版社,2007:232-235.
[3] 管俊,姜扬文,孙爱红,等.地西他滨联合半量预激方案对老年急性髓性白血病及高危骨髓增生异常综合征的影响[J/CD].中华临床医师杂志(电子版),2014,8(21):3897-3900.
[4] 邵宗鸿.中高危骨髓增生异常综合征的治疗选择[J].中华血液学杂志,2012,33(7):508-509.
[5] 中华医学会血液学分会.骨髓增生异常综合征诊断与治疗中国专家共识(2014年版)[J].中华血液学杂志,2014,35(11):1042-1048.
[6] 王萍.超小剂量的地西他滨联合CAG方案治疗中高危骨髓增生异常综合征及难治性白血病的效果分析[J].中国继续医学教育,2016,8(5):146-147.
[7] 李萨萨,陶千山,蒲莲芳,等.超小剂量地西他滨治疗骨髓增生异常综合征的近期疗效和不良反应观察[J].安徽医药,2016,20(6):1174-1178.
[8] 杨国华,钱锡峰,庄芸,等.地西他滨联合CAG方案治疗骨髓增生异常综合征与急性髓系白血病临床观察[J].白血病·淋巴瘤,2014(9):558-560.
[9] 张秀群,邓银芬,张磊,等.地西他滨序贯半量CAG方案治疗中高危骨髓增生异常综合征及白血病转化四例[J].白血病·淋巴瘤,2012,21(7):433-435.
[10] 刘丽娜,张青兰,刘玉章,等.超小剂量地西他滨联合HAG方案治疗骨髓增生异常综合征疗效观察[J].中国实用内科杂志,2016,36(8):688-689.
[11] STEENSMA DP,BAER MR,SLACK JL,et al.Multicenter study of decitabine administered daily for 5 days every 4 weeks to adults with myelodysplastic syndromes:the alternative dosing for outpatient treatment (ADOPT) trial[J].J Clin Oncol,2009,27(23):3842-3848.
[12] 唐元艳,熊涛,梁艳,等.地西他滨治疗高危骨髓增生异常综合征10例疗效观察[J].临床荟萃,2012,27(19):1731-1733.
[13] GARCIA-MANERO G,JABBOUR E,BORTHAKUR G,et al.Randomized open-label phase Ⅱ study of deciitabine in patients with low-or intermediate-risk myelodysplastic syndromes[J].J clin Oncol,2013,31(20):2548-2553.
[14] KANTARJIAN H,ISSA JP,ROSENFELD CS,et al.Decitabine improves patient outcomes in myelodysplastic syndromes:results of a phase Ⅲ randomized study[J].Cancer,2006,106(8):1794-1803.
[15] 刘真真,何广胜,吴德沛,等.减低剂量的地西他滨治疗骨髓增生异常综合征-难治性血小板减少[J].临床血液学杂志,2013,26(2):165-170.

