负载乙肝核心抗原-黑色素瘤抗原-A3融合蛋白的外周血单个核细胞对人非小细胞肺癌细胞体外杀伤作用的实验
林 知,陈 意,林童俊,焦顺昌解放军总医院 肿瘤内一科,北京 00853;达尔豪斯大学,加拿大哈里法克斯 B3K6R8
肺癌是全球范围内最常见的恶性肿瘤之一,发病率与死亡率均排在首位,严重威胁着人类的生命和健康。75%的肺癌患者在初次诊断时已是晚期,往往已伴发局部浸润或远处转移,放疗、化疗、靶向治疗是晚期肺癌的主要治疗方式,但5年生存率低[1-2]。肿瘤免疫治疗以其高效、低毒的特性成为一个新的治疗手段,给晚期肺癌患者带来了希望[3-4]。黑色素瘤抗原-A3(melanoma antigen gene-A3,MAGE-A3)被证实在正常的成熟组织中不表达(胎盘及睾丸除外),但在多种肿瘤组织中有不同程度的表达,其在肺癌中的表达率在40%以上,成为非小细胞肺癌免疫治疗中重要的靶抗原。MAGE-A3基因编码的肽段在免疫提呈细胞内被加工,特异性的肿瘤抗原与HLA-I类分子结合形成复合物,之后被效应T淋巴细胞识别,对MAGE-A3阳性表达的肿瘤细胞进行特异性杀伤[5]。
材料和方法
1 质粒与细胞株 含有2种MAGE-A3多肽(MAGEA3146-160-FFPVIFSKASSSLQL和MAGE-A3168-176-EVDPIGHLY)和乙肝核心抗原(hepatitis B core antigen,HBVc)的cDNA重组质粒pET28a-HBVc-MAGE-A3以及仅含有HBVc蛋白的pET28a-HBVc,两者均为加拿大Dr.Lin协助构建。非小细胞肺癌细胞株NCI-H358及人肾上皮细胞株HEK-293T购自美国ATCC公司。
2 主要试剂和耗材 DMEM培养基(购自Gibcobrl公司);RPMI-1640培养基(购自Gibcobrl公司);PBS(购自Hclyone);胎牛血清(购自BI公司);重组人白细胞介素-2(recombination human interleukin-2,rhIL-2)、重组人白细胞介素-4(recombination human interleukin-4,rhIL-4)(均购自 Peprotech公司 );二甲基亚砜(dimethyl sulfoxide,DMSO)(购自Sigma公司);淋巴细胞分离液Ficoll(购自上海生化试剂二厂);鼠抗人MAGE-A3单克隆抗体(购自abcam公司);羊抗鼠二抗(购自Santa Cruz公司);GAPDH抗体(购自Santa Cruz公司);LDH释放检测试剂盒(购自DojinDo)细胞培养瓶、细胞培养皿;6孔板、12孔板、96孔板(均购自corning公司);镍柱 (GE Healthcare;Ni SepharoseTM6 Fast Flow);Amicon Ultra-15 10K Centrifugal Filter Devices。
3 HBVc-MAGE-A3多肽融合蛋白的诱导表达及分离纯化 将构建的重组质粒pET28a-HBVc-MAGE-A3转化大肠埃希菌BL21,取适量转化成功的大肠埃希菌BL21菌液接种至转接至400 ml含10 mmol葡萄糖和100 g/ml卡那霉素(Kan)的LB液体培养基,37℃、140 r/min振荡培养至对数生长期,加入终浓度为1.0 mmol/L的异丙基硫化-β-D-半乳糖苷诱导表达16 ~ 18 h;收集诱导表达的菌体。HBVc-MAGE-A3多肽融合蛋白的分离和纯化加入160 ml Binding Buffer重悬菌体;添加Lysozyme至终浓度为0.2 mg/ml,室温孵育10 min;超声处理裂解菌体;4℃,10 000 r/min离心20 min,收集沉淀;30 ml Solubilization Buffer重悬沉淀,超声处理促进沉淀溶解,4℃孵育过夜;并处理样品,行考马斯亮蓝染色取1 000 ml诱导表达的菌液,10 000×g、4℃离心5 min;菌体沉淀用50 ml磷酸盐缓冲液重悬,冰浴,超声裂解细菌,加入Triton X-100至终体积分数为1%,混匀,冰浴放置30 min;12 000×g、4℃离心20 min;取上清液,采用十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecy1 sulfate polyacrylamidegel eletrophoresis,SDS-PAGE)鉴定目的蛋白。镍层析柱分离HBVc-MAGE-A3融合蛋白,经SDS-PAGE及凝胶薄层扫描鉴定纯化蛋白的纯度,最后将纯化的蛋白进行超滤脱盐,直至脱盐至合适浓度,0.22μm膜过滤除菌,-70℃保存。HBVc蛋白也按照以上步骤获取。
4 PBMC疫苗的制备 选取一名健康志愿者(男性,30岁)外周血100 ml,分装至4个50 ml离心管,等体积(1:1)加入人淋巴细胞分离液Ficoll,密度梯度离心,获得PBMC,调整其细胞密度为1×106/ml、分别加入 0.88μmol的 HBVc-MAGEA3融合蛋白,0.88μmol的HBVc蛋白以及等体积的PBS,共培养培养2 h后,PBS洗涤3次,使用40μg/ml丝裂霉素C处理冲击后的PBMC 1 h,PBS洗3次。
5 细胞株培养及MAGE-A3蛋白表达检测 分别传代培养非小细胞肺癌细胞株NCI-H358和人肾上皮细胞株HEK-293T,提取两种细胞的目的蛋白,通过Western blot技术检测MAGE-A3蛋白的表达。
6 效应细胞的体外诱导 用含IL-2、20%胎牛血清的RPMI-1640培养基调整细胞密度为1×106/ml;按照PBMC疫苗细胞与淋巴细胞数量比1:10的比例混合培养并分为以下几组:NTC组为未负载任何蛋白的PBMC+正常PBMC细胞;HBVc组为负载HBVc蛋白的PBMC+正常PBMC细胞;HBVc-MAGE-A3组为负载HBVc-MAGE-A3融合蛋白的PBMC+正常PBMC细胞。使用20 U/ml IL-2、10 U/ml IL-7和 10% FBS的 RPMI-1640培养基培养14 d,以获得效应细胞。
7 效应细胞的杀伤效应检测 使用LDH释放检测试剂盒检测各组效应细胞杀伤能力。反应组分为NTC、HBVc和HBVc-MAGE-A3三组。NTC组:肿瘤细胞+未负载任何蛋白PBMC刺激的淋巴细胞;HBVc组:肿瘤细胞+负载HBVc蛋白PBMC刺激的淋巴细胞;HBVc-MAGE-A3组:肿瘤细胞+负载HBVc-MAGE-A3融合蛋白PBMC刺激的淋巴细胞。每组分别以效靶比1∶1、2∶1、5∶1、10∶1、20∶1的比例加入效应细胞和肿瘤靶细胞各50μl,总体积为100μl。根据肿瘤细胞的不同,分为NCI-H358细胞组和HEK-293T细胞组。
8 LDH法检测淋巴细胞的杀伤活性 将上述杀伤试验96孔板放置于于37℃、5% CO2培养箱中培养3.5 h。最大释放组每孔加入5μl裂解液,继续孵育15 min。每孔加LDH反应液100μl,室温避光反应15 min。每孔加50μl终止液,轻摇10 s终止反应。酶标仪检测,波长490 nm,读取OD值。特异性杀伤活性计算:细胞毒%=(反应组OD值-效应细胞自然释放OD值-靶细胞自然释放OD值)/(靶细胞最大释放OD值-靶细胞自然释放OD值)×100%。
9 统计学分析 采用SPSS20.0统计软件进行分析,计量资料以-x±s表示,组间比较采用单因素方差分析,事后检验采用SNK检验方法。P<0.05为差异有统计学意义。
结 果
1 HBVc-MAGE-A3融合蛋白的获得 首先将HBVc DNA或者HBVc-MAGE-A3 DNA片段克隆到原核表达载体pET28a质粒中,构建pET28a-HBVc重组质粒和pET28a-HBVc-MAGE-A3重组质粒(图1A、图1B)。然后将重组质粒pET28a-HBVc-MAGEA3和pET28a-HBVc转染大肠埃希菌BL21,经IPTG诱导后,含重组质粒pET28a-HBVc-MAGEA3和pET28a-HBVc的大肠杆埃希菌BL21能够表达分子量约22.45 kU的HBVc-MAGE-A3融合蛋白和18.70 kU的HBVc蛋白(图1C、图1D)。经SDS-PAGE及凝胶薄层扫描鉴定纯化蛋白的纯度约为90%。
2 癌细胞株中MAGE-A3蛋白的表达 采用Western blot法检测非小细胞肺癌细胞株NCI-H358和人肾上皮细胞株HEK-293T中MAGE-A3蛋白的表达,可见NCI-H358表达量较高,而HEK-293T几乎不表达(图2)。因此,以MAGE-A3阳性的NCI-H358肺癌细胞为效应细胞攻击的细胞,而MAGE-A3弱表达的HEK-293T为阴性对照组。
3 效应细胞杀伤肿瘤细胞检测 实验结果显示,经负载HBVc-MAGE-A3融合蛋白的PBMC细胞刺激的HBVc-MAGE-A3组对NCI-H358的杀伤率显著高于其他两组(P<0.05),而经负载HBVc蛋白的PBMC细胞刺激的HBVc组与未负载任何蛋白的PBMC细胞刺激的NTC组对NCI-H358的杀伤作用无统计学差异(P>0.05)(图3)。从效靶比来看,三组的最高杀伤效率均在20∶1。以MAGEA3弱表达的HEK-293T为靶细胞的杀伤实验组杀伤率均非常低且三组之间差异无统计学意义。
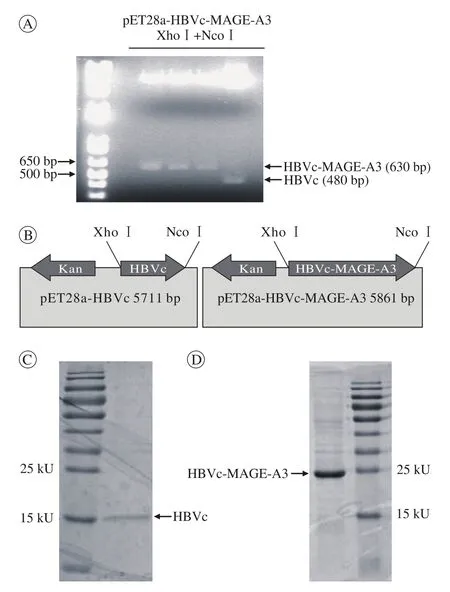
图1 质粒构建结果A:质粒图谱; B:pET28a-HBVc-MAGE-A3质粒和pET28a-HBVc质粒构建; C:HBVc蛋白分离纯化结果(SDS-PAGE);D:HBVc-MAGE-A3融合蛋白分离纯化结果(SDS-PAGE)Fig. 1 Plasmid construction A: Plasmid profile; B: Constructions of pET28a-HBVc-MAGE-A3 plasmid and pET28a-HBVc plasmid; C: HBVc protein separation and purification (SDS-PAGE); D: HBVc-MAGE-A3 fusion protein separation and purification (SDSPAGE)
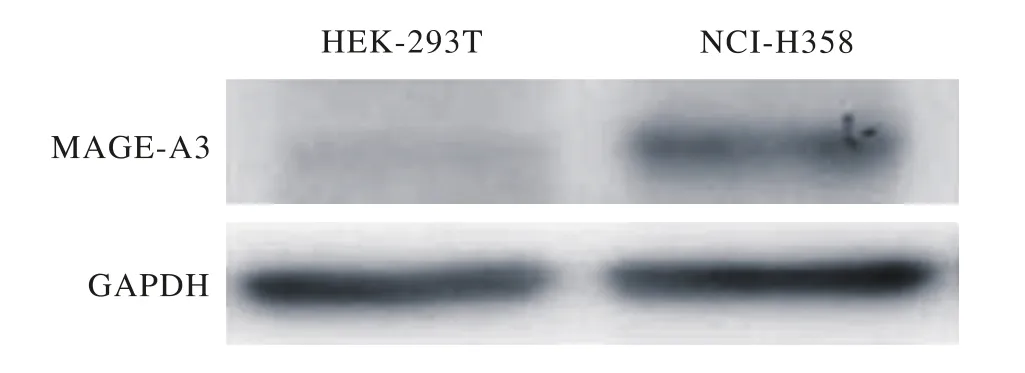
图2 靶细胞NCI-H358和HEK-293T细胞中MAGE-A3表达检测Fig. 2 MAGE-A3 expression detection in NCI-H358 cells and HEK-293T cells
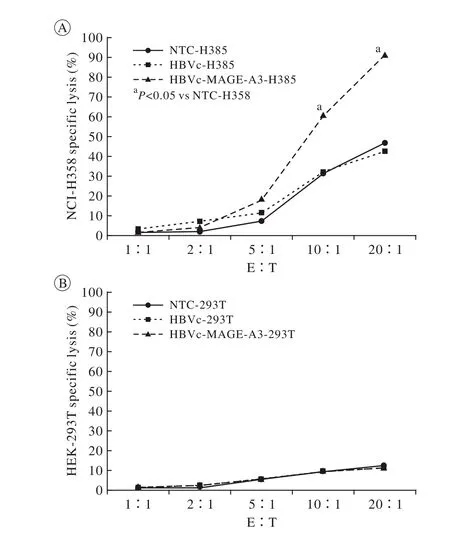
图3 三种效应细胞对两组靶细胞杀伤效果A:以NCI-H358细胞为靶细胞(aP<0.05,与HBVc组及NTC组比较); B:以HEK-293T细胞为靶细胞(P>0.05,与HBVc组及NTC组比较)Fig. 3 Specific killing effects of different effector cells on target cells A: NCI-H358 cell group (aP<0.05, vs HBVc group & NTC group); B: HEK-293T cell group (P>0.05, vs HBVc group& NTC group)
讨 论
黑色素瘤抗原(melanoma antigen,MAGE)基因是最早被发现的一族人类肿瘤特异性抗原基因。MAGE基因的表达产物中MAGE-3蛋白的免疫原性较强,是肿瘤特异性抗原的典型代表。MAGEA3是广泛存在于多种肿瘤中的肿瘤特异性抗原,除了在胎盘和睾丸中低水平表达外,在其他正常成熟组织均不表达,而睾丸是免疫豁免器官,所以MAGE-A3是一种可以作为多种肿瘤免疫治疗靶点的理想肿瘤相关抗原[6]。目前已经有大量的Ⅰ/Ⅱ期临床试验证明基于MAGE-A3细胞治疗的疫苗是有效的,如Belagenpumatucel-l可以明显改善肿瘤病人的生存状况[7-8]。本研究选用的多肽正是用于疫苗的多肽,具有较强的免疫原性,并且得到了与先前研究相同的效果[9-10]。在细胞学试验结果中可以看出,我们融合了多肽疫苗的融合蛋白HBVc-MAGE-A3可以诱导出针对MAGE-A3高表达靶细胞的特异性杀伤,效靶比为20∶1时,HBVc-MAGE-A3组的杀伤效率可以达到90%,而HBVc组和NTC组只有45%。而使用MAGE-A3低表达的细胞HEK-293T作为靶细胞时,三组之间无统计学差异。说明我们的HBVc-MAGE-A3融合蛋白疫苗具有诱导出MAGE-A3特异性杀伤的能力。
以往的MAGE-A3疫苗多数使用的是DC细胞作为抗原递呈细胞,因为DC细胞是人体内主要的递呈细胞,但DC细胞在外周血中的比例较低,大约只有0.1%,并且获得过程复杂,获得率很低,对老年患者和肿瘤晚期患者的体质要求较高,这对后期的临床转化造成较大的障碍[11-13]。我们研究发现,使用PBMC作为抗原递呈细胞也可以得到较好的杀伤肿瘤细胞的效果,并且PBMC具有获得过程容易,获得率高的特点,较DC细胞对患者体质要求较低。
以往的MAGE-A3疫苗研究大都使用抗原递呈细胞与CD8+T细胞共培养,促使CD8+T细胞产生特异性的识别,并特异性地扩增针对MAGE-A3阳性肿瘤细胞杀伤功能的细胞[11,14-15]。我们使用PBMC细胞作为抗原递呈细胞的共培养对象,不仅可以刺激特异性的CD8+T细胞增殖,还可以充分发挥CD4+T细胞的辅助功能,使CD8+T的杀伤功能更强[16]。并且使用PBMC作为杀伤效应细胞,还可以充分发挥其他杀伤细胞的功能,如NK细胞和NKT细胞。
我们使用了更有优势的佐剂分子HBVc。HBVc与MAGE-A3多肽融合以后,可以在体外自发形成类病毒颗粒状,并把MAGE-A3多肽包裹在最外层,使抗原递呈细胞接触抗原的机会大大增加[17]。
我们的实验发现,负载HBVc-MAGE-A3融合蛋白抗原的外周血单个核细胞能够成功诱导出特异性的细胞毒性T淋巴细胞,并且对MAGE-A3高表达的非小细胞肺癌细胞的杀伤作用显著优于MAGE-A3低表达的靶细胞,证实了MAGE-A3作为肿瘤免疫治疗的靶点具有特异性免疫杀伤效果。
MAGE-A3特异性地在肿瘤细胞表面的表达,为特异性免疫治疗开辟了一条新的道路。但是也有很多的问题有待论证:临床试验中MAGE-A3疫苗的剂量、细胞的输注方式、人体内的免疫环境等是否会影响肿瘤的特异性杀伤,是否与细胞实验的结果一致。相信通过逐步优化的实验设计与科学论证,针对晚期癌症的特异性免疫治疗有效率将会逐步提高。
1 Binder D, Hegenbarth K. Emerging options for the management of non-small cell lung cancer[J]. Clin Med Insights Oncol, 2013, 7:221-234.
2 Mountzios G, Linardou H, Kosmidis P. Immunotherapy in nonsmall cell lung cancer: the clinical impact of immune response and targeting[J]. Ann Transl Med, 2016, 4(14): 268.
3 孙琼, 焦顺昌. 非小细胞肺癌疫苗治疗的现状[J]. 解放军医学院学报, 2014, 35(4): 398-401.
4 杨纪华, 焦顺昌. 小细胞肺癌免疫治疗临床和基础研究现状[J].解放军医学院学报, 2014, 35(5): 516-518.
5 王胜杰, 陈绍水. MAGE-A3在非小细胞肺癌中的临床研究进展[J]. 临床合理用药杂志, 2016, 9(2): 180-181.
6 Esfandiary A, Ghafouri-Fard S. MAGE-A3 : an immunogenic target used in clinical practice[J]. Immunotherapy, 2015, 7(6): 683-704.
7 Lu YC, Parker LL, Lu T, et al. Treatment of Patients With Metastatic Cancer Using a Major Histocompatibility Complex Class II-Restricted T-Cell Receptor Targeting the Cancer Germline Antigen MAGE-A3[J]. J Clin Oncol, 2017, 35(29): 3322-3329.
8 Pujol JL, Vansteenkiste JF, De Pas TM, et al. Safety and Immunogenicity of MAGE-A3 Cancer Immunotherapeutic with or without Adjuvant Chemotherapy in Patients with Resected Stage IB to III MAGE-A3-Positive Non-Small-Cell Lung Cancer[J]. J Thorac Oncol, 2015, 10(10): 1458-1467.
9 Shimato S, Maier LM, Maier R, et al. Profound tumor-specific Th2 bias in patients with malignant glioma[J]. BMC Cancer, 2012,12: 561.
10 Liddy N, Bossi G, Adams KJ, et al. Monoclonal TCR-redirected tumor cell killing[J]. Nat Med, 2012, 18(6): 980-987.
11 Batchu RB, Gruzdyn O, Potti RB, et al. MAGE-A3 with cellpenetrating domain as an efficient therapeutic cancer vaccine[J].JAMA Surg, 2014, 149(5): 451-457.
12 Liu X, Li J, Liu Y, et al. Calreticulin acts as an adjuvant to promote dendritic cell maturation and enhances antigen-specific cytotoxic T lymphocyte responses against non-small cell lung cancer cells[J].Cell Immunol, 2016, 300 : 46-53.
13 Domingues D, Turner A, Silva MD, et al. Immunotherapy and lung cancer: current developments and novel targeted therapies[J].Immunotherapy, 2014, 6(11): 1221-1235.
14 Vanderstraeten A, Tuyaerts S, Everaert T, et al. In Vitro Assessment of the Expression and T Cell Immunogenicity of the Tumor-Associated Antigens BORIS, MUC1, hTERT, MAGE-A3 and Sp17 in Uterine Cancer[J]. Int J Mol Sci, 2016, 17(9): e1525.
15 Tzeng A, Kauke MJ, Zhu EF, et al. Temporally Programmed CD8α+DC Activation Enhances Combination Cancer Immunotherapy[J].Cell Rep, 2016, 17(10): 2503-2511.
16 田垒. 抗原肽、DC及CD4+ T细胞对CD8+ T细胞免疫应答的影响[D]. 杨凌: 西北农林科技大学, 2009.
17 Berlanda Scorza F, Tsvetnitsky V, Donnelly JJ. Universal influenza vaccines: Shifting to better vaccines[J]. Vaccine, 2016, 34(26):2926-2933.

