RP-HPLC法同时测定七味冬青叶散中苦杏仁苷、丹酚酸B 和杜鹃素的含量
陈龙,张珂,刘雪滢,夏祥,黄健,王航宇,王金辉,**
(1 石河子大学药学院/新疆植物药资源利用教育部重点实验室,新疆 石河子,832002;2 兰州和盛堂制药股份有限公司,甘肃 兰州730000;3 哈尔滨医科大学药学院,黑龙江 哈尔滨150081)
七味冬青叶散由冬青叶、北沙参、甘草、天竺黄、丹参、杜鹃叶和苦杏仁七味药材组成,用于止咳、化痰、平喘、润肺;急慢性气管炎、支气管炎,肺纤维化,支气管扩张及肺炎,为内蒙古民族大学附属医院蒙药制剂室配制。方中丹参具有活血祛瘀,通经止痛,清心除烦,凉血消痈等功效,丹酚酸B 为丹参主要指标性成分,且具有抗氧化、抗纤维化等作用[1-4]。苦杏仁具有润肺、止咳、滑肠等功效,苦杏仁苷为苦杏仁主要指标性成分,常作为祛痰止咳剂、辅助性抗癌药物[5,6]。杜鹃叶具有清热解毒,止血,化痰止咳等功效,杜鹃素为杜鹃叶主要指标性成分[7-8]。
目前,对于该制剂的测定方法尚未见报道,为了更有效的控制该制剂质量,本实验建立了同时测定七味冬青叶散中苦杏仁苷、丹酚酸B 和杜鹃素的RP-HPLC 方法,可用于该制剂的质量控制。
1 材料与方法
1.1 仪器与试剂
Waters 2695 型高效液相色谱仪,Waters 2998 型检测器,Empower 2.0 色谱工作站,DV215CD 型十万分之一电子分析天平(美国Ohaus 公司),KQ3200B型超声波清洗机(昆山市超声仪器有限公司),XH-C型旋涡混合仪(金坛市医疗仪器厂),FW-100 型高速万能粉碎机(北京市永光明医疗仪器有限公司),TGL-16G 型离心机(上海安亭科学仪器厂)。
七味冬青叶散(哲卫准字9604-105 号,生产批号:20150426,规格:15 g),苦杏仁、丹参、杜鹃叶均由内蒙古民族大学附属医院蒙药制剂室提供,杜鹃素(批号:110850-201605,中国食品药品检定研究院),苦杏仁苷(批号:110820-201607,中国食品药品检定研究院),丹酚酸B(批号:111562-201716,中国食品药品检定研究院),甲醇(色谱级,J.K Baker 公司,美国),分析级磷酸(武汉化学试剂厂),纯净水(杭州娃哈哈集团有限公司)。
1.2 方法
1.2.1 色谱条件
1.2.1.1 检测波长的选择
参照中国药典2015 版一部正文苦杏仁、丹参、杜鹃项下,分别选择在210、286、297 nm 波长处测定含量。
1.2.1.2 流动相的选择
色谱柱:Sunfire C18 (150 mm ×4.6 mm,5 μm),流动相A:甲醇,流动相B:0.1%磷酸水溶液,梯度洗脱:0 ~15 min:20% A →20% A、15 ~20 min:20% A →42% A、20 ~36 min:42% A →42%A、36~40 min:42% A→65% A、40~50 min:65%A→65% A,流速:1.0 mL·min-1,柱温:30 ℃,进样量:10 μL。
1.2.2 对照品溶液的制备
精密称取对照品苦杏仁苷、丹酚酸B 和杜鹃素各适量,分别置于5 mL 容量瓶中,加甲醇溶解后,定容至刻度,摇匀,即得浓度为1.018、0.9740 和0.9940 mg/mL 的苦杏仁苷、丹酚酸B 和杜鹃素对照品储备溶液。
精密吸取1.018、0.9740 和0.9940 mg/mL 的苦杏仁苷、丹酚酸B 和杜鹃素对照品储备溶液适量,置于5 mL 容量瓶中,用甲醇定容至刻度,摇匀,即得每1mL 含苦杏仁苷407.2 μg、丹酚酸B 389.6 μg、杜鹃素19.80 μg 的混合溶液A。
精密吸取1.018、0.9740 和0.9940 mg/mL 的苦杏仁苷、丹酚酸B 和杜鹃素对照品储备溶液适量,置于100 mL 容量瓶中,加甲醇溶解后,定容至刻度,摇匀即得每1mL 含苦杏仁苷217.0 μg、丹酚酸B 158.5 μg、杜鹃素5.900 μg 的混合溶液B。
1.2.3 阴性样本溶液的制备
取冬青叶、北沙参、甘草和天竺黄各药材适量,粉碎成细粉,过60 目筛,取过筛后细粉按照处方中一定比例配制样品,混合均匀后置于具塞锥形瓶中,精密加入甲醇25 mL,密塞,摇匀,称取重量,室温下超声处理30 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,离心(8000 r/min,10 min),离心后吸取上清液用微孔滤膜(0.22 μm)滤过,即得阴性样本溶液。
1.2.4 供试品溶液的制备
1.2.4.1 七味冬青叶散溶液的制备
取七味冬青叶散粉末约1.0 g,精密称定,置具塞锥形瓶中,精密加入甲醇10 mL,密塞,摇匀,称定重量,室温下超声处理30 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,离心(8000 r/min,10 min),离心后吸取上清液用微孔滤膜(0.22 μm)滤过,取滤液作为七味冬青叶散供试品溶液,每次吸取10 μL注入高效液相色谱仪中分析。
1.2.4.2 苦杏仁、丹参、杜鹃叶供试品溶液的制备
取各药材适量,粉碎,过60 目筛,精密称定苦杏仁粉末约0.1 g、丹参及杜鹃叶粉末约0.25 g,分别置于具塞锥形瓶中,精密加入甲醇25 mL,密塞,摇匀,称定重量,室温下超声处理30 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,离心(8000 r/min,10 min),离心后吸取上清液用微孔滤膜(0.22 μm)滤过,即得苦杏仁、丹参及杜鹃叶供试品溶液,吸取各供试品溶液10 μL 注入高效液相色谱仪中分析。
2 结果与分析
2.1 专属性考察
精密吸取甲醇溶剂、阴性样本溶液、混合溶液A和七味冬青叶散供试品溶液在“2.1”色谱条件下进样分析,进样量10 μL,苦杏仁苷、丹酚酸B 和杜鹃素色谱峰与相邻色谱峰的分离度均大于1.5,对称因子均在0.95~1.05 之间,理论板数按丹酚酸B 峰计算大于5000,在对照品色谱峰位置处,供试品具有相同保留时间的色谱峰,空白溶剂甲醇在此保留时间处无色谱峰,各药材在相同波长下具有同一保留时间的色谱峰(图1)。
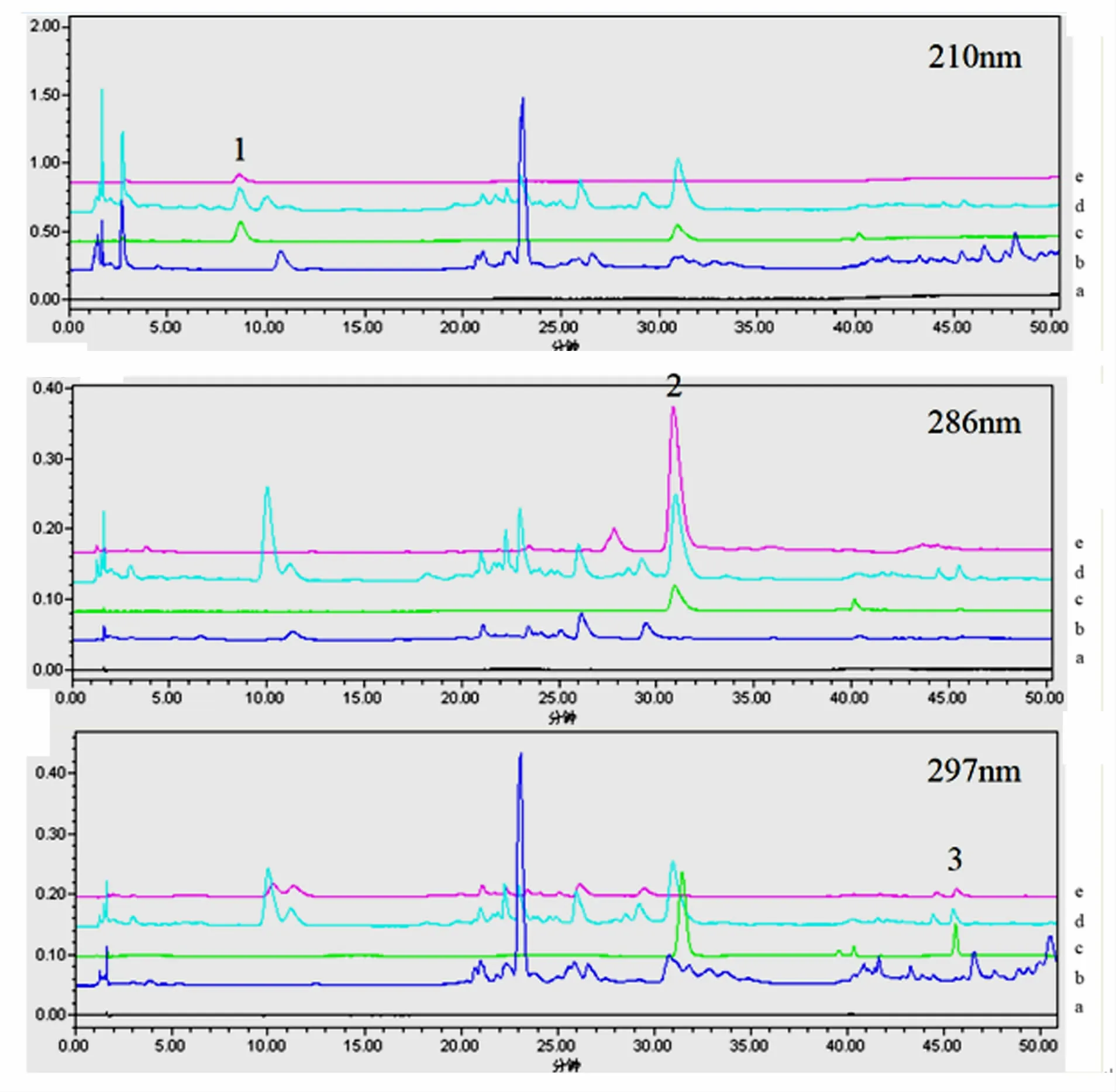
图1 空白溶剂、对照品、供试品和阴性溶液的HPLC 图Fig.1 HPLC chromatograms of blank solvent,reference substance,sample and negative solution
2.2 线性关系考察
取混合溶液A,分别精密吸取1、2、6、10、14、18、22 μL 在“2.1”色谱条件下注入高效液相色谱仪分析,以混合对照品溶液中各对照品的浓度(C)为横坐标,峰面积A 为纵坐标,计算回归方程,结果显示苦杏仁苷、丹酚酸B 和杜鹃素在一定范围内呈良好线性关系,所得回归方程及线性范围见表1。

表1 苦杏仁苷、丹酚酸B 和杜鹃素的线性回归方程n=7Tab.1 Regression equation of nitrilosides,salvianolic acid B and farrerol
2.3 精密度试验
取同一混合溶液A 重复进样6 次,进样量10 μL。计算苦杏仁苷、丹酚酸B 和杜鹃素峰面积的RSD 值分别为:0.70%、0.55%和0.45%,表明仪器精密度良好。
2.4 稳定性试验
取室温下放置的同一份七味冬青叶散供试品溶液,分别在0、2、4、8、12、18、20 h 进样分析,进样量10 μL,测得苦杏仁苷、丹酚酸B 和杜鹃素的峰面积的RSD 值分别为1.3%、0.94%和0.86%,表明七味冬青叶散供试品在室温下放置20 h 稳定。
2.5 重复性试验
取同一批号七味冬青叶散供试品6 份,按“2.4.1”供试品制备方法制得供试品溶液,在“2.1”色谱条件下进样分析,进样量10 μL,测得苦杏仁苷、丹酚酸B 和杜鹃素的含量分别为0.43%、0.32%、0.012%,RSD 值分别为1.5%、1.9%和1.5%,表明该方法重复性良好。
2.6 加样回收率试验
取已测含量的同一批次七味冬青叶散供试品6 份,每份约0.5 g,精密称定,分别精密加入与样品中各成分等量的混合对照品溶液B 10 mL,按“2.4.1”项下方法制备供试品溶液,在“2.1”色谱条件下进样分析,进样量10 μL,测得苦杏仁苷、丹酚酸B 和杜鹃素平均回收率结果见表2。
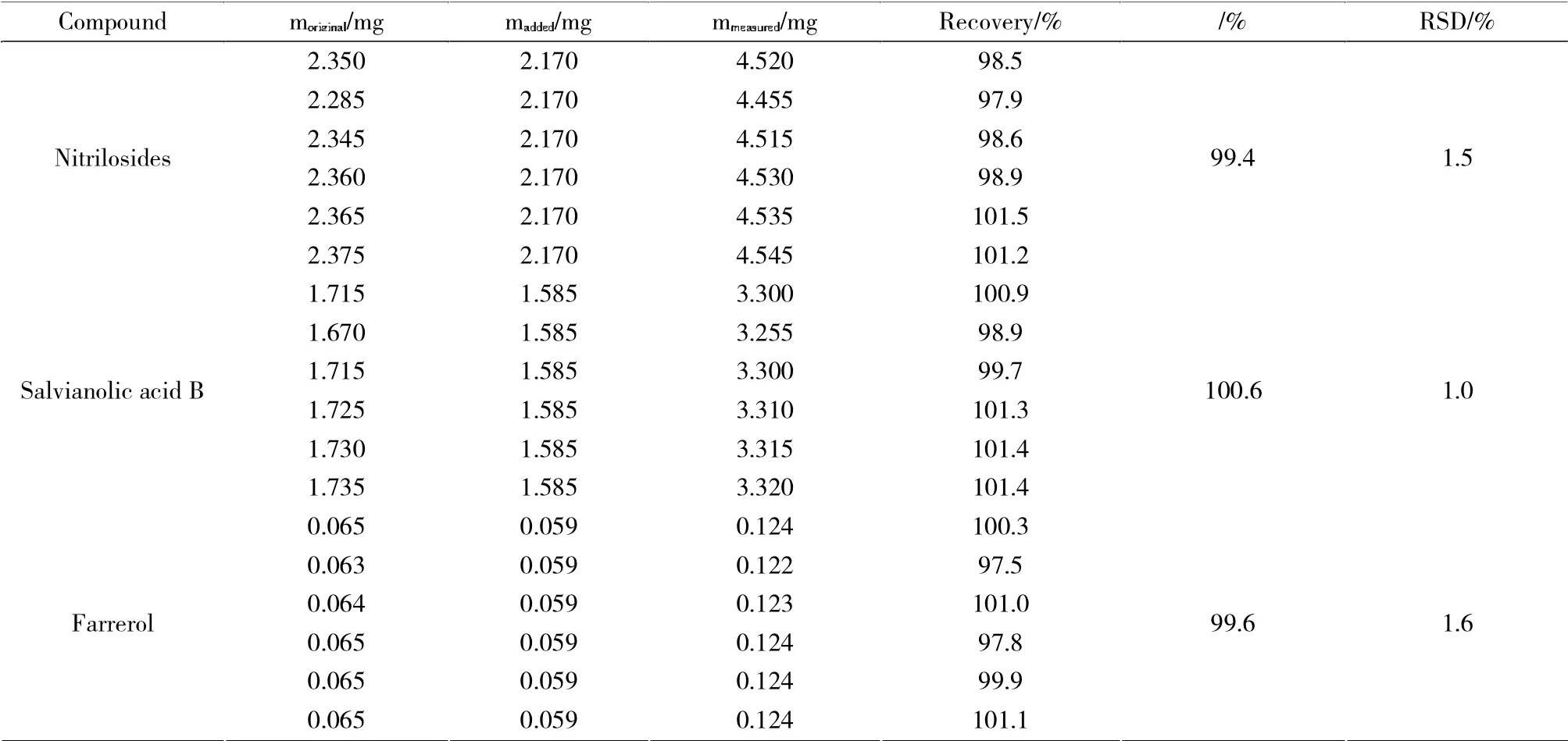
表2 苦杏仁苷、丹酚酸B 和杜鹃素的回收率测定结果 n=6Tab.2 Recovery of nitrilosides,salvianolic acid B and farrerol
2.7 样品测定
取七味冬青叶散按“2.4.1”方法制备供试品溶液,苦杏仁、丹参、杜鹃叶按“2.4.2”方法制备供试品溶液,在“2.1”色谱条件下进样分析,每次进样10 μL,测定各样品苦杏仁苷、丹酚酸B 和杜鹃素的含量,结果见表3。
以七味冬青叶散中苦杏仁苷为例,称取七味冬青叶散粉末1.00297 g,加入色谱甲醇10 mL,超声离心处理后,进入液相分析,进样量为10 μL,计算结果为:
供试品溶液的浓度=1.00297g/10mL=0.100297 g/mL=100.297 mg/ml=100.297 μg/μL。100.297 μg/μL×0.436%=0.4372949 μg/μL。
进样量G=0.4372949 μg/μL×10 μL=4.372949 μg。苦杏仁苷进样量G 的范围为:0.4072-8.958 μg,符合范围。
同理,单味药材以杜鹃叶中杜鹃素为例,称取杜鹃叶粉末0.25240 g,加入25 mL 色谱甲醇,超离心处理后,进入液相分析,进样量为10 μL,计算结果为:
杜鹃叶供试品溶液的浓度=0.25240 g/25 mL=0.010096 g/mL=10.096 mg/mL=10.096 μg/μL。0.096 μg/μL ×0.088%=0.00888448 μg/μL。进样量G=0.00888448 μg/μL×10 μL=0.0888448 μg。杜鹃素 进样量G 的范围为0.01988-0.4374 μg,符合范围。
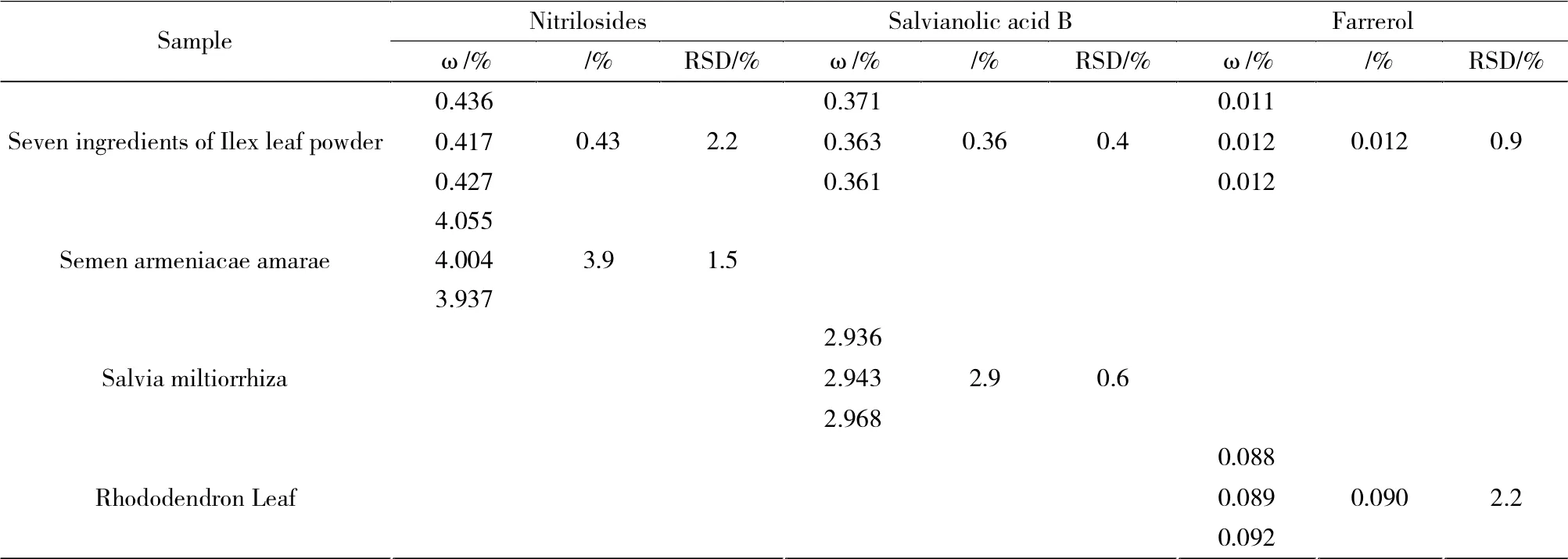
表3 样品含量测定结果 n=3Tab.3 Results of the contents determination of samples
3 讨论
(1) 参照2015 版《中华人民共和国药典》,苦杏仁苷的最大吸收波长为210 nm,丹酚酸B 的特征吸收波长为286 nm,杜鹃素的最大吸收波长为297 nm,在本实验中,选用了210、286、297 nm 为检测波长,能兼顾各个组分的检测,且各组分响应值均匀,具有良好的代表性。
(2) 为了使苦杏仁苷、丹酚酸B 和杜鹃素更好的分离,且不受其他组分和溶剂的干扰,在方法建立的过程中,对流动相的组成进行了优化,采用乙腈-0.1%的磷酸溶液、甲醇-0.1%的磷酸溶液和甲醇- 水为流动相,梯度洗脱。结果显示,以甲醇为有机相的流动相系统,分离效果好,加入磷酸使峰型得到了优化,故选择甲醇-0.1%的磷酸溶液作为流动相。
(3)考察了提取溶剂用量对提取率的影响,分别选择了10 mL、25 mL 的甲醇对供试品进行超声提取30 min,结果显示,溶剂用量为10 mL 时,既可以将上述3 种成分完全提取,同时也满足实验中3 种成分的用量,因此,本实验选择10 mL 甲醇提取溶剂,超声时间30 min 作为供试品的处理方法。
本方法快速简单,结果准确,重现性好,稳定性高,应用于七味冬青叶散的含量测定,完善其质量控制。

