两种新辅助化疗方案治疗乳腺癌的疗效比较
李佳珍, 权 毅
(西南医科大学附属第一医院乳腺外科, 四川 泸州 646000)
近年来,乳腺癌发病率逐年上升,发病越来越趋于年轻化,已成为我国妇女身心健康的重大威胁。如何让乳腺癌患者得到更有效的治疗是医生关注的重点,因此乳腺癌治疗方法越来越多元化、规范化。其中新辅助化疗(neoadjuvant chemotherapy,NCT)对局部晚期乳腺癌的治疗价值已得到肯定[1],是治疗局部晚期乳腺癌的重要方法之一。它是指在手术前予以全身性、系统性的细胞毒性药物治疗,以达到降低肿瘤分期,提高手术切除率的目的,并且有利于医生了解肿瘤细胞对化疗药物的敏感性[2-3]。新辅助化疗方案的选择目前国际上无统一标准,大多参照辅助化疗方案,主要为含蒽环类药物和(或)紫杉类药物的化疗方案。TEC方案及EC→T方案仍然是目前一线辅助化疗方案,本研究主要对比探讨TEC与EC→T方案新辅助化疗疗效及不良反应。现报告如下。
1 资料与方法
1.1 临床资料 选择2013—2016年于我科收治的Ⅱ~Ⅲ期乳腺癌新辅助化疗的女性患者52例,年龄38~69岁,中位年龄51岁。纳入标准:(1)Ⅱ~Ⅲ期的可手术乳腺癌患者;(2)初诊单侧乳腺浸润性导管癌,未接受过任何治疗,不包括复发转移患者;(3)患者经空心针穿刺确诊为乳腺浸润性导管癌,并获得其免疫组化相关指标;(4)全部患者一般情况良好,Karnofsky评分>80分;(5)心、肺、脑、肾等重要器官功能良好;(5)不伴发其他恶性肿瘤。
1.2 治疗方法 EC→T方案第1~4个周期:盐酸表柔比星(EPI)100 mg/m2静脉滴注, d 1;环磷酰胺(CTX) 600 mg/m2静脉滴注,d 1。EC→T方案第5~8个周期:多西他赛(TXT)100 mg/m2静脉滴注,d 1。TEC方案第1~6个周期:EPI 75 mg/m2静脉滴注,d 1;CTX 500 mg/m2静脉滴注,d 1;多西他赛(TXT)75 mg/m2静脉滴注,d 2。每21天为1个周期,使用多西他赛化疗前予以地塞米松预处理,化疗过程中行护心、保肝、防过敏、止吐等对症治疗。化疗结束后第3天、第7天复查血常规、肝肾功,若出现白细胞、中性粒细胞降低或转氨酶升高等,则在医生指导下及时予以升白细胞、保肝等对症处理。每次化疗用药前完善查体及乳腺彩超,评估化疗疗效。52例患者均于完成3~4个新辅助化疗周期后,于我院接受乳腺癌改良根治术治疗。所有患者初次化疗前及术前均完善乳腺增强MIR检查以评估肿瘤情况,化疗前及术前心脏彩超均提示左心室射血分数未见明显异常。两组患者绝经与否、临床分期及免疫组化指标方面均无显著性差异(P>0.05),具可比性。
1.3 疗效评价 新辅助化疗后肿瘤原发灶的疗效依据国际抗癌联盟(UICC)实体瘤疗效评定标准评估疗效[4]。临床完全缓解(CR):彩超显示所有靶病灶消失,全部病理淋巴结短直径必须减少至<10 mm;部分缓解(PR):彩超显示与基线病灶最长直径总和比较,靶病灶直径总和至少下降30%;病情稳定(SD):彩超显示靶病灶减小的程度未达到PR,增加程度也未达到PD水平,介于两者之间;疾病进展(PD):彩超显示靶病灶的直径总和与开始治疗以来记录的病灶最小直径总和比较增加至少20%,并且直径总和的绝对值增加至少5 mm。当出现1个或多个新发病灶,也视为疾病进展。有效率=(CR+PR)/总例数×100%。
1.4 不良反应评估 骨髓抑制、消化系统反应(恶心、呕吐、腹泻、肝功能损伤等)、脱发、心脏毒性等依据WHO抗癌药物常见不良反应分级进行评估。
1.5 统计学方法 采用SPSS 19.0统计软件进行统计学分析,计数资料比较采用χ2检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 两组疗效比较 EC→T组治疗有效率为72.73%,TEC组治疗有效率为86.67%,两组有效率比较差异无统计学意义(P>0.05)。见表1。
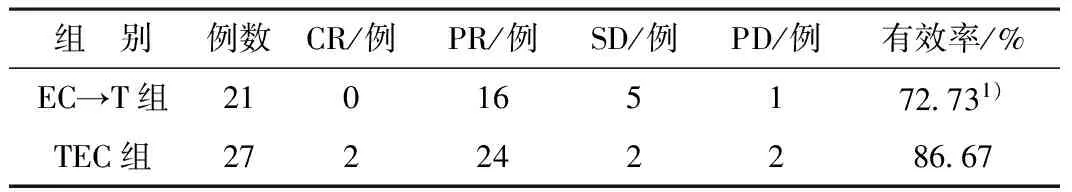
表1 两组疗效比较
注:1)与TEC组比较P=0.290
2.2 两组化疗不良反应比较 所有患者完成新辅助化疗疗程后均未出现化疗相关死亡或因不能耐受化疗不良反应而终止化疗者。EC→T组骨髓抑制及脱发严重程度均轻于TEC组(P<0.05),而两组消化系统反应严重程度的比较差异无统计学意义(P>0.05),见表2。本研究中心脏毒性发生率为0%。
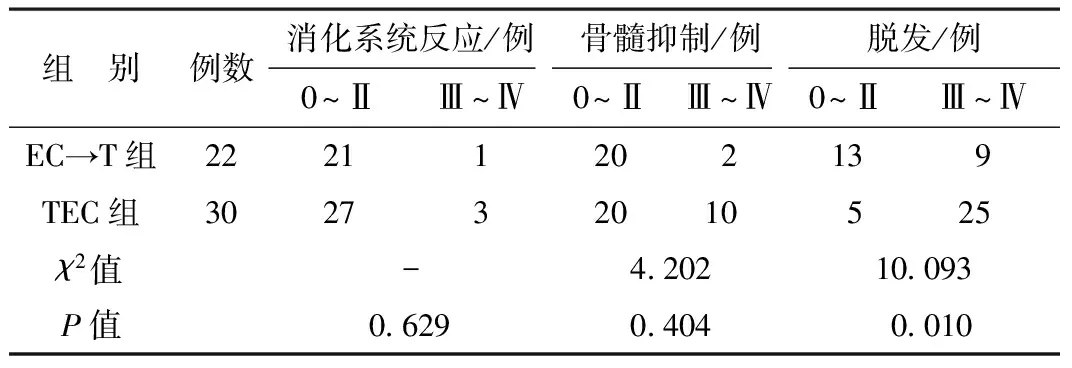
表2 两组化疗不良反应比较
3 讨 论
Frei于1982年提出新辅助化疗的概念,即术前化疗。2001 年美国乳腺与肠道外科辅助治疗研究组B-18大型随机临床试验研究结果指出,新辅助化疗疗效至少与术后辅助化疗疗效相当,且发现许多原本不可手术患者经化疗后肿瘤降期,接受了手术治疗,显著改善了生存期[5]。王永胜等[6]提出新辅助化疗后病理完全缓解(pathologic complete response, pCR)是预测乳腺癌患者远期生存的重要指标之一,治疗后达pCR的患者5年生存率明显提高且预后良好。随着新辅助化疗在乳腺癌治疗中应用越来越广,其方案的选择成为临床上亟待解决的问题。选择合适的新辅助化疗方案不仅能提高患者的近期疗效,减少不良反应,还能提高总生存率、无病生存率、无事件生存率。
在化疗药物的选择上,目前蒽环类及紫杉醇类仍是国际上公认的乳腺癌的一线化疗用药,当然,环磷酰胺也起到重要作用。多西他赛为紫杉类抗肿瘤药,通过促进微管双聚体装配成微管,同时防止去聚化过程而使微管稳定,阻止细胞于G2期和M期,从而抑制癌细胞的有丝分裂和增殖,单药用于乳腺癌患者有效率可达41%~75%[7]。环磷酰胺则通过与DNA鸟嘌呤的第7位氮共价结合,产生DNA的双链内的交叉联结或DNA的同链内不同碱基的交叉联结,使细胞由G期进入S期延迟,大剂量时对各周期的细胞和非增殖细胞均有杀伤作用。此外,它还可诱导细胞凋亡。表柔比星属于蒽环类药物,为乳腺癌辅助化疗的一线用药,
为直接嵌入DNA双链的碱基对之间,形成稳定复合物,干扰转录过程,阻止mRNA形成,可抑制DNA和RNA的合成,属于细胞周期非特异性药物。该类药物有效率为50%~85%,pCR率为0~24%[8]。
本研究结果显示,EC→T与TEC两种新辅助化疗方案有效率均较高,差异无统计学意义(P>0.05),但EC→T组骨髓抑制及脱发程度均轻于TEC组(P<0.05)。可见,EC→T方案在新辅助化疗中有一定的应用前景,对今后乳腺癌患者新辅助化疗方案的选择有一定的指导意义。由于本研究样本量较小,结论有待大样本、多中心的试验研究进一步论证。
[1]KUROSUMI M. Significance and problems in evaluations of pathological responses to neoadjuvant therapy for breast cancer[J]. Breast Cancer, 2006, 13(3): 254.
[2]CONNOLLY R M, STEARNS V. Current approaches for neoadjuvant chemotherapy in breast cancer [J]. Eur J Pharmacol, 2013, 717(1/3): 58-66.
[3]赵广章,刘海英,刘启龙,等.TAC与AT方案新辅助化疗治疗局部晚期乳腺癌疗效分析[J].现代肿瘤医学,2014,22(7):1587-1589.
[4]李龙飞,高艳丽,李孟圈,等.TAC方案在Ⅲ期乳腺癌新辅助化疗中的疗效观察[J].肿瘤基础与临床,2014,27(4):349-350.
[5]WOLMARK N, WANG J, MAMOUNAS E, et al. Preoperative chemotherapy in patients with operable breast cancer: nine-year results from National Surgical Adjuvant Breast and Bowel Project B-18[J]. J Natl Cancer Inst Monogr, 2001(30): 96-102.
[6]王永胜,廖宁.采用列线图对乳腺癌进行新辅助治疗后病理完全缓解及无复发生存的预测[J].循证医学,2007,7(3):144-148.
[7]李丽,张亚男,尤承忠.乳腺癌新辅助化疗的研究进展[J].东南大学学报:医学版,2013(6):766-771.
[8]TRUDEAU M, SINCLAIR S E, CLEMONS M, et al. Neoadjuvant taxanes in the treatment of non-metastatic breast cancer: a systematic review [J]. Cancer Treat Rev, 2005, 31(4): 283-302.

