铁氧化物与丙酸对土壤中六氯苯厌氧降解影响
刘翠英,王 宇,马煜春
铁氧化物与丙酸对土壤中六氯苯厌氧降解影响
刘翠英1,2*,王 宇3,马煜春3
(1.南京信息工程大学气象灾害预报预警与评估协同创新中心/江苏省农业气象重点实验室,江苏 南京 210044;2.中国科学院南京土壤研究所土壤环境与污染修复重点实验室,江苏 南京 210008;3.南京信息工程大学应用气象学院,江苏 南京 210044)
采用红壤性水稻土进行厌氧培养试验,设定灭菌对照、对照、丙酸、针铁矿、丙酸+针铁矿5个处理,分析铁氧化物、丙酸及其交互作用对土壤中六氯苯还原脱氯过程的影响及其反应机制.结果表明,培养40d后,5个处理的土壤中六氯苯可提取态残留量分别减少了26.9%、48.5%、63.4%、56.9%和72.9%;六氯苯还原脱氯主要生成五氯苯;添加丙酸在整个培养过程均显著促进六氯苯还原脱氯降解;添加针铁矿在培养前期促进六氯苯还原脱氯的效果明显;同时添加丙酸和针铁矿对促进六氯苯还原脱氯具有协同作用.
六氯苯;还原脱氯;针铁矿;丙酸;红壤性水稻土
六氯苯(HCB)是首批被列入《关于持久性有机污染物的斯德哥尔摩公约》的12种持久性有机污染物(POPs)之一[1].HCB具有高毒性和潜在的致癌性,且被美国国家环保署列为内分泌干扰物[2].其“憎水亲脂”的性质使HCB主要累积在土壤中[3].污染农田中的HCB能够通过食物链进入人体,对人类健康造成潜在的威胁.因此,如何消除土壤中HCB污染成为近年来亟待解决的重要科学问题.
厌氧条件下,还原脱氯是HCB降解的关键途径[4].厌氧还原脱氯是在得到电子的同时脱去一个氯取代基,H2是主要电子供体,但直接向污染源区导入H2比较困难,由于有机物能够在微生物作用下发酵生成H2,通常使用有机物(脂肪酸、醇类和糖类等)作为电子供体基质[5].H2作为有效的还原剂提供还原脱氯所需电子,HCB接受电子并在脱氯微生物作用下逐级脱氯转化为低氯代苯.厌氧条件下,土壤中存在多种还原反应,如产甲烷、硫酸盐还原、反硝化、产乙酸、异化铁还原等.由于还原脱氯所释放的自由能较高,在H2浓度较低的条件下还原脱氯也能够发生[6-8].因此,维持较低的H2浓度有利于避免其它还原过程与还原脱氯竞争电子.研究表明,淹水条件下,土壤中的有机物厌氧分解会产生大量脂肪酸[9],不同类型脂肪酸对促进还原脱氯的效果差异显著,主要原因是各脂肪酸分解生成H2的分压不同.丙酸发酵生成H2分压低于10-4.4个标准大气压,乳酸发酵生成H2分压比丙酸高出3个数量级[10].因此,本研究选择丙酸作为缓释H2的电子供体基质,探讨其加速氯代POPs还原脱氯降解的效果.
研究表明,红壤性水稻土中存在的大量铁氧化物可促进氯代POPs还原脱氯降解[11-12].土壤中的铁还原细菌,如S12、L17、CY01等可以直接参与氯代POPs降解过程,而铁氧化物可促进土壤中铁还原细菌生长[13-15];另外,铁氧化物可被铁还原细菌还原产生Fe(Ⅱ),而Fe(Ⅱ)可作为有效的电子供体促进HCB还原脱氯[16-17].然而,罕有关于土壤中铁氧化物和有机物脂肪酸对于氯代POPs还原脱氯交互作用的研究.
红壤性水稻土广泛分布于热带、亚热带地区,并含有大量的铁氧化物和铁还原菌[18].本研究选择红壤性水稻土作为供试土壤,选择丙酸作为电子供体基质,分析土壤中HCB还原脱氯速率与丙酸分解过程及Fe(Ⅲ)还原生成Fe(Ⅱ)动态之间的内在联系.研究结果将为探索加速土壤中氯代POPs消减途径提供参考.
1 材料与方法
1.1 供试土壤理化性质与污染土的制备
供试土样为江西省鹰潭地区的红壤性水稻土(28°12′N,116°55′E),取0~20cm表层土,风干后,过2mm筛备用.供试土壤的基本理化性质如下:pH值为5.1,有机质含量为35g/kg,可溶性有机碳含量为40.2mg/kg,游离氧化铁含量为27.3g/kg,无定形氧化铁含量为2.1g/kg,土壤中Fe(Ⅲ)与Fe(Ⅱ)的含量之比为20.7,黏粒、粉粒和砂粒含量分别为26.5%、42.1%和31.4%,具体分析方法参见文献[19].土壤中HCB的背景值为4.1ng/g.
污染土的制备方法参见文献[20].称取50mg的HCB完全溶解于100mL丙酮,将含有HCB的丙酮溶液加入140g细石英砂(100目),充分搅拌至丙酮全部挥发,制成HCB均匀污染的石英砂.称取5g污染石英砂和500g土壤拌匀,即得到HCB浓度为12.3µmol/kg的污染土壤,室温放置1周后备用.由于土壤对HCB的固持作用以及分析过程中HCB的损失,气相色谱检测到土壤中HCB的初始浓度为10.8µmol/kg.
1.2 试验仪器与化学试剂
安捷伦(Agilent,6890)气相色谱仪-ECD检测器63Ni;安捷伦7683自动进样器(Agilent,USA);岛津(Shimadzu,GC-12A)气相色谱仪-FID检测器;生化培养箱(LRH-250,上海印溪);旋转蒸发仪(RE-3000,上海亚荣).
各种氯代苯标样(纯度³99.5%,德国Ehrenstorfer博士提供);哌嗪-1,4-二乙磺酸(PIPES,纯度>98%)由美国Sigma-Aldrich公司提供.正己烷、丙酮、二氯甲烷和丙酸(分析纯)由上海国药集团化学试剂有限公司生产;无水硫酸钠在400ºC下干燥4h后备用;硅胶在130ºC下保持18h后,加入3.3%去离子水混匀,平衡6h后待用.
1.3 试验设计
本研究设以下5个处理:①灭菌土对照(灭菌对照);②HCB污染土壤(对照);③HCB污染土壤+丙酸(丙酸);④HCB污染土壤+针铁矿(针铁矿);⑤HCB污染土壤+丙酸+针铁矿(丙酸+针铁矿).将500g污染土壤装入1L棕色广口瓶,丙酸和针铁矿分别按10mmol/kg、20g/kg干土的比例添加.由于添加丙酸及针铁矿可导致土壤pH值变化,进而干扰其作为氧化/还原剂对HCB还原脱氯的作用,且淹水条件下土壤pH值逐渐趋于7.因此,本研究加入50mmol/L的PIPES缓冲溶液使土壤pH值保持7.0,并使土壤表面水层高度保持1.5cm,瓶中气体体积约为500mL,塞紧瓶塞后,从通气管通入高纯氮气30min排氧,然后用止水夹夹紧通气口连接的硅胶管,使培养瓶达到严格密封厌氧条件,随后将培养瓶置于25℃的生化培养箱中避光培养.试验设3个重复.培养周期为40d,分别于第0、4、8、12、16、24、32、40d采集土壤样品和气体样品,测定其中HCB及其降解产物含量,并测定土壤中Fe(Ⅱ)含量;分析每天甲烷释放速率;每次取样时测土壤氧化还原电位(Eh).每次取样完毕后,通氮30min除氧后密封,继续培养.
1.4 分析方法
每次采样之前,采用PHB-06型mV计测定土壤Eh.每周用不锈钢土钻取土壤样品约10g,用于测定反应体系中HCB及其降解产物和Fe(Ⅱ)含量.称取土样约1g置于50mL离心管中,加入30mL正己烷/丙酮(4/1,体积比),于25℃、60kHz条件下超声萃取2h后,将提取液转移至梨形瓶,在45℃旋转蒸发至2mL左右,经过填有2g Na2SO4和1g硅胶的SPE柱净化,净化时用15mL体积比为9/1的正己烷/二氯甲烷淋洗,再将淋洗液旋转蒸发浓缩定容至2mL,采用安捷伦气相色谱仪-ECD检测器测定HCB及其降解产物的浓度.气相色谱测定条件为:DB-5柱(30.0m× 0.32mm×0.25µm),载气为N2,流速为1.5mL/min.升温程序:柱初温为60℃,保持2min,以5℃/min的速度升温至190℃,保持0min,然后以20℃/min的速度升温至280℃,保持7min,进样口的温度为240℃,电子捕获检测器(ECD)的温度为290℃.采用不分流进样,进样量为1µL,外标法进行测定.
称取土样约1g于50mL离心管中,加入40mL 0.5mol/L的盐酸,震荡提取1.5h后离心过0.22µm滤膜,取1mL滤液加入1mol/L的碳酸钠缓冲溶液2mL和1g/L的邻菲罗啉2mL显色1h后,采用紫外-可见分光光度计于510nm测定Fe(Ⅱ)的浓度,详细分析方法参见文献[21].
甲烷浓度采用岛津气相色谱仪-FID检测器测定,具体测定和分析方法参见文献[22].
1.5 质量控制与数据分析
土壤中氯苯化合物的浓度均采用外标法测定(2>0.999).所有数据均为3个重复样品数据的算术平均值.显著性差异分析由SPSS 18.0完成,显著性水平为0.05.
2 结果与讨论
2.1 土壤Eh

图1 不同处理土壤Eh的变化过程
图1为各处理在整个培养周期内土壤Eh变化情况.可以看出,各体系中的氧化还原电位在培养前期均随时间下降.土壤Eh在整个培养周期内的平均值在灭菌对照处理为-60,对照处理为-181,丙酸处理为-351,针铁矿处理为-263,丙酸+针铁矿处理为-386.在培养的前8d内,各处理土壤Eh的大小顺序为:灭菌对照>对照>针铁矿>丙酸>丙酸+针铁矿(<0.05).从第12d至培养结束,土壤Eh仍然是灭菌对照处理最大,其次为对照,再次是针铁矿,丙酸和丙酸+针铁矿处理的土壤Eh最小(<0.05),而土壤Eh在丙酸和丙酸+针铁矿处理之间无显著差异(>0.05).该结果表明,灭菌土壤的还原性最弱;添加电子供体基质丙酸能显著增强土壤还原性,主要因为丙酸在厌氧条件下能够发酵生成还原性产物,如甲烷、氢气等[23-24],进而降低反应体系的Eh,已有研究发现乳酸、正丁酸等也能降低反应体系的Eh[25-26];添加针铁矿也使土壤还原性增强,但较添加丙酸的效果弱,主要归因于Fe(Ⅲ)还原生成Fe(Ⅱ),还原性产物使土壤Eh降低.整体而言,添加丙酸+针铁矿对增强土壤还原性的效果最强,但是因为铁还原菌和产甲烷菌之间存在底物竞争,所以添加丙酸+针铁矿的效果小于单独添加丙酸与单独添加针铁矿的作用之和.已有研究表明,在整个培养试验过程中,乳酸和针铁矿的交互处理对于降低反应体系Eh的作用强于单添加针铁矿的处理;而该交互处理在培养试验前期对于降低反应体系Eh的作用强于单添加乳酸的处理,之后在两个处理间无显著差异[25].
2.2 Fe(Ⅱ)含量

图2 不同处理土壤中Fe(Ⅱ)含量变化动态
图2为各处理土壤中Fe(Ⅱ)含量的变化动态.可以看出,各处理土壤中Fe(Ⅱ)含量在培养周期内整体上随时间逐渐增加,整个培养过程中灭菌对照处理的Fe(Ⅱ)含量始终显著低于其它处理.其余4个处理的土壤Fe(Ⅱ)含量差异如下:在培养前4d,土壤Fe(Ⅱ)含量在针铁矿和丙酸+针铁矿处理中显著高于对照和丙酸处理(<0.05),而在针铁矿和丙酸+针铁矿处理间无显著差异,在对照和丙酸处理间亦无显著差异(>0.05);第8~12d,各处理土壤中Fe(Ⅱ)含量的高低顺序为:丙酸+针铁矿>针铁矿>丙酸>对照(<0.05);第16d至培养结束,土壤Fe(Ⅱ)含量在针铁矿和丙酸+针铁矿处理中最高,其次为丙酸处理,对照处理中更低(<0.05),而在针铁矿和丙酸+针铁矿处理间无显著差异(>0.05).该结果表明,灭菌处理限制了铁还原菌将Fe(Ⅲ)还原为Fe(Ⅱ);土壤中添加电子供体基质丙酸能够显著促进Fe(Ⅲ)还原生成Fe(Ⅱ),主要原因可能是丙酸在厌氧条件下分解生成的H2能够作为Fe(Ⅲ)还原的电子供体[5],而且丙酸作为营养源可能刺激铁还原菌生长,因为前人研究表明,外加有机酸能够作为营养源增加铁还原菌的丰度[16,21];添加针铁矿显著促进Fe(Ⅲ)还原生成Fe(Ⅱ).由于添加丙酸+针铁矿对增强土壤还原性的效果最佳,因此,在整个培养过程中,丙酸+针铁矿处理的Fe(Ⅱ)含量始终有高于其它处理的趋势,这与前期研究结果一致[25].
2.3 甲烷生成速率

图3 不同处理甲烷生成速率随培养时间的变化
培养过程中土壤表层甲烷生成速率的变化规律如图3所示.可以看出,除灭菌处理的甲烷生成速率一直很低外,所有处理的甲烷生成速率均呈先增加后下降的趋势.在整个培养过程中,对照和针铁矿处理的甲烷生成速率在第16d时达到峰值,分别为0.68和0.33mmol/(kg×d),且在整个培养过程中,针铁矿处理的甲烷生成速率显著低于对照(<0.05).丙酸和丙酸+针铁矿处理的甲烷生成速率均在第12d达到峰值,分别为2.14和0.47mmol/(kg×d),在整个培养过程中,丙酸处理的甲烷生成速率显著高于丙酸+针铁矿处理(<0.05).整体而言,各处理的甲烷生成速率的次序为:丙酸>对照>丙酸+针铁矿>针铁矿>灭菌对照.该结果表明,灭菌处理杀死了大量的产甲烷菌,抑制了甲烷生成;添加丙酸显著促进甲烷生成,是因为丙酸厌氧分解生成乙酸和H2,而产甲烷菌主要利用乙酸作为产甲烷的基质[27];添加针铁矿抑制甲烷生成,因为产甲烷菌能够利用乙酸或H2还原铁氧化物,这一过程会消耗产甲烷基质,从而抑制甲烷生成[28].因此,针铁矿和丙酸+针铁矿处理的甲烷生成速率均处于较低水平.
2.4 土壤中HCB可提取态残留量的变化规律

图4 各处理土壤中HCB可提取态残留量随培养时间的变化
各处理土壤中HCB可提取态残留量随培养时间的变化过程见图4.厌氧培养40d后,灭菌处理的HCB可提取态残留量减少了26.9%;对照处理的HCB可提取态残留量减少了48.5%;丙酸处理的HCB消减速率在整个培养过程中均快于对照,最终HCB可提取态残留量减少了63.4%;针铁矿处理的HCB消减速率在前8d快于丙酸处理,之后针铁矿处理的HCB下降速率却慢于丙酸处理,最终针铁矿处理的HCB可提取态残留量减少了56.9%,且在整个培养过程中针铁矿处理的HCB残留量均低于对照;丙酸+针铁矿处理的HCB残留量始终最低,最终HCB可提取态残留量减少了72.9%.与DDT相比,HCB在土壤中的消减更缓慢,因为HCB的苯环上H全部被Cl取代,使HCB结构非常稳定,因而较难被还原脱氯降解[24-25].
2.5 土壤中HCB脱氯产物生成动态
本试验检测到HCB的主要脱氯降解产物为五氯苯(PeCB).各处理土壤中PeCB生成动态见表1.可以看出,在整个培养过程中,灭菌处理土壤中PeCB生成量很少,最高时仅为0.15μmol/kg;其余4个处理的PeCB生成量均随培养时间逐渐增加,第40d时4个处理土壤中PeCB生成量达1.46~ 2.83μmol/kg.在培养的前12d,各处理PeCB含量的顺序为:丙酸+针铁矿>针铁矿>丙酸>对照>灭菌对照(<0.05);从第16~32d,PeCB生成量仍然在丙酸+针铁矿处理中最高,其次为丙酸和针铁矿处理,对照处理中更低(<0.05),在针铁矿和丙酸处理间无显著差异(>0.05);第32d至培养结束,各处理PeCB含量的顺序变为:丙酸+针铁矿>丙酸>针铁矿>对照>灭菌对照.该结果表明,丙酸+针铁矿处理的HCB脱氯降解速率最快,培养前期针铁矿处理的HCB脱氯降解速率快于丙酸处理,而后丙酸处理的HCB脱氯降解速率快于针铁矿处理,它们均比对照处理的HCB脱氯降解速率快.
本实验测出的HCB脱氯产物中,除PeCB之外,从第24d开始在非灭菌处理中均检测到四氯苯(TeCB)和三氯苯(TCB),包括1,2,3,4-TeCB, 1,2,3,5-TeCB,1,2,3-TCB,1,2,4-TCB和1,3,5- TCB(表2、3),其中TeCB中1,2,3,5-TeCB生成量高于1,2,3,4-TeCB,TCB中以1,3,5-TCB为主.整体而言,TeCB和TCB生成量随培养时间逐渐增加,但TeCB和TCB生成量远低于PeCB.因此,可以推测HCB的主要脱氯途径为:六氯苯→五氯苯→1,2,3,5-四氯苯→1,3,5-三氯苯,与前人研究结果一致[4].主要原因是Cl在苯环上被取代的难易顺序为:邻位>对位>间位,即邻位最难脱氯,间位最易脱氯[29].
HCB脱氯产物总量随培养时间的变化动态如图5所示.可以看出,各处理HCB代谢产物的生成均呈明显上升趋势,在整个培养过程中,灭菌处理土壤中HCB脱氯产物总量远低于其余4个处理;第24d之前,各处理HCB脱氯产物生成总量的顺序为:丙酸+针铁矿>针铁矿>丙酸>对照>灭菌对照;24d之后,HCB脱氯产物生成量顺序变为:丙酸+针铁矿>丙酸>针铁矿>对照>灭菌对照.可见,单一添加丙酸或针铁矿均能够促进HCB还原脱氯降解,且针铁矿在前期的效果优于丙酸,而到了后期针铁矿的效果逐渐削弱,丙酸依然保持其加速脱氯效应;同时添加丙酸和针铁矿对促进HCB脱氯降解的效果最明显.分析表明,丙酸和针铁矿对加速HCB还原脱氯具有协同作用(<0.05).
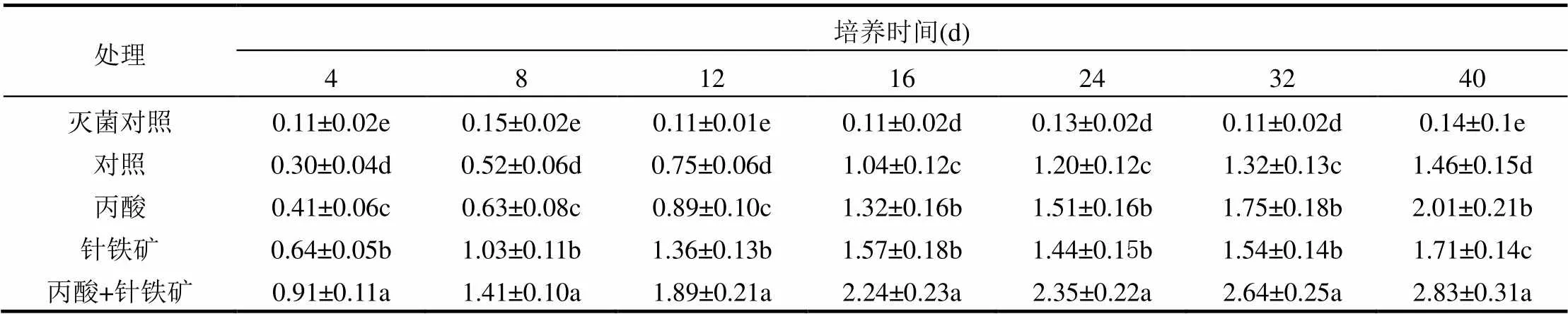
表1 不同处理土壤中PeCB生成动态(μmol/kg)
注:同一列数据后不同字母表示在0.05水平有显著差异.下同.

表2 第24~40d土壤中TeCB变化情况(μmol/kg)

表3 第24~40d土壤中TCB浓度变化情况(μmol/kg)
培养结束时,灭菌对照、对照、丙酸、针铁矿、丙酸+针铁矿处理的HCB脱氯产物总量分别为0.14、2.08、2.83、2.51、3.79μmol/kg,分别占HCB初始量的1.3%、19.2%、26.2%、23.2%、35.0%,远小于HCB可提取态残留的减少量.由于HCB及其降解产物的蒸汽压很低,辛醇/水分配系数很高,在淹水条件下HCB及其脱氯产物的挥发损失量很少,因此,一部分HCB及其降解产物在土壤中形成了结合态残留而不能被提取出来.由图4、5可见,结合残留主要发生在培养的前4d.结合态残留是被土壤黏粒和有机质牢固锁定而暂时失去生物活性和可降解性的部分,但随着土壤条件改变又可以释放出来重新具有活性[30].

图5 各处理土壤中HCB脱氯产物总量随培养时间的变化
由图5可以看出,添加丙酸在培养的前12d对促进HCB脱氯降解的作用并不明显,而在后期显著促进HCB脱氯降解,主要原因有以下两点:第一,添加丙酸在前12d显著增加产甲烷速率(图3),而甲烷的生成与还原脱氯竞争电子[24],第12d之后,随着产甲烷速率降低,丙酸发酵生成的直接电子供体H2能够促进HCB脱氯降解[10].第二,添加丙酸能够显著增加土壤中Fe(Ⅱ)含量(图2),表明丙酸能够刺激铁还原菌将Fe(Ⅲ)还原为Fe(Ⅱ),Fe(Ⅲ)还原能够快速降低反应体系的H2分压[12],进而抑制产甲烷过程与还原脱氯竞争电子,所以添加丙酸能够在第12d之后显著促进HCB脱氯降解.
在体系中加入铁氧化物,在培养前8d促进了HCB的还原脱氯,之后其影响减弱.可能因为铁氧化物是铁还原细菌的特异性生长因子[13],极大的促进了铁还原细菌的生长繁殖,而铁还原细菌可以参与HCB的还原脱氯过程,从而间接的促进了HCB的降解.而在培养后期,由于反应体系中营养源和电子供体的逐渐消耗,铁还原细菌的还原脱氯作用受到了限制.
由图5可看出,丙酸和铁氧化物的配合施用对促进HCB还原脱氯具有协同作用.可能原因如下:①丙酸可作为微生物生长的碳源,刺激了铁还原细菌的生长繁殖;②丙酸作为有效电子供体基质可发酵产生H2,促进Fe(Ⅲ)还原为Fe(Ⅱ),而Fe(Ⅱ)可作为还原剂加速HCB降解;③体系中的铁氧化物可有效抑制丙酸发酵生成甲烷,削弱了甲烷与HCB还原脱氯的电子竞争,从而促进了HCB的还原脱氯.因此,同时添加丙酸和铁氧化物是促进HCB还原脱氯的有效措施.
本研究发现,灭菌处理的HCB脱氯产物总量很少,表明HCB还原脱氯过程需要微生物的参与.由于微生物能够分解电子供体基质生成直接电子供体H2[31],Fe(Ⅲ)还原生成还原脱氯的电子供体Fe(Ⅱ)也需要铁还原微生物的参与[13],而且微生物能将电子传递给HCB使其发生还原脱氯反应[6,31].因此,HCB还原脱氯是微生物-化学耦合的复杂过程.
3 结论
3.1 单一添加铁氧化物或丙酸均可降低土壤体系的Eh、促进还原剂Fe(Ⅱ)的生成,从而促进HCB还原脱氯降解.
3.2 铁氧化物和丙酸配合施用更好的改善了其对Fe(Ⅱ)生成和HCB还原脱氯的效果.
3.3 厌氧淹水条件下,有一部分HCB发生了还原脱氯降解,也有部分HCB被土壤固持形成结合残留.
3.4 土壤体系中甲烷的生成在一定程度上与HCB还原脱氯产生竞争,丙酸作为缓释电子的有机物可以有效缓解这种竞争.
[1] UNEP. Stockholm Convention on Persistent Organic Pollutants [EB/OL]. (2001-05-22)[2016-05-23]. http://www.pops.int/ documents/signature/signstatus.htm.
[2] Bailey R E. Global hexachlorobenzene emissions [J]. Chemosphere, 2001,43(2):167-182.
[3] 刘翠英,王艳玲,蒋 新.六氯苯在土壤中的主要迁移转化过程[J]. 土壤, 2014,46(1):29-34.
[4] Brahushi F, Dörfler U, Schroll R, et al. Stimulation of reductive dechlorination of hexachlorobenzene in soil by inducing the native microbial activity [J]. Chemosphere, 2004,55(11):1477-84.
[5] 胡海珠,毛晓敏.地下水高浓度三氯乙烯厌氧生物降解的进展[J]. 科技导报, 2010,28(21):112-117.
[6] Aulenta F, Pera A, Rossetti S, et al. Relevance of side reactions in anaerobic reductive dechlorination microcosms amended with different electron donors [J]. Water Research, 2007,41:27-38.
[7] Yu S, Semprini L. Enhanced reductive dechlorination of PCE DNAPL with TBOS as a slow-release electron donor [J]. Journal of Hazard Materials, 2009,167:97-104.
[8] Smatlak C R, Gossett J M. Comparative kinetics of hydrogen utilization for reductive dechlorination of tetrachloroethene and methanogenesis in an anaerobic enrichment culture [J]. Environmental Science and Technology, 1996,30:2850-2858.
[9] 单玉华,蔡祖聪,韩 勇,等.淹水土壤有机酸积累与秸秆碳氮比及氮供应的关系[J]. 土壤学报, 2006,43(6):941-947.
[10] Fennell D E, Gossett J M. Comparison of butyric acid, ethanol, lactic acid, and propionic acid as hydrogen donors for the reductive dechlorination of tetrachloroethene [J]. Environmental Science and Technology, 1997,31:918-926.
[11] Fredrickson J K, Zachara J M, Kennedy D W, et al. Biogenic iron mineralization accompanying the dissimilatory reduction of hydrous ferric oxide by a ground water bacterium [J]. Geochemicaet Cosmochemica Acta, 1998,62(19):3239-3257.
[12] Wei N, Finneran K T. Influence of ferric iron on complete dechlorination of trichloroethylene (TCE) to ethene: Fe(III) reduction does not always inhibit complete dechlorination [J]. Environmental Science and Technology, 2011,45:7422-7430.
[13] Li X M, Zhou S G, Li F B, et al. Fe(III) oxide reduction and carbon tetrachloride dechlorination by a newly isolated Klebsiella pneumoniae strain L17 [J]. Journal of Applied Microbiology, 2009,106:130-139.
[14] Li F B, Li X M, Zhou S G, et al. Reductive dechlorination of DDT in dissimilatory iron-reducing system ofS12and α-FeOOH [J]. Environmental Pollution, 2010,158:1733-1740.
[15] Wu C Y, Zhuang L, Zhou S G, et al. Fe(III)-enhanced anaerobic transformation of 2,4-dichlorophenoxyacetic acid by an iron-reducing bacterium Comamonas koreensis CY01 [J]. FEMS Microbiology Ecology, 2010,71:106-113.
[16] Li F B, Wang X, Li Y, et al. Enhancement of the reductive transformation of pentachlorophenol by polycarboxylic acids at the iron oxide-water interface [J]. Journal of Colloid and Interface Science, 2008,321:332-341.
[17] 陶 亮,周顺桂,李芳柏.土壤有机氯脱氯转化的界面交互反应[J]. 化学进展, 2009,21(4):791-800.
[18] 李芳柏,王旭刚,周顺桂,等.红壤胶体铁氧化物界面有机氯的非生物转化研究进展[J]. 生态环境, 2006,15(5):1343-1351.
[19] 鲁如坤.土壤农业化学分析方法[M]. 北京:中国农业科技出版社, 2000.
[20] Yao F X, Yu G F, Bian Y R, et al. Bioavailability to grains of rice of aged and fresh DDD and DDE in soils [J]. Chemosphere, 2007,68:78–84.
[21] Chen M J, Cao F, Li F B, et al. Anaerobic Transformation of DDT related to iron (III) reduction and microbial community structure in paddy soils [J]. Journal of Agricultural and Food Chemistry, 2013,61:2224-2233.
[22] 刘翠英,余贵芬,蒋 新,等.小分子有机碳对土壤中六氯苯厌氧降解及挥发的影响[J]. 环境科学, 2008,29(5):1418-1424.
[23] 樊耀亭,李晨林,侯红卫,等.天然厌氧微生物氢发酵生产生物氢气的研究[J]. 中国环境科学, 2002,22(4):370-374.
[24] Liu C Y, Jiang X, Wang F, et al. Hexachlorobenzene dechlorination as affected by nitrogen application in acidic paddy soil [J]. Journal of Hazardous Materials, 2010,179(1–3):709-714.
[25] Liu C Y, Cade-Menun B J, Xu X H, et al. Electron donor substances and iron oxides stimulate anaerobic dechlorination of DDT in a slurry system with Hydragric Acrisols [J]. Journal of Environmental Quality, 2016,45:331-340.
[26] 刘翠英,王 壮,徐向华,等.AQDS加速红壤性水稻土中DDT厌氧脱氯效应研究[J]. 土壤学报, 2016,53(2):151-161.
[27] 李建政,王卫娜,马 超,等.丁酸甲烷发酵优势菌群的选育及其丁酸降解特性[J]. 科技导报, 2008,26(11):49-52.
[28] 唐子阳,汤 佳,庄 莉,等.土壤铁氧化物对有机质产甲烷过程的影响及其机制[J]. 生态学杂志, 2016,35(6):1653-1660.
[29] 贾青竹,王 昶,李桂菊,等.HCB与γ-HCH在辽河沉积物中的缺氧降解动力学[J]. 中国环境科学, 2005,25(增刊):52-55.
[30] Dankwardt A, Hock B. Immunolocalization of non-extractable (bound) residues of pesticides and industrial contaminants in plants and soil [J]. Chemosphere, 2001,45(4/5):523-533.
[31] 刘翠英,樊建凌,蒋 新.电子供体对土壤中多氯代有机化合物厌氧脱氯作用研究进展[J]. 土壤通报, 2014,45(4):1020-1024.
Effect of iron oxide and propionic acid on anaerobic degradation of hexachlorobenzene in soil.
LIU Cui-ying1,2*, WANG Yu3, MA Yu-chun3
(1.Collaborative Innovation Centre on Forecast and Evaluation of Meteorological Disasters/ Jiangsu Key Laboratory of Agricultural Meteorology, Nanjing University of Information Science & Technology, Nanjing 210044, China;2.Key Laboratory of Soil Environment and Pollution Remediation, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China;3.College of Applied Meteorology, Nanjing University of Information Science and Technology, Nanjing 210044, China)., 2018,38(3):1073~1080
To investigate the effects of iron oxide, propionic acid and their interaction on the reductive dechlorination of hexachlorobenzene (HCB) in soils and their reaction mechanisms, an anaerobic incubation experiment was conducted in Hydragric Acrisols with five treatments: sterile control, control, propionic acid, goethite, and propionic acid + goethite. Results showed that HCB residues for these five treatments decreased by 26.9%, 48.5%, 63.4%, 56.9%, and 72.9% compared to the initial quantities, respectively, after 40d of incubation, and pentachlorobenzene (PeCB) was the dominant product of HCB dechlorination. The addition of propionic acid significantly accelerated the reductive dechlorination degradation of HCB throughout the incubation. The application of goethite obviously promoted HCB dechlorination in the early incubation period. The application of propionic acid and goethite resulted in a synergistic effect on accelerating the dechlorination of HCB.
hexachlorobenzene;reductive dechlorination;goethite;propionic acid;hydragric acrisols
X131.3
A
1000-6923(2018)03-1073-08
刘翠英(1982-),女,安徽省太和县人,副教授,博士,主要研究方向为土壤污染控制.发表论文20余篇.
2017-07-26
江苏省农业气象重点实验室(南京信息工程大学)开放课题(JKLAM1605);中国科学院土壤环境与污染修复重点实验室(南京土壤研究所)开放基金课题(SEPR2017-4)
* 责任作者, 副教授, 002263@nuist.edu.cn

