螺旋CT在胃癌术前T分期中的价值
孙启飞,张 敏,诸晓艳
(宣城市人民医院 影像科,安徽 宣城 242000)
胃癌是最常见的消化道恶性肿瘤之一,发病率及病死率较高[1],进展期胃癌术后5年生存率仅20%~30%[2],其临床治疗方案的选择及预后与肿瘤分化程度、胃壁浸润深度、淋巴结及远处转移等多种因素相关,因此胃癌术前TNM分期尤为重要。目前,胃癌术前TNM分期主要依赖于影像学分期,包括超声内镜、多层螺旋CT(multi-slice CT,MSCT)及MRI,三者各有其优缺点。超声内镜对早期胃癌分期具有较高敏感性,但是对浆膜外侵犯情况敏感性较低,不适合检测肿瘤的远处转移。MRI由于受扫描时间长、上腹部呼吸运动和胃肠道蠕动等伪影干扰,限制了MRI在胃癌术前分期的作用。而MSCT由于其扫描快、范围广、呼吸影响小、图像质量高及强大的后处理功能,在胃癌术前分期评估中得到广泛的应用及认可。本研究旨在回顾性分析MSCT三期扫描横轴位,并结合多平面重建(multi-planar reconstruction,MPR)对63例胃癌患者的术前T分期与术后病理分期对照分析,评价MSCT三期扫描结合MPR在胃癌T分期的诊断价值。
1 资料与方法
1.1 一般资料 收集2014年1月~2017年1月经病理或手术证实的63例胃癌患者临床资料,其中男性45例,女性18例,年龄37~81岁,平均年龄(63.7±9.6)岁。所有患者均于术前1周内行MSCT平扫及增强三期扫描。
1.2 仪器与方法 患者禁食6 h以上,扫描前15 min口服800~1000 mL温水。采用Philips Brilliance 16排螺旋CT检查,扫描参数120 kV、250 mA,旋转速度0.5~0.75 s/周,准直器16 mm×1.5 mm,螺距0.938,扫描层厚5 mm,矩阵512×512,重建层厚2 mm。增强采用高压注射器,对比剂为碘海醇或碘普罗胺80~100 mL,注射速度2.0~3.0 mL/s。注药后分别于30、65、180 s行三期动态扫描。扫描原始簿层数据传入EBW V4.5工作站或PACS工作站进行MPR重建。由两名主治以上医师分别对横轴位、薄层图像及MPR后处理图像进行分析,记录病灶的部位、大小、胃壁浸润深度及周围侵犯等情况,作出具体的T分期,意见不统一时,通过双方协商后作出一致判定。
1.3 胃癌T分期标准 按照美国癌症联合委员会(American joint committee on cancer,AJCC)颁布的第7版胃癌TNM分期及Kim等[3]MSCT的T分期为标准。
表1 AJCC胃癌的病理分期及MSCT分期

分期病理分期MSCT分期T1T1a肿瘤侵犯固有层或黏膜肌层黏膜层的异常线状强化,伴或不伴黏膜层的增厚T1b肿瘤侵犯黏膜下层黏膜增厚,低密度黏膜下层被破坏,但并未完全消失(小于50%胃壁厚度)T2肿瘤浸润到固有肌层低密度黏膜下层破坏消失(大于50%胃壁厚度),但并未侵犯外周高密度层T3肿瘤浸润到浆膜下层结缔组织,但尚未侵犯浆膜病灶与外周高密度层区难以区分,胃壁浆膜面光整,周围脂肪间隙清楚或仅有少许高密度条索影T4T4a肿瘤细胞浸润到浆膜层,未浸润周围器官增厚胃壁浆膜面毛糙,外有不规则或结节样影,周围脂肪间隙模糊T4b肿瘤侵犯邻近结构肿瘤与邻近脏器间脂肪间隙消失或直接侵犯邻近脏器
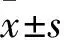
2 结果
2.1 一般情况 63例病理或手术证实的胃癌患者中,早期胃癌(T1期)10例,进展性胃癌(T2~T4期)53例。胃癌各期CT表现见图1。肿瘤位于胃窦部32例,胃角-体部19例,胃底部12例。7例侵犯周围脏器,1例胃癌根治术并胰尾部切除,6例为剖腹探查术,其中贲门癌侵犯食管2例,侵犯胰腺4例,横结肠1例。肿瘤发生部位与胃癌T分期之间无统计学差异(χ2=3.180,P>0.05),肿瘤大小与胃癌T分期有统计学意义(χ2=8.403,P<0.05),详见表2。
2.2 胃癌术前MSCT分期评估和术后病理分期对照 由表3可知术后病理分期T1a 5例,T1b 5例,T2 7例,T3 12例,T4a 27例,T4b 7例。MSCT分期结果中横轴位对T1a、T1b、T2、T3、T4a、T4b诊断的准确率分别为20.00%、40.00%、57.14%、58.33%、66.67%、71.43%;横轴位结合MPR对T1a、T1b、T2、T3、T4a、T4b诊断的准确率分别为60.00%、60.00%、71.43%、75.00%、81.48%、100%。两者比较发现横轴位结合MPR对胃癌T分期准确率77.78%(49/63)高于横轴位T分期准确率58.73(37/63),且差异具有统计学意义(χ2=6.050,P<0.05),详见表3、4。
表2 入组胃癌T分期的临床病理特征
项目临床病理分期T1(n=10)T2(n=7)T3(n=12)T4(n=34)P肿瘤位置0.786 胃窦54716 胃角⁃体部4249 胃底部1119肿瘤大小0.044 ≤3cm6449 >3cm43825
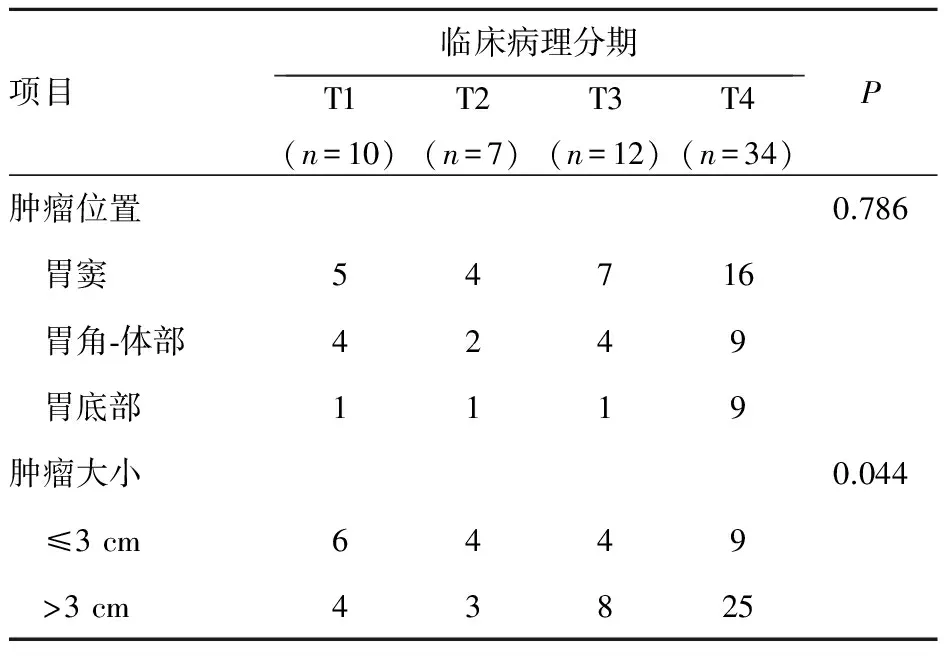
表3 MSCT术前T分期与手术病理对照
术前MSCT分期术后病理分期T1a(n=5)T1b(n=5)T2(n=7)T3(n=12)T4a(n=27)T4b(n=7)准确率/%P横轴位 T0400000/ T1a11000020.00 T1b02200040.00 T202430057.14 T300177058.33 T4a000218266.67 T4b00002571.43横轴位结合MPR T0200000/ T1a31000060.000.192 T1b03100060.000.527 T201520071.430.577 T300195075.000.386 T4a000122081.480.214 T4b000007100.00 0.129
注:采用χ2检验。
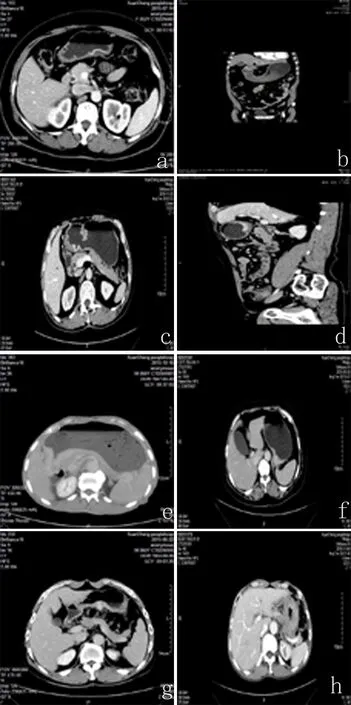
a.T1a,胃窦小弯侧黏膜层局灶性增厚伴明显增强,黏膜下层低密度带完整;b.T1b胃窦部胃壁增厚伴明显强化,黏膜下层低密度带中断,小于胃壁全层50%;c~d.同一患者,横轴位胃窦部胃壁增厚,中央可见溃疡,黏膜下层低密度带破坏,小于胃壁全层50%,未侵犯外层高密度,低估为T1b,而MPR重建显示病灶大于胃壁全程50%,则为T2;e.T3胃窦部胃壁明显增厚,累及全层,浆膜面光滑;f.T4a胃底部胃壁明显增厚、强化,邻近浆膜面毛糙,并见浆膜亮线征,周围脂肪间隙模糊,条索影;g.T4a胃角胃壁明显增厚、强化,浆膜面不规则,见结节状突起;h.T4b胃体部小弯侧胃壁明显增厚,不均匀强化,周围脂肪间隙模糊,并侵犯胰腺尾部。
图1 胃癌各期CT表现
表4 横轴位与横轴位结合MPR T分期比较

横轴位结合MPR+-配对χ2P横轴位图像+3346.0500.012-1610
3 讨论
胃癌多呈环周生长,在CT横轴位上有时很难判断肿瘤确切位置、浸润深度及邻近脏器是否受侵,尤其是胃角,容易出现判断不足。而MPR是基于MSCT在横轴位方向上各项同性的特性,获得任意角度不失真的重建图像,可以从不同角度及方位观察胃壁结构,评估肿瘤浸润的深度和胃周脂肪浸润及肿瘤与邻近器官关系,避免部分容积效应,并能很好区分淋巴结及小胃周血管。因此MPR不仅能提高早期胃癌的检出率及胃癌的分期准确率,且对预测邻近脏器是否受侵具有重大价值[4-5]。本组MSCT胃癌检出率为92%,结合MPR对胃癌T分期77.8%的准确性,高于横轴位T分期的准确性58.7%,与文献报道[6]MSCT三期扫描联合MPR对胃癌T分期准确率提高10%~20%相符。
AJCC颁布的第7版胃癌TNM分期,将T1期分为T1a和T1b期。T1a期胃癌在MSCT图像中多数不能被发现[7-8]。本组T1a和T1b期各5例,其分期准确率均为60%,与一项Meta分析结果相一致[9]。其中2例T1a期胃癌MSCT未发现病灶,笔者分析可能原因:①癌肿较小,黏膜增厚及强化不明显时,MSCT横轴位图像上很难显示,尤其是EGC中的TypeⅡ型(浅表型),其Ⅱc型即使结合MPR仍不能发现病灶,本组1例MSCT未发现病灶者手术病理证实为TypeⅡ型(浅表型)。②常规腹部动脉期时像过早,导致癌肿强化不明显,Tsurumaru等[10]认为胃癌动脉期最佳时像应该在40 s左右。在MSCT图像上,部分胃壁层次分辨不清,呈单层结构时,T1和T2期区分较困难。Kim等[3]根据胃癌CT增强特点及病理对照,认为当低密度层破坏程度小于胃壁厚度的50%时,肿瘤为T1b期,反之则为T2期。当胃壁肌层水肿时,易误认为是黏膜下层,导致过低分期。
浆膜受侵与否是影响胃癌预后的一项重要独立因素,也是判定T3及T4分期标准。MSCT图像中肿瘤浆膜侧毛糙、伴不规则结节状外突、毛刺或胃周脂肪间隙条索状影是判定其侵出浆膜面的重要指标。然而浆膜外脂肪间隙内索条或高密度影并非一定是肿瘤浸润造成,也可能是炎性。另外部分消瘦患者胃周脂肪间隙减少或显示不清、胃解剖上存在无浆膜覆盖“裸区”等因素,容易造成过度分期现象。Kim等[11]认为肿瘤浆膜侧形成线样高强化,即浆膜面“亮线征”,可作为癌肿侵出浆膜的独立预测因素,有助于T4a分期。部分胃癌病变与邻近脏器仅是相贴,而非侵犯或粘连,容易误认为是T4b。为了提高浆膜面侵出的判断,减少过分期现象,笔者认为应做到以下几点:①合理利用窗技术:利用窄窗可以突出显示胃壁分层及胃癌原发灶,而宽窗则有利于观察胃癌浆膜侧脂肪间隙索条及片状浸润的情况。②三期动态增强扫描:受细胞分化、浸润模式及有无溃疡等多种病理因素的影响,胃癌强化表现为多样性[10,12]。Takao等[13]报道MSCT三期扫描胃癌内纤维组织间质逐渐增强,最终整个肿瘤在平衡期完全强化。因此对于肿瘤侵犯,若只观察动脉期或实质期,容易出现过低分期。③薄层重建基础上结合MPR:当横轴位无法显示肿瘤与周围结构情况,MPR重组可以选择最佳角度及方位,显示肿瘤周边结构的脂肪层是否消失以及有无周围脏器侵犯,从而明确分期。本组对浆膜侵犯诊断准确率为85.3%,与文献报道一致[14]。
总之,MSCT三期增强横轴位并MPR不仅能提高胃癌的检出率,还能显示肿瘤对胃壁浸润深度及侵犯周围器官和远处转移情况,在胃癌术前T分期有其独特的优越性,特别是T4期分期有较高准确率,对胃癌临床治疗及预后有重要指导意义。
[1] TORRE LA,BRAY F,SIEGEL RL,etal.Global cancer statistics,2012[J].A Cancer Journal for Clinicians,2015,65(2):87-108.
[2] 梁玉萍,刘维花,杨落落,等.早期胃癌的筛查[J].中华内科杂志,2014,53(4):325-326.
[3] KIM JW,SHIN SS,HEO SH,etal.Diagnostic performance of 64-section CT using CT gastrography in preoperative T staging of gastric cancer according to 7th edition of AJCC cancer staging manual[J].Eur Radiol,2012,22(3):654-662.
[4] 陈岩,梁盼,高歌,等.能谱CT多向调整多平面重组在术前评估胃癌T分期中的价值[J].临床放射学杂志,2016,35(2):213-219.
[5] KIM YH,LEE KH,PARK SH,etal.Staging of T3 and T4 gastric carcinoma with multidetector CT:added value of multiplanar reformations for prediction of adjacent organ invasion[J].Radiology,2009,250(3):767-775.
[6] CHEN CY,HSU JS,WU DC,etal.Gastric cancer:preoperative local staging with 3D multi-detector row CT-correlation with surgical and histopathological results[J].Radiology,2007,242(2):472-482.
[7] LEE IJ,LEE JM,KIM SH,etal.Diagnostic performance of 64-channel multidetector CT in the evaluation of gastric cancer:differentiation of mucosal cancer (T1a) from submucosal involvement (T1b and T2)[J].Radiology,2010,255(3):805-812.
[8] KIM JW,SHIN SS,HEO SH,etal.The role of three-dimensional multidetector CT gastrography in the preoperative imaging of stomach cancer:emphasis on detection and localization of the tumor[J].Korean Journal of Radiology,2015,16(1):80-89.
[9] SEEVARATNAM R,CARDOSO R,MCGREGOR C,etal.How useful is preoperative imaging for tumor,node,metastasis (TNM) staging of gastric cancer?A meta-analysis[J].Gastric Cancer,2012,15(Suppl 1):S3-S18.
[10] TSURUMARU D,MIYASAKA M,NISHIMUTA Y,etal.Differentiation of early gastric cancer with ulceration and resectable advanced gastric cancer using multiphasic dynamic multidetector CT[J].Eur Radiol,2016,26(5):1330-1337.
[11] KIM TU,KIM S,LEE JW,etal.MDCT features in the differentiation of T4a gastric cancer from less-advanced gastric cancer:significance of the hyperattenuating serosa sign[J].British Journal of Radiology,2013,86(1029):508-520.
[12] 王弢,程涛.CT对浸润性胃癌的诊断[J].中国医学影像学杂志,2014,22(6):446-450.
[13] TAKAO M,FUKUDA T,IWANAGA S,etal.Gastric cancer:evaluation of triphasic spiral CT and radiologic-pathologic correlation[J].J Comput Assist Tomogr,1998,22(2):288-294.
[14] HASEGAWA S,YOSHIKAWA T,SHIRAI J,etal.A prospective validation study to diagnose serosal invasion and nodal metastases of gastric cancer by multidetector-row CT[J].Annals of Surgical Oncology,2013,20(6):2016-2022.

