肛洗二号中药软膏剂皮肤刺激性考察及质量控制研究❋
庞晓晨,成睿珍,李 玥,赵 静△
(1. 天津市滨海新区中医医院,天津 300451; 2. 天津中医药大学,天津 300193)
肛洗二号中药软膏剂原处方为本院使用多年的肛肠科外用熏洗经验方,由黄柏、槐花、五倍子、苦参等12味中药组成,临床用于治疗湿热瘀阻型混合痔术后的水肿及疼痛,具有清热解毒、消肿止痛的功效[1-2]。由于此方在使用过程中发现了诸多缺点,故本研究在传统中医理论指导下,利用现代制药技术研究方法,对其制备工艺进行优化研究,在原方的基础上改良成中药软膏剂这一现代药物剂型。
为确保制剂临床皮肤用药的安全性,本研究以SD大鼠为试验动物,通过皮肤刺激性试验考察制剂单次和多次给药,对完整皮肤的刺激性、对其用药安全性给予客观评价[3]。为保障该制剂在有效期内的安全有效,制定出科学、合理、可行的质量标准,本试验采用专属性较强的超高效液相色谱法,同时测定多种有效成分含量,以外观性状、pH值、离心试验以及含量测定为质量控制指标,对其进行耐冷耐热、3个月加速试验和6个月常期试验等稳定性考察,建立该制剂的质量控制方法,从而为该制剂的进一步开发利用和临床应用提供理论依据和质量保障。
1 试验材料
1.1 仪器与试药
ACQUITY H-Class型超高效液相色谱系统 (美国Waters公司),XP205型电子分析天平(瑞士梅特勒-托利多公司),DELTTA320 pH计(瑞士梅特勒-托利多公司),Sorvall ST 16R型高速离心机(德国Thermo Fisher公司),盐酸小檗碱、芦丁、槲皮素对照品(中国食品药品检定研究院,批号分别为110713-201212,100080-201409,100081-201509),乙腈、甲酸为色谱纯,其他试剂均为分析纯。
1.2 试验动物
SD雄性大鼠,体质量200~250 g(合格证号SCXK(军)2014-001)。
2 方法与结果
2.1 皮肤刺激性试验[4]
2.1.1 试验动物处理及分组 给药前24 h将SD大鼠背部脊柱两侧毛使用8%Na2S溶液脱掉5×5 cm面积,脱毛后用酒精消毒脱毛区皮肤,待脱毛后第2天观察脱毛区皮肤是否恢复正常,待无任何皮损后开始涂药。将SD大鼠随机分为2组各6只,分别为单次给药组和多次给药组。
2.1.2 单次给药的皮肤刺激性试验 取软膏剂1 g,空白基质1 g,分别涂在第1组SD大鼠的左侧和右侧脱毛区内。24 h用无菌温水清洗药物和溶剂,观察皮肤是否有红斑、水肿反应,观察时间1~72 h。
2.1.3 多次给药的皮肤刺激性试验 取软膏剂1 g、空白基质1 g分别涂在第2组SD大鼠的左侧和右侧脱毛区内,固定涂敷6 h后用温水去除脱毛部位残留药物,每天涂1次,连续涂7 d,末次涂药后6 h用温水去除残留药物,1 h后观察皮肤有无红斑、水肿。然后继续每天观察皮肤情况,连续1周皮肤状况。
2.1.4 皮肤刺激性试验结果 按皮肤刺激性反应和强度评分标准判断、观察皮肤反应,主要考查皮肤红斑和焦痂程度及皮肤水肿程度2项指标,对皮肤刺激性进行评分[5-7]。结果显示,软膏剂和空白基质对大鼠完整皮肤用药部位均未见红斑、水肿等刺激反应,各组在72 h内各个不同时间点剌激反应平均分值均为0,均未出现皮肤刺激性反应。
2.2 质量控制
2.2.1 性状 本品为棕色或深棕色半固体,质地均匀、稠度适宜,容易涂展。
2.2.2 pH值 取本品0.5 g加蒸馏水10 ml,超声使溶解放至稳定,补重、过滤、测量,pH值应在6.5~7.5之间[8]。
2.2.3 离心试验 取3批样品各2 g置于10 ml离心管中,离心30 min (3000 r/min),3批样品应均无分层现象。
2.2.4 含量测定 检测指标为制剂原处方的君药和臣药中黄柏和槐花的主要有效成分盐酸小檗碱、芦丁和槲皮素,样品含量以相当于标示量的百分含量表示,本品含量应为标示量的90%~110%[9]。
(1)色谱条件:ACQUITY UPLC BEH C18色谱柱(2.1 mm×100 mm,1.7 μm),流动相乙腈(A)-0.1%甲酸(B)梯度洗脱(0~6 min,15% A; 6~7 min,15%~25% A; 7~13 min,25% A; 13~16 min,25%~70% A),流速0.3 mL·min-1,检测波长260 nm,柱温30 ℃,进样量2 μL。
(2)混合对照品溶液的制备:依次精密称取10.08 mg芦丁、5.05 mg盐酸小檗碱和5.11 mg槲皮素对照品,将其置于同一50 mL容量瓶中,用甲醇溶解并稀释至刻度即得。制成每1 mL含有芦丁、盐酸小檗碱和槲皮素分别为201.6 μg、101.0 μg和102.2 μg的混合对照品贮备液。
(3)供试品的制备:称取适量制剂于50 mL容量瓶中,加入甲醇超声溶解,全部溶解后用甲醇定容,取出部分溶液于离心机内10000 rpm离心10 min,取上清液经0.20 μm 有机滤膜过滤即得。
(4)标准曲线的制备:以芦丁含量(μg)为横坐标,峰面积为纵坐标,绘制标准曲线得回归方程(Y=13006x-15688),线性范围为(4.03~160.28 μg,r=0.9999);以小檗碱含量(μg)为横坐标,峰面积为纵坐标,绘制标准曲线得回归方程(Y=25602x-15123),线性范围为(2.02~80.80 μg,r=0.9999);以槲皮素含量(μg)为横坐标,峰面积为纵坐标,绘制标准曲线,得回归方程(Y=24824x-13535),线性范围为(2.04~81.76 μg,r=0.9999)。结果表明,本法对3个被检测成分的线性关系良好。
(5)精密度试验:精密吸取低、中、高浓度的芦丁、盐酸小檗碱和槲皮素对照品溶液,连续进样5次、连续进样3 d测定峰面积,计算日内、日间精密度。结果表明,芦丁、盐酸小檗碱和槲皮素日内、日间精密度RSD均小于2%,仪器精密度良好。
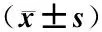
表1 精密度-芦丁日内、日间精密度比较
(6)稳定性试验:取同一供试品0.5 g,加入甲醇超声溶解后,分别于0、2、4、6、8、10、12、24 h各进样2 μL,测定芦丁、盐酸小檗碱和槲皮素浓度值的RSD分别为1.91%,1.14%和1.69%,表明供试品溶液在24 h内稳定。
(7)重复性试验:取同一供试品0.5 g共6份,加入甲醇超声溶解后进行含量测定。结果芦丁、盐酸小檗碱和槲皮素的平均浓度值分别为89.73 μg·mL-1、14.00 μg·mL-1和6.81 μg·mL-1,RSD分别为0.97%、0.93%和1.09%,表明该方法重复性良好。
(8)加样回收率试验:精密称取同一供试品0.5 g共6份,加入甲醇超声溶解后,分别精密加入适量芦丁、盐酸小檗碱和槲皮素对照品进样测定,计算加样回收率。结果表明,芦丁、盐酸小檗碱和槲皮素平均回收率分别为101.52%、99.60%和100.65%,RSD均小于2%。
(9)3批样品验证试验:取3批样品精密称取0.5 g,加入甲醇超声溶解后,分别测定盐酸小檗碱、芦丁和槲皮素的峰面积。结果表明,芦丁的含量分别为139.93、149.61、149.40 μg·g-1,盐酸小檗碱的含量分别为21.27、22.63、22.57 μg·g-1,槲皮素的含量分别为10.18、11.06、11.13 μg·g-1,样品含量以相当于标示量的百分含量表示,本品含量为标示量的99%~100%均符合要求。
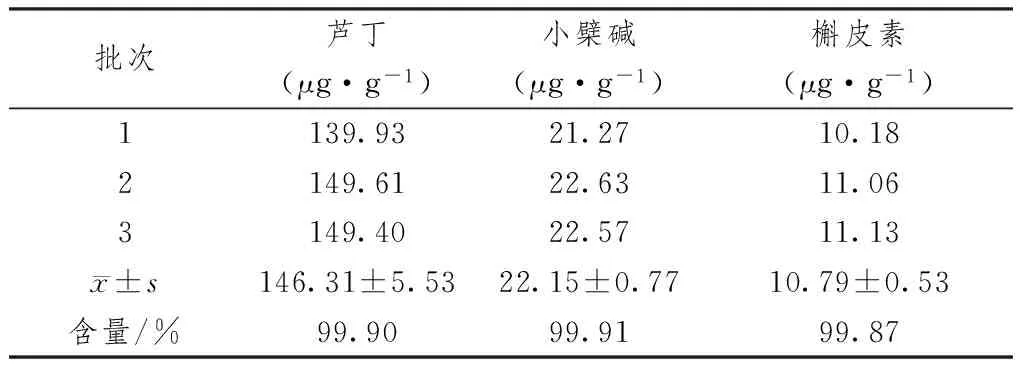
表2 含量测定结果
2.3 稳定性研究[10]
2.3.1 耐冷及耐热性试验 表3显示,分别称取3批样品模拟上市包装,分别置于(-15±2)℃ 冰箱24 h和(55±2)℃恒温箱6 h,取出恢复室温,观察制剂外观性状变化及各项指标。结果表明,在上述条件下,外观无明显变化,各项指标基本保持不变,均符合质量控制标准,提示在市售包装条件下本品稳定性良好。

表3 3批样品耐冷、耐热性试验
2.3.2 加速试验 表4显示,分别称取3批样品模拟上市包装,置于恒温箱(37±2 ℃、RH 75±5%)中,分别于0、1、2、3个月取样,观察制剂外观性状变化及各项指标。结果表明,在上述条件下,3个月内外观无明显变化,各项指标基本保持不变,符合质量控制标准,提示在市售包装条件下本品稳定性良好。
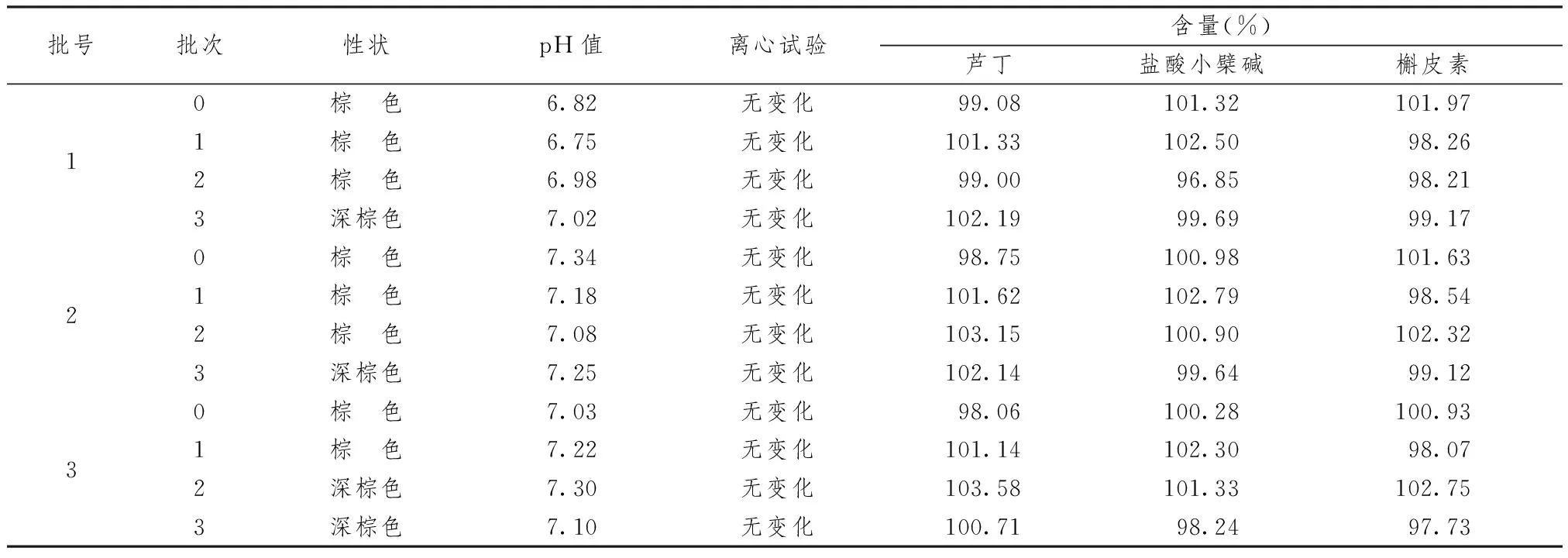
表4 3批样品加速试验结果
2.3.3 常期试验 表5显示,分别称取3批样品模拟上市包装,室温放置,分别于0、1、3、6个月取样,观察制剂外观性状变化及各项指标。结果表明,在上述条件下,6个月内外观无明显变化,各项指标基本保持不变,符合质量控制标准,提示在市售包装条件下本品稳定性良好。
3 讨论
痔疮是最常见的肛肠疾病,包括内痔、外痔和混合痔。随着社会节奏的加快,人们生活、饮食习惯的不合理,痔疮发病率逐年增长,越来越多的人被痔疮、肛瘘等肛肠疾病所困扰[11]。原处方主要由五倍子、苦参、黄柏、槐花、乳香、没药等12味中药材组成,是临床用于湿热瘀阻型混合痔术后患者熏洗的经验方,具有消肿止痛、清热解毒、活血化瘀、敛疮生肌的功效,对于混合痔术后缓解水肿及疼痛有着显著的疗效。中药软膏剂是中医药学的一种独特的外治疗法,充分显示了中医药的优势[12]。
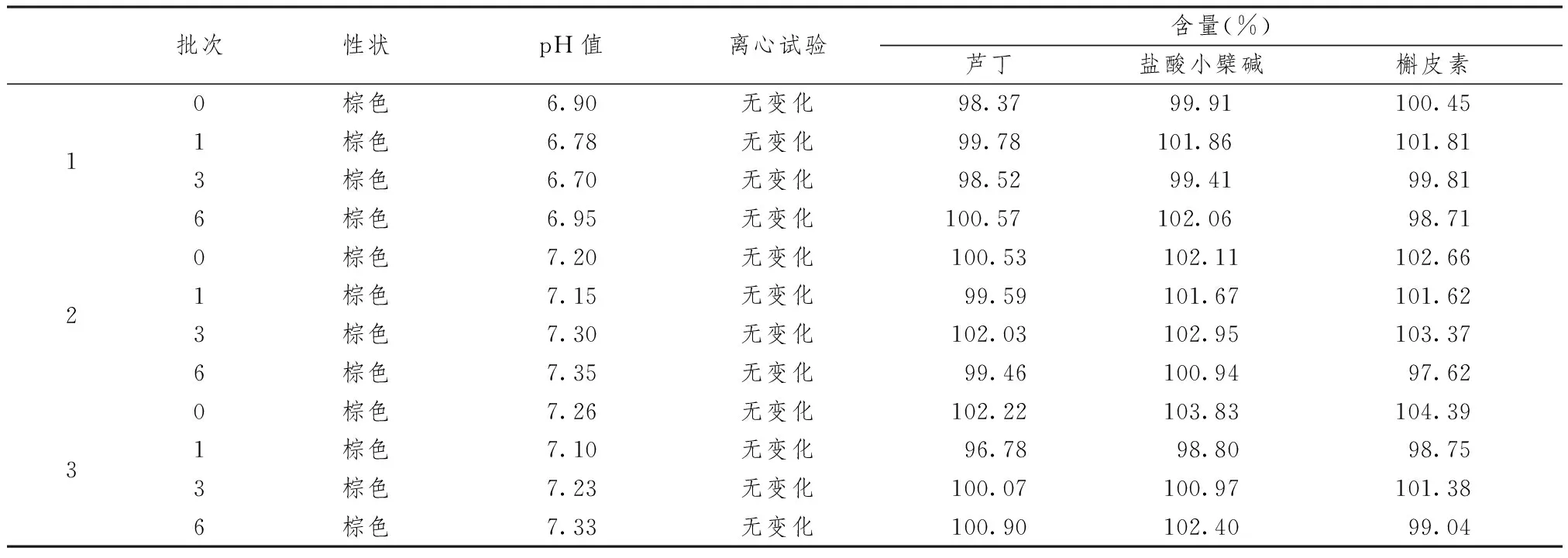
表5 3批样品常期试验结果
中医学认为外用药物贴近皮肤,通过皮肤、肌肉纹理将药物的性味传入脏腑,扶正祛邪,从而治愈疾病,即“药达病所,投之可至”[13]。该制剂直接作用于痔疮部位,副作用小,作用时间长,同时具有易于涂布、性质稳定等特点,在保护创面的同时实现了与外界环境隔离[14]。透皮给药制剂同时具有延长有效作用时间、维持恒定的最佳血药浓度、减少给药频率、改善患者用药顺应性、减少胃肠给药副作用,提高药物的生物利用度的优点,同时可以避免肝脏的“首过效应”对胃肠道造成的破坏。
中药制剂特别是中药复方制剂的皮肤刺激性试验研究是透皮制剂研究以及新药临床前安全性评价的重要组成部分[15]。很多研究报道也都将皮肤刺激性试验作为透皮制剂的重点研究内容之一[16-18]。本研究以大鼠为试验动物,考察该透皮制剂单次和多次给药对完整皮肤的刺激性。皮肤刺激性试验结果表明,单次和多次给药对正常皮肤均未造成红斑和水肿现象,刺激评分均为零。
另外,中药复方制剂的质量控制也是目前现代制剂开发应用过程中研究的热点[19]。只有建立起较为完整的中药复方制剂质量控制方法,确定质量控制标准,才能更加有效地发挥药物的药效,保障制剂的临床疗效。本研究通过初步稳定性实验考察,在耐寒耐热、高湿、高温和离心等条件下,制剂性状稳定、无沉积、分层等现象,pH值、离心试验以及药物含量也无明显变化。
综上所述,该制剂成品稳定性好、质量可控,且无皮肤刺激性,符合临床治疗需要,适合于临床应用和推广,具有很好的开发前景。
[1] 庞晓晨, 刘志东, 黄瑞, 等. 多指标加权评分法优选肛洗二号凝胶剂的提取工艺[J]. 中国实验方剂学杂志, 2016,22(16):31-34.
[2] 庞晓晨, 成睿珍, 李玥, 等. 肛洗二号中药复方熏洗剂的含量测定及其临床应用[J]. 中国中西医结合外科杂志, 2017,23(5):527-531.
[3] 袁伯俊. 新药评价基础与实践[M]. 北京:人民军医出版社, 1998:136.
[4] 路孝兵, 聂奎, 肖蓉. 中药“连蒲”透皮剂的稳定性、刺激性和安全性试验[J]. 四川畜牧兽医,2014,2:34-36.
[5] 刘昌孝. 药物评价学[M]. 北京:化学工业出版社, 2006:255-256.
[6] 谢秀琼. 中药新制剂开发与应用[M]. 北京:人民卫生出版社, 2002:565-571.
[7] 梁炳文. 中药经皮给药制剂技术[M]. 北京:化学工业出版社, 2006:171-244.
[8] 张国友, 宣艳. 阿奇霉素凝胶的制备及质量控制[J]. 中国药师, 2003,6(4):207-208.
[9] 李暮霞, 张涛, 田永强,等. 茶多酚硬脂酸酯凝胶剂的稳定性研究[J]. 山西医药杂志, 2014,43(20):2439-2441.
[10] 孙淑英, 蒋捷, 张东增,等. 水包油(O/W)型乙氧苯柳胺软膏的体外溶出及稳定性实验[J]. 沈阳药学院院报, 1990,7(3):157-161.
[11] 华玉玲. 蜂珍膏的制备及其质量标准的研究[D]. 贵阳: 贵阳中医学院,2008.
[12] 周青,陈玉根,王艳花. 中药软膏在痔切除术后创面愈合中的机理及应用研究[J]. 长春中医药大学学报,2011,27(2):216-217.
[13] 周青,张丹,陈玉根. 中药软膏在痔疮术后的应用研究进展[J]. 山东中医药大学学报,2011,35(5):466-469.
[14] 王业皇. 肛肠科疾病治疗全书[M]. 广州:广东科技出版社,2000:40.
[15] 王洁, 寇俊萍. 退热贴的急性毒性、刺激性及过敏性试验观察[J]. 药学与临床研究, 2007, 15(2):165-166.
[16] 杨良月, 常建华, 曹晓东, 等. 苦参碱制剂及其透皮制剂的皮肤刺激性试验[J]. 中国畜牧兽医文摘, 2015,31(2):203-204.[17] 曹晓东, 常建华, 吴树清, 等. 苦豆子总碱及其透皮制剂的皮肤刺激性试验[J]. 黑龙江畜牧兽医, 2014,9:159-161.
[18] 蔡铮, 黄娟, 吴越, 等. 天麻苷元体外透皮特性与皮肤刺激性研究[J]. 中草药, 2011,42(2):266-270.
[19] 方睿, 王成芳, 刘子沐, 等. 灯盏花素凝胶剂的制备及质量控制[J]. 中国实验方剂学杂志, 2011,17(24):52-55.

