基于磁流体组装的空心磁性碳微球的合成及其重金属污染去除性能
余荣台 ,刘健聪 ,马 湘 ,谢志鹏 ,汪长安
(1. 景德镇陶瓷大学 材料科学与工程学院,江西 景德镇 333403;2. 清华大学 材料学院,北京 100084)
0 引 言
碳材料由于其特殊的结构以及独特的物理化学性能引起国内外学者的研究热潮,特别是石墨烯、碳纳米管等碳家族材料。而球型碳材料的发现,为碳家族材料增添了新的研究热点,球型碳材料由于其独特的物化性能,在纳米器件、能量存储、润滑等方面具有非常区大的应用前景。碳微球作为球型碳材料的一员,表面具有非常丰富的羟基和羧基,同时具有非常大的比表面积,在环境污水处理中具有非常大的应用前景。然而,碳微球由于密度小,在污水处理过程中很难进行泥水分离,因此碳微球包裹磁性材料成为可行的方法。但实心磁性碳微球由于稳定性差和机械强度不高,在应用上受到限制。因此,空心磁性碳微球成为研究热点和重点,目前空心材料合成方法包括硬模板法[1]、牺牲模板法[2]、软模板法[3]和无模板法[4]。不同合成方法存在着各自的优缺点,本实验采用软模板法合成空心磁性碳微球,相对于实心磁性碳微球来说,具有比重轻的优点,在吸附过程中,有利于碳微球在水中悬浮和流化,增加和污染物的接触机率,提高吸附效果。而碳微球包裹的磁性粒子,则在泥水分离过程中,起着至关重要的作用,为碳微球的有效分离提供保障。然而,碳微球在环境污染物去除方面的应用研究还处在起始阶段,对重金属的吸附目前主要停留在参数优化及简单机理推导阶段,对于更深层次的吸附机理,以及工程应用推广方面,仍有很长的路要走。因此,本实验以FeCl3和FeCl2为材料合成磁流体,以葡萄糖为碳源,采用水热方法,合成空心磁性碳微球,并用于重金属镉离子和铅离子的去除研究,考察了合成方法、pH值、投加量和反应温度对重金属吸附的影响,优化了空心磁性碳微球吸附镉离子和铅离子的参数。
1 材料与方法
1.1 实验试剂
葡萄糖(A.R.)、无水乙醇(A.R.)、十二烷基苯磺酸钠(A.R.)、PbCl2(A.R)、Cd(NO3)2(A.R)、NaOH(A.R.)、HCl(浓)、FeCl3(A.R.)、FeCl2(A.R.)。
1.2 实验仪器
电子天平 (FA2004, 上海舜宇恒平科学仪器有限公司)、离心机(800,上海浦东物理光学 仪器厂)、pH计(DZS-780-A,上海仪电科学仪器股份有限公司)、数显恒瀑水浴锅(HH-6,国华电器有限公司)、干燥箱(DGH-9202,上海三发科学仪器有限公司)、电位测定仪(ZD-2,上海精密仪器厂)、XRD (D8 Advance, Bruker)、SEM(JSM-6700F,日本)、TEM(JEM-2010,日本电子)。
1.3 空心磁性碳微球的制备
磁流体的合成[5]:(1)将FeCl3和FeCl2溶解在含有浓盐酸的去离子水中,在氮气保护下搅拌直至固体完全溶解;(2)缓慢滴入配好的的氢氧化钠溶液,溶液颜色逐渐变深,直至反应结束;(3)将得到黑色沉淀通过“磁场分离—水洗—再分散”过程处理3次;(4)将上步中得到的磁性粒子再次分散到去离子中,其中对照组加入偶联剂十二烷基苯磺酸钠,水浴加热至90 ℃,持续搅拌2 h,冷却即得磁流体液体。
空心磁性碳微球的制备:(1)准确称取7 g葡萄糖溶于去离子水中,分别加入上述制备的磁流体2 mL、3 mL、4 mL,同时加入一滴氨水,搅拌;(2)把混合液移入反应釜,填充率为70%; (3)水热条件为:180 ℃,6 h;(4)冷却,0.45 μm滤膜过滤;(5)40 ℃干燥箱烘 48 h,收集待用。
1.4 pH值对重金属吸附性能的影响
(1)分别配制浓度为20 mg/L 的镉溶液和铅溶液;(2)分别调节溶液pH值至2-11;(3)加入步骤1.3所制得的空心磁性碳微球1.25 g/L(3 mL磁流体);(3)搅拌20 min,离心;(4)取上清液,采用离子选择性电极法测镉离子和铅离子浓度;(5)残留物于40 ℃条件下烘干,收集待用。
1.5 投加量对重金属吸附性能的影响
(1)分别配制浓度为 20 mg/L的镉溶液和铅溶液;(2)加入步骤1.3所制得的空心磁性碳微球,分别为 0.25 g/L、0.5 g/L、1.25 g/L、2.5 g/L、5 g/L(3 mL 磁流体),不调 pH 值;(3)其余步骤同1.4。
1.6 不同温度条件下重金属吸附能性
(1)镉和铅溶液浓度分别为 20 mg/L;(2)空心磁性碳微球的投加量为 1.25 g/L(2 mL,3 mL,4 mL磁流体);(3)搅拌温度分别为 10 ℃、15 ℃、20 ℃、25 ℃(水溶加热);(4)其余步骤同1.4。
1.7 不同合成方法对重金属吸附的影响
(1)配制浓度分别为20 mg/L的镉和铅溶液;(2)加入步骤1.3所制得的空心磁性碳微球(1.25 g/L);(3)常温,不调节溶液 pH 值,搅拌20 min;(4)其余步骤同1.4。
2 结果与讨论
2.1 形貌表征

图1 不同合成条件下碳微球的 XRD图 (A空心磁性碳微球;B实心磁性碳微球 (未加氨);C 空心碳微球(未加活性剂))Fig.1 XRD patterns of carbon microspheres synthesized under different conditions (A. hollow magnetic carbon microspheres;B. Solid magnetic carbon microspheres (no ammonia); C. hollow carbon microspheres (no active agent))
采用水热方法,以葡萄糖为碳源,十二烷基苯磺酸钠(SDBS)为活性剂,氯化铁/氯化亚铁为磁性材料合成空心磁性碳微球。XRD 结果表明(图 1),合成的碳微球并没有明显的碳衍射峰;在2 θ=35.6 ° 时出现比较弱的衍射峰,查找 XRD 卡片库,发现为 Fe3O4晶体衍射峰,表明碳微球合成过程中生成了 Fe3O4晶体颗粒。而氨水和活性剂不会对碳微球的结晶过程产生影响。SEM 结果表明合成的碳微球表面光滑,粒径在 5-10 μm,但散落部分碎屑,推测认为散落的碎屑为未被包裹进碳微球的Fe3O4或Fe2O3颗粒(图2a)。从TEM结果可以看出(图2b),在碳微球内部存在着高密度的黑色颗粒物质,可以推断认为是被包裹的Fe3O4或/和Fe2O3颗粒,表明在合成过程中,磁性物质被有效的包裹进碳微球内部。由于碳微球的吸附性能,散落在碳微球外部的部分碎屑被吸附在碳微球表面(图2a和c),影响碳微球吸附其他重金属的效率。因此,需进一步优化碳微球包裹磁性粒子的条件,提高磁性粒子包裹效率。

图2 不同条件下的空心磁性碳微球的SEM/TEM图(a) SEM;(b)TEM;(c) TEM)Fig.2 SEM/TEM images of hollow magnetic carbon microspheres synthesized under different conditions: a) SEM; b) TEM; c) TEM
碳微球具有非常大的比表面积,采用氨水作为起泡剂合成空心的碳微球,进一步增加了 碳微球的比表面积,增加了催化活性位的空腔结构。然而,由于碳微球的密度比较低,空心碳微球在水溶液中很难通过重力自然沉降。因此,通过包裹磁性物质,一方面增加了碳微球 功能复合体的比重,另一方面磁性材料的磁性有利于碳微球的回收。Ryu等[6-7]FTIR 分析结 果表明,碳微球表面含有丰富的[—OH]、[C=O]基团,而[—OH]、[C=O]基团在重金属吸附 方面具有非常重要的作用。
2.2 pH 值对重金属吸附性能的影响
空心磁性碳微球吸附Pb2+、Cd2+离子的效果如图 3所示。在pH值为2-11之间,空心碳微球具有较高的Pb2+、Cd2+离子吸附效率,Pb2+离子最大吸附率接近98%,而Cd2+离子吸附效率也达到90%以上。其中,在中碱性条件下,Pb2+离子吸附效率明显高于酸性条件,而Cd2+离子吸附效率在不同pH值条件下变化不明显。
Pb2+、Cd2+离子在水溶液中会发生水解,随着pH值的升高,Pb2+、Cd2+离子形态会逐步向Pb(OH)+、Pb(OH)2、Cd(OH)+、Cd(OH)2过度,pH越高,形成 Pb(OH)2和Cd(OH)2的速率就越大。而Pb2+、Pb(OH)+、Pb(OH)2、Cd2+、Cd(OH)+、Cd(OH)2在不同吸附剂表面的吸附效率存在差异,因此,在不同pH值条件下,Pb2+、Cd2+离子的吸附效率也会发生变化。pH实验结果表明,空心磁性碳微球在中碱性条件下对Pb2+离子吸附效率要高于酸性条件,表明碳微球对Pb(OH)+、Pb(OH)2的吸附效率要高于Pb2+离子,而对Cd2+、Cd(OH)+、Cd(OH)2则没有选择性吸附。Qin等[8]研究认为,Pb2+离子及其水解产物主要竞争羧基吸附位点,Pb(OH)+、Pb(OH)2易与[C=O]配对形成[COOH],提高了 Pb(OH)+、Pb(OH)2的竞争吸附能力[9]。
2.3 投加量对重金属吸附性能的影响
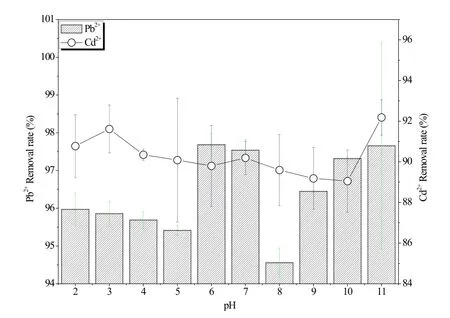
图3 pH 值对空心磁性碳微球吸附Pb2+、Cd2+离子的影响Fig.3 The effect of pH on the adsorption of Pb2+ and Cd2+ by hollow magnetic carbon microspheres
投加量对空心磁性碳微球吸附Pb2+、Cd2+离子的影响如图4所示。结果表明,当投加量为0.25 g/L时,Pb2+、Cd2+离子的吸附效率接近最高值,继续提高空心磁性碳微球的投加量, 不管是Pb2+还是Cd2+离子,吸附效率都没有提高。表明当投加量为0.25 g/L时,仍没有达到空心磁性碳微球的最大吸附能力。
Zhou等[10]采用碳纳米管磁铁功能复合体吸附Pb2+离子时,其吸大吸附效率可达到140.1 mg/g。作为在结构、比表面积和碳纳米管相类似的碳微球,其对Pb2+、Cd2+离子的吸附效率。理论上不会出现极大的下降。当投加量为0.25 g/L 时,空心磁性碳微球对Pb2+、Cd2+离子的吸附量分别为约76 mg/g和70.4 mg/g,远没有达到所报道的最大吸附值。因此,继续提高空心磁性碳微球的投加量,Pb2+、Cd2+离子吸附效率没有明显提高。然而从另一个侧面来看,空心磁性碳微球具有非常好的Pb2+、Cd2+离子吸附能力。
2.4 不同温度条件下重金属吸附性能
温度会改变吸附速率,影响吸附效率;同时温度也有可能改变脱附速率。因此,考察了不同温度条件下空心磁性碳微球对Cd2+离子的吸附效果,同时为了考察磁流体添加量对吸 附性能的影响,考察了磁流体添加量分别为2 mL、3 mL、4 mL时Cd2+离子的吸附效率。结果表明(图5),在10-25 ℃温度条件下,空心磁性碳微球吸附Cd2+离子的效率变化不大,去除率约为87%左右。而磁流体添加量也不会影响Cd2+离子的吸附效率,从图2可以发现,未被包裹的磁流体,部分会被吸附在空心碳微球表面,推测认为随着磁流体的量增加,空心碳微球表面吸附的碎屑磁流体的量相应也会出现增加,从而导致重金属的效率下降。但是实验结果 并没有支持这一推测,Cd2+离子的吸附和磁流体的量没有相关性,推测认为,碳微球有可能 没有达到吸附饱和,或者存在着置换吸附[11]。
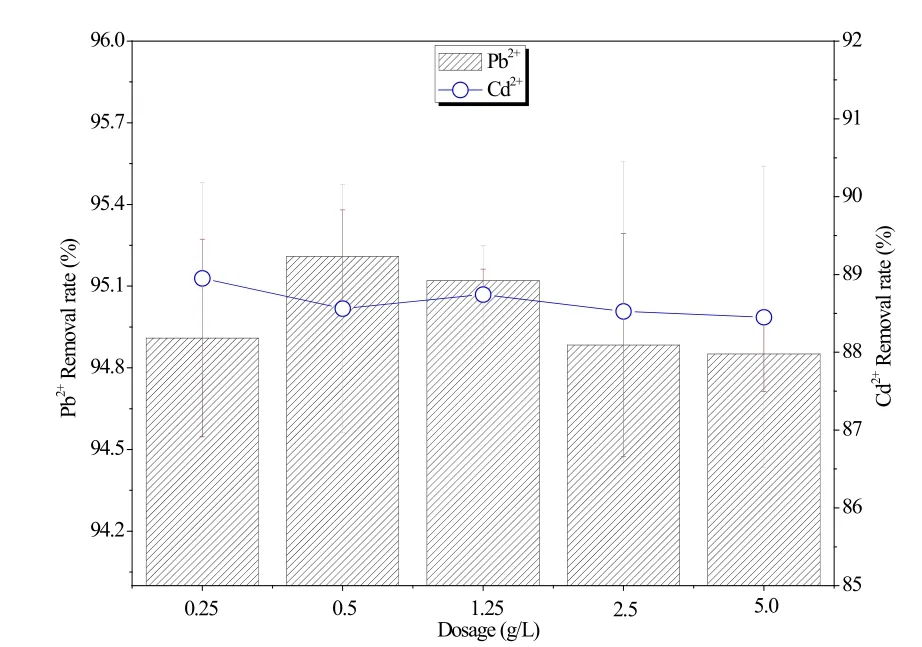
图4 不同投加量对空心磁性碳微球吸附Pb2+、Cd2+离子的影响Fig.4 The effect of dosage on the adsorption of Pb2+ and Cd2+ by hollow magnetic carbon microspheres
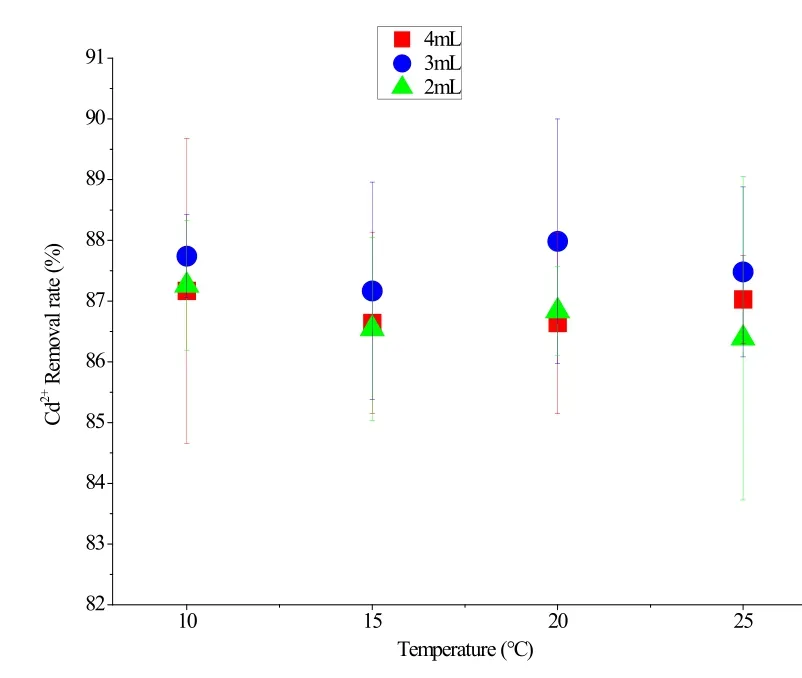
图5 不同温度条件下空心磁性碳微球对Cd2+离子的吸附Fig.5 The adsorption of Cd2+ by hollow magnetic carbon microspheres at different temperatures
2.5 不同合成方法对重金属吸附性能的影响
在碳微球合成过程中,十二烷基苯磺酸钠(SDBS)为活性剂、氨水为起泡剂, FeCl2/Fe2Cl3制备磁流体。其中,十二烷基苯磺酸钠具有分散磁流体、降低界面张力,提高碳微球形成过程中包裹磁流体的作用。而氨水则起到提供空腔模板的作用,有利于碳微球合成过程中形成 空腔结构。不同合成条件下的碳微球吸附Pb2+、Cd2+离子的效果如图6所示,结果表明,磁流体的添加量对Pb2+、Cd2+离子的吸附影响不大;而氨水改变了碳微球的空腔结构,但与Pb2+、Cd2+离子的吸附效率没有直接的线性关系。表面活性剂则对Pb2+、Cd2+离子的吸附效率存在着比较弱的影响,在不添加表面活性剂的条件下,碳微球对Pb2+、Cd2+离子的吸附效率稍低于添加表面活性剂的吸附效率,Pb2+去除率分别约为93.6%和94.6%,Cd2+去除率分别约为83.5%和85%。活性剂提高了磁流体和碳微球的接触机率,提高了其被包裹的可能性; 而过量的残留在碳微球外的碎屑磁流体被吸附在碳微球表面,会和重金属离子竞争吸附位点,当磁流体碎屑量达到一定程度时,影响到重金属离子的吸附效率。
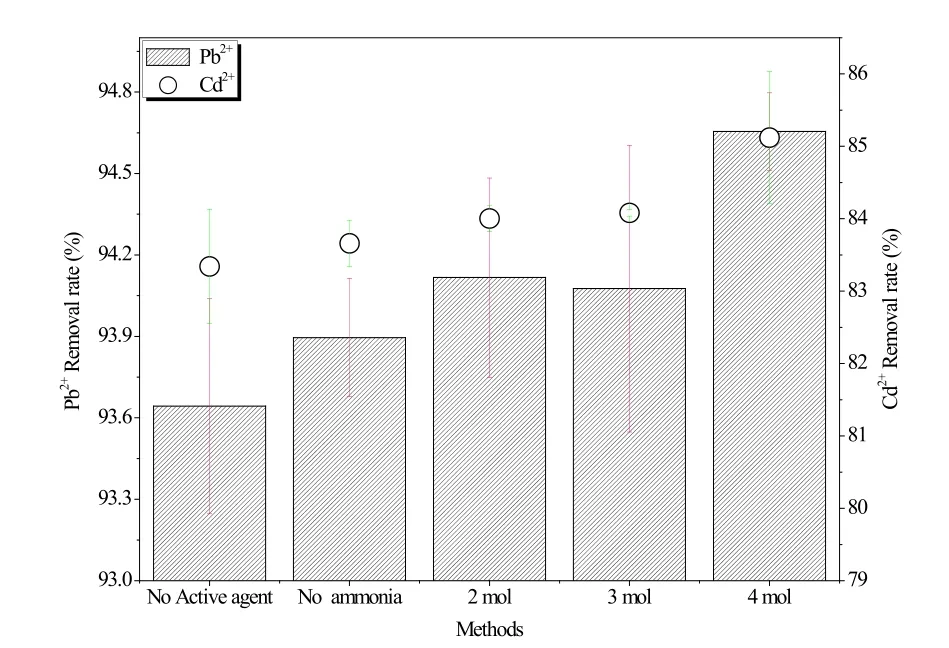
图6 不同合成方法对Pb2+、Cd2+离子的吸附Fig.6 The adsorption of Pb2+ and Cd2+ by carbon microspheres synthesized by different synthetic methods
3 结 论
(1)空心磁性碳微球对Pb(OH)+、Pb(OH)2吸附效率要高于Pb2+,而pH值对Cd2+离子的吸附效率影响不大;
(2)当投加量为0.25 g/L时,空心磁性碳微球对Pb2+、Cd2+离子的吸附效率达到最大值,去除率分别约为95%和88.5%;
(3)在10-25 ℃温度条件下,吸附反应温度与吸附效率不存在正比例关系,同时磁流体的添加量也不影响Pb2+、Cd2+离子的吸附效率;
(4)氨水提供了气泡模板的作用,为碳微球提供空腔结构,但不影响碳微球吸附Pb2+、Cd2+离子的效率,而活性剂则起着连接磁流体和碳微球的作用,促进磁流体被包裹进碳微球内,在不添加活性剂的条件下,由于磁流体碎屑吸附在碳微球表面,和重金属竞争碳微球的表面 吸附位点,影响重金属的吸附效率。

