金属覆膜支架联合鼻胆管治疗内镜逆行胰胆管造影术Ⅲ型Stapfer穿孔的研究(附6例报告)
(甘肃省兰州市第二人民医院 消化科,甘肃 兰州 730046)
内镜逆行胰胆管造影术(endoscopic retrograde cholanggiopancreatography,ERCP)相关的穿孔是少见而严重的并发症,发生率约为0.35%~2.10%[1-2]。而Ⅲ型Stapfer穿孔是其中一个重要类型,放置鼻胆引流管充分引流,同时联合保守治疗,常可以取得满意的疗效。然而也有极少数患者会并发胆瘘,造成腹腔感染,从而不得不再次放置支架或转手术治疗,给患者带来了巨大的痛苦及经济负 担。在当前的国内医疗环境中,更是引起医疗纠纷的重要因素和限制ERCP技术发展的一个重要方面。我院近年来采取金属覆膜支架封堵联合鼻胆管治疗ERCP术中Ⅲ型Stapfer穿孔取得了良好的效果。现报道如下:
1 资料与方法
1.1 一般资料
2013年6月-2016年3月本院共行ERCP 1 978例。其中,胆总管结石1 405例,恶性肿瘤150例,其他423例。预切开80例,单纯双导丝法355例,插管时间大于30 min者68例,发生Ⅲ型Stapfer穿孔6例。其中,男2例,女4例,年龄45~82岁,平均(65.5±12.14)岁。5例为胆总管结石并胆管狭窄,1例单纯胆总管下段炎性狭窄,6例均无十二指肠降部憩室。2例有胆囊切除术病史,1例伴2型糖尿病,1例伴高血压病2级。所有穿孔均在术中发现。
1.2 手术器械
南京微创公司胆道覆膜支架及支架释放系统,上海辛菖公司鼻胆引流管,Olympus-H260Z电子十二指肠镜,FLEX公司弓形切开刀,Boston斑马导丝,奥林巴斯公司直径0.25 mm超硬黑导丝,波科公司黄斑马导丝。碘佛醇造影剂,生理盐水,利多卡因胶浆等。
1.3 临床表现及治疗方法
6例均为插管困难病例,插管时间大于10 min。6例中所有导丝走行开始均和正常胆总管解剖方向相似,但在肝内胆管位置导丝走行与正常解剖方向有偏差,跟进弓形切开刀有困难。第1例用力后切开刀进入腹腔,造影见肝内外胆管未显影,造影剂呈弥散状(图1)。留置导丝,再换导丝超选胆管成功,造影肝内外胆管显影良好,考虑导丝已致胆管穿孔。因为导丝穿孔一般为微穿孔,故拔出腹腔内导丝后,继续行乳头括约肌切开并取石,胆总管直径约1.8 cm,内镜下未见乳头部明显穿孔(图2)。取石结束后放置胆道覆膜支架(7.0 cm×1.0 cm),行鼻胆管引流后退镜。第2例因反复插入胰管无法超选胆管,而行胰管预切开后再次超选胆管,见导丝在肝内胆管部位走行不正常,切开刀在入口处造影不显影,根据第1例的经验即考虑可能为导丝穿孔,换导丝重新超选胆管成功,胆总管直径约1.5 cm,成功取石后,放置胰管支架及胆管覆膜支架(6.0 cm×1.0 cm)和鼻胆引流管。其余4例发现导丝在肝内胆管部位走行异常,切开刀跟进困难,立即在跟进困难处造影,胆管不显影,即判断为可能导丝造成胆管穿孔。第3例胆总管直径1.5 cm,发现穿孔,取石后单纯放置鼻胆引流管结束操作。第4例胆总管直径1.6 cm,取石后单纯放置覆膜胆管支架(6.0 cm×1.0 cm)。其余2例胆总管直径分别为1.2和1.3 cm,均放置胆管覆膜支架及鼻胆引流管,支架规格均为6.0 cm×1.0 cm(图3和4)。6例支架上端均位于肝门部,尾端位于十二指肠腔内,露出乳头外1.0~2.0 cm。

图1 造影剂弥散于胆管外Fig.1 Contrast agent spread out of the bile duct

图2 术中内镜下所见Fig.2 Intraoperative endoscopic view

图3 支架放置后内镜图Fig.3 After endoscopic stent placement diagram
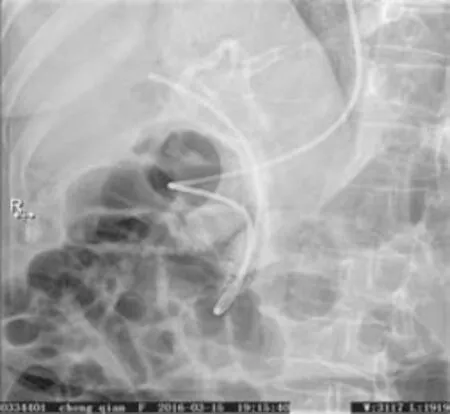
图4 支架放置后X线图Fig.4 X-ray map after placement of stents
2 结果
2.1 疗效
4例术中放置胆管覆膜支架联合鼻胆管者,其中2例术后1周内有轻微腹痛,给予禁食水及抑酶、抗生素治疗后好转,术后1周带鼻胆管出院。随访1个月后行覆膜支架及鼻胆引流管取出术。第4例单纯放置覆膜支架者住院期间无特殊不适,1周后出院。第3例单纯放置鼻胆引流管者术后24 h出现胆瘘及腹腔感染表现,腹部立位平片未见膈下游离气体,鼻胆管造影未见腹腔内造影剂弥散。腹部CT可见十二指肠球、降部轮廓模糊,邻近腹膜渗出、水肿(图5)。48 h后急诊放置胆管覆膜支架及鼻胆引流管,术后病情不能缓解,转ICU病房治疗1个月后好转出院。6例患者中2例术后轻微腹痛,占33.33%。1例住院期间出现腹腔感染症状,发生率为16.67%。6例患者均好转出院,有效率100.00%。死亡率为0.00%,转外科手术率0.00%。

图5 腹部CT所示Fig.5 Image of abdominal CT
2.2 安全性
放置金属覆膜支架有可能并发支架移位、十二指肠穿孔、出血和支架无法取出等并发症。笔者根据胆管穿孔位置及胆总管的长度来选择支架,支架上段位于肝门部,尾端露出乳头1.0~2.0 cm左右。这样在完全覆盖穿孔位置后,可以防止支架向胆管内移位。本研究中,单纯放置金属覆膜支架的1例患者,在随访1个月后行支架取出术时发现支架已自行脱落,占16.67%,随访6个月,无其他并发症发生。其余患者均于1个月后安全取出支架及鼻胆引流管,6例患者均未发生十二指肠穿孔、出血、胰腺炎、反流性胆管炎、胆囊炎和支架向胆总管内移位等。这也说明,放置金属覆膜支架联合鼻胆管治疗Ⅲ型 Stapfer穿孔是安全的。
3 讨论
ERCP相关穿孔是ERCP术中严重的并发症,处理不及时、不正确会造成弥漫性腹膜炎、腹膜后脓肿,脓毒血症,常常会因严重感染等并发症而死亡,严重威胁着患者的生命。文献报道,ERCP相关穿孔的死亡率约16.00%~25.00%[3]。ERCP相关穿孔分型较多,主要有Howard、Stapfer、Kim等[4-6]。Howard分型:Ⅰ型,导丝引起的穿孔;Ⅱ型,壶腹部周围、后腹膜穿孔;Ⅲ型,远离乳头部的穿孔。Stapfer分型:Ⅰ型,十二指肠外侧或内侧壁穿孔;Ⅱ型,十二指肠乳头周围穿孔;Ⅲ型,远端胆管损伤;Ⅳ型,后腹膜积气。Kim分型:1型为十二指肠镜镜头所致肠管穿孔,直径大,污染严重,主要以外科治疗为主;2型为插管导管或括约肌切开刀所致,往往合并胆胰瘘,部分可通过保守治疗,有明显腹腔渗液者目前主张积极手术治疗;3型主要为导丝及网篮所致胆管穿孔,多主张放置鼻胆管充分减压保守治疗。前两者主要根据解剖位置及机制为分类标准。或者根据ERCP进行的步骤过程及所用器械分类,每种分型各有优势。主要是在插管过程中导丝及切开刀损伤远端胆管所致。
传统的诊断方法主要为胆管内造影,腹部X线,以及腹部CT检查等。但有些隐匿性穿孔通过上述方法尚无法明确诊断,往往造成治疗上的延误。据KAWAGUCHI等[7]报道,隐匿性穿孔可通过术中荧光成像技术早期确诊,能够发现ERCP后很小的胆道渗漏,为手术修补及内镜下治疗提供依据,但在我国目前操作性不强。因此,如何在术中操作过程中及时发现、诊断穿孔,从而能及时治疗就成为摆在ERCP操作者面前的重要课题。笔者通过本组病例对术中导丝穿孔的表现有了一些浅显的认识,总结后希望对ERCP同仁有借鉴作用。总结本组病例的经验,可得出ERCP术中判断导丝穿孔的方法如下:导丝在胆总管部位与胆总管走行相似,但如果肝内胆管部位导丝走行异常,切开刀跟进困难,提示有可能已经出现胆管穿孔,切忌继续暴力跟进切开刀,以免扩大胆管穿孔。应该立即造影,如果胆管不显影,应留置该导丝,换用导丝重新超选胆管。超选成功后造影胆管显影方向与原导丝走行不同,即能确诊导丝造成了胆管穿孔。分析这种临床表现的机制,有可能导丝开始并未完全穿透胆管壁,而是在管壁内的夹层中走行一段后才穿破胆管,进入腹腔。因此,术中导丝走向与胆总管方向一致,并不能成为判断插管成功的方法。这种判断方法经济适用,有利于术中立即采取不同的处理方法,避免延误病情及加重胆管损伤。
据报道80.00%的ERCP相关胆道穿孔可通过保守治疗而痊愈[8],如果出现弥漫性腹膜炎及腹膜后穿孔需立即行外科修补术[9-11]。对于Stapfer Ⅲ型穿孔,通常认为放置鼻胆管引流联合保守治疗方法可以获得良好的效果。但自2011年JEON等[8]报道了用胆道覆膜支架治疗ERCP相关胆道穿孔的方法后,用覆膜胆道支架治疗ERCP相关胆管穿孔成了学者探索研究的另一条有效途径。本组6例均为术中发现的StapferⅢ型穿孔。分别采取了3种不同的治疗方法,出现了不同的结局。笔者经过认真思考后认为,首先对于导丝穿孔,虽然目前通行的方法为放置鼻胆管充分引流联合保守治疗,但在手术过程中,由于切开刀跟进、导丝切割等原因,往往会合并穿孔口径较大等复杂情况。而术中及时准确判断穿孔口径是否为微穿孔可能难度较大。因此,单纯放置鼻胆管引流可能会出现引流不彻底而并发胆瘘、腹腔感染等情况。另外放置胆管覆膜可回收支架虽然增加了治疗费用,增加反流性胆管炎、胆囊炎和胰腺炎等的发生率,但可以有效封堵胆管破口,充分引流,有利于胆管愈合,提高了治愈率。由于取石时切开、球囊扩张等操作破坏乳头括约肌,或者胆管扩张明显、支架直径过小等原因,单纯放置覆膜可回收支架可能会出现支架移位,甚至十二指肠穿孔、出血等并发症。而联合放置鼻胆引流管不但有固定支架,防止脱落的作用,也可以起到充分胆管减压,促进愈合,还可以随时观察胆汁中有无出血,必要时可行冲洗治疗。
放置胆管覆膜支架虽然可以提高治愈率,但也可能会发生放置不成功、增加胰腺炎、反流性胆管炎、肠道穿孔和出血等的发生率,安全性也是要重点关注的。在笔者的研究中,6例患者全部放置成功,成功率100.00%。除有2例轻微腹痛患者,没有出现明显胰腺炎、反流性胆管炎和胆囊炎等并发症。在支架取出过程中,没有发生穿孔、出血和支架无法取出等情况。虽然由于病例数过少,无法充分观察到各种并发症,影响了对安全性的判断,但是随着时间的推移,经验的不断积累,技术的不断进步,会出现更加安全有效的治疗方法而造福患者。
综上所述,胆道覆膜支架可以封堵胆管破口,有效防止胆汁向腹腔及腹膜后渗出,预防感染,是主要的治疗措施。而鼻胆引流管除了充分进行胆管减压,治疗胆瘘外,还可以固定支架,预防支架相关并发症的发生。两者联合提高了治疗的有效性及安全性。在本组病例中,笔者采取这种方法治疗ERCP术中Stapfer Ⅲ型穿孔取得了较好的效果。特别是1例出现严重并发症的患者最终通过保守治疗痊愈出院,随访无远期并发症发生,避免了手术治疗。经过多年的发展,目前ERCP技术已非常成熟,发生导丝穿孔的概率很小。因此,本组积累的病例非常少,结果准确性有待临床实践中进一步扩大样本量进行验证。
[1]COTTON P B, LEHMAN G, VENNES J, et al. Endoscopic sphincterotomy complications and their management:an attempt at consensus[J]. Gastrointest Endosc, 1991, 37(3):383-393.
[2]FREEMAN M L, NELSON D B, SHERMAN S, et al. Complications of endoscopic biliary sphincterotomy[J]. N Engl J Med, 1996, 335(13):909-918.
[3]BOOTH F V, DOERR R J, KHALAFI R S, et al. Surgical management of complications of endoscopic sphincterotomy with precut papillotomy[J]. Am J Surg, 1990, 159(1):132-135.
[4]HOWARD T J, TAN T, LEHMAN G A, et al. Classification and management of perforations complicating endoscopic sphincterotomy[J]. Surgery, 1999, 126(4):658-663.
[5]STAPFER M, SELBY R R, STAIN S C, et al. Management of duodenal perforation after endoscopic retrograde cholangiopancreatography and sphincterotomy[J]. Ann Surg, 2000, 232(2):191-198.
[6]KIM B S, KIM I G, RYU B Y, et al. Management of endoscopic retrograde cholangiopancreatography-related perforations[J]. J Korean Surg Soc, 2011, 81(3):195-204.
[7]KAWAGUCHI Y, ISHIZAWA T, HARADA Y, et al. Intraoperative identification of bile duct perforation following ERCP using indocyanine green-fluorescence imaging[J]. Dig Dis Sci, 2014, 59(5):1063-1065.
[8]JEON H J, HAN J H, PARK S, et al. Endoscopic sphincterotomyrelated perforation in the common bile duct successfully treated by placement of a covered metal stent[J]. Endoscopy, 2011, 43 Suppl 2 UCTN:E295-E296.
[9]MALLERY J S, BARON T H, DOMINITZ J A, et al. Complications of ERCP[J]. Gastrointest Endosc, 2003, 57(6):633-638.
[10]ENNS R, ELOUBEIDI M A, MERGENER K, et al. ERCP-related perforations:risk factors and management[J]. Endoscopy, 2002, 34(4):293-298.
[11]STAPFER M, SELBY R R, STAIN S C, et al. Management of duodenal perforation after endoscopic retrograde cholangiopancreatography and sphincterotomy[J]. Ann Surg, 2000, 232(2):191-198.
——导丝概述及导丝通过病变技巧

