微泡强化臭氧传质及其对产生羟基自由基的影响
程 雯,全学军,罗 丹,李瑞恒,杨 鲁
1.重庆理工大学化学化工学院,重庆 400054;2.重庆市生活垃圾资源化处理协同创新中心,重庆 401331
化工废水特别是生物难降解废水,由于缺乏高效低成本的处理技术,大量难降解有机物排入水体,已造成严重的环境污染[1]。高级氧化技术利用各种活性自由基攻击有机物,可以有效地将有毒难降解有机物矿化或转化为低毒及易生物降解的低分子有机物,受到了学术与产业界的高度重视。该类技术主要包括Fenton法、湿式催化氧化、光催化、电催化和臭氧氧化等。其中,Fenton法会产生大量污泥;光催化受废水色度和胶体等限制;湿式催化氧化受高温高压的限制;电催化处理还存在能耗高等问题。相比之下,臭氧氧化法具有不受废水色度和废水胶体物质的影响,同时也不会产生大量的二次污染物等优势,且对难降解有机物具有较好的降解与矿化能力[2,3],可作为很好的彻底矿化难降解有机物和难降解废水生化处理的预处理手段[4,5]。因此,先进实用的臭氧高级氧化技术在难降解化工废水等领域具有广阔的应用前景。
然而,传统的臭氧处理技术存在气液传质效率低[6]、以臭氧分子直接氧化为主,氧化能力弱和有机物彻底矿化反应速率慢等缺点[7]。臭氧氧化处理废水过程中,臭氧向液相的传质和氧化反应速率是决定该过程效率的两个主要因素。为提高工程应用中臭氧向液相的传质和反应性能,国内外众多学者探索了很多强化措施,如:中空纤维膜反应器[8]、微通道反应器[9]和多孔陶瓷膜[10]等新型反应器被开发研究,通过超声波[11,12]、光催化[13]和电催化[14,15]等技术强化臭氧化过程。据报道,微气泡有助于提高气液传质效率,臭氧微气泡在液相中收缩破裂瞬间激发产生·OH[16,17]。Takahashi等[18]研究表明臭氧微气泡收缩破裂时更容易产生·OH,从而提高其氧化能力。
本工作提出了一种利用新型高效的气液混合泵实现臭氧微泡化的反应器,并考察了该反应器在不同压力、温度、进口臭氧浓度和流量条件下,对液相中臭氧浓度以及羟基自由基生成量的影响。同时,还对比研究了传统鼓泡反应器与该微泡反应器液相中臭氧浓度和羟基自由基的产生量,并用模拟染料废水对比考察了降解与矿化效果,为新型高效臭氧氧化反应器的研发提供了一定的依据。
1 实验部分
1.1 臭氧氧化反应器
气液混合泵是实现气体微泡化的一种很好的方式[19,20],本工作采用一种气液混合泵(25QY-2DS)实现臭氧化气体的微泡化,据厂家提供的测试数据,气体在液相中可以分散为20~30 μm的微气泡。以气液混合泵实现气体微泡化以及整个反应体系的循环过程,形成了微泡反应体系,如图1所示。整个实验体系主要由臭氧发生器(HBO3-20)1、管式反应器8、液体储槽12、气液混合泵10、臭氧检测仪15以及流量计、压力表和尾气吸收装置组成,实验所用反应管为直径70 mm,长900 mm有机玻璃管,反应器出口连接球形阀6用于调节反应器内压力和废水流量,整个反应体系构成一个连续循环的反应体系。液体储槽中放置聚四氟乙烯管作为换热体系,保持实验过程中温度恒定,换热面积约为0.53 m2。实验所用臭氧由臭氧发生器高压电击纯氧生成,流入气液混合泵,流量由气体流量计3控制,其入口浓度由紫外臭氧检测器(JSA9-03-UV)检测。来自臭氧发生器的臭氧-氧混合物被吸入气液混合泵中,在废水中产生微气泡,然后将两相混合物输入臭氧氧化反应器,在反应器中臭氧化反应后,两相混合物从反应器顶部流出并流入废水储槽中,气相分离后进入排气管道系统。从插入液体储槽中的取样管收集液体样品,液体再循环流量和反应系统的压力由反应器出口管上的球阀控制。
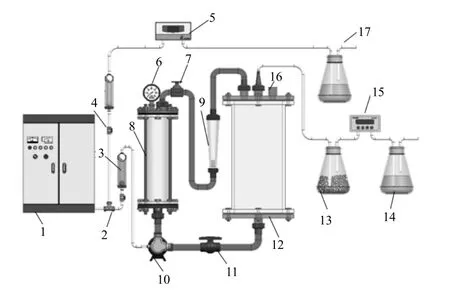
图1 臭氧氧化系统实验装置Fig.1 Experimental setup for ozone oxidation system
臭氧鼓泡反应器:鼓泡反应体系中臭氧产生系统、臭氧检测系统及尾气吸收系统与微泡反应体系相同。鼓泡反应器中采用陶瓷曝气头分散混合气液两相,曝气头置于储液槽底部。
1.2 实验过程与分析方法
1.2.1 液相中臭氧浓度测定
取8 L去离子水于储液槽中,启动混合泵;同时启动臭氧发生器,待臭氧浓度稳定后,打开进气管上阀门;在一定实验条件下通入臭氧开始计时,定时取样,采用靛蓝二磺酸钠分光光度法[21]测定水中臭氧浓度。
1.2.2 液相中羟基自由基浓度测定
根据Nohemi等[22]对羟基自由基的测定方法,本工作采用对苯二甲酸(TA)捕捉羟基自由基形成2-羟基对苯二甲酸(TAOH),化学反应式如式(1)。其中捕捉剂对苯二甲酸不具荧光性,而2-羟基对苯二甲酸(TAOH)的荧光测定中,在激发光谱为315 nm,发射波长为425 nm条件下有较强吸收峰,因此本实验采取该方法测定羟基自由基含量。
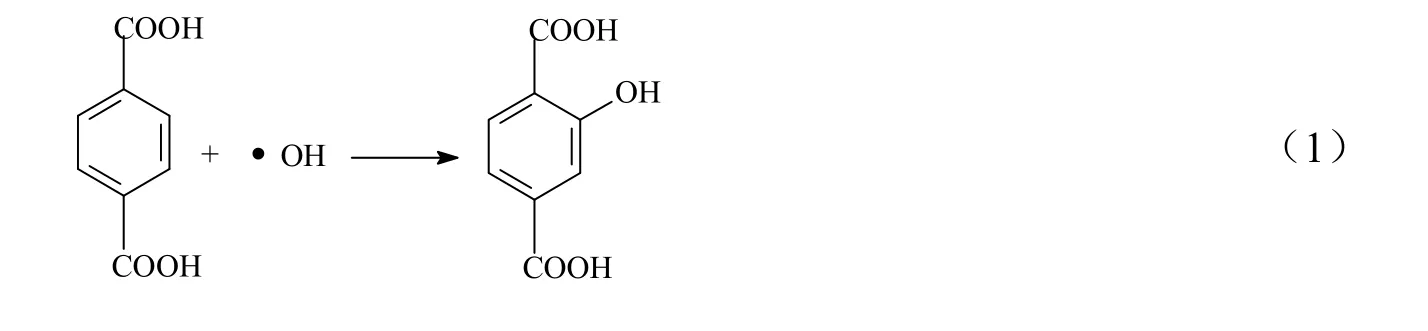
根据文献[23]中羟基自由基累积测定方法,配制初始浓度为4×10-3mol/L的对苯二甲酸溶解于10×10-3mol/L的NaOH溶液中,取8 L该溶液于储液槽中,启动混合泵,同时启动臭氧发生器,待臭氧浓度稳定后,打开进气管上阀门,通入臭氧开始计时,定时取样,测定液相样品的荧光吸光度,计算其羟基自由基浓度。
1.2.3 染料废水的臭氧氧化处理
配制一定浓度的酸性红18模拟染料废水,取该模拟废水8 L于储液槽中。启动混合泵,待臭氧浓度稳定后,通入臭氧开始计时,定时取样,测定其色度及总有机碳(TOC)含量。酸性红18染料废水的色度采用紫外可见光分光光度计(TU-1901型,北京普析通用仪器有限责任公司)分析检测(测定波长为510 nm),废水中TOC含量采用TOC测定仪(TOC-LCPH型,日本岛津公司)进行测定。废水体系 pH值用 pH精密酸度计测定,反应体系入口及出口臭氧浓度采用紫外臭氧浓度检测仪(JSA9-03-UV型,深圳市吉顺安科技有限公司)检测。
2 结果与讨论
2.1 微泡反应器中液相O3和·OH浓度的影响参数
2.1.1 反应器压力的影响
在臭氧进口浓度约为65 mg/L,流量3.5 L/min,温度25 ℃条件下,考察反应器压力对液相中臭氧浓度和羟基自由基浓度的影响规律,结果如图2所示。
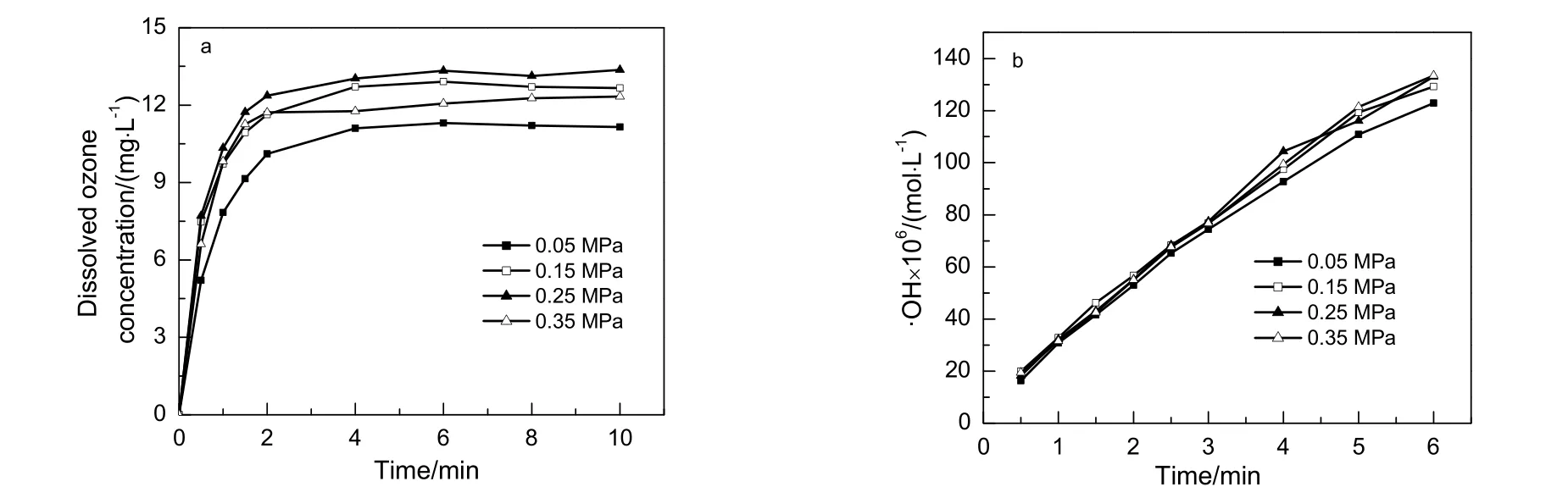
图2 反应器压力对水中O3和·OH浓度的影响Fig.2 Effect of reactor pressure on the concentration of O3 and ·OH in water
由图2a可知,在不同反应器压力下,液相中臭氧浓度在运行时间大约2 min前迅速增大,然后缓慢增大,大约在4~6 min时达到稳定值。当反应器压力在0.05~0.25 MPa时,随着体系压力的增加,液相中臭氧浓度略有增加。由亨利定律可知,气相压力增加有利于提高水中臭氧饱和溶解度,从而提高臭氧在水中的传质效率[23]。但当反应器压力在0.25~0.35 MPa时,随着压力增加液相中臭氧浓度略有减小的现象。这可能与液相中臭氧微气泡的复杂的聚并引起的物理化学过程相关。由图 2b可知,在不同反应器压力下,液相中由于羟基自由基捕获量随着运行时间的延长而增大,其浓度也逐渐升高。但随着反应器中压力增加,液相中·OH浓度的增加更加明显,表明压力升高有助于羟基自由基的产生。
2.1.2 液相温度的影响
在臭氧进口浓度约为65 mg/L,流量3.5 L/min,体系压力0.35 MPa条件下,考察不同温度对液相中臭氧浓度和羟基自由基浓度的影响规律,结果如图3所示。由图3a可知,在不同液相温度下,液相中臭氧浓度在运行时间大约2 min之前迅速增大,然后缓慢变化,在46 min左右达到稳定值。液相中臭氧浓度随着温度增加而有明显的降低。根据亨利定律,在其他条件一定,体系温度与液相中臭氧浓度成反比,这与Rischbieter等[24]研究结果基本一致。由图3b可知,温度在25~35 ℃时,水中羟基自由基浓度随温度的增加而增加。这是由于随着体系温度升高臭氧在水中稳定性减弱,分解速率上升,微气泡臭氧在分解过程中气泡收缩破裂现象更加剧烈,从而加快了羟基自由基产生速率。而在35~40 ℃时,液相中·OH基本保持不变,这主要是由于·OH的产生来源于液相中臭氧的分解反应,而在温度较高情况下,液相中臭氧浓度较低[25],因此·OH不再随体系温度的升高而明显增加,实验中最佳温度为35 ℃。
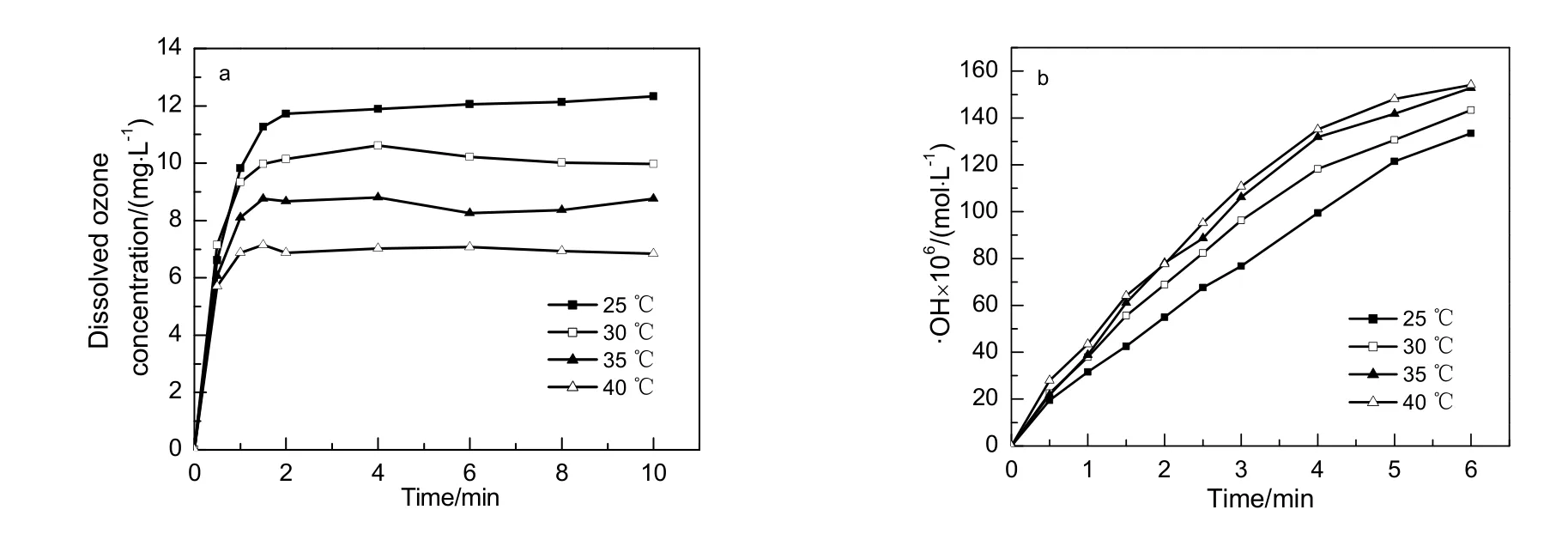
图3 液相温度对液相中O3和·OH浓度的影响Fig.3 Effect of liquid phase temperature on the concentration of O3 and ·OH in water
2.1.3 臭氧进口浓度的影响
在O3进口流量3.5 L/min,体系压力0.35 MPa,温度25 ℃条件下,考察不同进口臭氧浓度对液相中臭氧浓度和羟基自由基浓度的影响规律,结果如图4所示。
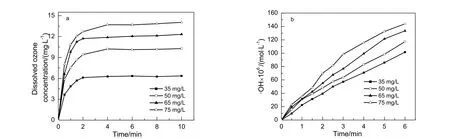
图4 臭氧进口浓度对液相中O3和·OH浓度的影响Fig.4 Effect of inlet ozone concentration on the concentration of O3 and ·OH in water
由图4可知,液相中臭氧及羟基自由基浓度均随进口臭氧浓度的增加而增加。这主要是由于进口臭氧浓度的增加,提高了气相进入液相的传质推动力,使液相中臭氧浓度增加,提高了生成羟基自由基反应的速率,从而使液相中羟基自由基浓度也随之增加[22]。
2.1.4 臭氧进口流量的影响
在O3进口浓度65 mg/L,体系压力0.35 MPa,温度25 ℃条件下,考察不同进口臭氧流量对液相中臭氧浓度和羟基自由基浓度的影响规律,结果如图5所示。由图可知,液相中臭氧及羟基自由基浓度均随进口臭氧流量的增加而增加。这主要是由于增加进口臭氧流量就会增大液相中气泡数量,从而增加了气液传质面积,有利于传质的高效进行。此外,流量增加提高了单位时间内臭氧的进入量,从而提高了臭氧及羟基自由基浓度。

图5 臭氧进口流量对液相中O3和·OH浓度的影响Fig.5 Effect of ozone flow rate on the concentration of O3 and ·OH in water
2.2 微泡与鼓泡反应器性能比较
2.2.1 反应器臭氧传质及其产生羟基自由基性能比较
在臭氧进口浓度65 mg/L,流量3.5 L/min,温度25 ℃,体系压力0.35 MPa条件下,微泡反应体系与鼓泡反应体系的液相中O3以及·OH浓度随时间的变化情况如图6和7所示。

图6 微泡与鼓泡体系液相中臭氧浓度随时间的变化Fig.6 The change of ozone concentration in liquid phase with the reaction time in microbubble and bubbling reactors

图7 微泡与鼓泡体系液相中羟基自由基浓度随时间的变化Fig.7 The change of ·OH concentration in liquid phase with reaction time in microbubble and bubbling reactors
由图6可知,微泡反应器中臭氧溶于水的速率较快,在通入臭氧2 min后水中臭氧浓度基本达到稳定状态,而鼓泡体系中曝气6 min后,水中臭氧浓度才基本达到稳定状态。而且,液相中臭氧浓度达到稳定后,微泡体系中臭氧浓度为14 mg/L,比鼓泡体系约高10%。这表明鼓泡体系中臭氧传质速率低于微泡反应体系。这是由于相对鼓泡体系而言,微泡体系中气泡粒径更小,微气泡具有较大的表面积,且微气泡内压更大,两者结合能有效地提高传质面积和传质推动力,从而提高其传质效率,增加臭氧溶解度[7,8]。由图7可知,微泡反应体系中·OH的含量明显高于传统鼓泡体系,臭氧通入5 min,微泡体系中·OH浓度高达121.45×10-6mol/L,而鼓泡体系中较低,仅为10.86×10-6mol/L,微泡体系中羟基自由基产生能力提高了约11倍。这说明微气泡强化不仅能改善臭氧传质性能,提高液相臭氧浓度,同时也产生更大量的羟基自由基,其化学氧化能力也必然有很大的提高。
2.2.2 微泡与鼓泡反应器中酸性红18降解与矿化动力学比较
在臭氧进口浓度70 mg/L,流量3.0 L/min,温度25 ℃,pH值约为8,染料初始浓度为300 mg/L,其TOC初始浓度约为95 mg/L,微泡体系中压力0.35 MPa的条件下,考察微泡体系和鼓泡体系对酸性红18脱色(即发色团的破坏,使颜色去除)及矿化(有机污染物转化为矿物质,比如水、二氧化碳和无机盐等)处理效果,结果如图8所示。由图可知,微泡反应体系中废水脱色速率更快,完全脱色仅需处理8 min。而在鼓泡体系中氧化处理20 min,其脱色率约为96%。由图8还可以看出,微泡反应体系中染料矿化速率远大于鼓泡体系,鼓泡体系中臭氧氧化处理35 min,对废水TOC去除率仅为21.76%,而在微泡体系中TOC去除率高达70%以上。
为了量化比较两种反应体系中臭氧氧化降解酸性红18的动力学速率,可用拟一级动力学方程式进行拟合[28,29]:

式中:Ct为t时刻废水中染料浓度或TOC浓度;t为反应时间;k为反应速率常数。
将公式(2)进行积分:

其中,Ct0为反应初始时废水中染料浓度或TOC浓度。
根据一级动力学方程对微泡体系与鼓泡体系对酸性红18脱色以及TOC去除情况进行拟合,结果见图9。由图可知,酸性红18脱色数据拟合线性相关系数(R2)均大于0.99,微泡体系中脱色反应速率常数为0.586 5 min-1,约为鼓泡体系中4倍;TOC去除数据线性相关系数均大于0.97,微泡和鼓泡体系中矿化一级反应速率常数分别为0.034 3和0.004 7 min-1,微泡体系中反应速率常数约高一个数量级。微泡体系中脱色率和矿化率都高于鼓泡体系,证实了本臭氧微泡化体系的高效性,这与2.2.1小节中臭氧和羟基自由基浓度测定结论一致。

图9 微泡体系与鼓泡体系对酸性红18脱色以及TOC去除动力学拟合结果Fig.9 Kinetic fitting results on the color and TOC removal efficiency of acid red 18 in the microbubble and bubbling reactors
3 结 论
a)提出了一种基于气液混合泵的臭氧微泡反应器,与传统的鼓泡反应器相比,该反应器能够提升臭氧在液相中的溶解度,增加臭氧的质量转移速率,具有优良的臭氧传质和产生羟基自由基的性能。当两种反应器运行达到稳定之后,微泡体系水中臭氧浓度比鼓泡体系高约 10%,自由基产生量高达11倍以上。采用微泡反应器处理酸性红18染料废水,其降解与矿化效率都明显高于传统鼓泡反应器。
b)在该微泡反应器中,反应器压力对液相中臭氧浓度影响较小,但增加压力有助于羟基自由基产生;液相中臭氧浓度以及羟基自由基产生量随进口臭氧浓度及流量的增加而增加;液相中臭氧浓度随温度升高而降低,但羟基自由基产生量随温度升高而增加。
[1]赵岳阳, 钱丹丹, 秦树林. 我国化工废水特性、治理重点及微电解工艺可行性探讨[J]. 浙江化工, 2013, 44(6): 40-42.Zhao Yueyang, Qian Dandan, Qin Shulin. Study on the characteristics of chemical wastewater, the emphasis of treatment and the feasibility of micro electrolysis process[J]. Zhejiang Chemical Industry, 2013, 44(6): 40-42.
[2]Sarkar S, Ali S, Rehmann L, et al. Degradation of estrone in water and wastewater by various advanced oxidation processes[J]. Journal of Hazardous Materials, 2014, 278: 16-24.
[3]Aken P V, Lambert N, Degreve J, et al. Comparison of different oxidation methods for recalcitrance removal of landfill leachate[J].Ozone: Science and Engineering, 2011, 33: 294-300.
[4]laconi C D, Sanctis M D, Rossetti S, et al. Bio-chemical treatment of medium-aged sanitary landfill leachate in a high synergy system[J].Process Biochemistry, 2011, 46: 2322-2329.
[5]Zhang Jianlin, Yu Hongtao, Quan Xie, et al. Ceramic membrane separation coupled with catalytic ozonation for tertiary treatment of dyestuff wastewater in a pilot-scale study[J]. Chemical Engineering Journal, 2016, 301: 19-26.
[6]Lu X, Ma H, Zhang Q, et al. Degradation of methyl orange by UV, O3and UV/O3systems: analysis of the degradation effects and mineralization mechanism[J]. Research on Chemical Intermediates, 2013, 39(9): 4189-4203.
[7]Gao M, Zeng Z, Sun B, et al. Ozonation of azo dye acid red 14 in a microporous tube-in-tube microchannel reactor: decolorization and mechanism[J]. Chemosphere, 2012, 89(2): 190-197.
[8]Zhang H, Jiang M, Zhang D, et al. Decomposition of 4-nitrophenol by ozonation in a hollow fiber membrane reactor[J]. Chemical Engineering Communications, 2009, 197(3): 377-386.
[9]Gao M, Zeng Z, Sun B, et al. Ozonation of azo dye acid red 14 in a microporous tube-in-tube microchannel reactor: decolorization and mechanism[J]. Chemosphere, 2012, 89(2): 190-197.
[10]Zhu Y, Chen S, Quan X, et al. Hierarchical porous ceramic membrane with energetic ozonation capability for enhancing water treatment[J]. Journal of Membrane Science, 2013, 431: 197-204.
[11]Song S, Ying H, He Z, et al. Mechanism of decolorization and degradation of CI direct red 23 by ozonation combined with sonolysis[J].Chemosphere, 2007, 66(9): 1782-1788.
[12]He Z, Lin L, Song S, et al. Mineralization of CI reactive blue 19 by ozonation combined with sonolysis: performance optimization and degradation mechanism[J]. Separation and Purification Technology, 2008, 62(2): 376-381.
[13]Hsing H J, Chiang P C, Chang E E, et al. The decolorization and mineralization of acid orange 6 azo dye in aqueous solution by advanced oxidation processes: a comparative study[J]. Journal of Hazardous Materials, 2007, 141(1): 8-16.
[14] Özcan A, Şahin Y, Koparal A S, et al. Carbon sponge as a new cathode material for the electro-Fenton process: comparison with carbon felt cathode and application to degradation of synthetic dye basic blue 3 in aqueous medium[J]. Journal of Electroanalytical Chemistry,2008, 616(s 1/2): 71-78.
[15]Xu Y, He Y, Cao X, et al. TiO2/Ti rotating disk photoelectrocatalytic (PEC) reactor: a combination of highly effective thin-film PEC and conventional PEC processes on a single electrode[J]. Environmental Science & Technology, 2008, 42(7): 2612-2617.
[16]Chu L B, Xing X H, Yu A F, et al. Enhanced ozonation of simulated dyestuff wastewater by microbubbles[J]. Chemosphere, 2007,68(10): 1854-1860.
[17]王 璐, 冯 玥, 韦彦斐, 等. 臭氧气泡大小对分散染料废水氧化处理效果的影响[J]. 环境污染与防治, 2013, 35(2): 11-16.Wang Lu, Feng Yue, Wei Yanfei, et al. Influence of ozone bubble size on the treatment of dispersed dyestuff wastewater[J].Environmental Pollution & Control, 2013, 35(2): 11-16.
[18]Takahashi M, Ishikawa H, Asano T, et al. Effect of microbubbles on ozonized water for photoresist removal[J]. Journal of Physical Chemistry C, 2012, 116(23): 12578-12583.
[19]朱兆亮, 曹相生, 孟雪征, 等. 气液混合泵气浮系统处理低浓度二级出水的研究[J]. 中国给水排水, 2008, 24(1): 26-29.Zhu Zhaoliang, Cao Xiangsheng, Meng Xuezheng, et al. Study on advanced treatment of low concentration secondary effluent by DAF process with gas-liquid mixed pump[J]. China Water & Wastewater, 2008, 24(1): 26-29.
[20]朱兆亮, 孟雪征, 曹相生, 等. 三种气液混合泵气浮系统处理低浓度二级出水的对比研究[J]. 环境污染与防治, 2008, 30(8): 4-7.Zhu Zhaoliang, Meng Xuezheng, Cao Xiangsheng, et al. Advanced treatment of secondary effluent by dissolved air flotation employing air-liquid mixing pump in three DAF systems[J]. Environmental Pollution & Control, 2008, 30(8): 4-7.
[21]Bader H, Hoigne J. Determination of ozone in water by the indigo method[J]. Water Research, 1981, 15(4): 449-456.
[22]Milan-Segovia N, Wang Y, Cannon F S, et al. Comparison of hydroxyl radical generation for various advanced oxidation combinations as applied to foundries[J]. Ozone: Science and Engineering, 2007, 29(6): 461-471.
[23]Moslemi M, Davies S H, Masten S J. Ozone mass transfer in a recirculating loop semibatch reactor operated at high pressure[J]. Journal of Advanced Oxidation Technologies, 2010, 13(1): 79-88.
[24]Rischbieter E, Hendrik Stein A, Schumpe A. Ozone solubilities in water and aqueous salt solutions[J]. J Chem Eng Data, 2000, 45(2): 338-340.
[25]Nothe T, Fahlenkamp H, Sonntag C V. Ozonation of wastewater: rate of ozone consumption and hydroxyl radical yield[J].Environmental Science & Technology, 2009, 43(15): 5990-5995.
[26]Song S, Liu Z, He Z, et al. Degradation of the biocide 4-chloro-3,5-dimethylphenol in aqueous medium with ozone in combination with ultraviolet irradiation: operating conditions influence and mechanism[J]. Chemosphere, 2009, 77(8): 1043-1051.
[27]Bai C P, Xiong X F, Gong W Q, et al. Removal of rhodamine B by ozone-based advanced oxidation process[J]. Desalination, 2011,278(1): 84-90.
[28]Barik A J, Gogate P R. Degradation of 4-chloro 2-aminophenol using a novel combined process based on hydrodynamic cavitation, UV photolysis and ozone[J]. Ultrasonics Sonochemistry, 2016, 30: 70-78.
[29]Chen H W, Kuo Y L, Chiou C S, et al. Mineralization of reactive black 5 in aqueous solution by ozone/H2O2in the presence of a magnetic catalyst[J]. Journal of Hazardous Materials, 2010, 174(1): 795-800.

