ZnO/g—C3N4复合材料的制备及其光催化性能研究
刘艳丽+刘倩


摘 要:采用一步法成功制备了氧化锌/石墨相氮化碳(ZnO/g-C3N4)复合光催化材料,通过XRD,SEM,TEM,FT-IR和UV-vis DRS对所得样品的微观形貌和吸光特性进行了表征.结果表明,ZnO颗粒均匀分布在片状g-C3N4表面上,ZnO/g-C3N4最大光吸收边的位置相对于纯相ZnO发生了明显的红移.利用光催化降解甲基橙溶液评估了所得样品的光催化活性,发现ZnO/g-C3N4复合材料的光催化效率远高于纯相ZnO和纯相g-C3N4,分别达到ZnO的14倍和g-C3N4的9倍.复合材料光催化性能得以提升的主要原因有两点:复合样品材料具有比纯相ZnO更大的光吸收范围,提高了太阳光的利用率;ZnO纳米颗粒与g-C3N4紧密耦合形成的异质结构有效促进了光生电子-空穴对的分离.
关键词:半导体;ZnO;g-C3N4;异质结;光催化活性
中图分类号:O612;TQ174 文献标志码:A
Preparation of ZnO/g-C3N4 Composite Photocatalyst with Enhanced Photocatalytic Activity
LIU Yanli1,2,LIU Qian1,2
(1.College of Materials Science and Engineering,Hunan University,Changsha 410082,China;
2.Hunan Province Key Laboratory for Spray Deposition Technology and Application,Hunan University,Changsha 410082,China)
Abstract:ZnO/g-C3N4 composite was prepared by one-step calcining.The microstructure and absorption property of the as-prepared samples were characterized by XRD,SEM,TEM,FT-TR,and UV-vis DRS.The results showed that ZnO particles distributed uniformly on the surface of g-C3N4,and the light absorption edge of the composite had an obvious red shift compared with pure ZnO.Photocatalytic degradation of methyl orange solution experiments was conducted to evaluate photocatalytic activities of the as-prepared samples.The results indicated that ZnO/g-C3N4 exhibited higher photocatalytic activity than pure ZnO and pure g-C3N4.The photocatalytic efficiency was 14 and 9 times as high as that of ZnO and g-C3N4,respectively.The photocatalytic performance of the composite got promoted mainly due to the formation of heterogeneous structure between ZnO and g-C3N4,which decreased recombination rate of photo-induced electron-hole pairs.Furthermore,the composite had wider photoabsorption region compared with pure ZnO,which increased utilization rate of solar energy.
Key words:semiconductor; ZnO; g-C3N4; heterojunction; photocatalytic activity
利用清洁、储量大的太阳能催化降解水中有机污染物是一种既环保又节能的手段,而作為光催化技术核心的半导体光催化材料引起了广泛关注[1-5].通常情况下,纯相半导体光催化剂太阳能利用率低、光生电子-空穴对复合率高等缺点导致其光催化活性不佳.大量研究表明,将能带匹配的两种或多种单相半导体光催化材料复合形成具有异质结构的复合光催化材料可有效改善其光催化性能[6-8].因此,与单相半导体光催化剂相比,复合半导体光催化材料的光催化性能更为优异,具有非常广泛的应用前景.氧化锌禁带宽度约为3.2 eV,是一种Ⅱ-Ⅵ族宽禁带n型半导体材料[9].纳米尺寸的ZnO由于表面效应、宏观量子隧道效应等而具备较好的光催化、电学、磁学等性能[10-12].然而,ZnO带隙较宽,只能吸收太阳光中很少部分的紫外光,在可见光下基本无响应,限制了ZnO在光催化方面的应用.一直以来,众多学者为改善ZnO的光催化活性尝试了很多方法.Zheng等人[13]通过两步溶剂热法成功制备了摩尔比Zn/Sn=1的SnO2/ZnO异质结纳米催化剂,实验结果表明,SnO2/ZnO异质结纳米催化剂比纯相ZnO具有更优异的光催化活性.石墨相氮化碳(g-C3N4)是一种非金属n型半导体材料,带隙约为2.7 eV[14],对可见光有较高的利用率.较多的理论研究工作证实,g-C3N4是氮化碳最稳定的存在形式,不易与其他物质发生反应,并且它有一定的抗酸、碱腐蚀能力,同时也有较高的量子效率,是一种廉价的光催化剂,在光催化领域应用较为广泛[15-17].然而g-C3N4光生电子-空穴复合率高,在一定程度上其光催化活性受到了限制.endprint
为改善ZnO的性能并进一步提高g-C3N4的光催化活性,本文从材料的制备出发,以三聚氰胺和六水合硝酸锌为原料,通过一步煅烧法制备ZnO/g-C3N4复合物粉末,并以甲基橙溶液(MO)作为模拟污染物,对所得材料的光催化活性进行了系统测试,结合实验结果进一步讨论了材料的光催化降解机理.
1 实验部分
实验过程中使用的试剂均为分析纯,使用时不需进一步纯化,所用水均为二次去离子水.
1.1 纯相g-C3N4的制备
称取5.0 g三聚氰胺(C3H6N6)粉末置于坩埚中,升温速率设定为4 ℃/min,在温度520 ℃下,于马弗炉中煅烧4 h.随炉冷却至室温后,收集所得淡黄色产物,即为纯相g-C3N4.
1.2 ZnO/g-C3N4复合材料的制备
称取0.010 mol六水合硝酸锌(Zn(NO3)2·6H2O),将其溶于20 mL去离子水中,磁力搅拌10 min至其完全溶解,形成澄清溶液后,加入0.010 mol三聚氰胺粉末,再次磁力搅拌30 min,后转移至80 ℃的水浴锅中边加热边搅拌,蒸干部分溶剂至粘稠状后,转移至鼓风干燥箱中,于60 ℃温度下干燥12 h后,置于马弗炉中,520 ℃下煅烧4 h,所得产物即为ZnO/g-C3N4复合物.
采用上述同样的过程制备纯相ZnO,只是不加入三聚氰胺粉末.
1.3 样品的表征
利用Rigaku D/Max-2400型转靶全自动X射线粉末衍射仪(X-ray Diffraction,XRD)确定产品的物相和纯度,Cu Kα线(λ= 1.541 78 )作为发射光源,加速电压为40 kV,电流为100 mA,扫描速度为8°/min;扫描电镜照片(FE-SEM)来自Hitachi S-4800冷场发射扫描电子显微镜,工作电压分别为10 kV和15 kV;透射电镜照片(TEM)来自日本JEOL公司生产的JEM-3010型透射电子显微镜;紫外/可见吸收光谱来自Hitachi Model U-4100固相紫外/可见/近红外吸收光谱仪,扫描范围为300~800 nm,测试过程中,BaSO4作为参比材料;本实验采用岛津IRAffinity-1型傅里叶变换红外光谱仪获取所得样品的红外光谱图,以溴化钾作为参照物.
1.4 光催化性能测试
本实验中采用甲基橙(MO,methyl orange)溶液作为模拟污染物,在甲基橙溶液中加入光催化剂并在光照射一定时间后,根据甲基橙溶液浓度的变化评估样品的光催化性能.具体操作过程如下:在石英杯中加入400 mL浓度为5.0 mg/L的MO溶液,称取0.30 g样品粉末分散于MO溶液中,调整搅拌速度为360 r/min左右.首先MO溶液置于暗态下处理40 min,使其达到吸附-脱附平衡.之后打开氙灯光源(XQ350W可调型氙灯电源),设置电流为12.6 A,不断搅拌下,对溶液进行光照,光照时间为120 min.从暗态处理至光照的整个过程中,每隔20 min取样约10 mL,迅速离心,取上清液,采用上海元析有限公司生产的UV-6000PC型紫外-可见分光光度计对上清液做紫外-可见吸收光谱测试,测试范围为200~800 nm,扫描速率为0.002 nm/s.为排除MO溶液自降解性的可能,在不加入任何光催化剂的前提下,以相同的处理方法测定了一组空白MO溶液的自降解.
2 结果与讨论
2.1 所得样品的物相分析
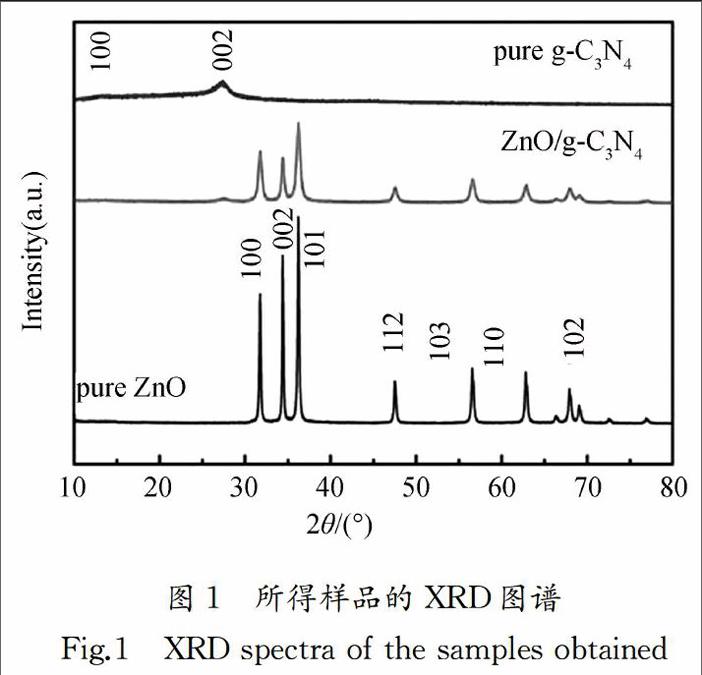
通過X射线衍射仪分析所得样品的物相结构及组成.图1为所得纯相ZnO、纯相g-C3N4以及ZnO/g-C3N4复合材料的XRD图谱.如图1所示,对于ZnO样品的XRD图谱,与PDF卡片中的JCPDS No.36-1451相符合,衍射峰所对应的2θ值31.7°,34.4°,36.2°,47.5°,56.6°,62.7°,66.4°,67.9°,69.0°,72.5°,76.9°分别对应(100),(002),(101),(102),(110),(103),(200),(112),(201),(004)和(202)晶面,证明该样品为具有六方纤锌矿结构的ZnO,其晶格参数为a=b=3.25 , c = 5.21 .对于g-C3N4样品的XRD图谱,2θ值为13.5°和27.3°处的衍射峰分别为g-C3N4的(100)和(002)晶面,对应于共轭碳环(002)晶面的层间堆垛及(100)晶面的面内结构堆垛.ZnO/g-C3N4复合材料的XRD图谱具有与ZnO,g-C3N4衍射峰位置相同的衍射峰,这表明该样品为ZnO/g-C3N4复合材料.此外,3种样品的XRD图谱中均没有出现多余的衍射峰,表明所得样品没有其他杂质,纯度较高.
2.2 样品形貌分析
图2给出了纯相ZnO,g-C3N4以及ZnO/g-C3N4复合物样品的SEM图.图2(a)中,纯相ZnO呈分散的颗粒状,大小不一,尺寸分布不均匀,可能是因为在煅烧过程中,六水合硝酸锌中结晶水的析出,使得ZnO形成大小不一、没有固定形状的ZnO颗粒.从图2(b)可以看到,g-C3N4呈现出片层结构.图2(c)为ZnO/g-C3N4复合材料,从图中可以明显看出g-C3N4上覆盖了很多ZnO颗粒,与上述XRD结果相符合.另外,ZnO颗粒没有完全覆盖g-C3N4表面,因此不会影响g-C3N4对光的吸收.图3是ZnO/g-C3N4复合物样品的TEM和HR-TEM图.从图3(a)可以发现,图中明显有两种不同的物相:一种物相呈短棒状,而另一种呈片状.从图3(b)中可以观察到短棒状的物质有明显的晶格条纹,其条纹间距为0.26 nm,与ZnO (002)晶面的晶面间距相符.结合上述XRD结果,可以推断短棒状的物质为ZnO,片状物相为g-C3N4.透射表征表明了复合物中形成了ZnO和g-C3N4之间异质结构.与纯相g-C3N4相比,ZnO和g-C3N4之间异质结构的形成,更有助于光生电子空穴对的有效分离,提高材料的光催化性能.endprint
2.3 红外光谱分析
图4为所制得样品的红外光谱(FT-IR)图.从图中可以看出,纯相ZnO在500 cm-1范围内有一个较宽的吸收峰,这归结于Zn-O伸缩振动[18-19] ,另外两个不太显著的较宽吸收峰在3 500和1 650 cm-1处,这归结于样品表面吸附的水和羟基引起的[20].对于纯相g-C3N4而言,则存在3个明显的特征区域峰:在3 000~3 600 cm-1之间的宽吸收峰归结于N-H伸缩振动引起的[21-22];在1 240~1 640 cm-1之间的强吸收峰归结于C-N和C@N杂环的典型伸缩振动引起的[23-24];在810 cm-1附近的吸收峰与s-嗪环的振动有关[25-26].对于复合材料ZnO/g-C3N4,从其谱图中可以看到,既具有ZnO的典型吸收峰,又具有g-C3N4的典型吸收峰,其中1 240~1 640 cm-1和810 cm-1附近的吸收峰归属于g-C3N4的典型伸缩振动引起的,这也表明了复合物中g-C3N4的存在.而在500 cm-1范围内的吸收峰则表明了ZnO的存在.
2.4 紫外-可见漫反射光谱分析
图5是纯相ZnO,g-C3N4以及ZnO/g-C3N4复合物样品的漫反射光谱图.从图中可以看出,纯相ZnO的吸收限约为400 nm,对可见光几乎不响应.而g-C3N4吸收限接近470 nm,在可见光区域有强烈的吸收.与纯ZnO和g-C3N4相比,将两者复合制成的ZnO/g-C3N4复合物的吸收限介于ZnO和g-C3N4之间,显示出复合物的光吸收特点,其最大光吸收边的位置相对于纯相ZnO发生明显的红移,向长波长方向移动,扩大了太阳光的利用范围,可以更加有效地利用可见光.
半导体禁带宽度是导带的最低能级和价带的最高能级之间的带隙,用符号Eg表示,由式(1)可计算半导体物质的禁带宽度[21]:
ahv=A(hv-Eg)n/2(1)
式中:a,h和v分别为吸收系数、普朗克常数(6.626×10-34 J·s)和光的频率;A为常数;n取决于半导体材料光跃迁的类型.ZnO和g-C3N4的n均取值为1[27].图5(b)是分别用纯相ZnO和g-C3N4的(ahv)2对(hv)的关系作出的两条曲线,将曲线的直线部分外推,可求出ZnO和g-C3N4的禁带宽度分别约为3.12 eV和2.79 eV,与文献值基本相符[9,14].
2.5 光催化性能研究
本实验以甲基橙(MO)溶液作为模拟污染物,对所得样品的光催化性能进行了系统研究,实验结果如图6所示.图6(a)为不加入催化剂时,仅有光照存在MO溶液的自降解情况,由图可见,MO在465 nm处有一个最大吸收峰,不加入光催化剂时,各个测试时间段的吸光度曲线基本重合,表明整个测试过程中,MO溶液浓度几乎不变,即不加任何光催化剂时,MO溶液不具有自降解性能.图6(b),(c),(d)分别为加入ZnO,g-C3N4和ZnO/g-C3N4复合物时,MO溶液吸光度随时间变化的关系曲线,图6(e)为各样品的降解率随处理时间的变化曲线.由图6可知,纯相ZnO和g-C3N4的暗态0 min与暗态40 min曲线基本重合,表明ZnO和g-C3N4粉末对MO吸附非常少,而ZnO/g-C3N4复合物粉末对MO吸附较大(图6(d)),ZnO/g-C3N4复合物粉末对MO的吸附量明显比相同质量的ZnO和g-C3N4粉末大.对3种所得样品,暗态处理20 min和暗态处理40 min后的吸光度曲线基本重合,表明加入了ZnO,g-C3N4以及ZnO/g-C3N4复合物的MO溶液经暗态处理40 min后均达到了吸附-脱附平衡.光照120 min后,纯相ZnO和g-C3N4粉末对MO的降解度分别达到18%,30%左右,而ZnO/g-C3N4复合材料对MO溶液的降解度则达到94%左右,结果表明复合样品的光催化性能显著增强.
为了更为直观地比较各个组分之间的光催化性能,对纯相ZnO,纯相g-C3N4及ZnO/g-C3N4复合材料的降解速率进行了计算,结果示于图6(e)中.从图可以看出,各个组分的实验数据经过式(2)变换后[28],能很好地与一阶模型相吻合.
ln(C/C0) = -kt(2)
式中k值代表光催化降解速率,单位是min-1,能够很好地反映样品光催化降解性能的优劣;C0代表MO溶液的初始浓度;C代表在光照时刻t时MO溶液的浓度,单位均是mg/L.由朗伯-比尔定律(Lambert-Beer Law)可知,MO溶液的浓度则是与
溶液的吸光度成正比,即有:C/C0 =A/A0=t時刻最大吸收峰强度/零时刻的最大吸收峰强度.经计算得知,空白样直线的斜率大小为9.854 9×10-5,接近于0,而纯相ZnO,纯相g-C3N4及ZnO/ g-C3N4复合材料的光催化降解速率k分别为:0.001 66 min-1,0.002 76 min-1,0.023 98 min-1,表明复合材料表现出最优异的光催化性能,其对MO的降解速率分别约为纯相ZnO的14倍和g-C3N4的9倍.这一结果表明将ZnO与g-C3N4复合能够明显提高样品的光催化性能.
2.6 光催化降解机理讨论
从上述实验结果可知,ZnO/g-C3N4复合材料相对于纯相ZnO和纯相g-C3N4,其光催化性能显著增强.这种现象可以从两个方面进行解释:1)复合样品材料具有比纯相ZnO更大的光吸收范围,提高了太阳光的利用率;2)ZnO/g-C3N4界面处形成内电场驱动光生载流子有效分离.由上述计算结果可知,ZnO和g-C3N4的禁带宽度分别约为3.12 eV和2.79 eV.半导体物质的价带和导带带势可由式(3)和(4)计算[29]:
EVB=χ-Ee+0.5Eg(3)
ECB=EVB- Eg(4)endprint
式中: EVB和ECB分别为半导体价带和导带的电位;χ为半导体的电负性值; Ee为自由电子的能量;Eg为半导体的禁带宽度.ZnO和g-C3N4的χ分别取值为5.95 eV和4.72 eV,Ee取值为4.5 eV[30].计算可得,ZnO的价带和导带的带势分别为3.05 eV和-0.15 eV,而g-C3N4的价带和导带的带势分别为1.5 eV和-1.13 eV.显然,g-C3N4的价带和导带的电位分别比ZnO的价带和导带电位更负.
如图7所示,当太阳光照射复合材料时,价带上的自由电子吸收光子能量跃迁到导带上,同时在其价带上留下相同数目的空穴.ZnO和g-C3N4匹配的能带结构形成
“台阶”,光生电子移动到ZnO的导带上,而空穴则聚集在g-C3N4的价带上,因此大大降低了電子和空穴的复合率.移动到催化剂表面的光生电子与复合物光催化剂表面吸附的溶解氧结合生成超氧自由基(·O2-),而空穴与OH-和水反应生成羟基自由基(·OH-),并进一步形成H2O2. ·O2-,·OH-以及H2O2等都具有很强的氧化性,它们与甲基橙发生氧化还原反应,实现对甲基橙的降解[31-32].
3 结 论
本文以分析纯三聚氰胺和六水合硝酸锌为原料,通过一步法得到ZnO/g-C3N4复合物,并进行光催化降解甲基橙溶液实验来评测样品的光催化活性.结果表明,复合后的ZnO/g-C3N4复合材料形成异质结构,降低了光生电子和空穴的复合率.此外,与纯相ZnO相比,复合材料的最大光吸收边位置发生了明显的红移,扩大了对太阳光的吸收范围,提高了对太阳能的利用率.因此,ZnO/g-C3N4复合材料展现出比纯相ZnO,g-C3N4更优异的光催化降解性能.
参考文献
[1] LINSEBIGLER A L,LU G Q,JOHN T,et al.Photocatalysis on TiO2 surfaces,mechanisms,and selected results[J].Chemical Reviews,1995,95(3):735-758.
[2] LIU W,ZHAO G S,AN M Z,et al.Solvothermal synthesis of nanostructured BiVO4 with highly exposed (010) facets and enhanced sunlight-driven photocatalytic properties[J].Applied Surface Science,2015,357:1053-1063.
[3] LUAN Y B,JING L Q,WU J,et al.Long-lived photogenerated charge carriers of 001-facet-exposed TiO2 with enhanced thermal stability as an efficient photocatalyst[J].Applied Catalysis B:Environmental,2014,147(7):29-34.
[4] 余健,赵令晖,唐浩,等.In2S3-Ag/TiO2三元纳米体系光催化降解2,4-D的实验研究[J].湖南大学学报:自然科学版,2015,42(12):107-114.
YU Jian,ZHAO Linghui,TANG Hao,et al. The investigation of photodegration of 2,4-D by the three-componment system In2S3-Ag/TiO2 Nanotube arrays[J].Journal of Hunan University:Natural Sciences,2015,42(12):107-114 .(In Chinese)
[5] JIANG J,LI H,ZHANG L Z.New insight into daylight photocatalysis of AgBr@Ag:synergistic effect between semiconductor photocatalysis and plasmonic photocatalysis[J].Chemistry:A European Journal,2012,18(20):6360-6369.
[6] ZHAO S S,CHEN S,YU H T,et al. g-C3N4/TiO2 hybrid photocatalyst with wide absorption wavelength range and effective photogenerated charge separation[J].Separation and Purification Technology,2012,99(8):50-54.
[7] WANG Y J,SHI R,LIN J,et al.Enhancement of photocurrent and photocatalytic activity of ZnO hybridized with graphite-like C3N4[J].Energy & Environmental Science,2011,4(8):2922-2929.
[8] YANS C,LI Z S,ZOU Z G.Photodegradation of rhodamine B and methyl orange over boron-doped g-C3N4 under visible light irradiation[J].Langmuir,2010,26(6):3894-3901.endprint
[9] 崔義慧,赵丹,李玲美,等.无水体系制备ZnO/CdSe-ZnO及光催化性能研究[J].辽宁化工,2016,45(3):265-267.
CUI Yihui,ZHAO Dan,LI Lingmei,et al.Study on preparation of ZnO/CdSe-ZnO in anhydrous system and its photocatalytic properties[J].Liaoning Chemical Industry,2016,45(3):265-267.(In Chinese)
[10]ZGR ,ALIVOV Y I,LIU C, et al.A comprehensive review of ZnO materials and devices[J].Journal of Applied Physics,2005,98(4):041301-041404.
[11]李小明,张志贝,杨伟强,等.ZnO-Sm纳米复合物制备及可见光催化降解RhB[J].湖南大学学报:自然科学版,2016,43(6):130-136.
LI Xiaoming,ZHANG Zhibei,YANG Weiqiang, et al.Facile synthesis of samarium-doped ZnO nanostructures and their photocatalytic performance for RhB degradation under visible light irradition[J].Journal of Hunan University:Natural Sciences,2016,43(6):130-136.(In Chinese)
[12]CHENG H M,CHIU W H,LEE C H,et al.Formation of branched ZnO nanowires from solvothermal method and dye-sensitized solar cells applications[J].The Journal of Physical Chemistry C,2008,112(42):16359-16364.
[13]ZHENG L R,ZHENG Y H,CHEN C Q,et al. Network structured SnO2/ZnO heterojunction nanocatalyst with high photocatalytic activity[J].Inorganic Chemistry,2009,48(5):1819-1825.
[14]LV H L,JI G B,YANG Z H, et al.Enhancement photocatalytic activity of the graphite-like C3N4 coated hollow pencil-like ZnO[J].Journal of Colloid and Interface Science,2015,450:381-387.
[15]YANG M,FENG J Q,HUANG Q.Influence of mechanical milling on photocatalytic activity of g-C3N4 prepared by heating melamine[J].Journal of Wuhan University of Technology:Materials Science Edition,2010,25(6):914-918.
[16]CUI Y J,DING Z X,LIU P,et al. Metal-free activation of H2O2 by g-C3N4 under visible light irradiation for the degradation of organic pollutants[J].Physical Chemistry Chemical Physics,2012,14(4):1455-1462.
[17]DONG F,WU L W,SUN Y J, et al.Efficient synthesis of polymeric g-C3N4 layered materials as novel efficient visible light driven photocatalysts[J].Journal of Materials Chemistry,2011,21(39):15171-15174.
[18]JO W,SELVAM N C S.Enhanced visible light-driven photocatalyticperformance of ZnO-g-C3N4 coupled with graphene oxide as a novel ternary nanocomposite[J].Journal of Hazardous Materials,2015(299):462-470.
[19]SURYA P A,PANT H R.Deposition of ZnO flowers on the surface of g-C3N4 sheets via hydrothermal process[J].Ceramics International,2015,41(10):12923-12929.
[20]YU J G,SU Y R,CHENG B,et al.Effects of pH on the microstructures and photocatalytic activity of mesoporous nanocrystalline titania powders prepared via hydrothermal method[J].Journal of Molecular Catalysis A:Chemical,2006,258(1/2):104-112.endprint
[21]PANY S,PARIDA K M.A facile in situ approach to fabricate N,S-TiO2/g-C3N4 nanocomposite with excellent activity for visible light induced water splitting for hydrogen evolution[J].Physical Chemistry Chemical Physics,2015,17(12):8070-8077.
[22]XU M,HAN L,DONG S J.Facile fabrication of highly efficient g-C3N4/Ag2O heterostructured photocatalysts with enhanced visible-light photocatalytic activity[J].ACS Applied Materials & Interfaces,2013,23(5):12533-12540.
[23]DONG F,WU L W,SUN Y J,et al.Efficient synthesis of polymeric g-C3N4 layered materials as novel efficient visible light driven photocatalysts[J].Journal of Materials Chemistry,2011,39(21):15171-15174.
[24]BOJDYS M J,MULLER J O,ANTONIETTI M,et al.Ionothermal synthesis of crystalline,condensed,graphitic carbon nitride[J].Chemistry-A European Journal,2008,27(14):8177-8182.
[25]LIAO G Z,CHEN S,QUAN X,et al.Graphene oxide modified g-C3N4 hybrid with enhanced photocatalytic capability under visible light irradiation[J].Journal of Materials Chemistry,2012,22(6):2721-2726.
[26]LIY B,ZHANG H M,LIU P R,et al. Cross-linked g-C3N4/rGO nanocomposites with tunable band structure and enhanced visible light photocatalytic activity[J].Small,2013,19(9):3336-3344.
[27]WANG X J,WANG Q,LI F T, et al. Novel BiOCl-C3N4 heterojunction photocatalysts:In situ preparation via an ironic-liquid-assisted solvent-thermal route and their visible-light photocatalytic activities[J].Chemical Engineering Journal,2013,234(12):361-371.
[28]SUN J X,YUAN Y P,QIU L G,et al.Fabrication of composite photocatalyst g-C3N4-ZnO and enhancement of photocatalytic activity under visible light[J].Dalton Transactions,2012,41(22):6756-6763.
[29]MA J Q,GUO X H,ZHANG Y Y,et al.Catalytic performance of TiO2@Ag composites prepared by modified photodeposition method[J].Chemical Engineering Journal,2014,258(258):247-253.
[30]KUANG P Y,SU Y Z.g-C3N4 decorated ZnO nanorod arrays for enhanced photoelectrocatalytic performance[J].Applied Surface Science,2015,358:296-303.
[31]IKEDA K,SAKAI H,BABA R,et al.Photocatalytic reactions involving radical chain reactions using microelectrodes[J].Journal of Physical Chemistry B,1997,101(14):2617-2620.
[32]KUBO W,TATSUMA T.Mechanisms of photocatalytic remote oxidation[J].Journal of the American Chemical Society,2006,128(50):16034-16035.endprint

