磷灰石和石灰稳定化修复对污染土壤铜和镉垂直迁移的影响①
范玉超,吴求刚,崔红标,夏睿智,陈 剑,周 静
(1安徽理工大学地球与环境学院,安徽淮南 232001;2 中国科学院土壤环境与污染修复重点实验室(南京土壤研究所), 南京 210008)
重金属在土壤中无法被生物和化学降解,一旦进入土壤将会长期存在[1]。由于重金属污染的土壤对人体健康和动植物生长具有极大的危害性,土壤重金属污染引起人们的高度关注。在我国,土壤重金属污染形势尤其严峻。2016年5月31日发布的《土壤污染防治行动计划》中“有序开展治理与修复”部分提出“到2020年,受污染耕地治理与修复面积达到1 000万亩”。因此,降低土壤中重金属总量或其有效性成为国内外研究的热点。
稳定化修复技术具有低成本、方便操作等优点,目前在重金属污染土壤修复中得到广泛应用[2-3]。该方法不能减少土壤重金属的总量,仅能够通过改良材料与重金属之间的吸附、沉淀和络合等降低重金属的活性,达到稳定化的目的[4]。常见的石灰、磷酸盐、沸石、泥炭等有机和无机物质已经被广泛应用于重金属污染土壤的稳定化修复,其中泥炭和磷酸盐等还具有通过提供土壤有机质和其他养分的方式减少肥料输入的功能[5-7]。
当前,关于重金属污染土壤的稳定修复方法已有大量的报道,但修复时间通常在1年左右,或局限于室内模拟[8-10]。如Liang等[11]向土壤中添加海泡石显著降低土壤 CaCl2、HCl、TCLP和离子交换态镉的含量,并减少水稻对镉的吸收。早期已有的稳定化修复多是采用连续添加钝化剂的方法[12-13],若钝化剂本身含有大量的重金属,长期连续添加势必导致土壤重金属总量进一步增加。但实际上,钝化剂添加到土壤后在一段时间内对重金属具有较好的稳定化效果[14],此时钝化剂即便本身重金属含量较高,只要用量合理,一次性添加稳定化修复也不会具有较高的风险。
另外,以往的研究对象多集中在钝化剂与污染土壤混合的土层[11,15],对其下层土壤重金属的淋溶和有效性变化的影响鲜有报道。由于重金属在不同土层的分布对于评估改良材料稳定化修复效率和地下水环境风险具有重要的意义,并可直接影响受污染区居民的居住安全[1]。因此,本文对不同剂量的磷灰石和石灰稳定化修复的江西贵溪某铜镉长期污染土壤进行分层采样,考察铜和镉在不同土层的分布特征,并分析铜和镉有效性的垂直分布特点,以对不同用量改良材料稳定化修复的潜在风险进行科学评估,为重金属污染土壤修复提供科学指导。
1 材料与方法
1.1 区域概况
试验小区位于江西省贵溪市,属于亚热带季风气候,年平均降水量为 1 808 mm。该区域分布有冶炼厂、肥料厂、防腐厂、电子废弃物拆解厂等。由于早期技术上的限制,冶炼过程中所产生的废渣、废水和废气经过多年的排放、累积,导致周边130 hm2农田遭受重金属污染(主要污染物是铜和镉)[16]。前期的调查研究[17]发现,该区域内的农田土壤铜和镉超标率分别为100% 和87%~100%。2009年前,该区域大部分农田处于抛荒状态,部分重度污染区寸草不生。布置试验前试验区土壤pH 4.56,容重1.29 g/cm3,有机碳16.3 g/kg,总铜678 mg/kg,总镉0.53 mg/kg。
1.2 改良材料
试验用石灰(粒径0.16 mm)购自江西鹰潭建材大市场,磷灰石(粒径0.25 mm)购自湖北南漳县鑫泰磷化工厂,石灰和磷灰石pH分别为12.2和8.40,铜含量分别为1.36和9.54 mg/kg,镉含量分别为0.87和1.18 mg/kg。
1.3 试验设计和过程
试验于2009年11月布置,每个小区长3 m,宽2 m。试验共设7 个处理,其中磷灰石用量分别为5.8、11.6和 23.2 g/kg,记为 L-磷灰石、M-磷灰石和 H-磷灰石;石灰用量分别为1、2和4 g/kg,记为L-石灰、M-石灰和H-石灰,以及对照处理,记为CK。
将改良材料与表层(0~13 cm)土壤(13 cm以下是犁底层)用铁耙混合均匀,对照处理不添加任何钝化材料。每小区添加自来水100 kg清水平衡一周后施加复合肥,播种黑麦草。整个试验过程中仅在2009年施加一次改良材料,且黑麦草仅在2010—2013年能够存活,其生物量逐渐降低,但试验过程中除对照处理外均有土著杂草金黄狗尾草生长。2014年后不再播种黑麦草,仅考察土著植物金黄狗尾草的生物量和重金属吸收变化。另外,试验过程中各小区施肥、播种、田间管理方式均保持一致。
土壤样品采集于2016年1月,此时小区杂草已经移除。按照 0~13、13~30、30~50 cm,从底向上分别采集土壤样品。样品带回实验室风干,研磨,用于土壤基本化学性质及铜、镉、钙和磷含量的分析。
1.4 分析方法
采用重铬酸钾湿式氧化法测定土壤有机碳含量,土壤和改良材料的pH采用固液比为1∶2.5的比例添加无CO2蒸馏水,用pH电极测定。采用HF-HNO3-HClO4(10 ml-5 ml-5 ml)电热板消解,原子吸收(或石墨炉)分光光度计法测定铜、镉和钙总量,采用钼锑抗-抗坏血酸法测定磷的含量[18]。土壤标准物质为国家标准物质研究中心购买的 GBW07405,准确率为96%~103%。土壤碱解氮、有效磷、速效钾、阳离子交换量、交换性酸和交换性铝按照常规方法测定[19]。土壤铜和镉有效态含量采用 0.01 mol/L CaCl2以1∶5的土水比振荡提取2 h,4 000 r/ min离心10 min,过滤后测定。
1.5 数据处理
用 Excel 2010对试验数据进行整理,SPSS 19.0软件对数据进行单因素方差分析,不同处理间的最小显著性差异检验在P<0.05(LSD)水平下进行。
2 结果分析
2.1 土壤基本化学性质变化
如表1所示,不同剂量的磷灰石和石灰处理均未对土壤全氮、有机碳和碱解氮含量产生显著影响。对照处理0~13 cm土层土壤全磷含量为895 mg/kg,随着磷灰石用量从5.8 g/kg增加到23.2 g/kg,土壤全磷从1 364 mg/kg增加到3 139 mg/kg,但是石灰处理对土壤全磷含量没有影响。随着磷灰石(5.8~23.2 g/kg)和石灰(1~4 g/kg)用量的增加,0~13 cm 土层土壤全钙含量增加到4 g/kg石灰处理下的395 mg/kg和23.2 g/kg 磷灰石处理下的4 179 mg/kg,分别比对照增加了1.67倍和27.3倍。与对照相比,石灰用量的增加未对土壤有效磷的含量产生显著影响,但是土壤有效磷含量由5.8 g/kg 磷灰石处理的74.2 mg/kg增加到23.2 g/kg 磷灰石处理下143 mg/kg,提高了0.93倍。另外,磷灰石和石灰的添加均增加了土壤速效钾的含量,且均随着用量的增加而提高,但是磷灰石和石灰的添加均未提高土壤阳离子交换量。对照处理交换性酸和交换性铝的含量分别为4.21 cmol/kg和3.63 cmol/kg,磷灰石和石灰的添加均显著降低了土壤交换性酸和交换性铝的含量,且磷灰石处理的降幅要显著高于石灰处理的降幅。如石灰处理用量由 1 g/kg 提高到4 g/kg 时,土壤交换性酸含量由3.56 cmol/kg降低到 0.79 cmol/kg;磷灰石用量由 5.8 g/kg 提高到23.2 g/kg 时,土壤土壤交换性酸含量由2.43 cmol/kg降低到0.12 cmol/kg。
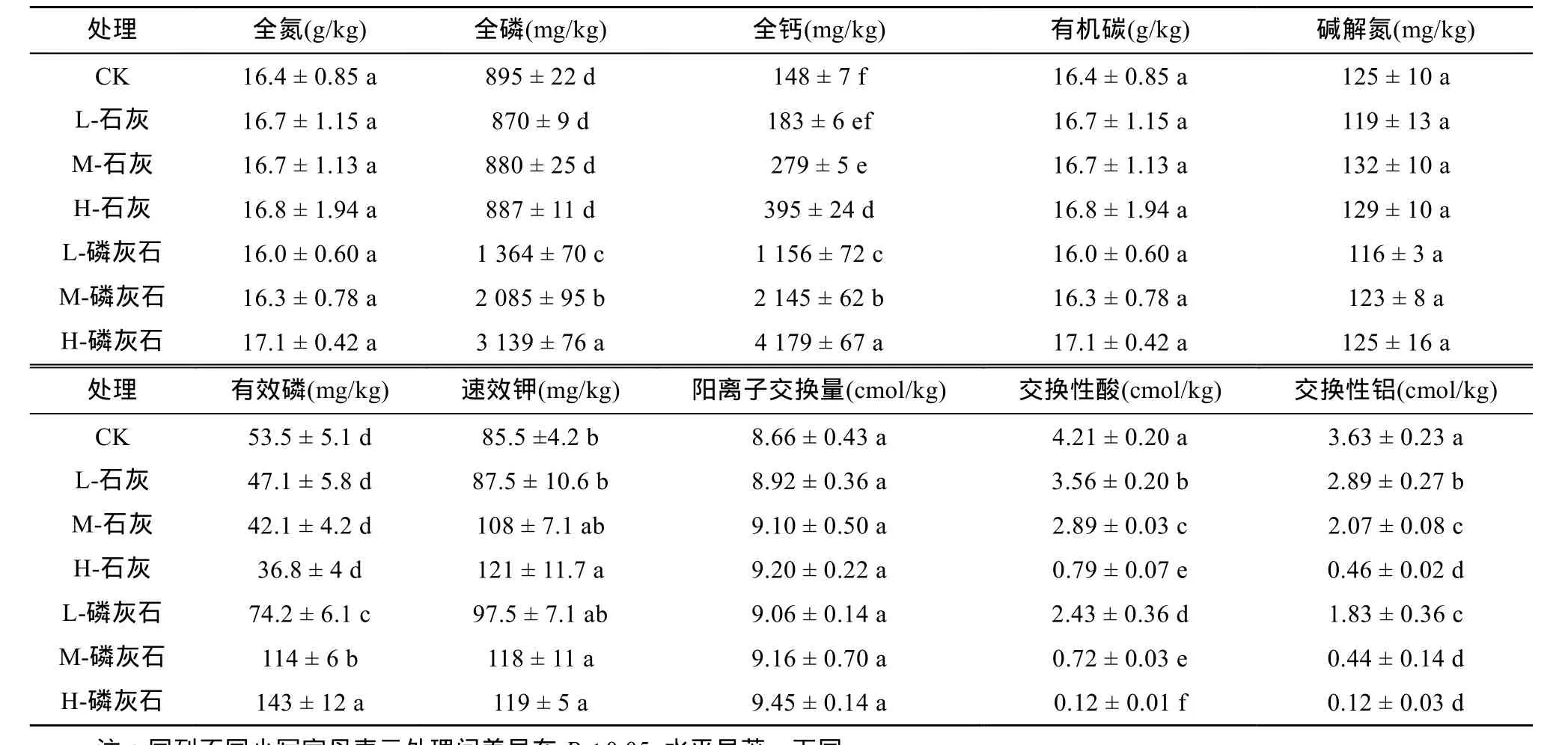
表1 不同剂量磷灰石和石灰处理表层土壤的基本化学性质Table 1 Basic chemical characteristics of tested soils amended by different dosages of lime and apatite
2.2 土壤pH和全量铜镉垂直分布
如图1所示,磷灰石和石灰原位添加7 a后,0 ~13 cm表层土壤pH显著高于对照处理,且土壤pH随着磷灰石和石灰用量的增加而显著增加,其中23.2 g/kg 磷灰石处理和4 g/kg 石灰处理土壤pH分别较5.8 g/kg 磷灰石处理和1 g/kg 石灰处理增加0.98和1.1个单位。13~30 cm土层,与对照相比,仅有4 g/kg石灰处理和11.6、23.2 g/kg磷灰石处理显著增加土壤pH。30~50 cm土层,仅有23.2 g/kg 磷灰石处理较对照处理显著增加土壤pH。以上结果表明,改良剂的应用对土壤pH的影响主要局限在土壤表层,随着土层深度的增加,影响逐渐减弱,且土壤pH的提高幅度随着改良材料用量的增加而增加。
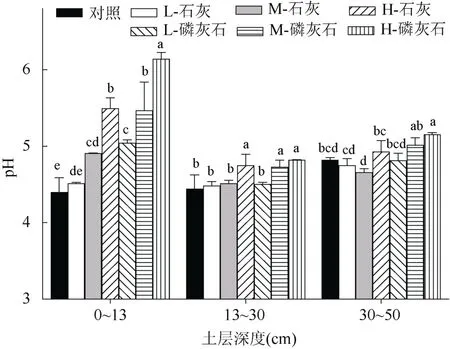
图1 磷灰石和石灰处理0~50 cm土层土壤pH的变化Fig. 1 Changs of soil pH in 0-50 cm soils amended by lime and apatite
如图2A所示,在0~13 cm土层,土壤铜的含量随着磷灰石和石灰用量的增加略微提升,其中4 g/kg 石灰处理和23.2 g/kg磷灰石处理土壤铜含量分别显著增加10.9% 和10.4%。与0~13 cm(总铜690~765 mg/kg)土层相比,13~30 cm 土层土壤总铜含量显著增加到859~1 070 mg/kg,且土壤总铜含量均随着改良材料用量的增加而降低,如4 g/kg 石灰处理和23.2 g/kg 磷灰石处理土壤铜含量较对照显著降低18.3% 和19.8%。然而,土壤总铜含量在30~50 cm土层显著降低到354~512 mg/kg,且总铜含量随着磷灰石和石灰用量的增加而降低。
与土壤总铜含量变化相似,0~13 cm土层土壤镉的总量均随着磷灰石和石灰用量的增加而显著增加(图 2B)。添加磷灰石和石灰处理的土壤在13~30和30~50 cm土层均降低了总镉含量,且均随着表层磷灰石和石灰用量的增加而降低。但与土壤总铜含量在不同土层分布不同,土壤总镉在0~13 cm 土层(548~665 µg/kg)和 13~30 cm 土层(511~663 µg/kg)含量接近,30~50 cm 土层含量最低(442~540 µg/kg)。可见,改良材料的添加较好地将重金属固持在土壤表层,降低了重金属向土壤下层的淋溶迁移。
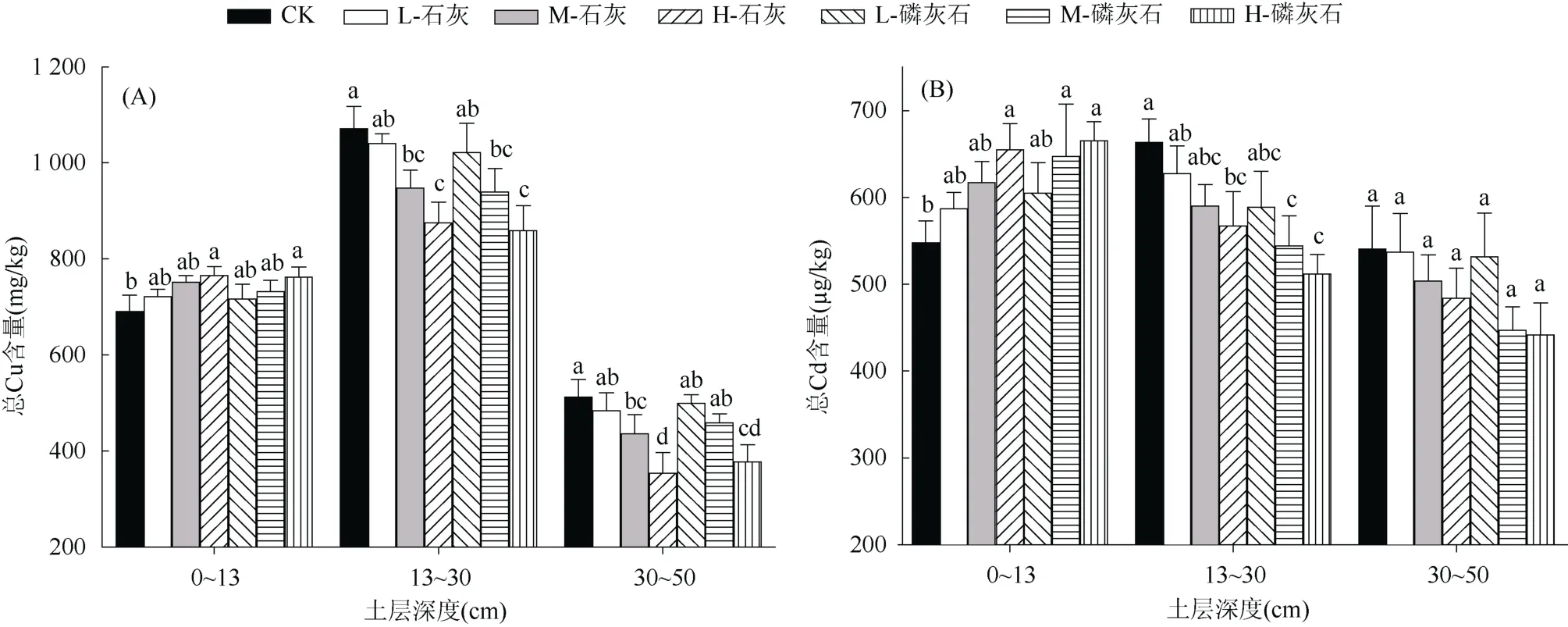
图2 磷灰石和石灰处理0~50 cm土层总铜(A)和总镉(B)含量变化Fig. 2 Concentrations of total Cu (A) and Cd (B) in 0-50 cm soils amended by lime and apatite
2.3 土壤有效态铜镉垂直分布
如图3A所示,表层土壤有效态铜含量最高(4.88 ~60.7 mg/kg),且土壤有效态铜含量随着土层深度的增加逐渐降低。磷灰石和石灰的添加显著降低了0~13 cm土层土壤有效态铜含量,且随着磷灰石和石灰用量的增加而显著降低。与对照相比,M-石灰、H-石灰、M-磷灰石和H-磷灰石处理分别使有效态铜含量降低59.3%、85.1%、69.2% 和92%。与0~13 cm土层变化相似,13~30 cm土层土壤有效态铜含量随着磷灰石和石灰的添加显著降低,但M-石灰(52.6%)、H-石灰(70.4%)、M-磷灰石(68.0%)和 H-磷灰石(72.5%)处理对有效态铜的降低幅度显著降低。30~50 cm土层土壤有效态铜含量最低(1.74~4.9 mg/kg),磷灰石和石灰的添加仅微弱降低了土壤有效态铜含量。
与对照相比,H-石灰和H-磷灰石处理使0~13 cm土层土壤有效态镉含量分别降低 21.3% 和 28.2%。对于13~30 cm土层,仅有H-石灰处理显著降低了土壤有效态Cd含量。与0 ~13 cm土层相同,仅有H-石灰和H-磷灰石处理显著降低30~50 cm土层土壤有效态Cd含量,降幅分别为18.8% 和23.5%。总体上,磷灰石和石灰对土壤有效态镉含量的降低效果显著低于有效态铜,且有效态镉含量在3个土层基本维持在204~322 µg/kg,表明镉在该污染土壤中具有较高的有效性。
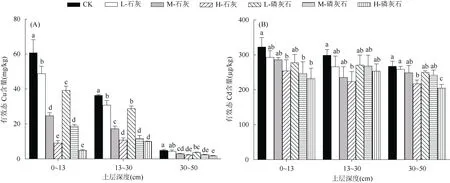
图3 磷灰石和石灰处理0~50 cm土壤有效态铜(A)和镉(B)含量变化Fig. 3 Concentrations of CaCl2 extractable Cu (A) and Cd (B) in 0—50 cm soils amended by lime and apatite
3 讨论
对于大多数碱性条件下低溶解性的重金属元素,提高土壤pH是重金属污染土壤最常用的修复方法[20]。磷灰石和石灰是自然界常见的廉价钝化材料,由于其本身含有大量的碱性物质,有助于土壤pH 的提高,因此在重金属污染土壤修复中应用广泛。如本试验中磷灰石和石灰中CaO的含量分别为135 g/kg 和258 g/kg,由于磷灰石的用量显著高于石灰,导致磷灰石处理土壤pH和全钙含量显著高于石灰处理和对照处理。同时,磷灰石和石灰的添加显著降低了土壤交换性酸和铝,表明这两种材料均有助于降低土壤胶体上吸附的可代换性H+和Al3+。
本研究中磷灰石全磷含量为109 g/kg,因此随着磷灰石用量的增加,表层土壤全磷和有效磷含量显著增加。但石灰本身含有的全磷含量为0.16 g/kg,且添加用量仅为1~4 g/kg,导致土壤全磷含量未与对照表现出显著差异。随着磷灰石和石灰的添加,土壤速效钾含量表现出增加的趋势,这可能是由于改良材料本身含有少量的钾,提高了土壤全钾的含量;同时重金属活性的降低以及黑麦草和金黄狗尾草的生长改变土壤微生物群落结构促进土壤速效钾含量的提高[21]。
对照处理土壤总铜和总镉最高含量均出现在13~30 cm 土层,其次是 0~13 cm 土层,30~50 cm土层含量最低。磷灰石和石灰添加到表层0~13 cm后,没有改变各处理土壤总铜在不同土层的分布,但各处理0~13 cm土层土壤总镉含量最高,其次是13~30 cm土层。早期的研究表明,稳定化修复后施加改良材料的土层土壤重金属总量没有发生显著变化或者略有降低[20,22]。然而,本试验中,与对照土壤相比,钝化剂应用后0~13 cm土层土壤总铜和总镉均随着磷灰石和石灰用量的增加而增加。这一结果背离了本研究最初通过稳定化联合植物提取降低土壤重金属总量的目的[20,23]。首先,本研究试验区域仍然存在大量外源重金属输入,尤其是大气干湿沉降的重金属输入。如陶美娟等[24]研究表明,该地区年均干湿沉降的铜和镉含量达到 1 973 mg/m2和15.2 mg/m2。而前人的研究多是在已经废弃且不存在大量外来重金属污染物输入的地区开展试验[20,23]。外源重金属的输入对每一个小区的影响基本是一致的,不会导致土壤重金属总量的差异。但是磷灰石和石灰的添加后,均提高了土壤对铜和镉的固持(吸附能力提升)能力,降低了地表径流和淋溶作用输出的重金属,使得更多的重金属被阻留在土壤表层[25]。另外,前期的研究也表明,由于植物生物量低,富集的重金属含量有限,导致植物提取输出的重金属总量对土壤重金属总量的影响微弱[26]。而且,尽管磷灰石和石灰材料本身也含有一定量的铜和镉,但其最高用量仅能分别提升0~13 cm土层土壤总铜5 µg/kg和221µg/kg 和总镉含量 3.48 µg/kg 和 27.4 µg/kg (改良剂带入的重金属总量除以0~13 cm表层土壤质量),对土壤重金属总量影响较小。因此,本研究中0~13 cm土层土壤重金属含量的增加归因于改良剂的添加均提高了土壤对铜和镉的吸附固定能力,减少了通过地表径流和淋溶作用输出的重金属,且这部分减少的重金属总量高于植物提取的重金属总量,导致改良后表层土壤重金属总量高于对照处理[25-26]。此外,与13 ~30和30~50 cm土层相比,土壤总铜和总镉含量均随着磷灰石和石灰用量的增加而降低(除30~50 cm土层总镉外),这表明,磷灰石和石灰的应用使重金属很好地被固定在土壤表层,并减少了铜和镉向下层土壤的淋溶。
研究表明在重金属污染土壤修复中,相对于土壤重金属总量,土壤有效态重金属的变化更具有重要意义[27-28]。由于CaCl2提取态重金属与植物具有较好的相关性[27],因此,本研究考察了不同土层0.01 mol/L CaCl2提取有效态铜和镉含量的变化,结果显示,对照处理土壤有效态铜含量在0~13 cm土层最高,30 ~50 cm土层最低;有效态镉含量在0~50 cm土层未表现出显著差异。磷灰石和石灰的添加均未改变土壤有效态铜和镉在3个土层的分布规律,但是与每一土层的对照处理相比,磷灰石和石灰处理土壤有效态铜和镉含量均呈现降低趋势。Bidar等[23]研究也表明,稳定化联合植物提取修复后尽管各土层重金属总量差异较小,但是飞灰应用后均降低了5~10、10~15和15~20 cm土层土壤0.01 mol/L CaCl2提取态镉、铅和锌的含量。同样,Madejón等[20]也报道,生物堆肥和风化褐煤处理后均降低了土壤CaCl2提取态铜、镉和锌在0~30 cm土层的含量。磷灰石和石灰均通过提高土壤pH来降低0~13 cm土层土壤铜和镉的有效态含量。这主要是因为土壤 pH的提升有助于提高土壤有机质、黏土矿物和铁锰氧化物等胶体所带的负电荷,增加土壤对重金属的吸附能力[29]。其次,石灰添加土壤后主要通过与铜和镉生成 CuCO3、CdCO3或者Cu(OH)2、Cd(OH)2沉淀以及离子交换方式降低铜和镉的有效态含量[30-32]。对于磷灰石,主要通过离子交换、表面络合和共沉淀等与重金属生成磷酸盐沉淀或络合物的方式降低土壤有效态铜和镉的有效态含量[33-34]。
相较 0~13 cm 土层,13~30 cm 和 30~50 cm土层有效态铜和镉含量的下降可能是磷灰石和石灰中碱性物质的向下淋溶,有助于提高土壤pH(磷灰石和石灰处理13~50 cm土层土壤pH均高于对照处理),降低了 CaCl2的提取效率[20]。如本研究中,不同土层土壤pH与有效态铜和镉呈极显著的负相关关系,相关系数分别为-0.444(P<0.01)和-0.409(P<0.01),表明土壤pH对重金属有效态活性降低有重要影响。Basta等[35]也表明,土壤pH是影响重金属在土壤中吸附、沉淀、溶解和有效性的重要因子。同时,本研究中土壤有效态铜和镉分别与总铜(相关系数为0.472,P<0.01)和总镉(相关系数为 0.379,P<0.05)呈显著正相关关系。可见,对于不同土层土壤来说,除了土壤pH,重金属总量的差异也是影响重金属有效态含量的因素之一。
大量的研究表明,不同土壤矿物组成对重金属的吸附固定能力差异显著[36-38],但在本研究中,除0 ~13 cm土层土壤矿物存在一定差异外(主要是23.2 g/kg磷灰石处理土壤中出现少量氟磷灰石和白云石),13~50 cm 土层各处理间土壤矿物没有明显差异(XRD数据未列出)。同样,Huggett和 Cuadros[39]研究也发现在0~70 cm深度的湖泊沉积物中土壤矿物的组成基本没有差异,超过 90 cm后才呈现微弱差异。土壤中活性硅、非晶形铁氧化物和含锰氧化物含量在不同土层存在显著差异,且其与土壤中重金属的富集具有较好的相关性[40-41]。因此,本研究中下层土壤中活性硅、无定形铁氧化物和含锰氧化物含量差异也可能是导致土壤有效态铜和镉含量差异的原因之一。尽管如此,后续的研究有必要进一步分析不同土层土壤活性硅、无定形铁氧化物和含锰氧化物含量以及土壤胶体含量,以明确不同土层重金属活性差异的主要机制。
4 结论
1) 磷灰石和石灰的添加降低了0~13 cm土层土壤交换性酸和交换性铝,提高了土壤钙的总量,且磷灰石处理显著增加了土壤总磷和有效磷含量。
2) 磷灰石和石灰应用提高了不同土层土壤pH,且随着磷灰石和石灰用量的提高,逐渐增加了表层0~13 cm土壤总铜和镉含量,但减少了土壤铜和镉向13~50 cm土层淋溶。
3) 磷灰石和石灰的应用均降低了0~50 cm土层土壤中铜和镉的有效态含量,且不同土层土壤pH和铜镉总量是影响铜镉有效态含量的主要因素。
[1] Bolan N, Kunhikrishnan A, Thangarajan R, et al.Remediation of heavy metal (loid) s contaminated soils-to mobilize or to immobilize?[J]. Journal of Hazardous Materials, 2014, 266: 141-166
[2] Huang G, Su X, Rizwan M S, et al. Chemical immobilization of Pb, Cu, and Cd by phosphate materials and calcium carbonate in contaminated soils[J].Environmental Science and Pollution Research, 2016,23(16): 16845-16856
[3] Tica D, Udovic M, Lestan D. Immobilization of potentially toxic metals using different soil amendments[J].Chemosphere, 2011, 85(4): 577-583
[4] Adriano D C, Wenzel W W, Vangronsveld J, et al. Role of assisted natural remediation in environmental cleanup[J].Geoderma, 2004, 122(2): 121-142
[5] Brown S, Sprenger M, Maxemchuk A, et al. Ecosystem function in alluvial tailings after biosolids and lime addition[J]. Journal of Environmental Quality, 2005, 34(1):139-148
[6] Park J H, Lee S J, Lee M E, et al. Comparison of heavy metal immobilization in contaminated soils amended with peat moss and peat moss-derived biochar[J]. Environmental Science: Processes & Impacts, 2016, 18(4): 514-520
[7] Matusik J, Bajda T, Manecki M. Immobilization of aqueous cadmium by addition of phosphates[J]. Journal of Hazardous Materials, 2008, 152(3): 1332-1339
[8] Alvarenga P, Gonçalves A P, Fernandes R M, et al.Organic residues as immobilizing agents in aided phytostabilization:(I) Effects on soil chemical characterristics[J]. Chemosphere, 2009, 74(10): 1292-1300
[9] Alvarenga P, Palma P, Gonçalves A P, et al. Organic residues as immobilizing agents in aided phytostabilization:(II) Effects on soil biochemical and ecotoxicological characteristics[J]. Chemosphere, 2009, 74(10):1301-1308
[10] Garau G, Castaldi P, Santona L, et al. Influence of red mud,zeolite and lime on heavy metal immobilization, culturable heterotrophic microbial populations and enzyme activities in a contaminated soil[J]. Geoderma, 2007, 142(1): 47-57
[11] Liang X, Han J, Xu Y, et al. In situ field-scale remediation of Cd polluted paddy soil using sepiolite and palygorskite[J]. Geoderma, 2014, 235: 9-18
[12] Madejón P, Pérez-de-Mora A, Burgos P, et al. Do amended,polluted soils require re-treatment for sustainable risk reduction?—Evidence from field experiments[J]. Geoderma, 2010, 159(1): 174-181
[13] Pérez-de-Mora A, Burgos P, Cabrera F, et al. “In situ”amendments and revegetation reduce trace element leaching in a contaminated soil[J]. Water, air, and soil pollution, 2007, 185(1): 209-222
[14] Hamon R E, McLaughlin M J, Cozens G. Mechanisms of attenuation of metal availability in in situ remediation treatments[J]. Environmental Science & Technology, 2002,36(18): 3991-3996
[15] Basta N T, McGowen S L. Evaluation of chemical immobilization treatments for reducing heavy metal transport in a smelter-contaminated soil[J]. Environmental pollution, 2004, 127(1): 73-82
[16] 周静, 崔红标. 规模化治理耕地土壤重金属污染技术工程与展望—以江铜贵冶周边区域九牛岗土壤修复示范工程为例[J]. 中国科学院院刊, 2014, 29(3): 336-343
[17] 周静, 崔红标, 梁家妮, 等. 重金属污染土壤修复技术的选择和面临的问题——以江铜贵冶九牛岗土壤修复示范工程项目为例[J]. 土壤, 2015, 47(2): 283-288
[18] 钱婷婷. 磷在固体废物热处理过程中的迁移转化及再利用[D]. 合肥: 中国科学技术大学, 2014
[19] 鲁如坤. 土壤农业化学分析法[M]. 北京: 中国农业科技出版社, l999
[20] Madejón E, Madejón P, Burgos P, et al. Trace elements, pH and organic matter evolution in contaminated soils under assisted natural remediation: A 4-year field study[J]. Journal of Hazardous Materials, 2009, 162(2): 931-938
[21] Lee C H, Ha B Y, Lee Y B, et al. Effect of alkalized phosphogypsum on soil chemical and biological properties[J]. Communications in Soil Science and Plant Analysis, 2009, 40(13/14): 2072-2086
[22] Madejón P, Pérez-de-Mora A, Burgos P, et al. Do amended,polluted soils require re-treatment for sustainable risk reduction?—Evidence from field experiments[J]. Geoderma, 2010, 159(1): 174-181
[23] Bidar G, Waterlot C, Verdin A, et al. Sustainability of an in situ aided phytostabilisation on highly contaminated soils using fly ashes: Effects on the vertical distribution of physicochemical parameters and trace elements[J]. Journal of Environmental Management, 2016, 171: 204-216
[24] 陶美娟, 周静, 梁家妮, 等. 大型铜冶炼厂周边农田区大气重金属沉降特征研究[J]. 农业环境科学学报, 2014,33(7): 1328-1334
[25] Cui H, Zhou J, Si Y, et al. Immobilization of Cu and Cd in a contaminated soil: one-and four-year field effects[J].Journal of Soils and Sediments, 2014, 14(8): 1397-1406
[26] Cui H, Fan Y, Xu L, et al. Sustainability of in situ remediation of Cu- and Cd-contaminated soils with onetime application of amendments in Guixi, China[J]. Journal of Soils and Sediments, 2016, 16(5): 1498-1508
[27] Meers E, Unamuno V R, Du Laing G, et al. Zn in the soil solution of unpolluted and polluted soils as affected by soil characteristics[J]. Geoderma, 2006, 136(1): 107-119
[28] Adriano D C, Trace Elements in Terrestrial Environments:Biogeochemistry, Bioavailability and Risks of Metals[M].2ed. New York: Springer, 2001
[29] Gray C W, Mclaren R G, Roberts A H C, et al. Sorption and desorption of cadmium from some New Zealand soils:effect of pH and contact time [J]. Australian Journal of Soil Research, 1998, 36(2): 199-216
[30] Bolan N S, Adriano D C, Mani P A, et al. Immobilization and phytoavailability of cadmium in variable charge soils.II. Effect of lime addition [J]. Plant and Soil, 2003, 251(2):187-198.
[31] Prasad M N V. Cadmium toxicity and tolerance in vascular plants[J]. Environmental and Experimental Botany, 1995,35(4): 525-545
[32] Gray C W, Dunham S J, Dennis P G, et al. Field evaluation of in situ remediation of a heavy metal contaminated soil using lime and red-mud [J]. Environmental Pollution, 2006,142(3): 530-539
[33] Cao X D, Ma L Q, Rhue D R, et al. Mechanisms of lead,copper, and zinc retention by phosphate rock[J]. Environmental Pollution, 2004, 131(3): 435-444
[34] Dong A, Ye X, Li H, et al. Micro/nanostructured hydroxyapatite structurally enhances the immobilization for Cu and Cd in contaminated soil[J]. Journal of Soils and Sediments, 2016, 16(8): 2030-2040
[35] Basta N T, Ryan J A, Chaney R L. Trace element chemistry in residual-treated soil: key concepts and metal bioavailability[J]. Journal of Environmental Quality, 2005, 34(1):49-63
[36] Bhattacharyya K G, Gupta S S. Adsorption of a few heavy metals on natural and modified kaolinite and montmorillonite: A review[J]. Advances in colloid and interface science, 2008, 140(2): 114-131
[37] Kocaoba S. Adsorption of Cd (II), Cr (III) and Mn (II) on natural sepiolite[J]. Desalination, 2009, 244(1/2/3): 24-30.
[38] Motsi T, Rowson N A, Simmons M J H. Adsorption of heavy metals from acid mine drainage by natural zeolite[J].International Journal of Mineral Processing, 2009, 92(1):42-48
[39] Huggett J M, Cuadros J. Glauconite formation in lacustrine/palaeosol sediments, Isle of Wight (Hampshire Basin), UK[J]. Clay Minerals, 2010, 45(1): 35-49
[40] Fujii K, Ikeda S, Akama A, et al. Vertical migration of radiocesium and clay mineral composition in five forest soils contaminated by the Fukushima nuclear accident[J].Soil science and plant nutrition, 2014, 60(6): 751-764
[41] Li Y, Zhang H, Chen X, et al. Distribution of heavy metals in soils of the Yellow River Delta: concentrations in different soil horizons and source identification[J]. Journal of Soils and Sediments, 2014, 14(6): 1158-1168

