HPLC法同时测定复方乳酸钠葡萄糖注射液中乳酸钠和葡萄糖的含量
周朝东,黄哲甦
(天津市药品检验研究院,天津 300070)
复方乳酸钠葡萄糖注射液为乳酸钠、氯化钠、氯化钾、二水氯化钙与无水葡萄糖的灭菌水溶液[1,2],可调节体液容量、渗透压,补充钠、钾、钙及氯离子,并供给热量。当体内循环血液量及组织液减少时,可作为组织液的补充调整剂,对电解质紊乱及酸中毒有纠正作用[3]。目前现行版《中国药典》收载的复方乳酸钠葡萄糖注射液中乳酸钠的含量测定方法是用阳离子交换树脂结合滴定的方法测定,葡萄糖含量的测定方法则是采用旋光法[2]。由于制备阳离子交换树脂比较费时费力,且离子交换过程比较长,同时乳酸钠与葡萄糖的测定是分开进行的,因此该方法特别不适用于大批量样品的检验。笔者通过查阅文献[1,4,5]发现,目前有报道用HPLC法测定乳酸钠的含量,均使用C18色谱柱,紫外检测器,检测波长为210 nm。同时也有文献[6]报道利用离子交换色谱柱结合示差折光检测器同时测定腹膜透析液(乳酸盐)中葡萄糖和乳酸钠的含量。笔者通过实验优化,建立了用离子排阻色谱柱结合紫外检测器同时测定乳酸钠和葡萄糖含量的高效液相色谱法,且通过了方法学验证,由于该方法简单易行,可以大大降低工作量,同时缩短分析时间,特别适用于大批量样品的检验。
1 仪器与试药
1.1仪器 Waters e2695型高效液相色谱仪,2489 UV/Vis检测器,Empower 3色谱工作站,METTLER XS205型十万分之一电子天平。
1.2试药 乳酸钠对照品(批号BCBS5446V,纯度≥99.0%),葡萄糖对照品(批号SLBF3437V,纯度≥99.5%),均购自sigma公司;3批复方乳酸钠葡萄糖注射液为中国大冢制药有限公司生产,批号分别为FNTRL-1、 FNTRL-2和 FNTRL-3;氯化钠为天津市华东试剂厂生产;氯化钾和二水氯化钙为天津市赢达稀贵化学试剂厂生产;水为纯化水。
2 方法与结果
2.1色谱条件 色谱柱为Bio-Rad Aminex HPX-87H ion exclusion column(300 mm×7.8 mm,9 μm),流动相为0.025 mol/L硫酸溶液,柱温为40 ℃,流速为1.0 ml/min,进样体积为20 μl,紫外检测器,检测波长为195 nm。理论板数乳酸钠为10 707,葡萄糖为6 809,均不低于2 000。葡萄糖与氯离子的分离度为5.84,葡萄糖与乳酸钠的分离度为8.66,均大于1.5。
2.2溶液的制备
2.2.1对照品溶液的制备 精密称取乳酸钠对照品约0.31 g和葡萄糖对照品约5.0 g置同一100 ml量瓶中,用水溶解并定容至刻度,摇匀,作为对照品贮备液。精密量取该贮备液5 ml置10 ml量瓶中,用水定容至刻度,摇匀,即得。此时乳酸钠对照品浓度约为1.55 mg/ml,葡萄糖对照品浓度约为25 mg/ml,平行制备2份对照品。
2.2.2供试品溶液的制备 精密量取复方乳酸钠葡萄糖注射液5 ml置10 ml量瓶中,用水定容至刻度,摇匀,即得。
2.2.3阴性对照溶液的制备 按复方乳酸钠葡萄糖注射液的处方称取除了乳酸钠和葡萄糖之外的成分配制成溶液,然后按“2.2.2”项下供试品溶液的制备方法制备成阴性对照溶液。
2.3专属性试验 取对照品溶液、供试品溶液和阴性对照溶液,按照“2.1”项下色谱条件分别进样,检查阴性对照溶液在乳酸钠和葡萄糖色谱峰相应的位置上有无杂质色谱峰的干扰,结果表明专属性较强,见图1。
2.4线性关系考查 分别精密量取“2.2.1”项下对照品贮备液2.5、4、5、6、7.5和10 ml置10 ml量瓶中,加水定容至刻度,摇匀,制成系列浓度的供试品溶液,分别精密吸取20 μl,注入液相色谱仪,按“2.1”项下色谱条件分析,测定各自峰面积,以浓度为横坐标,以峰面积为纵坐标,计算回归方程及相关系数。乳酸钠线性方程为Y=510 986X-7 701.4(r=0.999 9,n=6),其浓度在0.760~3.041 mg/ml内,浓度与峰面积呈良好线性关系。葡萄糖线性方程为Y=75 172X+93 510(r=0.999 9,n=6),其浓度在12.442~49.770 mg/ml内,浓度与峰面积呈良好线性关系。
2.5精密度试验 取“2.2.1”项下对照品溶液连续进样6次,按“2.1”项下的色谱条件测定,记录峰面积,乳酸钠峰面积的RSD为0.18%,葡萄糖峰面积的RSD为0.10%,表明仪器精密性良好。
2.6稳定性试验 取“2.2.1”项下对照品溶液1份,分别于0、4、8、12和24 h进样,按“2.1”项下的色谱条件测定,考查溶液的稳定性。结果乳酸钠峰面积的RSD为0.45%,葡萄糖峰面积的RSD为0.86%,表明溶液在24 h内稳定。
2.7回收率试验 按复方乳酸钠葡萄糖注射液处方称取氯化钠375 mg、氯化钾18.75 mg和二水氯化钙12.5 mg置25 ml量瓶中,用水溶解并定容至刻度,摇匀,作为阴性对照溶液贮备液。然后分别精密量取阴性对照溶液贮备液2 ml置10 ml量瓶中,同时分别加入“2.2.1”项下对照品贮备液4、5和6 ml,并用水定容至刻度,摇匀,制成乳酸钠和葡萄糖浓度分别相当于供试品溶液浓度80%、100%和120%的溶液,每个浓度平行做3份,共9份,按“2.1”项下的色谱条件测定,并计算回收率、平均回收率和相对标准偏差。结果乳酸钠平均回收率是100.3%,RSD是0.45%;葡萄糖平均回收率是100.2%,RSD是0.33%。回收率均在98%~101%范围内,RSD均不大于2%,结果见表1和表2。
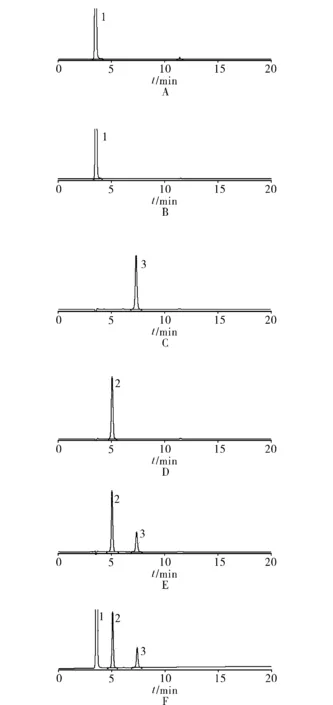
1.氯离子 2.葡萄糖 3.乳酸钠
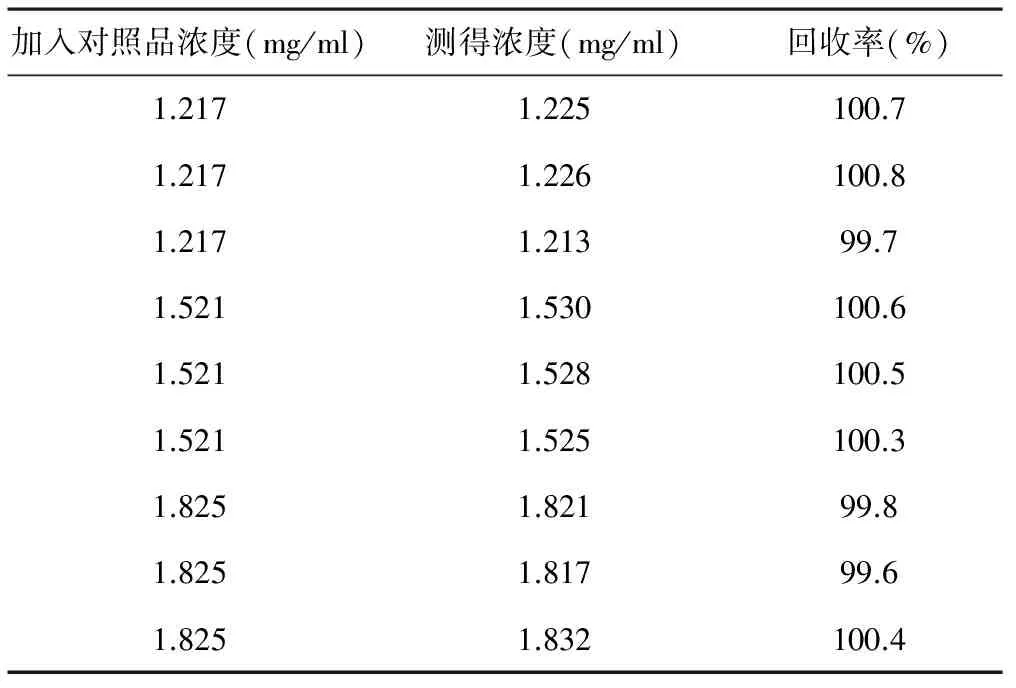
加入对照品浓度(mg/ml)测得浓度(mg/ml)回收率(%)1.2171.225100.71.2171.226100.81.2171.21399.71.5211.530100.61.5211.528100.51.5211.525100.31.8251.82199.81.8251.81799.61.8251.832100.4
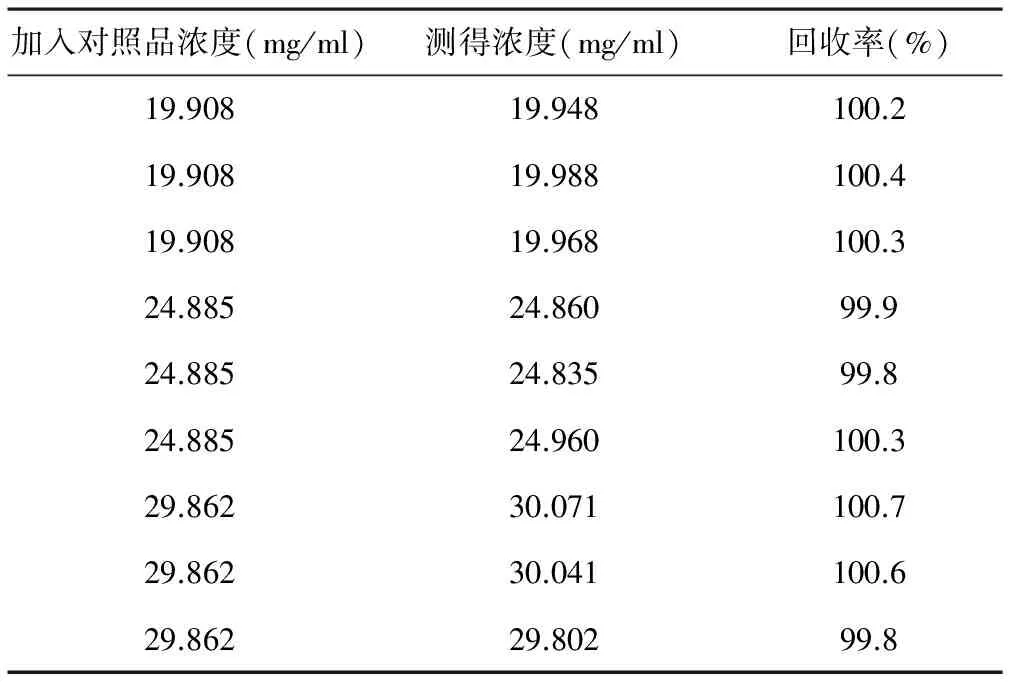
表2 葡萄糖回收率测定结果(n=9)
2.8检出限和定量限试验 取对照品溶液进行逐级稀释,并按“2.1”项下色谱条件进样分析,以信噪比S/N=3作为最低检出限,以信噪比S/N=10作为定量限。乳酸钠最低检出限为55.3 ng,定量限为184 ng;葡萄糖最低检出限为330 ng,定量限为1 μg。
2.9两种方法测定结果 《中国药典》测定方法和HPLC方法测得的结果非常接近,无明显差异,证明建立的该方法可用于复方乳酸钠葡萄糖注射液中乳酸钠和葡萄糖含量的同时测定。见表3。
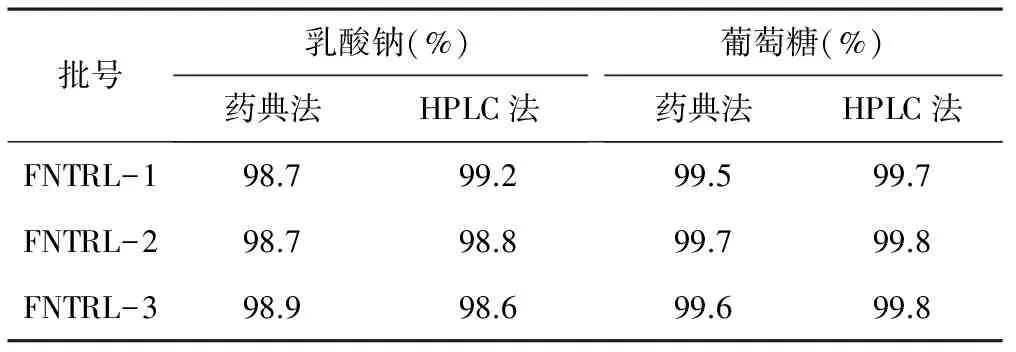
表3 《中国药典》法和HPLC法测定结果
3 讨论
目前,乳酸钠的含量测定方法有阳离子交换树脂法(《中国药典》法)[2]、HPLC法[4-6]、吸收比值法[3]和改进的氧化还原法[7]。葡萄糖含量测定方法有旋光法[2]、HPLC法[8-11]和碘量法[12]。现行版《中国药典》二部中,复方乳酸钠葡萄糖注射液中乳酸钠用阳离子交换树脂法结合滴定法进行测定,葡萄糖用旋光法进行测定。这两种物质的含量测定分别采用不同的方法,比较耗时,尤其乳酸钠测定,制备阳离子交换树脂以及离子交换过程比较耗时耗力,特别不适用于大批量样品的检验。在试验条件摸索过程中,笔者经过扫描乳酸钠溶液和葡萄糖溶液,发现乳酸钠最大吸收波长在198.5nm,葡萄糖最大吸收波长则在紫外吸收波长末端190nm,为了能够兼顾两种物质的测定,故选择195nm作为检测波长,而且文中所用的色谱柱对二者分离效果好,同时各自理论板数比较高,且色谱峰无拖尾。总而言之,笔者建立的高效液相色谱法经过了方法学验证,同时样品测定结果与法定方法(《中国药典》收载方法)经过比较,没有显著性差异。因此,该方法可以为未来《中国药典》标准提高提供参考。
1 徐雄良,张洪宇,刘革新,等. 对《中国药典》中复方乳酸钠葡萄糖注射液乳酸钠含量测定方法的探讨[J]. 中国药学杂志,2015,50(23):2081-2085
2 中国药典[S].二部.2015:805-806
3 王连兰,冯雅琳,郭小红.复方乳酸钠葡萄糖注射液乳酸钠含量测定[J]. 中国医药科学,2013,3(1):113-114
4 韩叶梅,彭淑贤. HPLC法测定复方乳酸钠葡萄糖注射液中乳酸钠含量[J]. 中国处方药,2016,14(6):33-34
5 张卫东. 高效液相色谱法测定复方电解质葡萄糖MG3注射液中乳酸钠含量[J]. 中国医院药学杂志,2011,31(24):2063-2064
6 梁伟娜,江雪欣.腹膜透析液(乳酸盐)中葡萄糖和乳酸钠的含量测定方法改进[J]. 中国药事,2016,30(11):1107-1111
7 马慧萍,贾正平,葛欣,等.复方乳酸钠注射液中乳酸钠含量测定方法的比较研究[J]. 西北国防医学杂志,2007,28(3):189-191
8 周娜.HPLC测定转化糖注射液中果糖、葡萄糖含量[J]. 中国现代应用药学,2011,28(13):1357-1359
9 董玮,陈加罡,陆斌.HPLC-RID法测定转化糖电解质注射液中果糖和葡萄糖含量[J]. 中国药师,2014,17(11):1883-1885
10 葛姗姗,施思,郭鑫艳,等.HPLC-ELSD法测定红腺忍冬叶抗氧化有效部位中果糖和葡萄糖的含量[J]. 中华中医药学刊,2014,32(4):882-885
11 张云楚,张新规.高效液相色谱-示差折光检测法同时测定维生素C葡萄糖注射液中维生素C与葡萄糖的含量[J]. 中国药品标准,2008,9(6):421-424
12 闻金玲.碘量法测定葡萄糖注射液中葡萄糖的含量[J]. 中国现代药物应用,2017,14(11):197-198

