骨水泥固定融合治疗腰椎退行性疾病合并骨质疏松效果研究
吴浩 何兴 王凯
(1首都医科大学宣武医院神经外科,北京 100053; 2武警总医院神经肿瘤外科,北京 100039)
骨质疏松症是以骨量减少、骨质量受损及骨强度降低,导致骨脆性增加、易发生骨折为特征的全身性骨病。老年男性和绝经后女性是骨质疏松的高发人群[1]。许多研究表明,骨质疏松症与脊柱骨质疏松性骨折、退行性脊柱畸形(包括脊柱后凸,脊柱侧弯,脊柱旋转畸形)、腰椎间盘退变突出、椎管狭窄、腰椎不稳滑脱及骨质增生退变、退行性颈椎病的发病均有密切的关系[2]。腰椎退行性疾病的手术方式较多,多采用椎弓根螺钉等固定,以便获得坚强固定效果,从而有效维持脊柱的稳定性,但骨质疏松患者脊柱手术中螺钉的固定强度显著降低,容易发生继发骨折、融合、固定失败等并发症[3-7],进一步影响了术后临床症状的改善。2013年1月至2015年2月,我们应用椎弓根螺钉固定治疗合并骨质疏松症的腰椎退行性疾病患者64例,并对应用骨水泥联合椎弓根螺钉固定效果、临床疗效及安全性进行了观察,现报告如下。
对象与方法
一、临床资料
本组64例,所有患者均诊断为骨质疏松伴腰椎退行性疾病,均为首都医科大学宣武医院的住院患者,其中男27例,女37例,年龄45~93岁,平均年龄(66.34±21.21)岁,平均骨密度绝对值62.55±14.37。腰椎失稳患者17例,腰椎管狭窄症22例,腰椎间盘突出症25例,所有患者均为3节段以下腰椎受累,其中单节段受累者39例,多阶段受累患者25例。将患者随机分为实验组30例和对照组34例。随机分组遵循以下原则:①医生和患者不能事先知道或决定患者将分配到哪一组接受治疗;②医生和患者都不能从一个患者已经进入的组别推测出下一个患者将分配到哪一组。随机组别的产生应用随机数字表法进行。实验组采用椎弓根螺钉加骨水泥强化治疗,对照组采用单纯椎弓根螺钉固定治疗。
二、入选标准
1.纳入标准:①症状:所有患者均出现腰部疼痛,行走功能明显受限等症状。②符合国家2011年版骨质疏松诊疗指南中推荐的参照世界卫生组织(WHO)诊断标准,并采用定量CT法测量骨密度,患者骨密度绝对值小于80 mg/cm3即诊断为骨质疏松。③对于腰椎滑脱患者均为退变型腰椎滑脱。④对于腰椎管狭窄的患者,测量椎管的矢状径<10 mm,侧隐窝的前后径均在3 mm以下。⑤X线显示腰椎退行性变,骨赘形成,腰椎生理前突减少或反常。⑥CT显示多个椎间盘膨出,关节突关节增生,关节突内聚。⑦腰椎MRI:提示椎间盘膨出或突出。
2.排除标准:①不符合骨质疏松诊断的患者;②仅出现腰部或下肢的轻微的症状,没有出现行走功能受限等临床表现,基本的生活受影响程度较小的患者;③单纯腰椎间盘突出症,或腰椎椎体真性滑脱及退行性滑脱>Ⅱ度以上患者;④椎管狭窄腰椎矢状径>10 mm,侧隐窝的前后径>3 mm;⑤合并有椎体骨折、严重腰椎侧弯(Cobb角>30°)以及病理性骨质疏松的患者;⑥4个阶段以上内固定患者;⑦不能坚持随诊复查者。
三、方法
1.手术方法:所有患者均采用全身麻醉,取俯卧位,C臂辅助下置入空心椎弓根螺钉,调制骨水泥,透视下注入骨水泥,每枚空心椎弓根螺钉注入骨水泥2~3 mL,常规行腰椎椎体间融合术置入融合器。腰椎中央椎管狭窄者,行开窗椎管减压术,切除椎板黄韧带及椎间盘,安装双侧纵形连接棒及横向连接,常规冲洗缝合切口,必要时术区放置引流管。术后24 h应用抗生素预防感染。术后根据患者恢复情况,指导其早期下地行走。嘱患者出院后常规应用抗骨质疏松药物。
2.疗效及安全性评价方法:分别于术前及术后1 w、1月、6个月、2年,采用视觉模拟量表(visual analogue scale, VAS)评定疼痛情况,采用日本骨科协会(Japanese Orthopaedic Association, JOA)腰痛疾患疗效评定标准评定综合疗效。术后进行X线等影像检查,观察椎弓根螺钉位置、骨水泥分布及腰椎融合等情况,随访观察并发症发生情况。
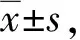
结 果
一、患者手术前后VAS评分比较
手术前、术后1 d及术后第1周两组患者VAS评分差异无统计学意义(P>0.05),实验组患者术后1月、6月及2年VAS评分较对照组患者显著降低,差异均具有统计学意义(P<0.05, 表1)。
二、患者手术前后JOA评分比较
手术前二组患者JOA评分差异无统计学意义(P>0.05),实验组患者术后术后1个月、术后半年及术后2年JOA功能评分较对照组患者显著提高,差异均具有统计学意义(P<0.05, 表2)。
三、患者术后融合及主要术后并发症比较
所有患者随访2年,实验组较对照组相比融合率显著提高,术后主要并发症包括:融合不良、椎管感染、螺钉松动或脱出、腰椎失稳、融合器移位、融合器陷入椎体及遗留神经症状,组间并发症比较无显著性差异(P>0.05, 表3)。
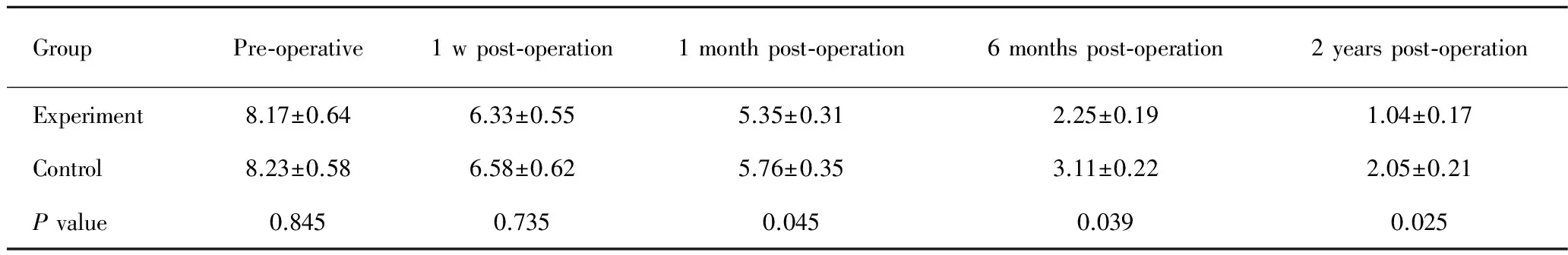
GroupPre-operative1wpost-operation1monthpost-operation6monthspost-operation2yearspost-operation Experiment8.17±0.646.33±0.555.35±0.312.25±0.191.04±0.17 Control8.23±0.586.58±0.625.76±0.353.11±0.222.05±0.21 Pvalue0.8450.7350.0450.0390.025
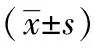
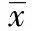
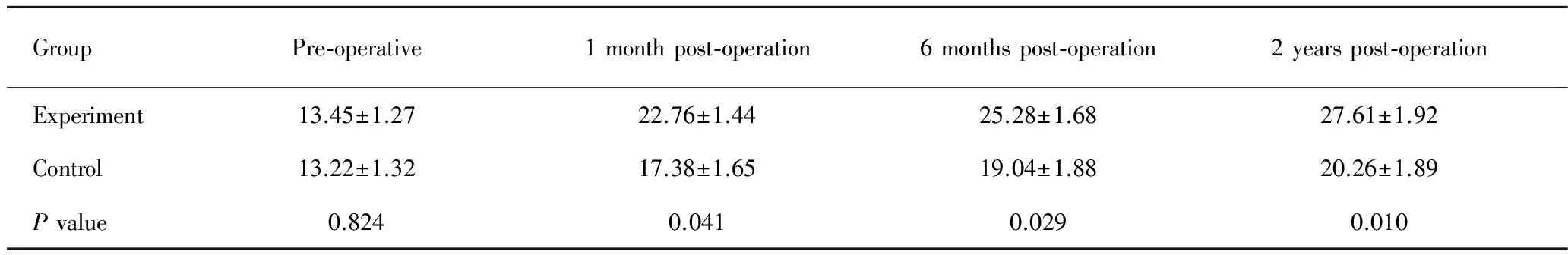
GroupPre-operative1monthpost-operation6monthspost-operation2yearspost-operation Experiment13.45±1.2722.76±1.4425.28±1.6827.61±1.92 Control13.22±1.3217.38±1.6519.04±1.8820.26±1.89 Pvalue0.8240.0410.0290.010
表3 两组患者术后椎体融合情况及术后并发症比较(n)
Tab 3 Comparison of vertebral fusion and complications after operation (n)
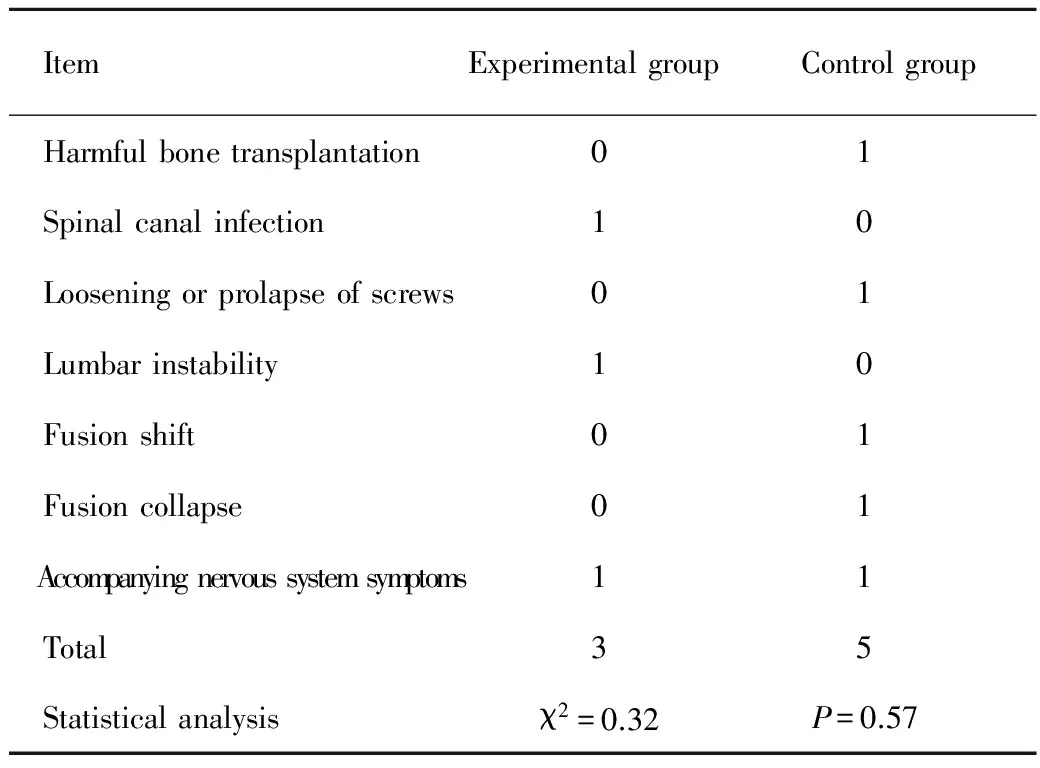
ItemExperimentalgroupControlgroup Harmfulbonetransplantation01 Spinalcanalinfection10 Looseningorprolapseofscrews01 Lumbarinstability10 Fusionshift01 Fusioncollapse01 Accompanyingnervoussystemsymptoms11 Total35 Statisticalanalysisχ2=0.32P=0.57
讨 论
许多文献表明,骨质疏松症与脊柱骨质疏松性骨折、退行性脊柱畸形(包括脊柱后凸,脊柱侧弯,脊柱旋转畸形)、腰椎间盘退变突出、椎管狭窄、腰椎不稳滑脱及骨质增生退变、退行性颈椎病的发病均有密切的关系[2]。而且,许多研究已经证实,在脊柱固定手术中固定螺钉的拉力、扭力矩与患者的骨密度值呈正比,骨质疏松患者螺钉的固定强度会显著降低,容易发生继发骨折、固定失败等并发症[3-7]。在骨质疏松患者固定融合手术中应用骨水泥强化能起到优良的生物力学作用,显著增强固定系统与脊柱的稳定性,本研究显示患者在骨水泥强化治疗术后1个月、术后半年及术后2年JOA评分均高于单纯固定融合治疗的患者,VAS评分亦是如此,提示:骨水泥强化固定椎间融合术治疗腰椎退行性疾病不但减少对患者创伤,促进患者术后功能的恢复、改善临床症状,还能够显著降低患者术后的疼痛感。
文献报道,骨质疏松患者脊柱固定失败在术后早(<3个月)晚期(≥3个月)均可发生[8]。脊柱后路植入物融合失败的可能原因为骨质疏松导致的固定螺钉、融合器的松动和脱落、塌陷等[9-11]。通过向椎弓根内注入骨水泥,使得内固定螺钉得以得到牢固的锚着点,同时向骨质疏松的压缩骨折椎体内灌注骨水泥,可有效地恢复病变椎体的生物力学性能,并在一定程度上恢复病变椎体的高度,预防术后椎体塌陷,有效地增强骨折椎体的强度,从而能够显著降低患者手术治疗后再次发生椎体骨折的可能性。Choma等[12]在体外骨质疏松椎体实验中对实心螺钉、PMMA强化实心螺钉、PMMA强化部分空心侧孔螺钉(Pfens)、PMMA强化全部空心侧孔螺钉(Ffens)的最大轴向拔出力及不同黏度PMMA强化Pfens进行比较,结果Pfens组轴向拔出力最大。Kebaish等[13]的实验表明在近端固定椎体和近端临近椎体中应用骨水泥进行椎体成形,能够显著减少骨折的发生。在本组研究中对照组患者术后存在螺钉松动或脱出融合器移位、融合器陷入椎体等并发症的发生,但是总体并发症统计组间并无显著差异,分析原因可能与随访时间较短,患者样本量较少有关。但本研究提示在骨质疏松患者应用骨水泥强化治疗存在减少并发症的发生的趋势。Schrieber等[14]的一项回顾性分析表明,骨质疏松会对脊髓融合手术术后椎体融合率产生显著的影响,而且骨质疏松患者腰椎融合术后CAGE的塌陷率也显著增高[15]。通过对本组患者两年的随访发现对照组患者有融合不良的病例发生,提示骨质疏松患者术后需密切观察椎体融合情况,必要时需进行二次翻修手术。另外骨质疏松患者脊柱固定手术后容易并发近端交界性后凸(proximal junctional kyphosis, PJK)和近端交界性失败(proximal junctional failure, PJF),文献报道PJK在成人骨质疏松脊柱矫形术后发生率约为39%,患者年龄较大且术前存在矢状不平衡者,术后PJF的发生率可高达38%,而且其中有近1/3的患者需要进行二次翻修手术[16]。但本组研究中实验组和对照组患者均无PJK和PJF的发生,可能与患者随访时间较短有关,有待进一步随访观察。
综上所述,在骨质疏松伴腰椎退行性变的患者应用骨水泥强化固定融合治,能够显著缓解术后患者疼痛、改善临床症状、增加增加螺钉固定的强度,有减少术后并发症发生的趋势,是一项值得推广的手术方案。
1NIH. Consensus development panel on osteoporosis prevention, diagnosis, and therapy [J]. JAMA, 2001, 285(6): 785-795.
2陈戈, 段洪, 卞鸿燕, 等. 脊柱退行性疾病的骨质疏松影响分析 [J]. 中国骨质疏松杂志, 2014, 20(7): 766-770.
3ZINDRICK M R, WILTSE L L, WIDELL E H, et al. A biomechanical study of intrapeduncular screw ixation in the lumbosacral spine [J]. Clin Orthop Relat Res, 1986, 203: 99-112.
4WITTENBERG R H, SHEA M, SWARTZ D E, et al. Importance of bone mineral density in instrumented spine fusions [J]. Spine (Phila Pa 1976), 1991, 16(6): 647-652.
5HALVORSON T L, KELLEY L A, THOMAS K A, et al. Effects of bone mineral density on pedicle screw fixation [J]. Spine (Phila Pa 1976), 1994, 19(21): 2415-2420.
6OKUYAMA K, SATO K, ABE E, et al. Stability of transpedicle screwing for the osteoporotic spine. An in vitro study of the mechanical stability [J]. Spine (Phila Pa 1976), 1993, 18(15): 2240-2245.
7PAXINOS O, TSITSOPOULOS P P, ZINDRICK M R, et al. Evaluation of pullout strength and failure mechanism of posterior instrumentation in normal and osteopenic thoracic vertebrae [J]. J Neurosurg Spine, 2010, 13(13): 469-476.
8PONNUSAMY K E, IYER S, GUPTA G, et al. Instrumentation of the osteoporotic spine: biomechanical and clinical considerations [J]. Spine J, 2011, 11(1): 54-63.
9COE J D, WARDEN K E, HERZIG M A, et al. Influence of bone mineral density on the fixation of thoracolumbar implants. A comparative study of transpedicular screws, laminar hooks, and spinous process wires [J]. Spine (Phila Pa 1976), 1990, 15(9): 902-907.
10GILBERT S G, JOHNS P C, CHOW D C, et al. Relation of vertebral bone screw axial pullout strength to quantitative computed tomographic trabecular bone mineral content [J]. J Spinal Disord, 1993, 6(6): 513-521.
11HITCHON P W, BRENTON M D, COPPES J K, et al. Factors affecting the pullout strength of self-drilling and self-tapping anterior cervical screws [J]. Spine (Phila Pa 1976), 2003, 28(1): 9-13.
12CHOMA T J, PFEIFFER F M, SWOPE R W, et al. Pedicle screw design and cement augmentation in osteoporotic vertebrae [J]. Spine, 2012, 37(26): 1628-1632.
13KEBAISH K M, MARTIN C T, O'BRIEN J R, et al. Use of vertebroplasty to prevent proximal junctional fractures in adult deformity surgery: a biomechanical cadaveric study [J]. Spine J, 2013, 13(12): 1897-1903.
14SCHREIBER J J, HUGHES A P, FADI T, et al. An association can be found between hounsfield units and success of lumbar spine fusion [J]. Hss J, 2013, 10(1): 25-29.
15TEMPEL Z J. Impaired bone mineral density as a predictor of graft subsidence following minimally invasive transpsoas lateral lumbar interbody fusion [J]. Eur Spine J, 2015, Suppl 3: 414-419.
16KIM Y J, BRIDWELL K H, LENKE L G, et al. Proximal junctional kyphosis in adult spinal deformity after segmental posterior spinal instrumentation and fusion: minimum five-year follow-up [J]. Spine (Phila Pa 1976), 2008, 33(20): 2179-2184.

