活性炭上挥发性有机化合物的真空脱附
左宋林, 张 杰, 刘军利, 孙 康
(1.南京林业大学 化学工程学院,江苏省绿色燃料与化学品重点实验室,江苏 南京 210037;2.中国林业科学研究院 林产化学工业研究所,江苏 南京 210042)
研究报告
活性炭上挥发性有机化合物的真空脱附
左宋林1, 张 杰1, 刘军利2, 孙 康2
(1.南京林业大学 化学工程学院,江苏省绿色燃料与化学品重点实验室,江苏 南京 210037;2.中国林业科学研究院 林产化学工业研究所,江苏 南京 210042)
以椰壳活性炭(AC)和硝酸氧化改性的活性炭(AC-O)作为吸附剂,选择了具有不同极性和分子大小的烷烃、芳烃、醇和酮等11种挥发性有机化合物(VOCs)作为吸附质,分析了这些VOCs在活性炭固定床上随脱附温度升高的脱附曲线,研究了挥发性有机化合物在活性炭上的真空脱附规律。结果表明:与其它的脱附方法相比,VOCs在活性炭上的真空脱附具有脱附温度低、脱附率高(能达到99%以上)、活性炭的重复利用次数多等优点,是一种具有很好发展潜力的VOCs回收方法。同时,对于化学结构类似的VOCs吸附质,沸点越低则越易于在活性炭上脱附;活性炭的表面化学性质对甲醇和乙醇的脱附影响显著,但对其它VOCs吸附质的脱附影响较小。活性炭的非极性表面非常有利于醇类有机蒸气分子的脱附,硝酸氧化改性则显著降低了醇类分子的脱附率。此外,在活性炭的重复利用过程中,甲醇和乙醇的羟基能与活性炭表面的羧基相互作用,导致活性炭表面羧基在较高温度脱附时发生脱除或转变成内酯基形式,有利于活性炭的重复使用。
活性炭;挥发性有机化合物;真空脱附;表面改性
含有挥发性有机化合物(VOCs)的废气是目前的主要空气污染物之一,主要来源于生产、储运和使用许多化工产品过程所发生的挥发、泄漏及排空等。世界上许多国家已制定了严格的VOCs排放标准,解决VOCs排放问题已成为环境保护领域的主要课题之一。目前,解决该问题的主要技术途径是实现VOCs的有效回收。由于活性炭的微孔结构发达,在加热、酸、碱和普通氧化剂条件下性质稳定,具有独特的吸附低浓度挥发性有机化合物优势,因此,活性炭成为回收低浓度VOCs的主要材料[1-2]。活性炭回收VOCs过程包括VOCs在活性炭上的吸附和脱附两个必不可少的步骤。活性炭的吸附是一项传统技术,有关活性炭的孔隙结构[3-6]和表面化学性质[7-9]、吸附条件以及VOCs的性质[3,10-11]等对活性炭吸附VOCs的影响已有较深入的研究。由于活性炭的脱附是活性炭再生技术的理论基础,因此,活性炭的脱附理论与技术一直是活性炭领域的研究重点。理论上,提高吸附剂的温度可以实现吸附质的脱附,因此采用加热活性炭的方法可以实现吸附质的脱附,即热脱附。通过长期的研究和开发,根据不同的加热介质和方式,热脱附已经发展有热空气[12-13]、热惰性气体[14-15]、过热水蒸气[16-17]、微波加热[18-19]以及电加热[20-22]等多种热脱附方法,并成为目前活性炭脱附的主要工业方法。由于VOCs具有较高的挥发性,因此热脱附适合于活性炭中VOCs的脱附[12-16]。有关活性炭的热脱附工艺、热脱附的动力学分析、脱附模型等已有较多的研究报道。尽管热脱附方式较容易在工业上应用,但不同的热脱附方法都存在一些不同的缺点,如热空气和惰性气体加热时容易引起吸附质的裂解甚至焦化[23-24]、过热水蒸气加热时严重影响活性炭的重复利用[16,25]、微波加热存在加热深度不够[26]等问题。近年来,Salvador等[27]系统综述了热脱附的加热介质种类、加热方式以及活性炭的种类对热脱附工艺和效果的影响。除提高温度外,降低压力是脱附的另一种方法,即真空脱附。目前真空脱附主要应用于活性炭的真空变压吸附技术中,用于工业气体的净化与分离[28-29]。由于真空变压吸附技术使用的加热介质少,大大提高了回收物质的纯度,因此,有关真空脱附技术在回收VOCs蒸气方面的应用已有较多的报道[30-35],主要针对活性炭的变压吸附循环次数、气体流量以及温度等工艺条件对富集或回收得到高浓度有机蒸气的影响等方面进行研究。然而,有关活性炭吸附剂的结构和吸附质的性质对VOCs真空脱附的影响等基础问题却很少见报道。因此,目前本研究选择了11种不同极性和分子尺寸的VOCs分子作为吸附质,研究它们在活性炭上的真空脱附规律,以期为真空脱附的应用提供新的理论依据。
1 材料与方法
1.1材料
椰壳颗粒活性炭(AC),市售。为了改变活性炭的表面化学性质,将AC进行硝酸氧化改性,改性过程如下:将50 g椰壳活性炭和300 mL质量分数为10%的稀硝酸在圆底烧瓶中混合加热到80 ℃,然后回流24 h后取出,用去离子水反复洗涤至滤液的pH值接近7,最后干燥得到氧化改性活性炭(AC-O)。
选择极性和分子尺寸不同的烷烃、芳烃、醇和酮等11种VOCs作为吸附质,分别是正丁烷、正己烷、环己烷、甲醇、乙醇、丙酮、苯、甲苯、邻二甲苯、间二甲苯和对二甲苯,其中正丁烷气体的纯度为99.5%,其它均为分析纯试剂。
1.2吸附与脱附
1.2.1吸附 本实验采用固定床吸附装置,其结构如图1所示;采用重量法测定活性炭的吸附量。吸附操作步骤如下: 1) 检查整个装置的气密性; 2) 装填吸附剂。将干燥的活性炭装填至U型吸附管的固定刻度,以保证每次装填活性炭的体积一致,然后将吸附管放入30 ℃恒温水浴中; 3) 吸附。调节进入蒸气发生器中的氮气流量,使气流中有机蒸气的相对压力保持在0.60~0.75之间,然后开始活性炭的吸附操作。吸附1 h后,关闭气流,取出U型管并用塞子密封,除去U型管外表面的水分后称质量,然后再将吸附管装入气路中再次进行吸附。重复上述吸附操作,直至连续两次吸附管的质量变化小于0.5%,即认为达到吸附饱和,计算活性炭的饱和吸附量。
1.2.2脱附 本实验采用的真空热脱附装置如图2所示,脱附温度采用油浴控制。脱附步骤如下:将装有达到饱和吸附状态活性炭的吸附管取出连接到真空热脱附装置上,开始升温并打开真空泵,脱附过程中真空度控制在10 kPa左右。从起始脱附温度(30 ℃)开始,当脱附达到平衡时(根据U型管的质量进行判断),以10 ℃为间隔逐渐提高脱附温度,直至活性炭中VOCs的脱附率达到90%以上,根据相应脱附温度下吸附管的质量变化计算脱附率。
为了对比,将图2中的真空泵换成氮气或空气储罐,采用热氮气或空气吹扫的方式对活性炭进行脱附。其中氮气或空气的流量为80 mL/min,在油浴中预热至脱附需要的温度后进入吸附管。

图1吸附装置图
Fig.1Schematicdiagramofadsorptiondevice

图2真空脱附装置图
Fig.2Schematicdiagramofvacuumdesorptiondevice
为了研究吸附/真空脱附过程对重复利用椰壳活性炭回收VOCs的影响,按照上述吸附/真空脱附的操作步骤,测试活性炭重复利用过程中,活性炭的有机蒸气吸附量及脱附率达到99%以上时的脱附温度。
1.3样品分析
采用EA300型元素分析仪(德国EURO公司生产)分析活性炭的元素(C、H和O)含量。
采用Boehm[8-9]滴定法分析活性炭中含氧官能团的含量,其操作过程为:分别称取0.100 0 g的绝干活性炭样品置于3个锥形瓶中,分别加入25.0 mL的0.1 mol/L的NaOH溶液、0.05 mol/L的Na2CO3溶液和0.1 mol/L的NaHCO3溶液,室温下振荡24 h后抽滤。在滤液中加入25 mL的0.1 mol/L的盐酸,中和剩余的碱液,然后用NaOH溶液滴定分析消耗的盐酸量,最后分别计算3种碱与活性炭表面酸性官能团反应的消耗量。由于NaHCO3主要中和活性炭表面的羧基,Na2CO3中和羧基和内酯基,NaOH中和羧基、内酯基和酚羟基,因此,根据这3种碱消耗量的差值可以计算得到不同酸性含氧官能团的含量。
2 结果与讨论
2.1VOCs脱附方式的比较
本研究比较了真空脱附、氮气吹扫和空气吹扫3种方式在不同温度下脱附苯、正丁烷和乙醇的脱附率,结果见表1。

表1 脱附方式对活性炭的VOCs脱附率的影响
由表1可以看出,不管是极性弱的苯、正丁烷还是极性较高的乙醇,在30~50 ℃脱附温度范围内,活性炭真空热脱附的脱附率都明显高于热氮气或空气吹扫脱附方式,而空气和氮气吹扫的热脱附率差别不大;或者说,真空脱附可以降低脱附温度。同时,乙醇的真空热脱附和气体吹扫热脱附之间脱附率的差异比苯和正丁烷的要高得多,这表明极性较大的醇类分子采用真空脱附更加有效。

图3 不同有机蒸气的脱附率与脱附温度的曲线图Fig.3 The desorption efficiency curves of different organic vapor under different desorption temperature
图3显示了11种VOCs的真空热脱附曲线。从图3可以看出,随着脱附温度的升高,有机蒸气的脱附率不断升高,除二甲苯外,其余的有机蒸气在脱附温度150 ℃之前,其脱附率都达到95%以上。早期采用的热重分析方法[24,36]研究VOCs气体在活性炭上的热脱附结果显示,丁烷、己烷和辛烷分别需要在220、360和425 ℃才能脱附完全,甲苯在大约310 ℃下脱附完全;而采用真空脱附的方式,当脱附率大于95%时,丁烷、己烷和甲苯的脱附温度分别为80、130和150 ℃,是热脱附温度的1/3~1/2,显著低于热脱附需要的温度。Kim等[37]采用热脱附活性炭上的甲苯和甲基乙基酮(沸点为79.6 ℃),脱附温度达到300 ℃时它们的脱附率分别为98.1%和99.1%。Boulinguiez等[38]研究建议,不管采用何种形态的活性炭,吸附在活性炭上的VOCs的脱附温度通常都需要200 ℃以上;Giraudet等[20]采用电热方法完全脱附活性炭纤维布上的甲苯所需温度为250 ℃。以上分析表明,采用真空热脱附可以显著降低有机蒸气的脱附温度。这也与表1的结果一致,真空热脱附比空气或氮气脱附所需要的温度低。因此,与气体吹扫热脱附相比,真空热脱附可以显著降低回收的能耗,而且较低的脱附温度有利于回收热不稳定的VOCs蒸气。
2.2VOCs性质对真空热脱附的影响
已有研究表明[10,11,39],弱极性有机蒸气分子在活性炭上的吸附主要是物理吸附。根据吸附理论,由于本实验中所采用的吸附温度低于吸附质的临界温度,因此有机蒸气在活性炭上的吸附类似于有机蒸气的液化。有机蒸气在活性炭上的热脱附研究[23-24]表明,有机蒸气的沸点越高,脱附就越难。总体上,图3所显示的11种有机蒸气的脱附曲线也基本符合这一规律。根据这11种有机蒸气的沸点(表2),图3中VOCs吸附质的脱附曲线可以分为3个明显的区域,脱附率最小的区域是由沸点为 140 ℃ 左右的二甲苯同分异构体的脱附率曲线所构成;脱附率较高的区域中包括正己烷、环己烷、苯和甲苯等4种VOCs,它们的沸点在68~110 ℃范围内;脱附率最高的区域是由甲醇、乙醇、丁烷和丙酮等4种所构成,除乙醇外,它们的沸点比其它VOCs分子都低。尽管不同分子结构的VOCs吸附质的脱附率大小与它们的沸点有所不一致,但具有相同化学结构的VOCs吸附质的沸点越高,如丁烷、己烷等烷烃,甲醇、乙醇等醇类,苯、甲苯和二甲苯等芳烃,则它们的脱附率越小。
这11种VOCs吸附质中,对于不同化学结构的VOCs吸附质,甲醇和乙醇的脱附率要明显高于其它吸附质。甲醇的沸点(64.8 ℃)比正丁烷的沸点(-0.5 ℃)要高得多,但甲醇的脱附率却高于正丁烷;丙酮、正己烷、环己烷和苯的沸点稍高于或低于甲醇和乙醇的沸点,但它们的脱附率比甲醇和乙醇要低得多。化学结构相似的苯与二甲苯之间沸点的差值和化学结构不同的正丁烷与丙酮之间沸点的差值相似,但前两者的脱附率的差值比后两者的差异要显著得多。这些结果表明,VOC吸附质分子的性质中,除沸点外,还有其它性质显著影响其在活性炭上的脱附。例如,尽管异丙醇的沸点比二氯甲烷的沸点高42 ℃,但在活性炭纤维上完全脱附吸附异丙醇的温度仅仅比二氯甲烷的高10 ℃[20]。
为了更加直观反映沸点对有机蒸气分子在活性炭上脱附的影响,根据图3的脱附曲线数据推算出了每种有机蒸气在沸点温度下的脱附率,其结果见表2。从表2可以看出,即使是在沸点温度下进行的真空脱附,只有甲醇和乙醇的脱附率能达到95%以上,其它有机蒸气的脱附率都在55%~75%之间。在沸点温度下不能完全脱附的主要原因是有机蒸气分子在活性炭中的微孔和中孔的吸附热通常大于液化潜热[10],即有机蒸气分子与活性炭表面的相互作用力大于有机蒸气分子之间的相互作用力;其中吸附在中孔的有机蒸气以液体状态存在,而吸附在微孔中的有机蒸气则以假固体的状态存在[18],即在活性炭微孔中VOCs的吸附热明显高于中孔的吸附热[10-11,18,39]。
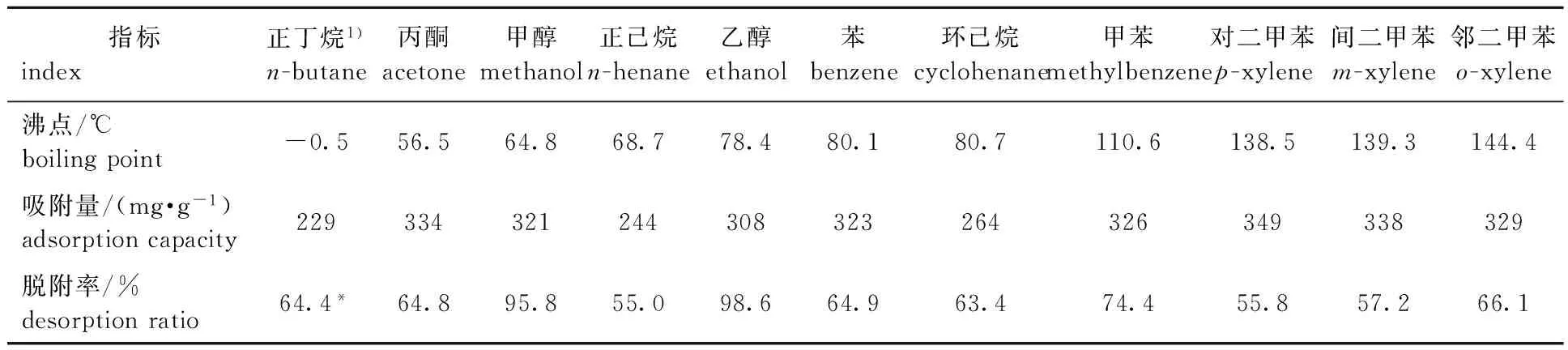
表2 11种有机蒸气吸附质的沸点、吸附量(30 ℃)以及在沸点温度下的脱附率
1)*:最低脱附温度30 ℃时的脱附率the desorption ratio of 30 ℃(minimum desorption temperature)
活性炭与有机蒸气分子之间的相互作用力取决于活性炭的孔隙结构和表面化学性质。与其它VOCs吸附质相比,在沸点温度下甲醇和乙醇所表现出的高脱附率表明,极性较强的吸附质与活性炭表面的作用力要明显弱于非极性或弱极性吸附质[39],吸附质的分子极性是影响VOCs在活性炭上脱附的主要因素之一。二甲苯的3种同分异构体的分子空间结构对它们在活性炭上的脱附影响可能较小。因此,极性较强的VOCs吸附质容易在活性炭上脱附。
2.3活性炭硝酸改性的影响
为了了解活性炭表面性质对VOC脱附的影响,测试了甲醇、乙醇、丙酮、甲苯和丁烷5种吸附质在硝酸氧化改性活性炭上的脱附曲线,其结果见图4。

图4 硝酸改性前后活性炭对有机蒸气脱附的影响
非常明显,硝酸氧化改性显著降低了甲醇和乙醇在活性炭上的脱附率(图4(a)和(b)),在脱附曲线的较低温度阶段(30~50 ℃),其脱附率降为未改性活性炭的一半左右;但对正丁烷、甲苯和丙酮等吸附质的脱附影响较小(图4(c)、(d)和(e)),与以往的研究结果一致[11]。
表3为吸附/脱附VOCs前后活性炭的元素和含氧官能团含量分析。由表3可以看出,硝酸氧化改性导致活性炭的碳元素减少了近10个百分点,氧元素增加了近8个百分点;酸性较强的表面羧基官能团从0.02 mmol/g显著增加至1.273 mmol/g,酸性相对较弱的内酯基和酚羟基含量明显降低。因此,可以判断,活性炭表面的羧基明显降低了甲醇和乙醇的脱附率,但对其它的吸附质影响不明显,从而使这5种吸附质的脱附率大小发生改变,如图5所示。在硝酸氧化改性活性炭上,这5种吸附质的脱附率基本符合沸点越高则脱附越困难这一基本规律。

表3 吸附/脱附VOCs前后活性炭的元素和含氧官能团含量分析

图5 硝酸改性后活性炭对不同有机蒸气脱附的影响Fig.5 Effect of AC-O on the desorption rate of different organic vapors
在这11种有机蒸气吸附质中,甲醇和乙醇的脱附率表现出与其它吸附质不同的规律。在羧基含量很少的活性炭上,甲醇和乙醇的脱附率比沸点要低50 ℃的丁烷更高,而且活性炭的表面羧基官能团对它们的脱附产生了显著影响。已有研究报道[19,40],活性炭的硝酸氧化改性可以显著提高羧基含量,同时提高低相对压力下活性炭对乙醇蒸气的吸附量[19],增强乙醇分子与活性炭表面的相互作用,不利于乙醇的脱附[40]。显然,甲醇和乙醇的极性不能合理解释甲醇和乙醇在活性炭上的脱附现象,因为丙酮的极性比甲醇和乙醇更大,但其脱附行为与烷烃与芳烃等非极性有机蒸气类似。最近,Bouzid等[41]采用统计方法研究了乙醇的吸附机理,结果显示乙醇分子在活性炭上的吸附是以垂直而不是平行于活性炭表面的方式进行排列的。因此,如果这种垂直活性炭表面的排列方式是通过乙醇的羟基与活性炭的表面直接接触实现的,那么可以很好解释乙醇在活性炭上的脱附行为。在未改性的活性炭上,乙醇的极性羟基与活性炭的非极性表面的作用力弱,导致乙醇在活性炭上容易脱附;活性炭的氧化改性显著提高了乙醇的羟基与活性炭表面的作用力,从而显著降低乙醇的脱附率。对于丙酮来说,由于丙酮是一种对称的刚性分子,在2个甲基之间的羰基难以直接与活性炭表面接触,因此,丙酮可能是以一种与活性炭表面平行的方式接触,导致丙酮表现出与其它非极性或极性弱的有机蒸气分子相似的脱附规律,提高活性炭表面极性降低了丙酮与活性炭表面的结合能[42]。同样的道理,也可以很好解释甲醇在活性炭上的脱附行为。因此,不能简单根据有机蒸气分子的极性来判断它们在活性炭上的脱附规律。
2.4活性炭吸附/脱附的重复使用性能
在回收VOCs的过程中,活性炭的重复利用性能是影响成本的主要因素,本研究考察了在重复吸附-真空脱附过程中,非极性苯、正丁烷和极性乙醇3种有代表性的有机蒸气在活性炭重复利用过程中的吸附量以及脱附率达到99%以上时的最终脱附温度,结果如表4所示。

表4 不同重复次数下活性炭重复吸附/脱附有机蒸气过程中的吸附量和完全脱附温度
由表4可以看出,氧化改性对活性炭的有机蒸气吸附量产生了或多或少的影响;在重复吸附/真空脱附过程中,真空脱附次数对活性炭的吸附量几乎没有影响。以上结果表明有机蒸气在活性炭上的吸附基本上是物理吸附,不可逆吸附很少[21,24,36];与热脱附方式[21,27]相比,真空脱附能够使有机蒸气在较低温度下完全脱附。然而,活性炭经过第一次吸附/真空脱附乙醇后,AC-O的氧和氢元素含量都明显减少,碳元素含量明显增加;活性炭表面含氧官能团中羧基从1.273 mmol/g急剧减少至0.022 mol/g,内酯基从0.995 mmol/g明显增加到1.301 mmol/g,酚羟基含量基本不变(见表3)。羧基含量的急剧减少可能是由于两方面原因所造成:一是由于加热容易导致羧基的脱除[43-44],真空脱附促进了活性炭表面的羧基在更低的温度下(真空脱附温度达140 ℃)脱除;二是在较高的真空脱附温度下活性炭表面的羧基与吸附质乙醇的羟基之间作用而转变为内酯基。然而,非极性有机蒸气苯在AC-O上和极性有机蒸气乙醇在未改性AC上进行真空脱附时,活性炭表面元素和表面含氧官能团的含量变化都较小。这些结果也支持了前面所述的乙醇在活性炭表面的吸附是醇的羟基与活性炭表面结合的推断。
从脱附率大于99%时所需的脱附温度来看,活性炭经硝酸改性后,苯和正丁烷在活性炭上的最终真空脱附温度都下降了20~30 ℃,而乙醇的最终脱附温度却升高了10 ℃。从脱附过程来看,与活性炭表面直接接触的吸附质分子是最后被脱附的,因此,最终脱附温度反映了吸附质分子与活性炭表面的相互作用力大小,最终脱附温度越高,则它们的相互作用力就越大;反之则越小。因此,可以推断,硝酸改性对活性炭表面极性的提高减弱了非极性分子与活性炭表面的相互作用力,但增大了吸附质分子的极性基团与活性炭表面的相互作用力。而且,从表4可以进一步看到,随着重复利用次数的增加,苯的最终脱附温度明显降低,在没有改性的活性炭上降低了40 ℃,而正丁烷和乙醇则基本没有变化。这可能是由于芳环分子的重复利用引起了活性炭孔隙结构的变化;甲苯也发现了类似的情况。因此,在活性炭的重复利用过程中,VOCs在活性炭上的真空脱附不仅不会引起脱附率的降低,相反会有利于脱附。
3 结 论
3.1通过研究11种有机蒸气(正丁烷、正己烷、环己烷、甲醇、乙醇、丙酮、苯、甲苯、邻二甲苯、间二甲苯和对二甲苯)在椰壳活性炭及其硝酸氧化改性活性炭上的真空脱附行为发现,真空脱附具有脱附温度低、脱附完全(脱附可达99%以上)、活性炭重复利用次数多等优点,是一种具有发展潜力的有机蒸气回收技术。
3.2具有相同化学结构的VOCs在活性炭上的脱附能力取决于有机蒸气的沸点,沸点越低则越易于在活性炭上脱附;对于分子结构不同的VOCs,甲醇和乙醇等醇类有机蒸气受到活性炭表面性质的影响显著,具体表现在:1) 非极性的活性炭表面有利于醇类有机蒸气分子的脱附;2) 增强活性炭的表面极性,可显著减弱醇类分子的脱附,而对非极性有机蒸气的脱附率影响很小;在活性炭的重复利用过程中,甲醇和乙醇的羟基能与活性炭表面的羧基相互作用,导致活性炭表面羧基在较高温度脱附时发生脱除或转变成内酯基形式,有利于活性炭的重复使用。
[1]DWIVEDI P,GAUR V,SHARMA A,et al. Comparative study of removal of volatile organic compounds by cryogenic condensation and adsorption by activated carbon fiber[J]. Separation and Purification Technology,2004,39(1/2):23-37.
[2]KHAN F I,GHOSHAL A K. Removal of volatile organic compounds from polluted air[J]. Journal of Loss Prevention in the Process Industries,2000,13(6):527-545.
[3]CHIANG Y C,CHIANG P C,CHANG E E.Effects of surface characteristics of activated carbons on VOC adsorption[J]. Journal of Enviromental Engineering,2001,127:54-62.
[4]FUERTES A B,MARBN G,NEVSKAIA D M. Adsorption of volatile organic compounds by means of activated carbon fibre-based monoliths[J]. Carbon,2003,41(1):87-96.
[5]DAS D,GAUR V,VERRNA N. Removal of volatile organic compound by activated carbon fiber[J]. Carbon,2004,42(14):2949-2962.
[6]LUO L G,RAMIREZ D,ROOD M J,et al. Adsorption and electrothermal desorption of organic vapors using activated carbon adsorbents with novel morphologies[J]. Carbon,2006,44(13):2715-2723.
[7]KIM K D,PARK E J,SEO H O,et al. Effect of thin hydrophobic film for toluene adsorption and desorption behavior on activated carbon fiber under dry and humid conditions[J]. Chemical Engineering Journal,2012,200-202:133-139.
[9]CUERVO M R,ASEDEGBEGA-NIETO E,DIAZ E,et al. Effect of carbon nanofiber functionalization on the adsorption properties of volatile organic compounds[J]. Journal of Chromatography A,2008,1188(2):264-273.
[10]LEE M G,LEE S W,LEE S H. Comparison of vapor adsorption characteristics of acetone and toluene based on polarity in activated carbon fixed-bed reactor[J]. Korean Journal of Chemical Engineering,2006,23(5):773-778.
[11]DAIFULLAH A A M,GIRGIS B S. Impact of surface characteristics of activated carbon on adsorption of BTEX[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects,2003,214(1/2/3):181-193.
[12]ION V A,PARVULESCU O C,DOBRE T,et al. Modelling of thermal desorption of volatile organic compounds from activated carbon[J]. Revista De Chimie(Bucharest),2015,66(5):703-706.
[13]YAZBEK W P P,DELEBARRE A. Adsorption and desorption of volatile organic compounds in fluidized bed[J]. Journal of Environmental Engineering,2006,132(5),442-452.
[14]YUN J H,CHOI D K,MOON H. Benzene adsorption and hot purge regeneration in activated carbon beds[J]. Chemical Engineering Science,2000(55):5857-5872.
[15]HWANG K S,CHOI D K,GONG S Y,et al. Adsorption and thermal regeneration of methylene chloride vapor on an activated carbon bed[J]. Chemical Engineering Science,1997,52(7):1111-1123.
[16]SHAN I K,PRE P,ALAPPAT B J. Steam regeneration of adsorbents:An experimental and technical review[J]. Chemical Science Transactions,2013,2(4):1078-1088.
[17]LEE D G,HAN Y J,LEE C H. Steam regeneration of acetone and toluene in activated carbon and dealuminated Y-zeolite beds[J]. Korean Journal of Chemical Engineering,2012,29(9):1246-1252.
[18]CHA C Y,CARLISLE C T. Microwave process for volatile organic compound abatement[J]. Journal of the Air & Waste Management Association,2001,51(12):1628-1641.
[19]POLAERT I,ESTEL L,HUYGHE R,et al. Adsorbents regeneration under microwave irradiation for dehydration and volatile organic compounds gas treatment[J]. Chemical Engineering Journal,2010,162(3):941-948.
[20]GIRAUDET S,BOULINGUIEZ B,CLOIREC P L. Adsorption and electrothermal desorption of volatile organic compounds and siloxanes onto an activated carbon fiber cloth for biogas purification[J]. EnergyFuels,2014,28(6):3924-3932.
[21]JOHNSEND L,MALLOUK K E,ROOD M J. Control of electrothermal heating during regeneration of activated carbon fiber cloth[J]. Environmental Science & Technology,2011,45(2):738-743.
[22]LI J J,LU R J,DOU B J,et al. Porous graphitized carbon for adsorptive removal of benzene and the electrothermal regeneration[J]. Environmental Science & Technology,2012,46(22):12648-12654.
[23]URANO K,YAMAMOTO E,TAKEDA H. Regeneration rates of granular activated carbons containing adsorbed organic matter[J]. Industrial & Engineering Chemistry Process Design and Development,1982,21(1):180-185.
[24]LIU P K T,FELTCH S M,WAGNER N J. Thermal desorption behavior of aliphatic and aromatic hydrocarbons loaded on activated carbon[J]. Industrial & Engineering Chemistry Research,1987,26(8):1540-1545.
[25]GUJ J,BART H J. Heat and mass transfer in steam desorption of an activated carbon adsorber[J]. International Communications in Heat and Mass Transfer,2005,32(3/4):296-304.
[27]SALVADOR F,MARTIN-SANCHEZ N,SANCHEZ-HERNANDEZ R,et al. Regeneration of carbonaceous adsorbents. Part I:Thermal Regeneration[J]. Microporous and Mesoporous Materials,2015,202:259-276.
[28]FARUQUE HASAN M M,BALIBAN R C,ELIA J A,et al. Modeling,simulation,and optimization of postcombustion CO2capture for variable feed concentration and flow rate. 2:Pressure swing adsorption and vacuum swing adsorption processes[J]. Industrial & Engineering Chemistry Research,2012,51(48):15665-15682.
[29]YANG H W,YIN C B,JIANG B,et al. Optimization and analysis of a VPSA process for N2/CH4separation[J]. Separation and Purification Technology,2014,134(25):232-240.
[30]RITTER J A,YANG R T. Pressure swing adsorption:Experimental and theoretical study on air purification and vapor recovery[J]. Industrial & Engineering Chemistry Research,1991,30(5):1023-1032.
[31]GALES L,MENDES A,COSTA C. Recovery of acetone,ethyl acetate and ethanol by thermal pressure swing adsorption[J]. Chemical Engineering Science,2003,58(23/24):5279-5289.
[32]MC INTYRE J A,HOLLAND C E,RITTER J A. High enrichment and recovery of dilute hydrocarbons by dual-reflux pressure-swing adsorption[J]. Industrial & Engineering Chemistry Research,2002,41(14):3499-3504.

[34]RAMALINGAM S G,SAUSSAC J,PRÉ P,et al. Hazardous dichloromethane recovery in combined temperature and vacuum pressure swing adsorption process[J]. Journal of Hazardous Materials,2011,198:95-102.
[35]BHATT T S,SLIEPCEVICH A,STORTI G,et al. Experimental and modeling analysis of dual-reflux pressure swing adsorption process[J]. Industrial & Engineering Chemistry Research,2014,53(34):13448-13458.
[36]SUDO Y,MISIC D M,SUZUKI M,et al. Concentration dependence of effective surface diffusion coefficient in aqueous phase adsorption on activated carbon[J]. Chemical Engineering Science,1978,33(9):1287-1290.
[37]KIM K J,KANG C S,YOU Y J,et al. Adsorption-desorption characteristics of VOCs over impregnated activated carbons[J]. Catalysis Today,2006,111:223-228.
[38]BOULINGUIEZB,CLOIREC P L. Adsorption on activated carbons of five selected volatile organic compounds present in biogas:Comparison of granular and fiber cloth materials[J]. Energy & Fuels,2010,24(9):4756-4765.
[39]CHIANG Y C,CHIANG P C,HUANG C P. Effects of pore structure and temperature on VOC adsorption on activated carbon[J]. Carbon,2001,39(4):523-534.
[40]SILVESTRE-ALBEROA,SILVESTRE-ALBERO J,SEPLVEDA-ESCRIBANO A,et al. Ethanol removal using activated carbon:Effect of porous structure and surface chemistry[J]. Microporous and Mesoporous Materials,2009,120(1/2):62-68.
[41]BOUZID M,SELLAOUI L,KHALFAOUI M,et al. Adsorption of ethanol onto activated carbon:Modeling and consequent interpretations based on statistical physics treatment[J]. Physica A:Statistical Mechanics and Its Applications,2016,444:853-869.
[42]KWON S,VIDIC R,BORGUET E.The effect of surface chemical functional groups on the adsorption and desorption of a polar molecule,acetone,from a model carbonaceous surface,graphite[J]. Surface Science,522(1/2/3):17-26.
[43]BOEHM H P.Some aspects of the surface chemistry of carbon blacks and other carbons[J]. Carbon,1994,32(5):759-769.
[44]VAN PELT A H,SIMAKOVA O A,SCHIMMING S M,et al. Stability of functionalized activated carbon in hot liquid water[J]. Carbon,2014,77:143-154.
Vacuum Desorption of Volatile Organic Compounds from Activated Carbons
ZUO Songlin1, ZHANG Jie1, LIU Junli2, SUN Kang2
(1.College of Chemical Engineering,Jiangsu Key Laboratory of Biomass-based Green Fuels and Chemicals,Nanjing Forestry University, Nanjing 210037, China; 2.Institute of Chemical Industry of Forest Products, CAF, Nanjing 210042, China)
In order to elucidate the patterns of vacuum desorption of volatile organic compounds(VOCs) from activated carbons, the vacuum desorption curves of the VOCs as a function of the temperature were investigated in a fixed bed by choosing 11 types of VOCs (including alkanes, aromatics, alcohols and ketones, and so on) of different chemical structures and molecular sizes. The results showed that vacuum desorption was a highly potential technology for recovering VOCs. Compared with conventional thermal desorption methods, vacuum desorption significantly reduced VOCs desorption temperatures, and allowed high desorption efficiency of greater than 99% and more reuse of activated carbons. The polar surfaces of activated carbon significantly weakened the desorption of alcohols while the non-polar surface was conducive. The surface property of activated carbons barely affected the desorption of the non-polar VOCs. Further, adsorbed alcohols molecules such as methanol and ethanol were arranged perpendicular to the surface of activated carbon in a way that hydroxyls of alcohols directly contacted with the carbon surface. This arrangement led to carboxyl groups of activated carbons prone to be removed or be changed into lactone in the vacuum thermal desorption process.
activated carbon; volatile organic compounds; vacuum desorption; surface modification
10.3969/j.issn.0253-2417.2017.06.003
2017- 10- 18
“十二五”国家科技支撑计划资助(2015BAD14B0601)
左宋林(1968— ),男,湖南湘潭人,教授,博士,主要从事生物质热化学转化与炭材料研究;E-mailzslnl@njfu.com.cn。

ZUO Songlin
TQ35;TQ424
A
0253-2417(2017)06- 0019- 09
左宋林,张杰,刘军利,等.活性炭上挥发性有机化合物的真空脱附[J].林产化学与工业,2017,37(6):19-27.

