PbO2复合电极预处理甲苯二胺废水
冯建俊,黎学明,苏德水,邵 方
(1. 重庆大学 化学化工学院,重庆 400030;2. 河北丰源环保科技股份有限公司,河北 沧州 061000)
甲苯二胺(TDA)是一种芳香胺,主要用于生产甲苯二异氰酸酯(TDI)[1],具有强毒性,难于生化降解,且在降解过程中易产生高毒性的中间物,已被美国环保署列为致癌物[2]。常规的焚烧法、吸附法等TDA废水处理方法降解效率低,很难达标排放。高级氧化技术具有氧化能力强、适用范围广等优点,主要包括光催化氧化法、超临界水氧化法、电催化氧化法等。光催化氧化法和超临界水氧化法对TDA的降解效果好但操作复杂、成本高,难于工业化应用[3-4]。电催化氧化技术具有氧化能力强、操作简便、反应条件温和、无二次污染以及成本低廉等诸多优点[5],已成为污染物降解的研究热点。但目前电催化氧化技术降解TDA的相关报道甚少。PbO2电极具有析氧电位高、导电性及耐蚀性良好、价格低廉等优点[6-8],常用做电催化氧化技术的阳极材料。但钛基PbO2电极处理废水时,基底易氧化,缩短电极寿命,因此,需对PbO2电极进行改性,即制备复合PbO2电极,增强电极的稳定性,提高电催化活性。
本工作以河北某化工厂的TDA废水为研究对象,采用涂覆—热分解法与电沉积法制备了β-PbO2/α-PbO2/SnO2-Sb2O3/Ti复合电极(PbO2复合电极),并对其进行了表征。结合电催化氧化技术,考察了PbO2复合电极降解TDA的能力。
1 实验部分
1.1 试剂、材料和仪器
乙醇、草酸、正丁醇、无水Na2SO4、NaOH、无水SnCl4、SbCl3、PbO、Pb(NO3)2、HNO3、HCl、H2SO4(质量分数为98%):均为分析纯;聚四氟乙烯(PTFE)乳液:质量分数为60%,美国杜邦公司。
TDA废水:由河北丰源环保科技股份有限公司提供,COD为4791.74 mg/L,TDA质量浓度为486.4 mg/L,pH为1。
OTF-1200X型真空管式高温烧结炉:合肥科晶材料技术有限公司;XRD-6000型X射线粉末衍射仪:日本Shimadzu公司;VEJAIILMU型扫描电子显微镜:捷克TESCAN公司;CHI660B型电化学工作站:上海辰华仪器公司;稳压恒流直流电源:艾德克斯电子有限公司;721型可见分光光度计:上海精密科学仪器有限公司;WMX型微波密封消解COD速测仪:苏州裕宸仪器有限公司。
1.2 PbO2电极的制备
钛基体的预处理:分别采用800,2000,4000目砂纸打磨尺寸为50 mm×20 mm×1 mm的钛片,直至表面为银白色,然后分别置于乙醇和蒸馏水中各超声处理15 min,去除表面油污及杂质。在质量分数为15%的沸腾的草酸溶液中刻蚀1.5 h,得到灰色麻面的钛片,于乙醇中保存待用。
电极底层的制备:通过涂覆—热分解法制备SnO2-Sb2O3底层[7]。将均匀涂敷SnCl4-SbCl3的钛片于120 ℃下干燥15 min,反复涂敷—烘干操作5次,烘干后的钛片在氧气气氛下500 ℃焙烧2 h。
电极中间层的制备:在碱性条件下,采用电沉积法制备α-PbO2中间层。电沉积液组成为浓度0.1 mol/L的 PbO和浓度4.0 mol/L的NaOH溶液。电沉积条件为电流密度1~25 mA/cm2,电沉积温度40℃,电沉积时间1 h。
电极表层的制备:在酸性条件下,通过电沉积法制备β-PbO2表层。电沉积液组成为质量浓度4 g/L的PTFE、浓度0.1 mol/L的HNO3、浓度0.1 mol/L的Pb(NO3)2。电沉积条件为电流密度10~25 mA/cm2,电沉积温度25~85 ℃,电沉积时间0.5~2.0 h。
1.3 电极的表征及性能分析
1.3.1 表面形貌及晶体结构分析
采用SEM照片显示电极表面形貌,观察镀层表面晶粒大小及分布情况。采用XRD谱图分析镀层的晶相结构及材料晶型。
1.3.2 电化学性能测试
以PbO2复合电极为工作电极、饱和Ag/AgCl电极为参比电极、石墨电极为辅助电极,建立三电极体系,并通过CHI660B型电化学工作站,采用循环伏安法和线性极化法测试电极的电化学性能。
循环伏安法:1)分别以浓度0.5 mol/L Na2SO4溶液和含有TDA的0.5 mol/L Na2SO4溶液为电解液,考察PbO2电极的电化学性能。扫描范围为0~2.0 V,扫描速率为200 mV/s[9];2)以含TDA的不同质量浓度(1~15 g/L)的Na2SO4溶液为电解液,考察Na2SO4质量浓度对TDA降解效果的影响。扫描范围为-0.8~2.0 V,扫描速率为200 mV/s。
线性极化法:电解液为浓度0.5 mol/L的 Na2SO4溶液,扫描范围为0.5~2.5 V,扫描速率为50 mV/s。1.3.3 电极稳定性测试
通过高电流密度下的加速寿命试验测试电极的稳定性。以PbO2复合电极为阳极、不锈钢片为阴极,浓度为1.0 mol/L 的H2SO4溶液为电解液,电流密度为2.0 A/cm2。以槽电压上升至10 V作为评价电极失活的依据[10]。根据式(1)换算电极的寿命。

式中:τ1是测试寿命,h;τ2是使用寿命,h;i1是初始电流密度,A/cm2;i2是实际电流密度,A/cm2。
1.4 电催化氧化法处理TDA废水实验
取250 mL TDA废水,加入一定量Na2SO4为电解质,以PbO2复合电极为阳极、不锈钢片为阴极,电极有效面积为3.0 cm2,电极间距为1.0 cm,在一定的电流密度下处理TDA 废水,每间隔一定时间取样,测定废水中TDA及COD的浓度。考察不同电流密度下TDA氧化降解的效果。
1.5 分析方法
TDA质量浓度的测定采用重氮偶合比色法,以芳胺类为偶合剂,测定波长为545 nm[11]。COD的测定采用微波快速消解-重铬酸钾法[9,12]。通过COD值计算氧化降解TDA的瞬时电流效率(ηi),计算公式见式(2)

式中:CODt为t时刻的化学需氧量,g/L;CODt+Δt为t+Δt时刻的化学需氧量,g/L;F为法拉第常数,96487 C/mol;I为电解电流,A;V为电解液体积,L。
2 结果与讨论
2.1 PbO2复合电极的表征
PbO2复合电极的XRD谱图见图1。图1a为SnO2-Sb2O3底层的XRD谱图,由图1a可见,在2θ=26.56°,33.86°,37.82°,51.77°,54.78°处出现了四方相SnO2的特征衍射峰(JCPDS 77-0447),2θ为40.21°,63.04°处的衍射峰与Sb2O3卡片(JCPDS 71-0143)基本一致。图1b为α-PbO2中间层的XRD谱图,由图1b可见,与卡片JCPDS(72-2440)在2θ=23.251°,28.471°,32.741°,34.301°,49.432°等处的衍射峰吻合,说明在碱性条件下可获得斜方晶型α-PbO2晶体。图1c为β-PbO2表层的XRD谱图,对比卡片JCPDS(89-2805)发现,2θ=25.400°,32.007°,36.228°,49.107°,58.891°等处的衍射峰与卡片基本吻合,说明在酸性条件下可制得四方晶型β-PbO2晶体。同时,图1b和图1c的谱图中,峰位置未发生偏移,峰强度大,说明两种PbO2晶相中没有晶格缺陷且晶体结晶度高。
PbO2复合电极的SEM照片见图2。由图2a可见,采用涂覆—热分解法制备的SnO2-Sb2O3底层分布均匀,呈龟裂状。图2b是电流密度为13.5 mA/cm2下制得的α-PbO2镀层的SEM照片。由图2b可见,镀层颗粒呈梭形,分布均匀致密,粒径约为200~400 nm,该镀层不仅有利于β-PbO2的形成,同时还可提高电极的稳定性。由图2c可见,通过优化反应制得的β-PbO2活性层由金字塔状的颗粒组成团粒堆积而成,呈花菜状,颗粒粒径约为300~500 nm。该结构可增大比表面积,利于催化反应进行。

图1 PbO2复合电极的XRD谱图

图2 PbO2复合电极的SEM照片
2.2 PbO2电极的电化学性能评价
2.2.1 循环伏安法和线性极化法
PbO2复合电极在TDA-Na2SO4体系和Na2SO4体系中测得的循环伏安曲线(CV曲线)见图3。由图3可见,TDA-Na2SO4体系的CV曲线在1.28 V附近出现了一个明显的氧化峰,且TDA-Na2SO4体系的CV曲线的电流响应值明显高于Na2SO4体系,表明电催化氧化过程中TDA消耗了大量的·OH,加快了电极表面溶胶-晶体系统内电子的移动,使反应电流增大[13]。3种PbO2电极的线性极化曲线(LSV曲线)见图4。由图4可见, PbO2复合电极的析氧电位最高,约为1.9 V,高于其他钛基电极(SnO2-Sb2O3/Ti 1.80 V, PbO2/ SnO2-Sb2O3/Ti 1.75V)[10],且高于TDA的氧化电位,表明该电极可以有效地降解TDA。
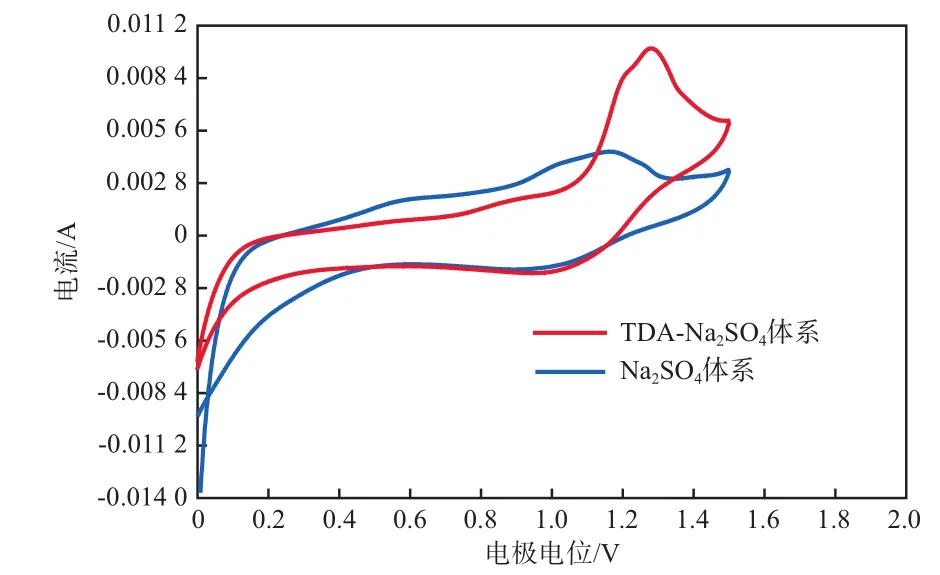
图3 PbO2复合电极的CV曲线
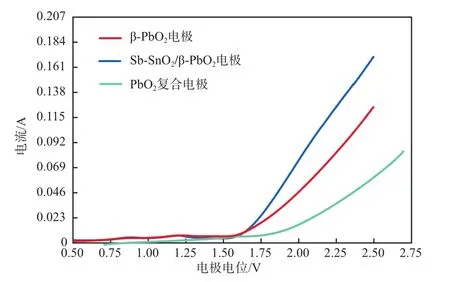
图43种PbO2电极的线性极化曲线
2.2.2 加速寿命试验
加速寿命试验中阳极电位与电解时间的关系见图5。
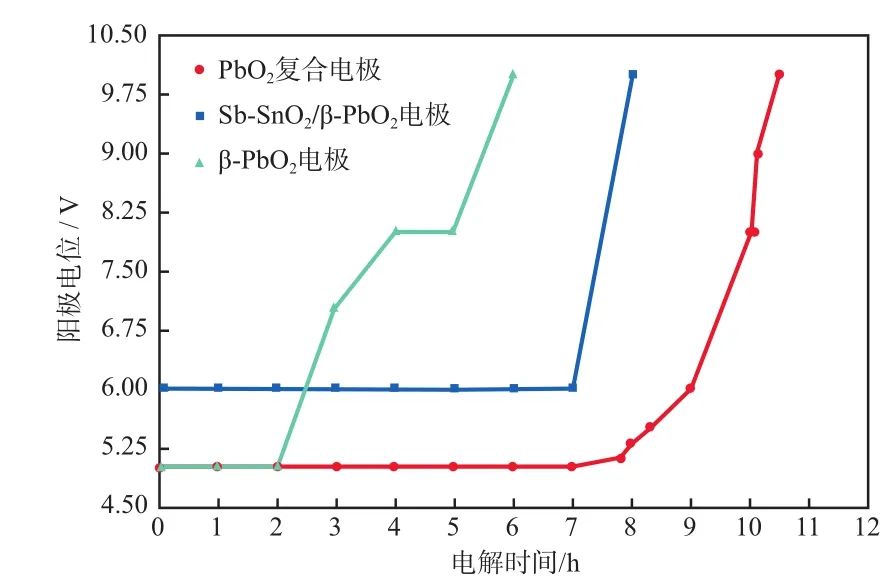
图5 加速寿命试验中阳极电位与电解时间的关系
由图5可见, PbO2复合电极的测试寿命最长约10.5 h。这可能是因为:SnO2-Sb2O3底层可以增强钛基体与PbO2的结合力,阻止基体钝化[14];并且α-PbO2作为中间层,有缓冲融合作用,有利于β-PbO2结晶[15-16],延长了电极的使用寿命。
2.3 电催化氧化TDA实验
2.3.1 Na2SO4质量浓度对TDA降解效果的影响
不同Na2SO4质量浓度下的CV曲线见图6。由图6可见,随着Na2SO4质量浓度增加,峰值电流增加,但峰值电位基本不变。这是由于随电解质增多,溶液的导电性增强,溶液电阻变小,使电流增大,加快了TDA的氧化反应速率。虽然高浓度Na2SO4溶液可提高电催化氧化反应速率,但是增加了成本,不利于工业化,因此,Na2SO4溶液的最佳质量浓度为10 g/L。

图6 不同Na2SO4质量浓度下的CV曲线
2.3.2 电流密度对TDA降解效果的影响
电流密度对TDA去除率的影响见图7。
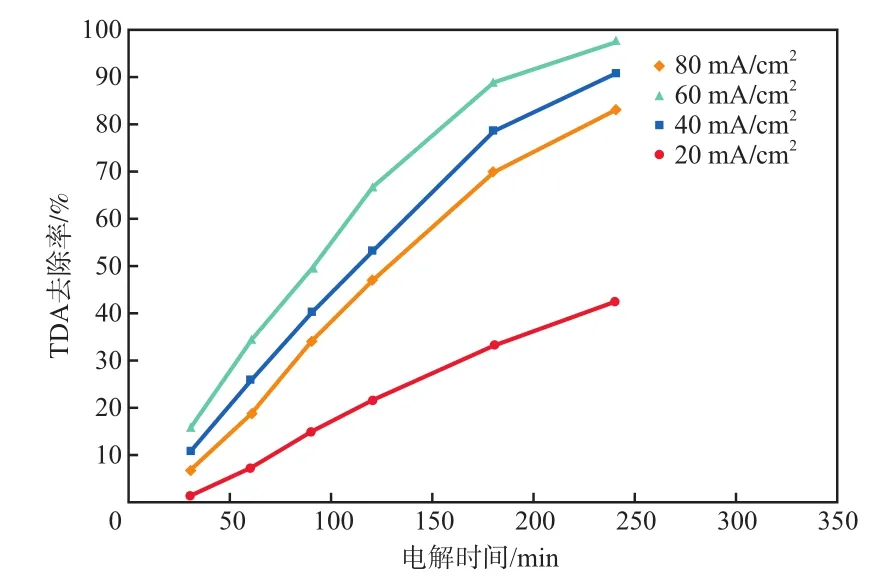
图7 电流密度对TDA去除率的影响
由图7可见:TDA去除率随着电流密度增大而增大,电流密度为60 mA/cm2时,TDA去除率最高,为97.3%;此后,继续增加电流密度,TDA去除率却下降。这是由于高电流密度下易发生析氧反应,降低了体系中·OH的浓度,削弱了体系的氧化能力,导致TDA去除率下降。由图7还可见,TDA去除率随着反应时间的延长而提高。PbO2复合电极电催化降解TDA的效果高于Ti4O7电极[17],说明相较于Ti4O7电极具有更大的优势。且相较于其他TDA废水处理方法,如过硫酸盐催化法[4],电化学催化氧化法可以缩短反应时间、提高处理效率。因此,最佳电流密度为60 mA/cm2。
电流密度对COD去除率的影响见图8。
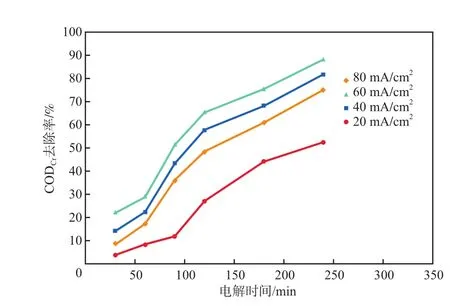
图8 电流密度对COD去除率的影响
由图8可见:COD去除率随着电流密度的增加而增大;当电流密度为60 mA/cm2、电解时间为240 min时,COD去除率最高,为88.1%;继续增大电流密度,COD去除率降低。
电流密度对ηi的影响见图9。由图9可见:电极ηi的变化趋势与COD去除率一致;当电流密度为60 mA/cm2时,电极的电流效率最高。
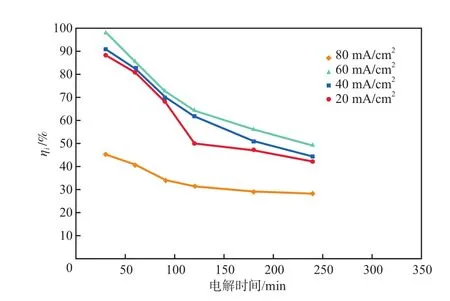
图9 电流密度对ηi的影响
同时,通过公式(1)可计算出电流密度为60 mA/cm2时,电极的使用寿命可达486 天。
综合考虑,60 mA/cm2为最佳电流密度。
2.4 TDA废水的处理效果
在Na2SO4质量浓度为10 g/L、电流密度为60 mA/cm2、电解时间为240 min的条件下,TDA废水的处理效果见表1。
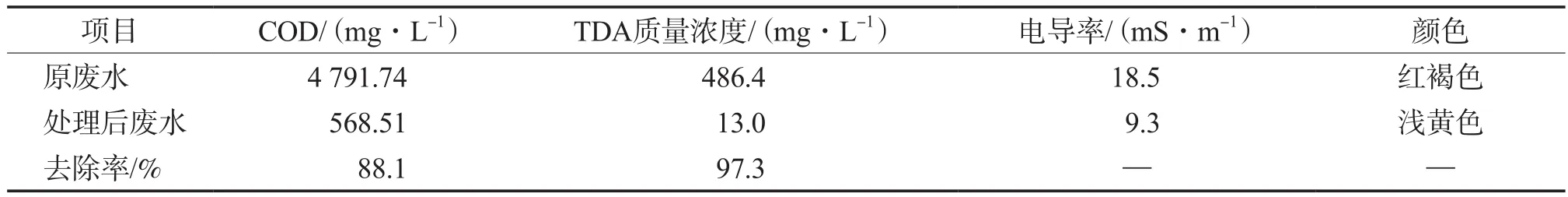
表1 TDA废水的处理效果
由表1可见,以PbO2复合电极为阳极的电化学高级氧化法对TDA废水具有较好的处理效果,COD及TDA的去除率分别达88.1%、97.3%。但出水的COD仍大于工业水二级排放标准,需经进一步常规生化处理达标后排放。
3 结论
a)通过涂覆—热分解法与电沉积法成功制备了β-PbO2/α-PbO2/SnO2-Sb2O3/Ti复合电极。XRD及SEM表征结果表明,在碱性条件下制备了单一、规整的梭型α-PbO2,酸性条件下制备了单一的呈花菜状的β-PbO2。
b)采用循环伏安法、线性极化法和加速寿命试验评价电极的电化学性能。实验结果表明:PbO2复合电极的析氧电位约为1.9 V,高于TDA的氧化电位(1.28 V),TDA可以在复合电极上发生氧化反应;并且电极可长期使用,当电流密度为60 mA/cm2时,电极使用寿命长达486 天。
c)采用PbO2复合电极的电催化氧化法对TDA的降解效果好。在Na2SO4质量浓度为10 g/L、电流密度为60 mA/cm2、电解时间为240 min的最佳反应条件下,TDA的去除率高达97.3%,COD去除率为88.1%。
[1] Schupp T. Modeling formation and distribution of toluene-2,4-diamine(TDA)after spillage of toluene-2,4-diisocyanate(TDI)into a river[J]. J Hazard Mater,2013,252/253:70 - 76.
[2] Jiang Yonghai,Zhang Jinbao,Xi Beidou,et al.Degradation of toluene-2,4-diamine by persulphate:Kinetics,intermediates and degradation pathway[J].Environ Technol,2015,36(11):1441 - 1447.
[3] 胡瑜娜. 高级氧化法处理甲苯二胺工业废水的研究[D]. 华东理工大学,2012.
[4] 李贵贤,陈江波,马建军,等. TDA废水超临界水氧化法降解[J]. 兰州理工大学学报,2013,39(3):57 - 60.
[5] 夏伊静. 高效金属掺杂PbO2电极的制备及用于降解典型制药废水的研究[D]. 浙江工业大学,2016.
[6] Xu Hao,Yuan Quansheng ,Shao Dan,et al. Fabrication and characterization of PbO2electrode modified with[Fe(CN)6]3-and its application on electrochemical degradation of alkali lignin[J]. J Hazard Mater,2015,286:509 - 516.
[7] Li Xiaolin,Li Xueming,Tang Sui,et al. High selectivity of benzene electrochemical oxidation to p-benzoquinone on modified PbO2electrode[J]. Appl Surface Sci,2014,311:357 - 361.
[8] Shmychkova O,Luk’yanenko T,Amadelli R,et al .Electrodeposition of Ni2+-doped PbO2and physicochemical properties of the coating[J]. J Electroanal Chem,2016,774:88 - 94.
[9] 段小月. 碳纳米管改性PbO2电极制备及降解水中酚类污染物的研究[D]. 哈尔滨工业大学,2013.
[10] 周礼,司士辉. 钛基金属氧化物电极的制备及性能[J]. 化工环保,2014,30(1):84 - 89.
[11] 杨晓芬,赵美萍,李元宗,等. 水中苯胺类化合物的分光光度法测定[J]. 分析化学,2002,5(30):540 - 543.
[12] 王智军,王峰,张江. COD的回流法和快速测试法方法验证[J]. 资源节约与环保,2013(12):91 -92.
[13] 敖雪,单明军,王艳秋,等. A/O—Fenton氧化—混凝组合工艺处理丁苯橡胶生产废水[J]. 化工环保,2015,35(1):49 - 54.
[14] Xie Ruzhen,Meng Xiaoyang,Sun Peizhe,et al.Electrochemical oxidation of ofloxacin using a TiO2-based SnO2-Sb/polytetrafluoroethylene resin-PbO2electrode:Reaction kinetics and mass transfer impact[J].Appl Catal B,2017,203:515 - 525.
[15] Chen Zhen,Yu Qiang,Liao Denghui,et al. Influence of nano-CeO2on coating structure and properties of electrodeposited Al/α-PbO2/β-PbO2[J]. Trans Nonf Metal Soc China,2013,23(5):1382 - 1389.
[16] Wu Jia,Xu Hao,Yan Wei. Fabrication and characterization of β-PbO2/α-PbO2/Sb–SnO2/TiO2nanotube array electrode and its application in electrochemical degradation of Acid Red G[J]. RSC Adv,2015,5(25):19284 - 19293.
[17] 田嫚. Zr还原法制备Ti4O7及其电催化处理2,4-二氨基甲苯废水的方法[J]. 功能材料,2017,48(2):2177 - 2181.

