复方龙芩草微乳提取液有效成分体外抗H1N1流感病毒的药效研究
刘晓艳,李妍,刘帅,李卫飞,顾立刚,刘晓婷,杜红
1.北京中医药大学中药学院,北京 100102;2.北京中医药大学中医药防治病毒性疾病教育部重点实验室,北京 100029
复方龙芩草微乳提取液有效成分体外抗H1N1流感病毒的药效研究
刘晓艳1,李妍1,刘帅1,李卫飞1,顾立刚2,刘晓婷2,杜红1
1.北京中医药大学中药学院,北京 100102;2.北京中医药大学中医药防治病毒性疾病教育部重点实验室,北京 100029
目的 研究复方龙芩草微乳提取液中有效成分体外抗H1N1流感病毒增殖的作用,观察微乳提取液中有效成分对流感病毒的抑制率。方法 用均匀设计法安排实验,MTT法检测药物对H1N1流感病毒致A549细胞病变的抑制效率(ER),以ER为指标,运用Minitab17软件建立数学模型得出各因素之间的回归方程,分析各成分对ER的作用关系并优选出具有最佳抗H1N1流感病毒效果的有效成分比例。结果 复方成分中,黄芩苷发挥最显著的抗病毒作用,甘草苷对细胞病变有一定的抑制作用,5种成分对ER存在协同或制约性的关系。每毫升药液含甘草苷、黄芩苷、亮氨酸、天冬氨酸、谷氨酸分别为13.94 μg、49.44 μg、0.23 mg、1.25 mg、2.50 mg时ER值最佳,经验证ER值为85.34%±4.72%。结论 复方龙芩草微乳提取液有效成分的优化组合能较好发挥抗H1N1流感病毒的作用。
复方龙芩草;微乳提取液;均匀设计;H1N1流感病毒;A549细胞
甲型H1N1流感是由H1N1流感病毒引起的一种传染迅速、死亡率高的呼吸道传染病[1]。复方龙芩草由黄芩、甘草和地龙3味中药组成,具有清肺利咽、解毒泻热之功效[2-3],对甲型H1N1流感具有较好的抵抗效果[4]。复方龙芩草微乳提取液是以生物相容性微乳为溶剂,运用渗漉法对复方龙芩草进行提取而得,能较好地抑制H1N1流感病毒增殖[5]。近年来,中药有效组分或成分配伍研究逐渐受到青睐,复方中有效成分配伍往往可提高疗效,改善复方成分复杂、作用机制不明确的缺陷[6],均匀设计法在复方有效成分或组方配伍的药效筛选中具有明显的优势[7-8]。本实验以复方龙芩草微乳提取液中含量较高的成分黄芩苷、甘草苷及地龙中的氨基酸为基础,从细胞水平探讨其对H1N1流感病毒致细胞病变的抑制作用,拟设计出药效物质基础明确、安全有效的抗H1N1流感病毒的有效成分组方,为后续研究提供思路。
1 实验材料
1.1 病毒和细胞
甲型H1N1流感病毒,A1/黔防/166/85株,中国中医科学院提供,-75 ℃冷藏,血凝滴度为2~7。人肺腺癌细胞(A549),中国协和医科大学基础医学院细胞中心。
1.2 药物
甘草苷(批号111610-201106,40 mg/支)、黄芩苷(批号110715-201318,100 mg/支)、谷氨酸(批号140690-201203,100 mg/支)、天冬氨酸(批号140691-200401,100 mg/支)、亮氨酸(批号140687-201102,100 mg/支),中国食品药品检定研究院;磷酸奥司他韦胶囊(达菲,75 mg/粒),瑞士巴塞尔豪夫迈罗氏公司,批号H20044397。
1.3 主要试剂与仪器
胎牛血清、McCoy's 5A培养基,美国Gibco公司;四甲基偶氮唑蓝(MTT)、二甲亚砜(DMSO),Sigma公司;0.25%胰酶-0.02%EDTA,北京普博欣生物科技有限公司;三联溶解液(含SDS 10 g、异丁醇5 mL、10 mol/L HCl 0.1mL);细胞培养液:McCoy's 5A培养基(含10%胎牛血清和1%青-链霉素);细胞维持液:McCoy's 5A培养基(含2%胎牛血清和1%青-链霉素)。细胞培养箱(BINDER WMK-02型),光学显微镜(日本Olympus公司),荧光倒置显微镜(日本Olympus公司),超净工作台(北京碧都净化设备有限公司),酶标仪(北京普朗新技术有限公司),水浴箱(北京医疗设备厂),Astell全自动高压灭菌器(北京东迅天地医疗仪器有限公司)。
2 实验方法
2.1 细胞毒性实验
从-75 ℃冰箱取出A549细胞复苏,传代3~4次,细胞生长良好时以0.25%胰酶-0.02%EDTA消化细胞,用细胞培养液调整细胞浓度为1.5×108个/L,充分混匀后将该细胞液以每孔100 μL加入96孔板中,35 ℃、5%CO2培养箱培养数小时使细胞以单层状态铺满培养瓶底层。用细胞维持液将黄芩苷、甘草苷、天冬氨酸、谷氨酸、亮氨酸和达菲分别连续对倍递次稀释至不同浓度,加入96孔板中,每孔100 μL,每个浓度平行设6个复孔,同时设正常细胞对照组。35 ℃、5%CO2培养箱培养48 h,加入MTT(终浓度为0.5 mg/mL),培养4 h后每孔加100 μL SDS,继续培养12 h,于酶标仪波长570 nm处测定细胞吸光度(A)值,计算细胞存活率(实验组A值÷正常细胞对照组A值×100%)。
2.2 病毒致细胞病变实验
取已长成单层细胞的96孔板,吸出培养液,每孔加PBS清洗2次,每孔接种100 µL 100TCID50病毒液,37 ℃、5%CO2培养箱中吸附2 h后吸出病毒液,加入最大无毒浓度下6个相应稀释度的黄芩苷、甘草苷、天冬氨酸、谷氨酸、亮氨酸溶液,以达菲为阳性对照组,同时设正常细胞对照组和病毒对照组,每孔100 µL,每浓度设4个复孔。37 ℃、5%CO2培养箱培养48 h观察结果,细胞病变效应(CPE)用0%~25%(+)、25%~50%(++)、50%~75%(+++)、75%~100%(++++)表示,当病毒对照组CPE为++++时记录结果。随后加入MTT(终浓度为0.5 mg/mL),每孔10 µL,4 h后加100 µL/孔SDS,培养8 h,于酶标仪波长570 nm处测定A值。计算药物抗病毒效率(ER)。ER(%)=(药物组平均A值-病毒对照组平均A值)÷(正常细胞对照组平均A值-病毒对照组平均A值)×100%。实验重复2次。
2.3 均匀试验设计
根据每个有效成分对流感病毒的ER及对细胞形态的影响情况设置均匀试验的上下限,根据均匀设计水平数不得少于2倍因素数的原则,本试验采用5因素10水平[U10*(105)]设计试验,D=0.241 4,指标数为1,见表1。
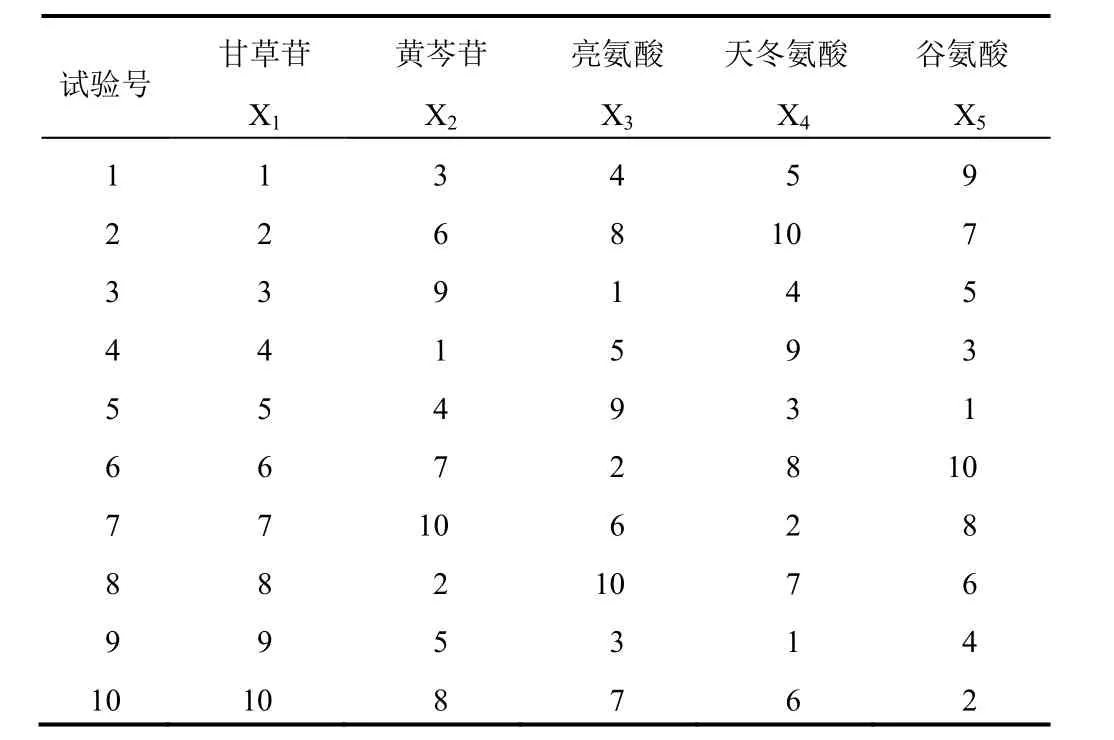
表1 均匀试验设计因素水平表
2.4 细胞病变抑制率测定
根据表1安排的试验进行药物组分对细胞病变抑制率检测,取已长成单层细胞的96孔板,吸出培养液,每孔加入100 µL 100TCID50病毒液,37 ℃、5%CO2培养箱吸附2 h后,吸出病毒液,加入表1中的10组药液,每孔100 µL,以达菲为阳性药物对照组,同时设正常细胞对照组和病毒对照组,每浓度设6个复孔,继续培养48 h后加入MTT(终浓度为0.5 mg/mL),继续培养4 h,加SDS,12 h后于酶标仪波长570 nm处测定A值,计算ER。实验重复2次。
2.5 组分配比的优选
根据均匀试验结果,运用Minitab17软件对结果进行分析处理,探讨各成分对抗病毒效率的影响及相互关系,并优选出具有最佳抗H1N1流感病毒效果的5种有效成分的配比。
2.6 最佳抗病毒效果的验证
取已长成单层细胞的96孔板,吸出培养液,加入PBS清洗细胞2次,按“2.4”项下方法进行操作,实验重复3次,验证有效成分配比的ER。
3 统计学方法
4 结果
4.1 有效成分的细胞毒性
较高浓度黄芩苷可使A549细胞变圆、破碎、折光率增加,当浓度为50 μg/mL时细胞存活率变化不明显,细胞形态、折光率、数量与正常细胞对照组无明显差异,25 μg/mL时与空白对照组比较,细胞形态几乎无变化。甘草苷对细胞形态的影响与黄芩苷相似,浓度为25 μg/mL时细胞形态、贴壁状态等与空白对照组比较无显著差异。天冬氨酸、谷氨酸、亮氨酸浓度均为5 mg/mL时,对细胞基本无毒性,与空白对照组比较无明显差异。
4.2 有效成分对病毒致细胞病变抑制率的影响
当黄芩苷浓度为50 μg/mL,ER值为87.810%± 1.905%时,对病毒致细胞病变的抑制作用最明显,随黄芩苷浓度降低,ER值逐渐变小。甘草苷浓度在25 μg/mL时能部分抑制细胞的病变,ER值也随浓度的降低而下降,二者ER均呈一定的量效关系,见表2。天冬氨酸、谷氨酸、亮氨酸抗病毒效果不明显,但在2.5~0.625 mg/mL浓度范围内,ER值大于空白对照组。
表2 黄芩苷、甘草苷对H1N1病毒CPE的影响及ER比较(±s,n=4)
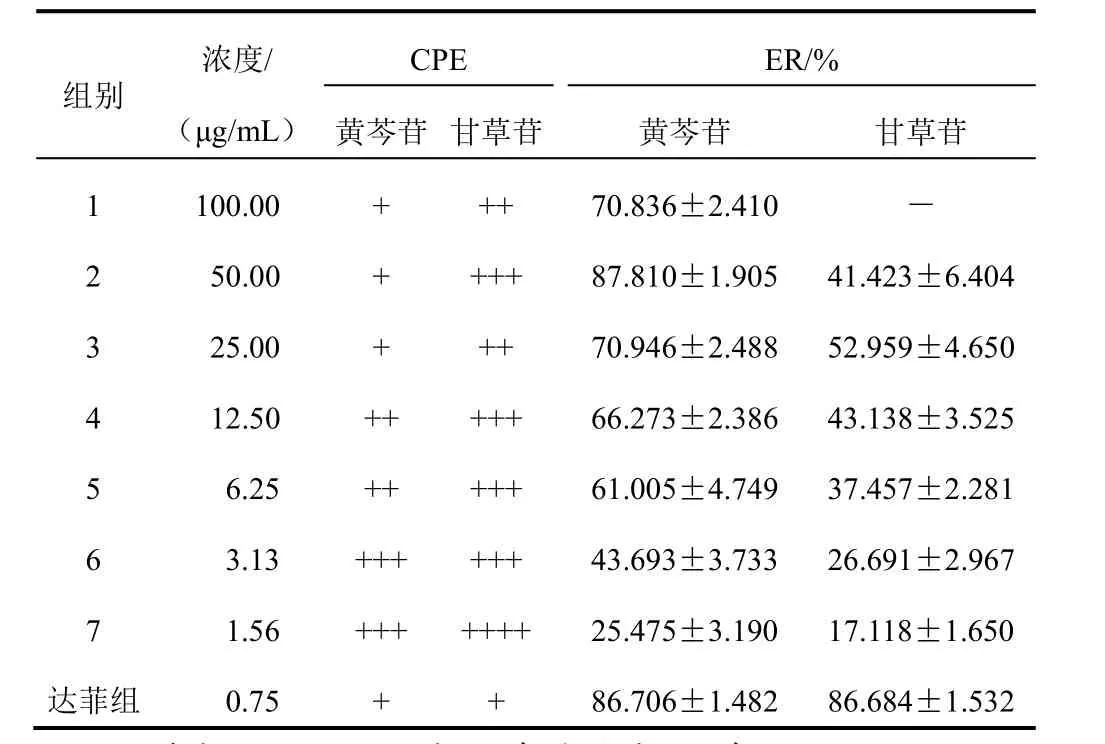
表2 黄芩苷、甘草苷对H1N1病毒CPE的影响及ER比较(±s,n=4)
CPE ER/%组别浓度/(μg/mL)黄芩苷甘草苷 黄芩苷 甘草苷1 100.00 + ++ 70.836±2.410 -2 50.00 + +++ 87.810±1.905 41.423±6.404 3 25.00 + ++ 70.946±2.488 52.959±4.650 4 12.50 ++ +++ 66.273±2.386 43.138±3.525 5 6.25 ++ +++ 61.005±4.749 37.457±2.281 6 3.13 +++ +++ 43.693±3.733 26.691±2.967 7 1.56 +++ ++++ 25.475±3.190 17.118±1.650达菲组 0.75 + + 86.706±1.482 86.684±1.532
4.3 药物不同配比对细胞病变抑制率的影响
根据“4.2”项中5个成分在细胞安全的剂量范围内ER值的大小,将每毫升药液中黄芩苷、甘草苷的用量范围分别设为50~12.5 μg和25~12.5 μg,结合氨基酸对细胞形态变化的影响,设亮氨酸用量范围为2.5~0.625 mg,天冬氨酸为1.25~0.625 mg,谷氨酸为2.5~1.25 mg。均匀试验设计及结果见表3。
表3 均匀设计试验各成分用量及抗H1N1流感病毒效率(±s)
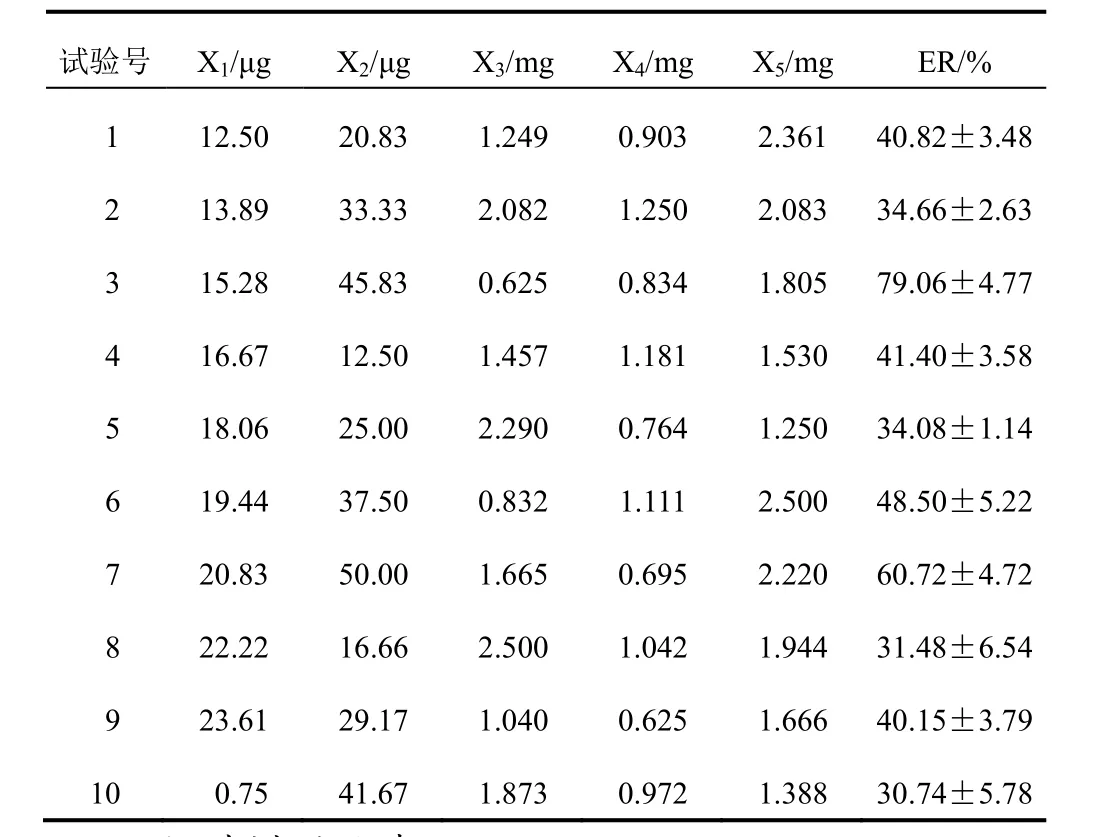
表3 均匀设计试验各成分用量及抗H1N1流感病毒效率(±s)
试验号X1/μg X2/μg X3/mg X4/mg X5/mgER/% 1 12.50 20.83 1.249 0.903 2.361 40.82±3.48 2 13.89 33.33 2.082 1.250 2.083 34.66±2.63 3 15.28 45.83 0.625 0.834 1.805 79.06±4.77 4 16.67 12.50 1.457 1.181 1.530 41.40±3.58 5 18.06 25.00 2.290 0.764 1.250 34.08±1.14 6 19.44 37.50 0.832 1.111 2.500 48.50±5.22 7 20.83 50.00 1.665 0.695 2.220 60.72±4.72 8 22.22 16.66 2.500 1.042 1.944 31.48±6.54 9 23.61 29.17 1.040 0.625 1.666 40.15±3.79 10 0.75 41.67 1.873 0.972 1.388 30.74±5.78
4.4 数学模型的建立
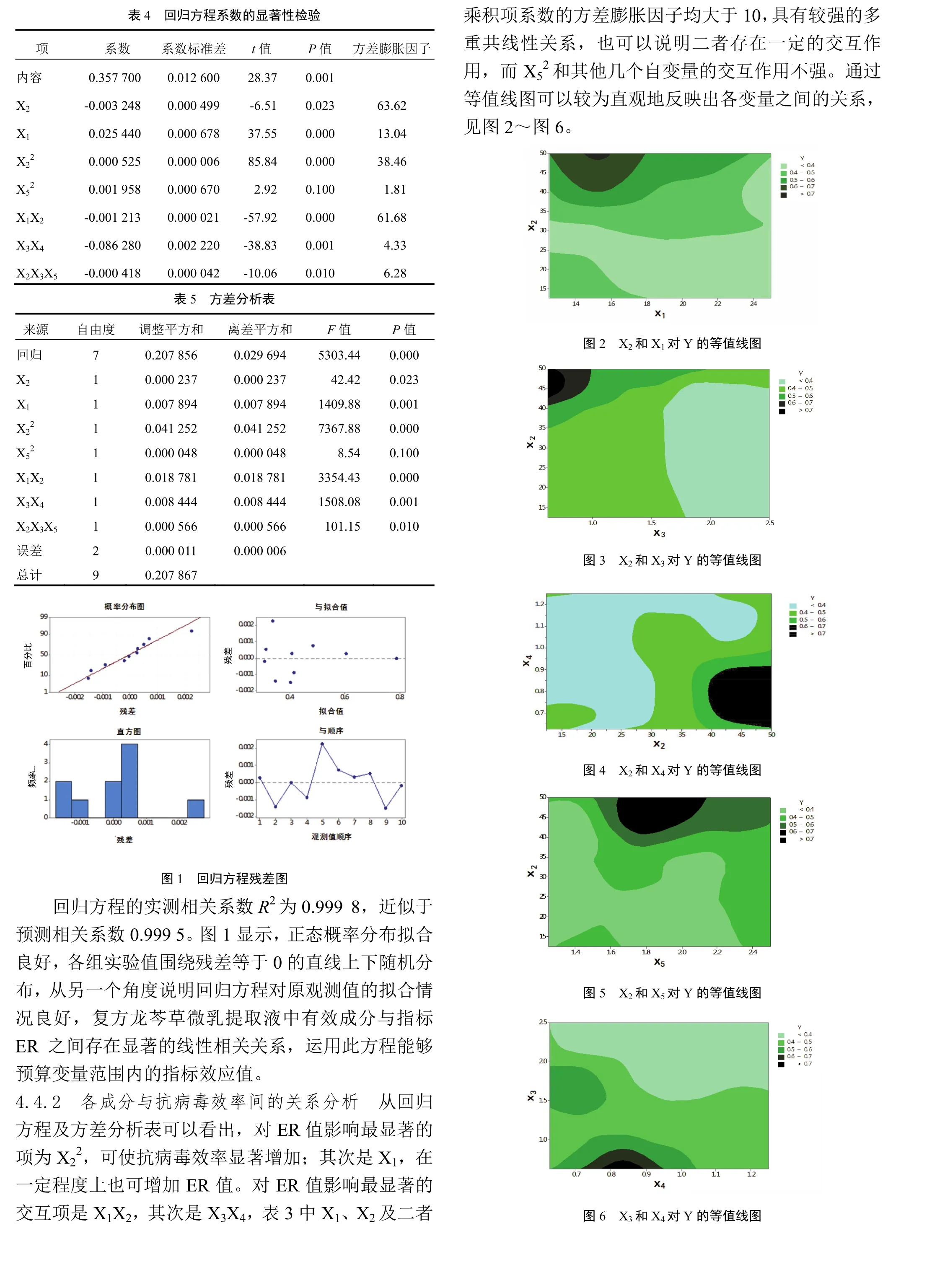
4.4.1 回归方程的建立 运用Minitab17.0软件处理均匀试验结果,运用逐步回归分析法,引入对ER显著变量,剔除不显著变量,拟合得到回归方程Y=0.357 700-0.003 248X2+0.025 440X1+0.000 525X22+0.001 958X52-0.001 213X1X2-0.086 280X3X4-0.000 418X2X3X5,其系数的显著性检验和方差分析见表4、表5。从表4可以看出,在回归方程模型中,除X52项外,其他各项系数均P<0.05,表5中回归方程P<0.001,说明该模型表示的指标与各变量间的关系具有统计学意义,方程拟合良好。回归方程残差图见图1。

参考文献:
[1] MICHAELIS M, DOERR H W, CINATL J J. An influenza a H1N1 virus revival-pandemic H1N1/09 virus[J]. Infection,2009,37(5):381-389.
[2] 李海燕.龙芩草、通络救脑组方成分的药学、药效学及作用机制[D].北京:北京中医药大学,2006.
[3] 成丽丽.龙芩草含片的药学、药效学及作用机制探讨[D].北京:北京中医药大学,2007.
[4] 李海燕,牛欣,司银楚.龙芩草喷雾剂抗流感病毒A1型(H1N1)作用的实验研究[J].北京中医药大学学报(中医临床版),2006,13(3):4-6.
[5] 刘晓艳,刘帅,李妍,等.复方龙芩草微乳提取液体外抗H1N1流感病毒的作用研究[J].天津中医药,2016,33(3):172-176.
[6] 刘新军,苏式兵.中药及其成分配伍组方的研究方法探析[J].中西医结合学报,2009,7(7):601-606.
[7] 仝欣,陈高峰,陆雁,等.基于均匀设计分析黄芪汤活性组分抗二甲基亚硝胺大鼠肝纤维化的配伍作用[J].中国中西医结合杂志,2011,31(10):1389-1393.
[8] 潘菊华,郑军,王彦云,等.基于均匀设计的开心解郁方抗抑郁主效应中药筛选研究[J].中国中医药信息杂志,2014,21(12):66-68.
[9] 张爱丽,章晨峰,邵杰.基于Minitab软件优化天舒胶囊一步制粒工艺[J].中草药,2013,44(22):3131-3135.
[10] 王丽,黄菱,李燕兵,等.黄芩苷对流感病毒性肺炎小鼠肺组织TLR3/ TRIF信号通路的作用[J].时珍国医国药,2014,25(10):2354-2356.
[11] 程妍,李祥,陈建伟,等.板蓝根有效部位的抗病毒药效研究[J].南京中医药大学学报,2011,27(2):155-157.
[12] 傅小达,符翠莉,李贵良.连花清瘟胶囊配合西药治疗甲型H1N1流感疑似患者33例[J].陕西中医,2011,32(11):1492-1493.
[13] 张沂,刘晓婷,顾立刚,等.疏风宣肺和解表清里方药体内外对流感病毒的影响[J].中华中医药杂志,2015,30(2):501-503.
[14] LAWRENCE M J, REES G D. Microemulsion-based media as novel drug delivery systems[J]. Advanced Drug Delivery Reviews,2000,45:89-121.
[15] MEHTA S K, KAUR G, BHASIN K K. Entrapment of multiple anti-Tb drugs in microemulsion system:quantitative analysis, stability, and in vitro release studies[J]. J Pharm Sci,2010,99(4):1896- 1911.
[16] GOMEZ del R J A, HAYES D G. Protein extraction by Winsor-Ⅲmicroemulsion systems[J]. Biotechnol Prog,2011,27(4):1091-1100.
[17] DING Y, DOU J, TENG Z J, et al. Antiviral activity of baicalin against influenza A (H1N1/H3N2) virus in cell culture and in mice and its inhibition of neuraminidase[J]. Arch Virol,2014, 159(12):3269-3278.
[18] QIN S, MO Z Y, ZHAO H S, et al. Inhibitory effect of baicalin on influenza A virus PR8 strain in vitro[J]. Chin Med Mat,2012, 35(2):280-283.
[19] 张春晶,顾立刚,于海涛,等.黄芩苷干预甲型H1N1流感病毒感染诱导的A549细胞周期分布及凋亡[J].病毒学报,2011,27(2):108-116.
[20] 唐亚军,孟胜喜,冯琴,等.基于均匀设计的防治脂肪肝中药有效组分复方筛选与验证[J].上海中医药大学学报,2013,27(4):53-57.
Study on Anti-influenza Virus H1N1 Activity of Main Ingredients from Microemulsion
Extract of Compound Longqincao in Vitro
LIU Xiao-yan1, LI Yan1, LIU Shuai1, LI Wei-fei1, GU Li-gang2,
LIU Xiao-ting2, DU Hong1(1.School of Chinese Pharmacy, Beijing University of Chinese Medicine, Beijing 100102, China; 2. Educational Ministry Key Laboratory of Preventing and Treating Viral Diseases with Chinese Medicine, Beijing University of Chinese Medicine, Beijing 100029, China)
Objective To study the effects of main ingredients from microemulsion extract of Compound Longqincao in vitro on anti-influenza virus H1N1 activity; To analyze effects of main ingredients from microemulsion extract on influenza virus inhibition rate. Methods Uniform design was used to conduct the experiment. MTT method was used to detect the effect rate (ER) of anti-influenza virus H1N1 on A549 cells. Setting ER as the index, Minitab17 software was used to establish mathematical model to come up with regression equations of all factors. The effects of ingredients on ER were analyzed and the efficient composition ratio of the optimum anti-influenza virus H1N1 was chosen. Results In the compound compatibility, baicalin showed the most obvious antivirus activity, and licorice glycosides had certain inhibition effects on pathological changes of cells. Five ingredients had coordinative or controlled relation with ER. When per milliliter liquids containing licorice glycosides, baicalin, leucine, aspartic acid, glutamic acid was 13.94 μg, 49.44 μg, 0.23 mg, 1.25 mg, and 2.50 mg, ER was the best. ER was 85.34%±4.72% after verification. Conclusion The optimized combination of main ingredients from microemulsion extract of Compound Longqincao can better play a role in anti-influenza virus H1N1.
Compound Longqincao; microemulsion extract; uniform design; H1N1 influenza virus; A549 cells
10.3969/j.issn.1005-5304.2017.01.013
R285.5
A
1005-5304(2017)01-0049-06
2016-03-29)
(
2016-04-25;编辑:华强)
国家自然科学基金(81102815);教育部博士点新教师基金(20110013120017);北京中医药大学研究生自主课题(2016-JYB-XS069)
杜红,E-mail:duhong@vip.163.com

