电针“百会”“涌泉”穴对APP/PS1双转基因小鼠海马β淀粉样蛋白及载脂蛋白E水平的影响*
张学婷,张 磊,周英奕,裴亚妮,薛卫国
(北京中医药大学,北京 100029)
电针“百会”“涌泉”穴对APP/PS1双转基因小鼠海马β淀粉样蛋白及载脂蛋白E水平的影响*
张学婷,张 磊,周英奕,裴亚妮,薛卫国△
(北京中医药大学,北京 100029)
目的:观察电针对4月龄APP/PS1双转基因小鼠海马载脂蛋白E(ApoE)及β淀粉样蛋白(Aβ)水平的影响,探讨针刺防治AD的机制。方法:将12只雄性4月龄APP/PS1双转基因阳性小鼠随机分为模型组和电针治疗组,以6只同月龄背景小鼠C57BL/6设为正常对照组,电针“百会”“涌泉”或同等条件束缚作为干预手段,每次持续15 min,每日1次,疗程为2周。以酶联免疫吸附测定法(ELASA)测定海马Aβ1-42的含量、ApoE2、ApoE4以及胆固醇-24S-羟化酶(CYP46)的含量。结果:模型组海马Aβ1-42的含量高于正常对照组(P<0.01);电针治疗组Aβ1-42的含量低于模型组(P<0.01)。模型组海马ApoE2、ApoE4的含量与正常对照组相比,差异无统计学意义,电针治疗组ApoE2、ApoE4的含量均高于模型组(P<0.05)。电针治疗组和模型组的CYP46含量均高于正常对照组,但其差异无统计学意义。结论:电针可降低APP/PS1小鼠海马Aβ1-42水平,其机制有可能是通过影响海马ApoE的水平从而实现的。
电针;阿尔茨海默病;β淀粉样蛋白;载脂蛋白E;胆固醇代谢
阿尔茨海默病(Alzheimer’s diseases,AD)是一种渐进性的中枢神经系统退行性疾病,目前尚未发现有效的治疗手段。中医针灸治疗脑病已有数千年的历史。β淀粉样蛋白(beta amyloid protein,Aβ)级联学说是当今比较公认的AD发病机制学说 。此学说认为AD发病的关键点是脑内Aβ水平的升高[1]。Aβ是由淀粉样前体蛋白(Amyloid protein precursor,APP) 水解产生的,病理状态下产生过量的Aβ,形成以Aβ沉积为核心的老年斑而致病,不仅如此,它的寡聚体和纤丝体形式还直接或间接的对神经元产生毒性作用[2],其中Aβ1~42是构成淀粉样斑块的核心蛋白[3]。
ApoE是1973年由Shore等[4]首先发现的一种富含精氨酸的碱性蛋白,人类ApoE基因位于19号染色体,含有299个氨基酸,分为3个亚型,即ε2、ε3和ε4[5]。流行病学和遗传学研究发现[6]ApoE4等位基因是目前公认的晚发性和散发性AD发病的重要危险因子[7]。目前大量研究表明,人体内淀粉样前体蛋白的分解与代谢即Aβ的产生受到ApoE基因多态性的影响,但ApoE作为一种可以在脑内合成的重要的载脂蛋白,它的一项重要的功能就是参与脑内胆固醇的转运,在脑内胆固醇代谢和神经系统发育及损伤修复过程中起着重要作用[8]。
脑是ApoE的第二大合成器官,ApoE在脑内负责脑内胆固醇和脂质蛋白的转运,实现细胞间的物质交换[9]。有研究表明ApoE结合脂质的部位与ApoE结合Aβ的部位相同,二者存在竞争关系[10]。实际上,大脑清除Aβ主要依靠的是脑实质细胞即星型胶质细胞和神经元细胞上的受体介导,因为脑内的Aβ大多数都是先与ApoE的受体相结合,然后再转运至细胞溶酶体内由蛋白水解酶进行降解,最后通过血脑屏障或细胞间液排出[11]。
对于正常人来说,24S-羟胆固醇可以穿过血脑屏障进入外周循环,是脑内胆固醇分解代谢的主要代谢产物[12],脑内胆固醇主要经胆固醇-24S-羟化酶(CYP46)转化为24S-羟胆固醇的形式转移至肝脏代谢排出体外,所以观察海马CYP46的水平可以反映海马的胆固醇的降解代谢[13]。
本课题组前期研究表明电针“百会”“涌泉”可以降低APP/PS1双转基因鼠海马Aβ水平,ApoE可以影响Aβ水平,所以猜测电针干预有效降低Aβ水平是通过影响海马ApoE的水平、调节胆固醇代谢、增加海马内Aβ的清除从而降低了Aβ的水平。因此本实验将观察电针“百会”“涌泉”对学习记忆中心-海马的ApoE、Aβ以及胆固醇的水平,探讨电针防治阿尔茨海默病的作用机制。
1 材料与方法
1.1 材料
1.1.1 实验动物模型及分组 本实验以SPF级APPswe/PS1dE9雄性4月龄小鼠为动物模型,在满4月龄时称重排序,运用随机数字表进行完全随机分组,将12只雄性APPswe/PS1dE9小鼠分为两组:电针组和模型组,每组6只,6只同月龄C57BL/6雄性小鼠为正常对照组。本实验通过北京中医药大学实验动物伦理委员会批准。
1.1.2 试剂和仪器 人Aβ42 ELASA试剂盒(美国,invitrogen,KHB3544);CYP46 试剂盒(MM-0667M1,酶免公司);ApoE2试剂盒(MM-0675M1,酶免公司);ApoE4试剂盒(MM-0676M1酶免公司);韩氏(HANs)LH202H型穴位神经刺激仪(北京华卫产业开发公司);一次性使用无菌针灸针(0.25 mm×13 mm,北京中研太和医药有限公司)。
1.2 治疗方法
电针组:以自制鼠袋将小鼠固定于实验操作台,按照小鼠标准针灸穴位图谱及动物解剖学方法,在小鼠顶骨正中取“百会”穴,在小鼠两足足底前、中1/3交界处取“涌泉”穴。本实验针具选用由北京中研太和医药公司生产的一次性针灸针,规格为0.25 mm×13 mm,穴位与针具进行常规消毒,进行针刺,针刺深度为2~3 mm,“百会” 穴运用手针,双“涌泉” 穴在小幅度捻转后接HANs电针仪,采用频率为1/50 Hz,强度0.5 mA的疏密波,以小鼠保持安静不挣扎嘶叫,针柄震颤为度。每次针刺持续15 min,每日1次,共治疗2周。
模型组以及正常对照组:以相同方法用自制鼠袋束缚15 min,每日1次,共束缚2周。
1.3 脑组织取材及相关指标ELISA检测
1.3.1 脑组织取材及ELISA样品制备 将每只小鼠予0.3%戊巴比妥钠(30 mg/kg)麻醉,脱颈后断头。开颅后,在冰上取海马,分别称取各组实验动物脑组织后放入各自的匀浆器中并进行编号,放置于冰上;按比例配制蛋白提取液:RIPA:PMSF=100∶1,按照10 mg组织加入100 μL提取液的比例进行配制,每次配制1 500 mL提取液;每个样品中需加入500 μL的蛋白提取液到匀浆器中;Aβ1-42ELASA样品制备需要在PMSF中加入8倍体积的5 mol盐酸胍、50 mmol Tris盐酸(pH 8.0)。在冰上进行匀浆器操作,将脑组织彻底研磨,在冰上孵育30 min,使组织细胞彻底裂解;4℃低温下离心5 min,转速为16000 rpm,离心后取上清液即所提取的蛋白转移至-80℃的冰箱保存。
1.3.2 ELASA检测 Aβ1~42检测:采用ELISA实验方法,用人Aβ1~42ELISA超敏试剂盒(96T,美国,invitrogen,KHB3544)对海马组织样品的Aβ1~42含量进行检测,具体操作步骤按照说明书操作,最后在450 mm处检测吸光度。将标准品按试剂盒的要求用标准稀释液稀释,制备标准曲线样品。标准品稀释后,立即置于冰上,待实验使用。根据样品稀释浓度计算小鼠海马组织的Aβ1~42浓度。
ApoE2水平的检测:采用ELISA双抗体夹心法,用小鼠ApoE2试剂盒(MM-0675M1酶免公司),具体操作步骤按照说明书操作,设置样品孔和标本孔。最后在450 mm处检测吸光度,根据样品稀释浓度计算小鼠海马组织ApoE2的浓度。
ApoE4水平的检测:采用ELISA双抗体夹心法,用小鼠ApoE4试剂盒(MM-0676M1酶免公司),具体操作步骤按照说明书操作,设置样品孔和标本孔。最后在450 mm处检测吸光度,根据样品稀释浓度计算小鼠海马组织的ApoE4的浓度。
CYP46水平的检测:采用ELISA双抗体夹心法,用小鼠CYP46试剂盒(MM-0667M1,酶免公司),具体操作步骤按照说明书操作,设置样品孔和标本孔。最后在450 mm处检测吸光度,根据样品稀释浓度计算小鼠海马组织的CYP46的浓度。
1.4 统计学分析

2 结果
2.1 电针对4月龄APP/PS1小鼠海马Aβ1~42水平的影响
见图1和表1。模型组海马Aβ1~42的含量显著高于正常对照组(P<0.01);电针组Aβ1~42的含量显著低于模型组(P<0.01)。

图1 电针对4月龄APP/PS1小鼠海马Aβ1~42水平的影响只小鼠/组)注:与模型组比较,▲▲P<0.01;与正常对照组比较,**P<0.01

组别nCYP46Aβ1~42正常对照组(C)6623.63±107.0611.93±5.02模型组(M)6567.65±130.7974.62±12.01▲▲电针组(EA)6583.11±145.5141.12±2.76**
注:与正常对照组比较,▲▲P<0.01;与模型组比较,**P<0.01
2.2 电针对4月龄APP/PS1小鼠海马ApoE2水平的影响
见图2和表2。模型组海马ApoE2的含量与正常对照组相比无统计学差异。电针组ApoE2的含量显著高于模型组(P<0.01),电针组ApoE2的含量显著高于正常对照组(P<0.01)。

图2 电针对4月龄APP/PS1小鼠海马ApoE2水平的影响只小鼠/组)注:与正常对照组比较,**P<0.01;与电针组比较,▲▲P<0.01

组别nApoE2ApoE4正常对照组(C)6144.37±12.75116.66±33.06模型组(M)6136.26±28.56▲▲94.96±38.19▲▲电针组(EA)6208.16±31.86**161.26±19.01*
注:与电针组比较,▲▲P<0.01;与正常对照组比较,**P<0.01,*P<0.05
2.3 电针对4月龄APP/PS1小鼠海马ApoE4水平比较
如图3和表2所示,模型组的ApoE4的含量低于正常对照组,但差异无统计学意义(P>0.05),电针组ApoE4的含量高于模型组的含量(P<0.01),电针组ApoE4的含量高于正常对照组(P<0.05)。

图3 电针对4月龄APP/PS1小鼠海马ApoE4水平的比较只小鼠/组)注:与电针组比较,**P<0.01;与正常对照组比较,▲P<0.05
2.4 4月龄APP/PS1小鼠海马CYP46水平的比较
如图4和表1所示,3组的CYP46水平,3组对比差异无统计学意义(P>0.05)。
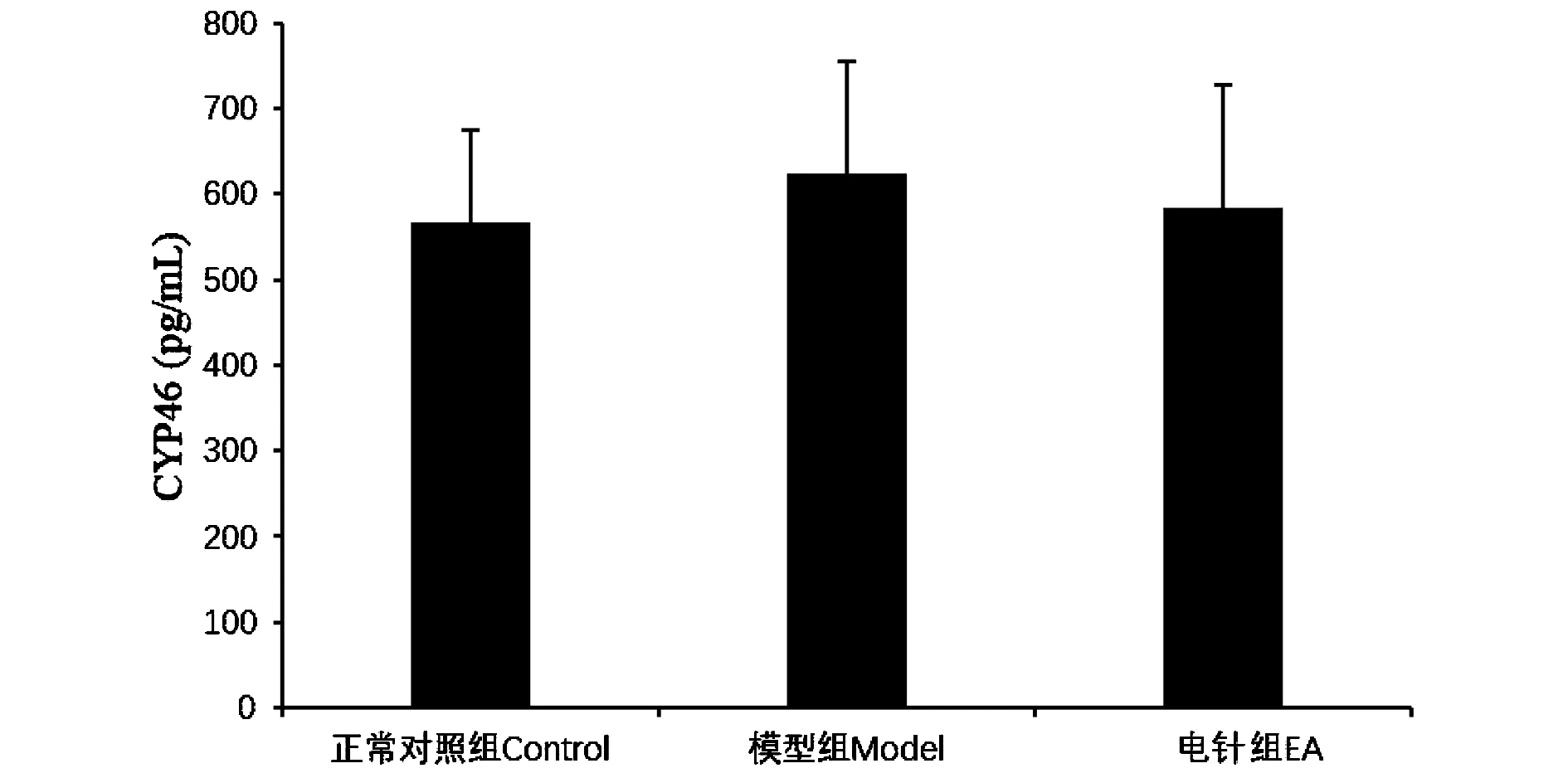
图4 4月龄APP/PS1小鼠海马CYP46水平的比较只小鼠/组)
3 讨论
Aβ级联学说认为Aβ的神经毒性以及沉积是AD发病的重要事件,正常情况下,Aβ在脑内的产生和清除存在动态平衡[14]。体外研究表明ApoE可以与Aβ结合,且结合具有型差异性:E2>E3>E4,并且Aβ的沉积量与ApoE成剂量依赖关系,在apoE(-/-)的老年性痴呆小鼠中转入人的apoE后,脑内 Aβ的沉积量减少,其机制可能是在LRP-1的参与下与ApoE结合的Aβ由于构型的改变,毒性下降,摄取和降解增多[15]。关于ApoE影响Aβ水平的机制, ApoE可以和Aβ结合成可溶性的复合物,从而调节Aβ的代谢、聚集和沉淀[16],ApoE在Aβ形成与清除过程中充当载体或分子伴侣,ApoE在细胞外与Aβ相互作用,从而导致Aβ的清除[17,18]。本研究结果电针能够增加APP/PS1小鼠海马组织内ApoE的水平,ApoE2和ApoE4相比都有提高,提高的含量没有体现分型差异;电针降低Aβ水平,提示电针能够促进ApoE和Aβ结合成可溶性复合物,从而促进Aβ的清除,减少其沉积。模型组ApoE和CYP46的水平与正常对照组相比没有统计学差异,提示该模型在进行基因双转后,暂时没有发现对4月龄小鼠ApoE和脑内胆固醇的水平造成影响。
近年研究提示脑内胆固醇的水平与Aβ水平密切相关,神经元膜胆固醇水平的改变和胆固醇在亚细胞结构中的分布被认为与Aβ的形成、异常聚集、神经毒性以及降解有着潜在联系[19-20]。最近的研究表明AD病人脑内出现胆固醇代谢紊乱,ApoE在脂蛋白颗粒和胆固醇代谢中起重要的作用,由于完美的血脑屏障阻止外周的胆固醇进入脑内,绝大多数脑内的胆固醇都是自身合成的[21]。大多数突触生成需要的胆固醇来自星形胶质细胞的大量合成,并且由含ApoE的脂蛋白运输到神经元,由ApoE介导的胆固醇回收功能受损会导致胆固醇在溶酶体的积累和降低质膜胆固醇的回收效率[22]。有研究表明[23]脑内胆固醇水平的增加提高了β和γ分泌酶的活性,促进Aβ的生成以及沉积。脑组织中如果胆固醇代谢出现紊乱,胆固醇会在组织内堆积,从而刺激β-分泌酶、γ-分泌酶活性以至于β-淀粉样蛋白的大量产生[24]。本研究结果并未体现电针对APP/PS1双转基因小鼠海马组织内胆固醇含量及代谢水平的影响,造成的原因可能是样本量小或者电针不能影响海马胆固醇水平。
ApoE在神经元修复和再生中起重要作用,于是越来越多的专家学者开始致力于研究ApoE蛋白亚型与ApoE受体的联合作用对淀粉样前体蛋白分解过程产生的影响[25]。有实验证明ApoE与APP的代谢有直接关系,培养基加入ApoE后,可引起Aβ分泌的减少[15]。ApoE通过竞争性结合Aβ,与LRP1、其他受体/转运体的结合,阻断Aβ的细胞摄取和转运的过程,从而降低脑内Aβ的水平[26]。近年针灸治疗老年痴呆的临床报告均显示出了针灸疗法对于防治AD的肯定疗效,本课题组研究阿尔茨海默病在以肾精亏虚为本,瘀血、毒邪、痰浊三浊互结为标的病理机制指导下,以“益肾、醒脑、祛浊”为治疗准则,运用电针治疗,取“百会”“涌泉”穴,两穴合用,既可补肾益髓,又可行气活血、化瘀祛浊通络、开窍醒神[27]。
本课题组自2012年起对电针干预APP/PS1双转基因小鼠,APPswe/PS1dE9双转基因小鼠是目前国际公认的影响Aβ水平的有效评价动物模型[28],现阶段该动物模型广泛运用于AD的治疗药物以及治疗方式的科学研究[29]。对改善小鼠学习记忆能力的淀粉样蛋白途径作用机制进行研究,初步肯定电针“百会、涌泉”穴对APP/PS1双转基因小鼠脑组织内Aβ整体水平的降低具有调节趋势。本次研究选用4月龄APP/PS1双转基因小鼠,进行为期2周的电针治疗,电针干预的介入时间选择未出现老年斑的AD早期,在小鼠4月龄时,早期电针干预可以降低海马内Aβ1~42的水平,同时提高了海马内ApoE2和ApoE4的水平,但CYP46的水平没有发生改变。综上所述在AD早期,Aβ生成增多,这时通过电针针刺“百会”“涌泉”使得小鼠海马ApoE的水平升高。ApoE的水平升高可以增加脑内Aβ的清除,从而降低Aβ的含量。所以提高脑内ApoE的水平,调节ApoE受体和转运体的水平和活性可能成为AD的防治手段。故ApoE可能为电针防治AD的一个靶点,本实验为针刺“益肾祛浊法”防治AD提供科学实验依据。
本研究下一步将扩大实验样本量,继续探讨不同的ApoE分型在AD中发挥的不同作用以及电针是否会对海马胆固醇代谢水平产生影响,并且测定CYP46的同时直接测定海马的总胆固醇水平。
4 结论
电针可降低4月龄APP/PS1双转基因小鼠海马Aβ水平,其机制可能是通过影响脑内ApoE的水平从而实现的,但电针是否影响了海马内的胆固醇代谢水平,还需进一步的实验研究。
[1] Rosenkranz SC,Geissen M,Härter K,et al.Amyloid-precursor-protein-lowering small molecules for disease modifying therapy of Alzheimer’s disease[J].PLoS One,2013,8(12):e82255
[2] Chen Y,Durakoglugil MS,Xian X,et al.ApoE4 reduces glutamate receptor function and synaptic plasticity by selectively impairing ApoE receptor recycling[J].Proc Natl Acad Sci USA,2010,107(26):12011-12016
[3] Meraz-Rios MA,Franco-Bocanegra D,Toral Rios D,et al.Early onset Alzheimer’s disease and oxidative stress[J].Oxid Med Cell Longev, 2014,14:375-968
[4] Simonovitch S,Schmukler E,Bespalko A,et al.Impaired Autophagy in APOE4 Astrocytes[J].Journal of Alzheimer's Disease Jad,2016,51(3):915-927
[5] De Chaves EP,Narayanaswami V.Apolipoprotein E and cholesterol in aging and disease in the brain[J].Future Lipidol,2008,3(5):505-530
[6] Holtzman DM,Hez J,Bu G.Apolipoprotein E and Apolipoprotei E Receptors: Normal Biology and Roles in Alzheimer Disease[J].Cold Spring Harbor Perspectives in Medicine,2012,2(3):a006312
[7] Xuesong Chen,Liang Hui,Jonathan D.Geiger Role of endolysosomes and cholesterol in the pathogenesis of Alzheimer’s disease: Insights into why statins might not provide clinical benefit[J].Austin J Pharmacol Ther,2014,2(6):1035
[8] Mattsson N,Zetterberg H,Bianconi S,et al.Gamma-secretase-dependent amyloid-beta is increased in Niemann-Picktype C:a cross-sectional study[J].Neurology,2011,76(4):366-372
[9] 彭羽瑶,张浩然,易明玉,等.ApoE与β淀粉样蛋白在阿尔茨海默病中相互作用的研究进展[J].现代生物医学进展,2017(2):396-400
[10] Yoon SY,Kim DH.Alzheimer's disease genes and autophagy[J].Brain Research,2016,1649:201-209
[11] Li L,Zhang S,Zhang X,et al.Autophagy enhancer carbamazepine alleviates memory deficits and cerebral amyloid-β pathology in a mouse model of Alzheimer's disease[J].Cur Alzheimer Res,2013,10(4):433-441
[12] Russell DW,Halford RW,Ramirez DM,et al.Cholesterol 24-hydroxylase: an enzyme of cholesterol turnover in the brain[J].AnnuRev Biochem,2009,78:1017-1040
[13] 胡敏予,毛敏,郭颖,等.脑胆固醇代谢对阿尔茨海默病的影响研究进展[J].中国现代医学杂志,2011(35):4426-4434
[14] Guo XH,Lu H,Niu RN,et al.Detection of serum matrix metalloproteinase 2 and 9 in patients with Alzheimer disease[J].J Zhengzhou Univ(Med Sci),2014,49(1):137-139
[15] 刘宇,王燕,汪华侨.胆固醇代谢与阿尔茨海默病关系的研究进展[J].国际内科学杂志,2007,34(5):301-311
[16] 董翔,常庚,赵莉,等.截断型ApoE对β-淀粉样蛋白代谢的影响[J].中国老年学杂志,2017(7):1621-1623
[17] Gavrilova SI,Kolykhalov IV,Korovaitseva GI,et al.ApoE genotype and efficacy of neurotrophic and cholinergic therapy in Alzheimer’s disease[J].Zhurnal Nevrologii L Psikhiatrii Imeni SS Korsakova,2005,105(4):27
[18] Meraz-Rios MA,Franco-Bocanegra D,Toral Rios D, et al. Early onset Alzheimer’s disease and oxidative stress[J].Oxid Med Cell Longev,2014,14:375-968
[19] Hashimoto T,Serrano-Pozo A,Hori Y,et al.Apolipoprotein E,especially apolipoprotein E4,increases the oligomerization of amyloid β peptide[J].J Neurosci,2012,32(43):15181-15192
[20] Philip B.Verghese,ApoE influences amyloid-beta (A beta) clearance despite minimal ApoE/A beta association in physiological conditions[J].Journal Article,2013,110(19):1807-1816
[21] 姚恺,祖恒兵.脂代谢紊乱在阿尔茨海默病发病机制中的作用[J].神经解剖学杂志,2015(2):261-264
[22] 王强,姜希娟.外周及中枢胆固醇代谢与阿尔茨海默病的关系[J].现代中西医结合杂志,2010(18):2323-2325
[23] 张万东.胆固醇代谢紊乱与阿尔兹海默氏老年性痴呆[C]//第五届海内外华人神经科学家研讨会论文集.长沙:中国生理学会,中国生物物理学会,中国神经科学学会,中华医学会,2008:487-503
[24] Lee JE,Han PL.An update of animal models of Alzheimer disease with a reevaluation of plaque depositions[J].Exp Neurobiol,2013,22(2):84-95
[25] 朱洪山,晏勇.脂质代谢在阿尔茨海默病发病机制中的研究进展[J].重庆医学,2009(3):347-350
[26] 黄高雅,王德生,汤颖.载脂蛋白E与阿尔茨海默病相关性研究进展[J].中国临床神经科学,2016(1):102-108
[27] 薛中华.补肾填髓法为主治疗老年性痴呆疗效体会[J].中华中西医学杂志,2009,7(7):36
[28] Chin J.Selecting a mouse model of Alzheimer's disease[J].Methods Mol Biol,2011,670:169-189
[29] Webster SJ,Bachstetter AD,Van Eldik LJ.Comprehensive behavioral characterization of an APP /PS-1 double knock-in mousemodel of Alzheimer's disease[J].Alzheimers Res Ther,2013,5(3):28
EffectofElectro-acupunctureStimulationofGV20andKI1onExpressoinsofHippocampalAβandApoEinAPP/PS1TransgenicMice
ZHANG Xue-ting, ZHANG Lei, ZHOU Ying-yi, PEI Ya-ni, XUE Wei-guo△
(BeijingUniversityofChineseMedicine,Beijing100029,China)
Objective:To observe the effect of electro-acupuncture on the levels of apolipoprotein E(ApoE) and Amyloid-β(Aβ) of hippocampus in 4-month-old APP/PS1 transgenic mice, and to explore the mechanism of acupuncture in the prevention of AD.Methods12 APP/PS1 transgenic mice (male, 4-month-old) were randomly divided into the model group and the electro-acupuncture group.Six C57BL/6 mice with same age were used as the blank control. In the electro-acupuncture group, the intervention was needling points of GV20 and KI1; whereas, in the control group, the mice were given equivalent constraint; the intervention was 15min per day for two weeks. The levels of Aβ1-42, ApoE2, ApoE4 and cholesterol-24S-hydroxylase(CYP46) in hippocampus were measured with ELASA method.ResultsIn terms of the content of Aβ1-42, it was higher in the model group than that in the blank control group(P<0.01); it was lower in the electro-acupuncture group than that in the model group(P<0.01). In terms of the the content of ApoE2 and ApoE4, there was no significant difference between the model group and the blank control group; they were highly increased in the electro-acupuncture group compared to those in the model group(P<0.05). In terms of the content of CYP46, it was higher both in the electro-acupuncture group and in the model group, compared to the blank control group; but the difference was not statistically significant.ConclusionElectro-acupuncture can reduce the level of hippocampal Aβ1-42 in APP/PS1 mice, and its mechanism may be associated with affecting the level of hippocampal ApoE.
Electro-acupuncture; Alzheimer’s diseases; Amyloid-β; ApoE; Cholesterol metabolism
R246.6
A
1005-0779(2017)12-0073-04
国家自然科学基金项目,编号:81273826;北京中医药大学研究生自主课题,编号:2017-JYB-XS-O49。
张学婷(1989-),女,2015级针灸推拿学专业硕士研究生。
△通讯作者:薛卫国(1968-),男,教授,主任医师,博士研究生导师,主要从事阿尔茨海默病机制研究。
2017-08-03

