SO2活化改性石油焦吸附剂的汞吸附特性
王晨平,段钰锋,佘敏,朱纯,杨志忠
(1东南大学能源热转换及其过程测控教育部重点实验室,江苏 南京 210096;2东方电气集团东方锅炉股份有限公司技术中心,四川 自贡 643001)
SO2活化改性石油焦吸附剂的汞吸附特性
王晨平1,段钰锋1,佘敏1,朱纯1,杨志忠2
(1东南大学能源热转换及其过程测控教育部重点实验室,江苏 南京 210096;2东方电气集团东方锅炉股份有限公司技术中心,四川 自贡 643001)
利用SO2气体对石化工业副产物石油焦进行活化改性以制成富硫高活性脱汞吸附剂(SAPC)。在固定床实验装置上进行SAPC吸附脱除汞的实验研究,考察吸附温度、入口Hg0浓度、烟气成分以及热再生等因素对脱汞特性的影响规律,同时结合比表面积及孔隙度分析、元素分析和X射线光电子能谱(XPS)等表征手段深入分析SAPC的汞吸附机理。结果表明,SO2活化改性石油焦的物理和化学特性得到极大改善,羰基、酯基以及非氧化态硫是Hg0的主要活性吸附位。吸附温度的升高会抑制对Hg0的吸附脱除,烟气中较高的Hg0浓度会降低汞脱除效率,但对其汞吸附速率有促进作用。SO2对SAPC的脱汞性能影响较小,O2易将Hg0氧化成为更容易与含氧、含硫官能团结合的氧化态汞,从而促进对Hg0的脱除。热再生时吸附态汞化合物受热分解的过程伴随着吸附剂表面化学活性位的损失,导致再生后汞吸附性能大幅下降。
石油焦;汞吸附;二氧化硫;硫形态
引 言
重金属汞作为燃煤烟气中的第四大污染物,由于其剧毒性、大气迁移性、生物累积性和高隐蔽潜伏性,对自然环境和人类健康的严峻危害已受到广泛关注[1]。烟道活性炭喷射技术被认为是目前最具前景的燃煤汞脱除技术,但其高昂的运行成本使得该项技术在工业应用上受到极大限制[2]。显然,开发廉价高效的替代吸附剂,尤其是利用工业副产物作为脱汞吸附剂,是发展我国燃煤工业高效低成本脱汞应用技术的重要研究方向。
石油焦是炼油工业中产生的如石油沥青和渣油等碳氢化合物经延迟焦化后得到的副产品。随着进口高硫原油和重质劣质油产量的不断增加,目前我国石油焦正处于资源过剩的阶段[3],其高效、清洁利用已成为能源科学领域迫切需要解决的关键问题。石油焦碳含量高、价格低廉,通过活化改性等方法能够成为制备脱汞吸附剂的优质原料[4]。赵可等[5]研究发现利用高压水热活化石油焦可以丰富其孔隙结构,结合 CuCl2溶液改性后脱汞效率接近100%,这是因为Hg0首先物理吸附在石油焦的表面及孔道中,然后被活性组分 CuCl2氧化为 HgCl2。洪亚光等[6]以Na2S与NH4Br溶液对高硫石油焦进行活化、改性以制成载溴富硫活性炭,并在模拟烟气管道喷射实验装置上进行了脱汞实验研究,结果表明,表面含硫官能团与溴活性因子的共同作用使高硫石油焦表现出较强的汞吸附脱除能力。可见,利用石油焦制备定向脱汞吸附剂具备一定的可行性,但由于其本身石墨化程度较高,结构非常紧致[7],因此探究经济有效的活化方法是国内外学者共同研究的课题。
SO2作为当前最为严重的空气污染源之一,不仅对人体健康造成危害,也是产生酸雨的主要因素[8]。目前含SO2废气主要来源于燃煤烟气、金属冶炼以及石油化工,其中有色金属矿物多以硫化物形态存在,冶炼烟气中SO2浓度可达20%~30%[9]。高浓度的含SO2废气给烟气的净化处理带来较大困难,Stacy等[10]研究发现,SO2在温度高于650℃时能够被C 迅速还原生成元素硫,工业上利用煤或焦炭等还原含硫废气中的SO2以制备硫磺,并发现还原剂中硫元素含量有所提高。因此,Asasian等[11]在700℃温度下采用SO2对活性炭恒温改性1 h,研究发现活性炭表面硫元素含量高达11%,脱汞效率比原始活性炭高出近50%。多伦多大学Charles教授的团队[12-15]研究利用50%的SO2气体在700℃高温下对高硫油砂流化焦进行活化改性,制备获得比表面积为400 m2·g-1以上的吸附剂,且表面含硫官能团数量明显增多,但未对其汞吸附性能进行深入性探究。
基于以上研究基础,本文利用SO2对工业副产物石油焦进行活化改性以制备富硫高活性脱汞吸附剂,并在小型固定床实验装置上考察其汞吸附性能,探究吸附温度、入口Hg0浓度、烟气成分以及热再生对脱汞性能的影响规律,结合 N2吸附/脱附、元素分析以及X射线光电子能谱等表征,通过程序升温脱附实验对吸附剂表面汞吸附形态进行分析,探明SO2活化改性石油焦吸附剂的汞吸附机理。不仅为研发廉价高效的喷射脱汞吸附剂打下基础,同时也能够实现对石油焦这一副产物的高附加值资源化利用,缓解我国SO2废气的治理压力。
1 实验材料和方法
1.1 吸附剂制备及表征
实验选取天津石化延迟焦为原料,其工业分析和元素分析如表1所示。表1分析结果表明,原始石油焦(raw petroleum coke,RPC)固定碳含量高达81.86%,硫含量≥4%,属于高硫石油焦。

表1 石油焦工业分析和元素分析Table 1 Proximate and ultimate analysis of petroleum coke
SO2活化改性过程如下:经破碎筛分,获得0.05~0.11 mm粒径范围内的RPC;首先称取2 g RPC样品放入石英反应管中并置于PID控制程序升温管式炉内,在高纯 N2气氛的保护下,管式炉以15℃·min-1的升温速率从室温升至700℃;随后切换SO2气氛使石油焦在700℃、50%(体积)SO2气氛的条件下恒温活化改性2 h;最后将SO2气氛切换为 N2并停止加热,待管式炉冷却至室温后取出样品,得到SO2活化改性石油焦吸附剂(SO2activated petroleum coke,SAPC),保存于干燥皿中待用。
本文采用 BEL SORP Ⅱ型比表面及孔隙度分析仪(BEL 公司,日本)表征分析吸附剂的比表面积和孔隙结构;采用Vario EL Cube型元素分析仪(Elementar,德国)测定吸附剂内部的元素含量;采用ESCALAB250Xi型X射线光电子能谱分析仪(Thermofisher Scientific,美国)对吸附剂表面含氧官能团和硫形态进行表征。
1.2 实验装置
在小型固定床汞吸附实验装置(如图 1)上进行石油焦吸附剂吸附脱除Hg0的实验研究,分析讨论吸附温度、入口汞浓度、烟气成分以及热再生对汞吸附的影响及其机制。实验过程中,200 ml·min-1的高纯载汞N2通过汞渗透管(VICI Metronics,美国)后携载适量的汞蒸气进入预混室,与平衡 N2混合预热形成总气体流量 2 L·min-1的含汞模拟烟气穿过固定床反应器与吸附剂进行吸附反应;实验中预热温度和吸附温度保持一致,固定床吸附反应器为内径8 mm的高硼硅玻璃管,内置吸附剂质量为25 mg,吸附剂床层高度约为2 mm,吸附后的含汞尾气经活性炭净化处理后排空。采用VM3000在线烟气汞分析仪(Mercury Instrument,德国,检测限:0.1 μg·m-3)测定吸附剂使用前后固定床吸附反应装置的出口烟气汞浓度,并采用汞穿透率η和单位质量累积汞吸附量q评价吸附剂的脱汞性能

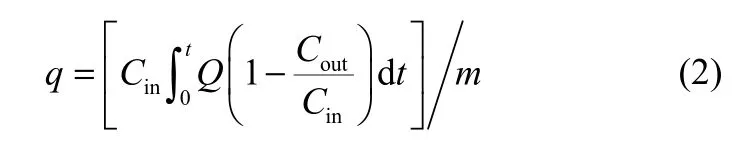
式中,Cin为入口 Hg0汞浓度,μg·m-3;Cout为出口 Hg0汞浓度,μg·m-3;Q为气体体积流量,m3·min-1;t为吸附时间,min;m为吸附剂质量,g。
2 实验结果与讨论
2.1 孔结构参数和元素分析
表2所示为SO2活化改性前后石油焦吸附剂的孔结构特征。活化改性前,RPC的比表面积仅为6.2464 m2·g-1,几乎不存在孔隙结构。经活化改性后,SAPC的孔隙结构得到极大改善,BET比表面积达到 347.98 m2·g-1,总孔容积达到 0.1864 cm3·g-1,其中微孔容积比高达76.07%,呈现出微孔吸附剂的特征。SO2高温活化改性过程中,一方面石油焦内部组分在高温下受热分解并向外析出 CO2、CH4、SO2、水蒸气等气体产物,从而在其内部形成微小气孔[16];另一方面在 700℃高温时,SO2会与石油焦内部活性的C原子发生碳热还原反应[17]
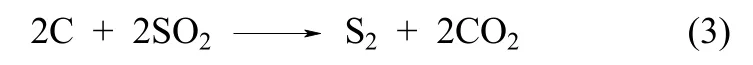
反应生成的 CO2气体以及 S2蒸气均会从石油焦内部析出,从而形成丰富的孔隙结构[18-19],这是活化后石油焦孔隙结构获得大幅改善的主要原因。
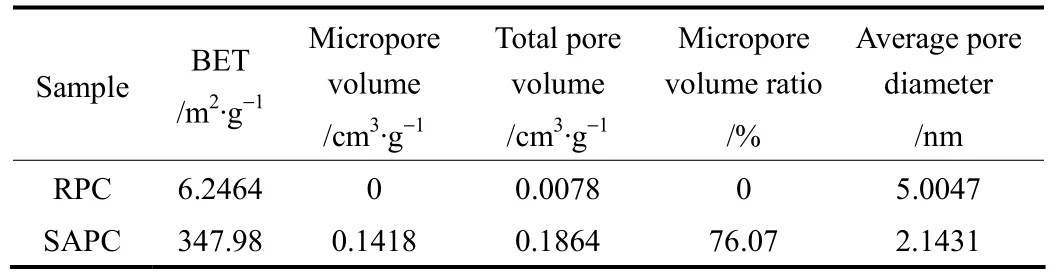
表2 石油焦孔结构特性分析Table 2 Pore structure analysis of petroleum coke
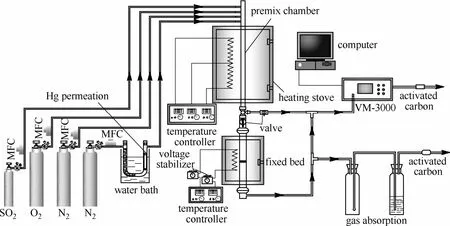
图1 固定床汞吸附实验系统Fig.1 Schematic diagram of fixed-bed Hg adsorption reactor system
表3所示为SO2活化改性石油焦吸附剂SAPC的元素分析,与表1中RPC相比,SAPC的碳含量减少为 73.13%,而硫、氧元素含量分别增加至18.49%、6.24%。Smaniotto等[20]研究发现,高温时SO2首先与碳表面不饱和活性位结合,迅速被还原形成化合物,导致石油焦表面硫、氧含量增多。Humeres团队[21-22]提出了详细的C-SO2反应机制,如图 2(a)所示,认为在预稳定阶段 SO2与双键反应生成中间产物1,3,2-二氧硫杂环戊烷(Ⅰ)和 1,2-氧硫杂环丁烯 2-氧化物(Ⅱ);中间产物Ⅰ分离出的S原子易与临近双键反应形成环硫化物(Ⅲ),同时释放出 CO2。当 C-SO2反应系统达到平衡阶段时,环硫化物、二硫化物、三硫化物是碳结构中硫的主要存在形态,图2(b)所示为其相互转化的主要反应机制,环硫化物(Ⅲ)能够与单个S原子结合并生成二硫化物(Ⅳ);二硫化物(Ⅳ)后续可分解产生硫分子S2和双键;同时环硫化物(Ⅲ)也能够与硫分子S2结合,形成三硫化物(Ⅴ);三硫化物(Ⅴ)可失去1个硫原子或硫分子S2形成二硫化物(Ⅳ)或环硫化物(Ⅲ);C-SO2系统通过不断捕获/释放硫原子或硫分子以形成环硫化物-二硫化物-三硫化物的动态循环。
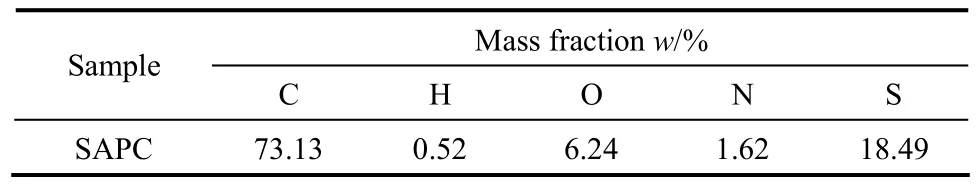
表3 SO2活化改性石油焦的元素分析Table 3 Elemental analysis of SO2 activated petroleum coke
2.2 XPS分析
采用 XPS方法对活化改性前后石油焦吸附剂的表面化学特性进行定性和定量分析。根据XPS原理,按照 2p3/2和 2p1/2劈裂峰分峰方法(设置两峰面积比约为2:1,裂距为1.18 eV,半峰宽及L-G%值相同)对SO2活化改性前后石油焦的S 2p谱图进行分峰拟合[23],其结果如图3所示。经SO2高温活化改性后,SAPC表面硫形态较为复杂,在结合能为162.04、164.06、164.35、167.35和168.88 eV处均出现硫峰,分别对应二硫化物硫化物(R-S)、亚砜(R-SO)、砜(R-SO2)和硫酸盐其中砜和硫酸盐属于氧化态硫,二硫化物、硫化物和亚砜属于非氧化态硫[24]。噻吩(Sth)和元素硫(S0)的结合能也均在164.00 eV左右,与硫化物相互重叠,难以区分。研究表明[16],噻吩是一种结构稳定的有机硫,900℃高温才会分解,RPC中硫绝大部分以噻吩的形态存在。由三硫化物释放出的元素硫(S2)在 700℃高温时会以硫蒸气的形态进入气相发生逃逸,因此SAPC中几乎不存在以元素硫的形式担载于孔隙结构内的硫分子[11]。
碳材料中有机氧的存在形式与碳原子密切相关,对石油焦吸附剂C1s谱图进行分峰拟合获得其表面含氧官能团分布特征,其结果如图4所示。原始石油焦RPC表面含氧官能团主要为C—O(285.50 eV)和羰基(286.50 eV)两种形态;经SO2活化改性后,羰基所对应的碳峰明显增强,且在288.50 eV处出现新的碳峰,对应官能团为COOH/C(O)—O—C(羧基/酯基)[25]。Stacy 等[10]认为C-SO2反应过程中伴随着O原子的转移,类似于CO2与C的反应,因此高温时O原子可能会与不饱和碳位结合形成一定数量的含氧官能团。
根据图3和图4的分峰拟合结果,表4列出了SO2活化改性前后石油焦吸附剂表面各形态硫以及含氧官能团的绝对含量。
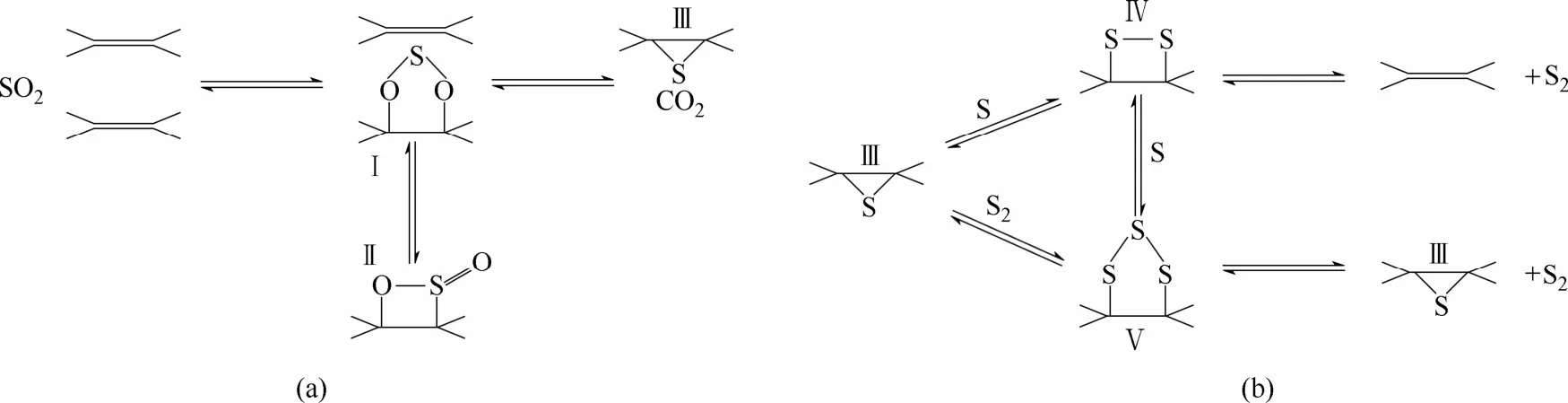
图2 C-SO2反应机理Fig.2 Reaction mechanism of C-SO2
分析发现,原始石油焦RPC表面的硫主要以噻吩和硫酸盐两种形态存在,其中噻吩相对含量高达95.08%。SO2活化改性后,SAPC表面硫形态以非氧化态为主,C-SO2反应生成的环硫化物热稳定较高,因此在结合能为164.06 eV处,除原始石油焦中本身赋存的噻吩外,明显出现较多的硫化物[21];二硫化物的热稳定性较差,含量较少。研究发现[26],高温条件下高价态硫易发生脱氧反应形成低价态硫,即砜可能会向硫化物或亚砜转化,因此在 700℃时砜型硫的含量相对较少。硫酸盐含量略微增加,可能是由于气相中的SO2与石油焦灰分中的金属元素等结合形成了硫酸盐沉积在石油焦表面[16]。比较SO2活化改性前后石油焦表面含氧官能团的绝对含量,可以看出相比于RPC,SAPC表面含氧官能团较为丰富,其中羰基和酯基能够为Hg0的吸附脱除提供化学活性位。
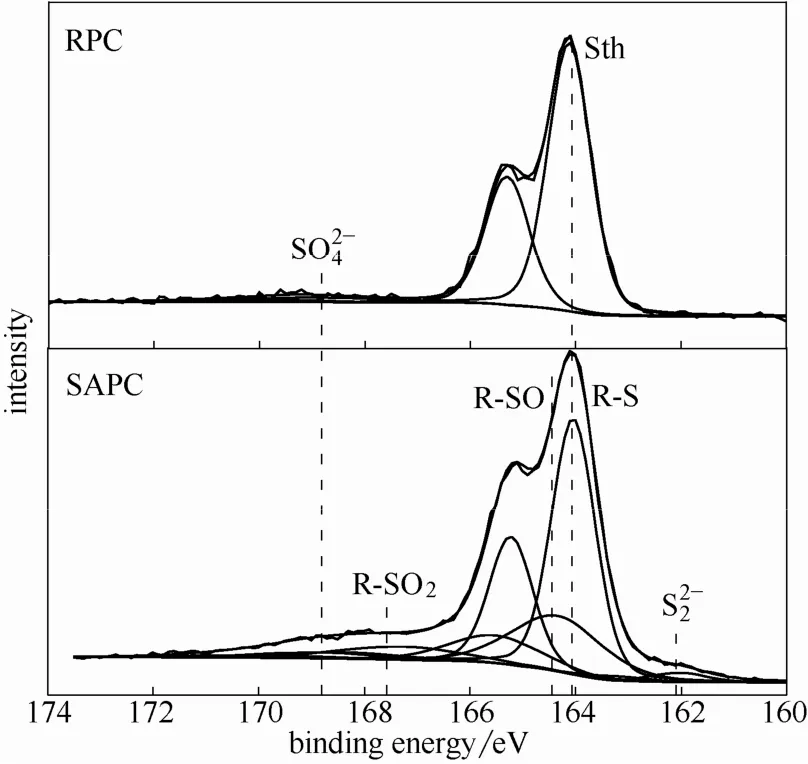
图3 石油焦S 2p谱图Fig.3 S 2p spectrum of petroleum coke
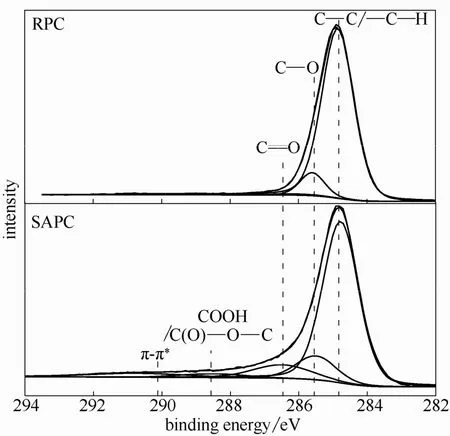
图4 石油焦C1s谱图Fig.4 C1s spectrum of petroleum coke
2.3 固定床汞吸附特性
2.3.1 SO2活化改性对石油焦汞吸附性能的影响图5所示为固定床入口Hg0浓度35 μg·m-3,吸附温度150℃条件下原始石油焦RPC及SO2活化改性石油焦SAPC的汞穿透率随时间变化曲线。如图所示,RPC汞穿透率接近90%,几乎没有汞吸附能力。这是由于RPC本身石墨化程度较高,结构紧致,物理吸附性能微弱;此外,含氧官能团数量较少且硫元素主要以结构稳定的噻吩形态为主,其表面与 Hg0分子间的相互作用力较弱。活化改性后的石油焦吸附剂SAPC的汞吸附脱除能力相比于RPC得到大幅提升,初始吸附效率达到 100%。一方面归功于SAPC孔隙结构的大幅改善,丰富的微孔结构有效促进了吸附剂对气相中Hg0的捕获脱除;另一方面,SO2活化改性后,SAPC中硫元素含量高达18.49%,表面富集了大量含硫官能团,能够将烟气中的气相汞以HgS的形式固定在吸附剂碳表面,其吸附反应式如下[27]
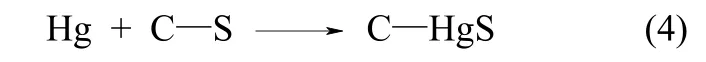
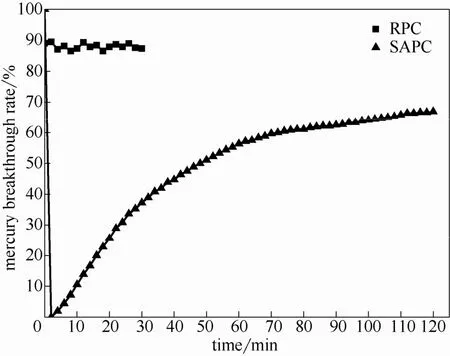
图5 原始及SO2活化改性石油焦汞穿透率Fig.5 Mercury breakthrough rate of raw and SO2 activated petroleum coke
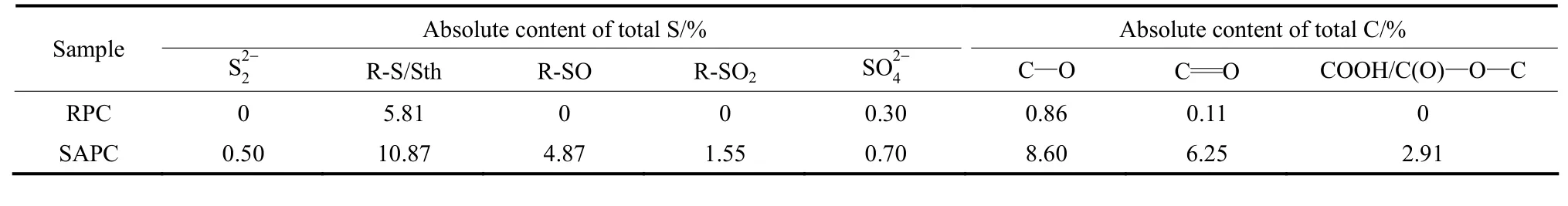
表4 石油焦表面硫形态及含氧官能团Table 4 Sulfur forms and oxygen functional groups of petroleum coke
研究发现[28],硫原子本身至少有一对孤电子与Hg0相互作用形成共价键,或者作为初始附着点以实现对Hg0的氧化和脱除。硫酸盐、砜等氧化态硫价态高,所有电子对均被占满,因此对Hg0的吸附脱除作用较弱;而硫化物等非氧化态硫因其本身具有未配对的孤对电子,与Hg0相互作用较强。此外活化改性后SAPC表面羟基、羰基、酯基、羧基等含氧官能团数量明显增多。Zhang等[29-30]认为酯基和羰基具有较强的氧化性,能够促进对Hg0的氧化吸附;Liu等[31]认为酯基和羰基并不直接提供活性位点,而是增加其邻近活性位点的活性以促进对Hg0的化学吸附。因此,在孔隙结构、硫含量及其形态分布和表面含氧官能团的共同影响作用下,SO2活化改性石油焦吸附剂SAPC的汞吸附效率明显提升。
2.3.2 吸附温度对汞吸附性能的影响 图6所示为固定床入口 Hg0浓度(35.0±0.5)μg·m-3,不同吸附温度条件下的汞穿透率和累积汞吸附量随时间变化曲线。可以看出,吸附温度越高,SAPC的脱汞效率越低,汞穿透速率越快,累积汞吸附量增长速率越慢。首先,随着吸附温度的升高,依靠范德华力的物理吸附发生汞的逆向解吸导致吸附剂的物理吸附性能下降。其次,研究表明[32],S与Hg0之间的反应高度放热,其平衡常数随着温度的升高急剧下降,反应温度升高会使反应平衡逆向移动,HgS分解增强。再次,Sun等[33]研究发现羰基官能团对Hg0的吸附作用会在吸附温度高于 130℃的情况下受到较大抑制。因此,高温时石油焦吸附剂的物理吸附和化学吸附作用均会受到抑制,导致其脱汞能力的降低,而低温更有利于对Hg0的吸附脱除。
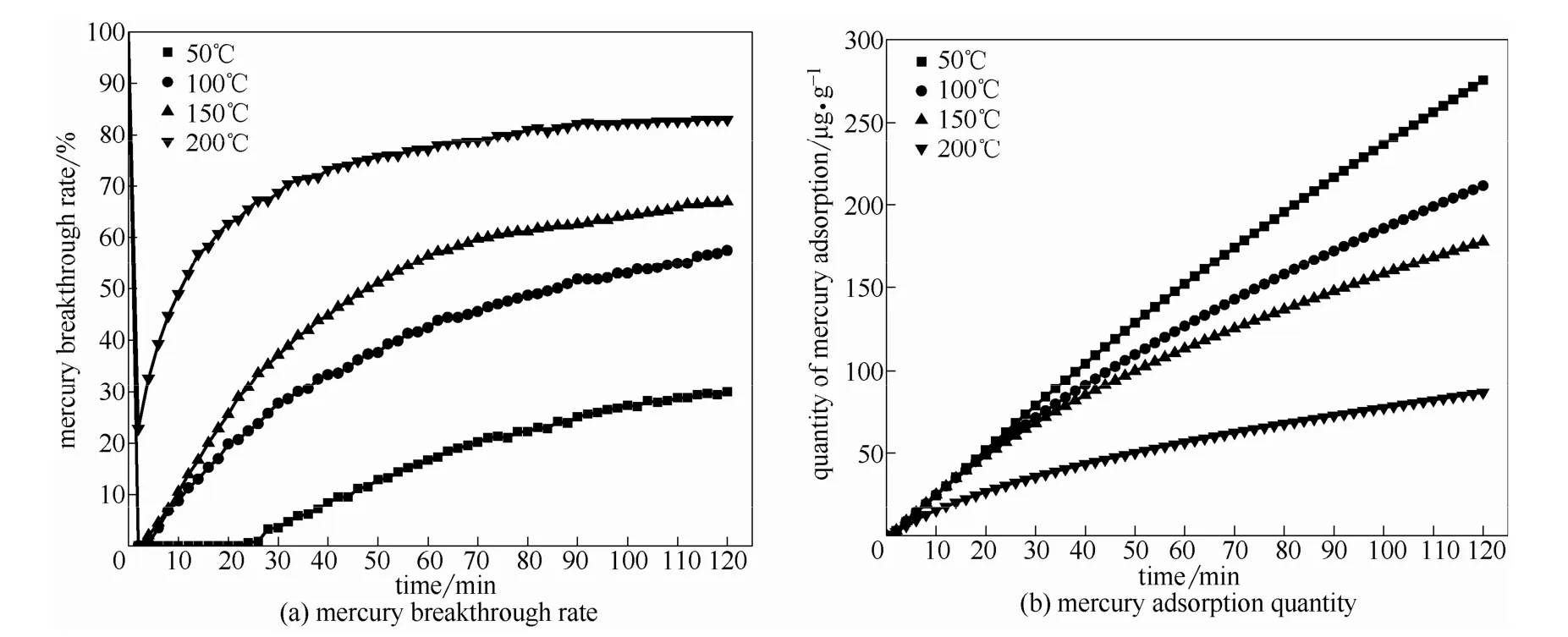
图6 吸附温度对汞脱除性能的影响Fig.6 Effect of adsorption temperature on mercury removal
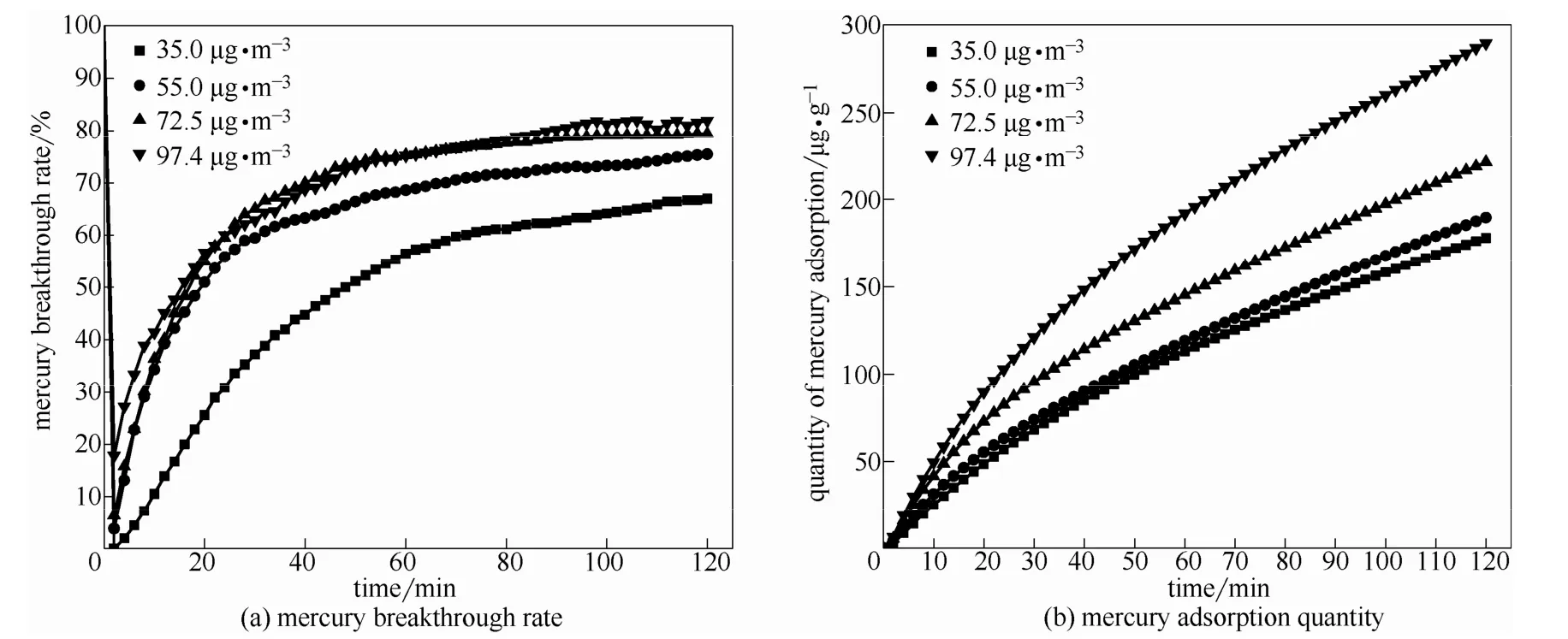
图7 入口Hg0浓度对汞脱除性能的影响Fig.7 Effect of inlet Hg0 concentration on mercury removal
2.3.3 入口汞浓度对汞吸附性能的影响 图 7(a)为固定床吸附温度150℃,入口Hg0浓度分别为35.0、55.0、72.5、97.4 μg·m-3条件下的汞穿透率随时间变化曲线。如图所示,在吸附初始阶段,模拟烟气中的Hg0浓度越高,SAPC的初始汞脱除率越低,并且整体汞脱除效果也受到限制。这可能是因为实验中吸附剂用量过少,C/Hg比较低,且空速过大,短时间内吸附剂表面活性位被占满,烟气中部分 Hg0还未参与吸附反应就快速穿透过吸附层。图7(b)所示为不同Hg0浓度下单位质量累积汞吸附量随时间变化曲线,曲线上任意点的切线斜率为对应该时刻的汞吸附速率,从图中可以看出,模拟烟气Hg0浓度的增加可以明显提升SAPC的初始汞吸附速率,但随着吸附时间的延长,其汞吸附速率的降低也越明显,汞吸附量曲线呈现明显的“凸”形。入口Hg0浓度的增加使得单位体积的烟气气流中Hg0分子数量增多,烟气中气相Hg0分子扩散至吸附剂微孔中的驱动力得到增强,能够促进S与Hg0的反应平衡正向移动以及羰基等含氧官能团对 Hg0的氧化吸附,因此汞吸附速率会随着烟气中Hg0浓度的增加而提高。从而入口Hg0浓度越大,单位质量累积汞吸附量也越多,吸附剂的利用效率越高。因此,在SO2活化改性石油焦吸附剂实际应用于燃煤电站喷射脱汞时,需针对烟气中不同的Hg0浓度来调节吸附剂的喷射量,在达到脱汞效率的条件下,实现吸附剂利用率的最大化。
2.3.4 SO2对汞吸附性能的影响 图 8(a)为固定床入口 Hg0浓度 35.0 μg·m-3,吸附温度 150℃,模拟烟气中SO2浓度为0.1%气氛下SAPC的汞穿透率曲线。如图所示,在吸附初始阶段,SO2气氛明显抑制了SAPC对汞的吸附作用,其初始汞脱除率从近100%下降至80%左右;随着吸附时间的延长,SO2的抑制作用逐渐减弱,1 h后SO2气氛汞穿透率曲线与 N2气氛汞穿透率曲线几乎重合。烟气中 SO2气氛对脱汞吸附剂的影响规律历来存在争议,沈彩琴[34]研究发现SO2吸附在活性炭纤维表面能够增加邻近活性位对Hg0的吸附,低浓度则有促进作用。而 Shao等[35]认为碳基吸附剂对 Hg0的吸附脱除与烟气中SO2的体积浓度密切相关。有学者认为[36-37]酯基对Hg0和SO2的吸附均有促进作用,且SO2在活性炭表面的吸附能比Hg0大,因此SO2与Hg0在吸附剂表面可能存在竞争吸附,从而降低汞脱除效率。SO2与Hg0的竞争吸附主要发生在吸附初始阶段,待竞争活性位消耗完毕,对比纯 N2气氛和含SO2气氛下SAPC的汞吸附量,可以发现SO2对汞脱除性能的影响较小,这与Liu等[32]的研究结果一致。
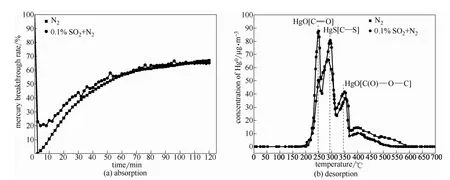
图8 SO2对汞脱除性能的影响Fig.8 Effect of SO2 on mercury removal
采用程序升温脱附(TPD)的方法分析吸附后样品表面汞吸附形态,图8(b)所示为SAPC在纯N2气氛和含SO2气氛下吸附汞后的热脱附曲线,如图所示,在 200℃时,汞开始从吸附剂表面析出,说明当吸附温度为 150℃时,吸附剂对 Hg0的物理吸附能力较弱。脱附曲线在近250℃和350℃时出现析出峰,应该是由石油焦表面(羰基)和C(O)—O—C(酯基)吸附 Hg0后分解形成[33]。而在 300℃左右出现的脱附峰则是由含硫官能团吸附Hg0后生成的HgS分解所得[38]。当模拟烟气中加入0.1%的SO2后,汞脱附峰的数量和温度区间并没有发生变化。但是由HgS分解形成的峰增大,这可能是由于SO2吸附在石油焦表面与不饱和碳结合形成C—S健,从而吸附Hg0产生更多的HgS;由羰基吸附Hg0后形成的峰减小,则说明SO2可能在吸附剂表面羰基上形成竞争吸附。
2.3.5 O2对汞吸附性能的影响 图9(a)为固定床入口 Hg0浓度35.0 μg·m-3,吸附温度 150℃,模拟烟气中O2浓度为6%气氛下SAPC的汞穿透率曲线,如图所示,O2有效地促进了SAPC对Hg0的吸附脱除,吸附反应进行2 h后仍能保持70%以上的汞脱除效率。研究表明[39],O2易通过吸附作用在吸附剂表面形成碳氧络合物,如羰基等含氧官能团,为烟气中Hg0提供活性吸附位。有学者认为[40],O2能够将烟气中的Hg0氧化成HgO,而HgO更容易化学吸附在吸附剂碳表面,从而极大地提高 Hg0的脱除率。
图9(b)所示为SAPC在纯N2气氛和含O2气氛下吸附汞后的热脱附曲线,对比发现析出峰数量和温度区间基本一致,但含O2气氛下吸附汞后的脱附峰值均有所增大,源于O2有效地促进了 SAPC对Hg0的吸附脱除,从而增大了其可脱附汞含量。纯N2气氛下,SAPC表面大量的含氧、含硫官能团能够通过化学吸附捕获气相中的Hg0分子。当模拟烟气中有O2存在时,可能会以分子或自由基O*的形式吸附在石油焦表面,一旦Hg0分子接近或吸附在碳表面时,部分会被O*氧化,而氧化态的汞更容易与碳表面丰富的含氧、含硫官能团结合,从而极大地提高了汞脱除效率[15]。
2.3.6 热再生特性 将汞吸附后的SAPC吸附剂放置于程序升温管式炉内,在 N2气氛下由室温升至600℃进行恒温热脱附再生,升温速率为 10℃·min-1,脱附后获得热再生 SO2活化改性石油焦吸附剂,标记为 RSAPC(renewable SO2activated petroleum coke)。图10为不同吸附温度条件下热再生吸附剂与原吸附剂的汞穿透率曲线,可见,在不同吸附温度下,热再生后SAPC的汞吸附性能均大幅下降。
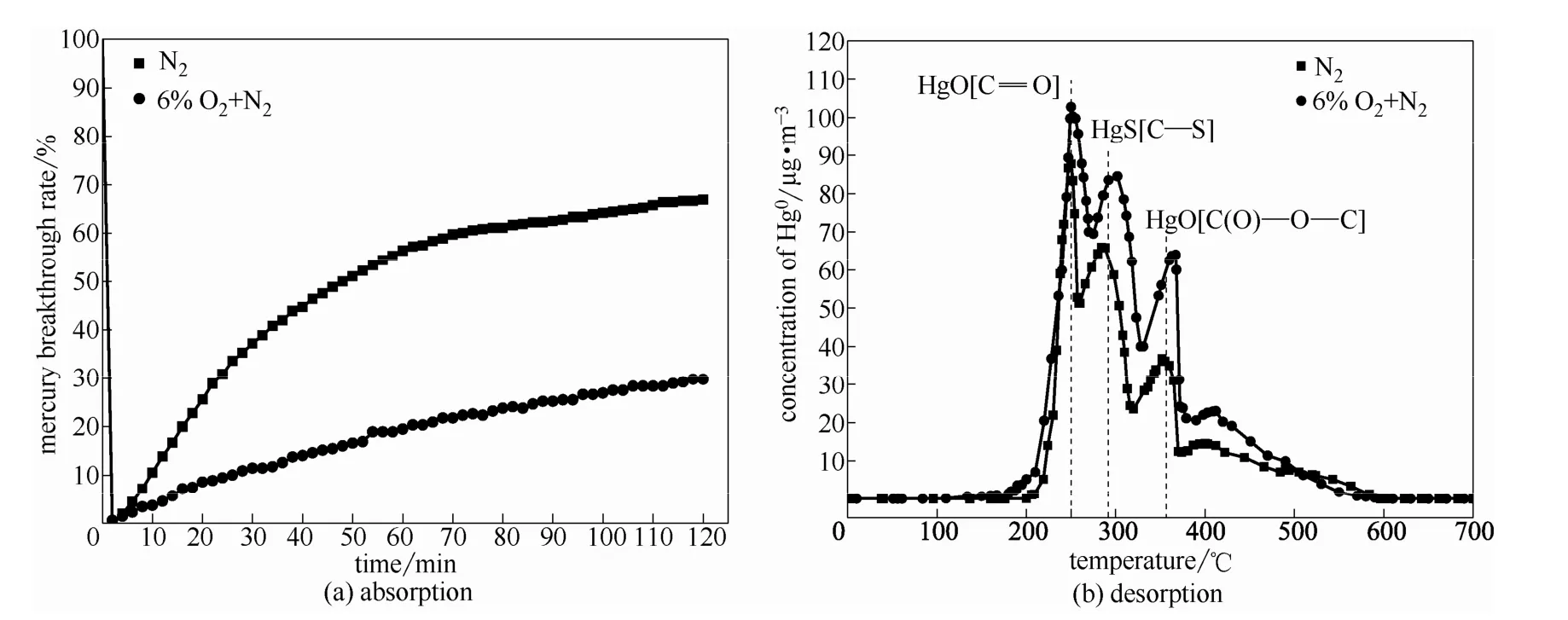
图9 O2对汞脱除性能的影响Fig.9 Effect of O2 on mercury removal
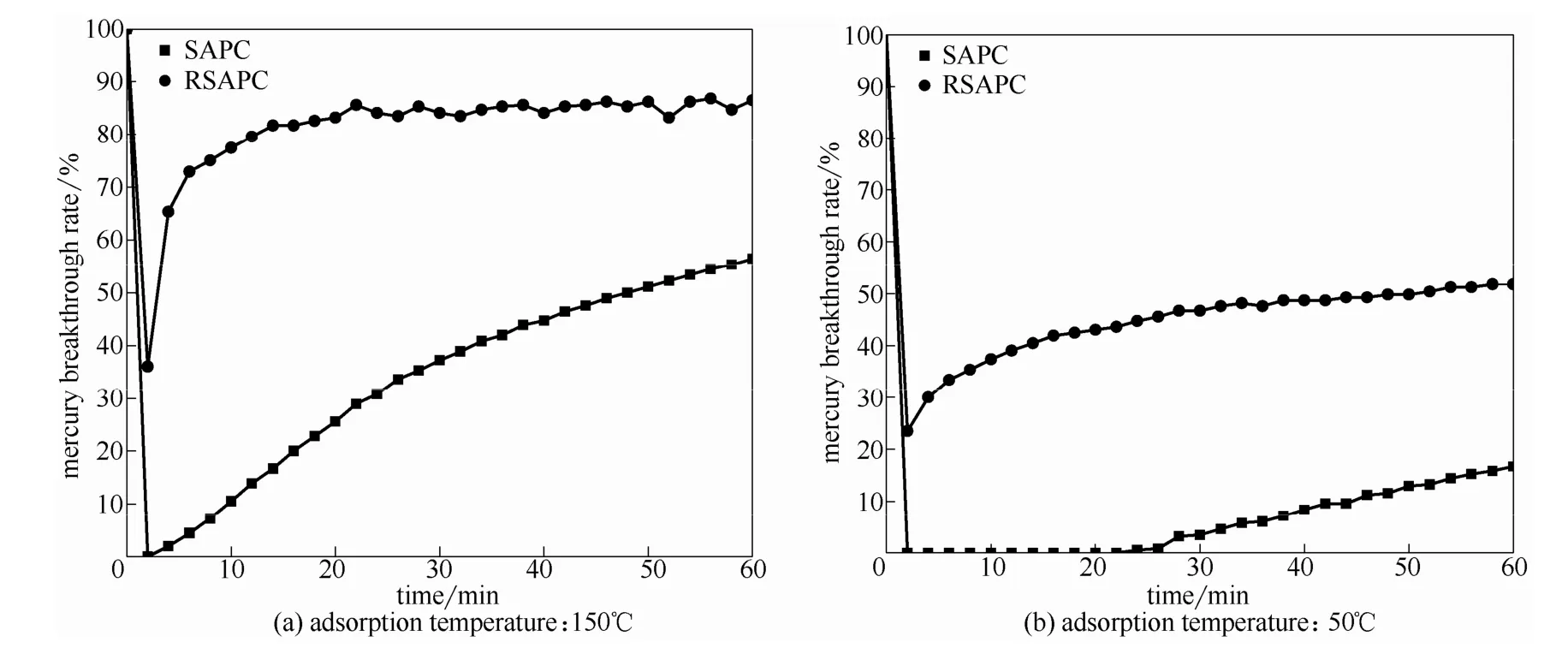
图10 SAPC的热再生特性Fig.10 Thermal regeneration characteristic of SAPC
当吸附温度为 150℃时,热再生后初始汞脱除率仅为65%,与再生前相比下降了约35%,且20 min后汞吸附效率基本稳定在85%左右;当吸附温度为50℃时,热再生后 SAPC的脱汞效率仍能保持在76%左右,与再生前相比下降了约25%。随着吸附时间的延长,RSAPC与SAPC吸附效率的差距越来越小。热脱附过程中,SAPC中汞化合物受热分解会以Hg0的形态析出,这一过程伴随着硫、氧原子的损失,导致吸附剂表面化学活性位点减少,汞脱除效率降低[41]。Yang等[42]发现不同的升温速率导致汞脱附行为不同,进而影响活性位点的释放,较高的升温速率促使SAPC活性位点更加活跃,热损失严重。此外,石油焦吸附剂的热稳定性较高,热再生时吸附剂孔隙中物理吸附形态的汞完全解吸,但碳表面孔结构不会出现烧蚀坍塌,仍能保持良好的物理吸附能力。不同吸附温度下,RSAPC与SAPC吸附剂汞脱除率之间的不同主要源于其化学吸附性能的下降,且由于吸附温度对硫改性石油焦吸附剂的影响规律,高温下热再生吸附剂对汞的吸附性能下降更为明显。
3 结 论
(1)工业副产物石油焦在SO2高温活化改性过程中会热解析出气体产物,同时SO2能够与内部C原子反应释放CO2和硫蒸气,从而达到活化扩孔的效果,使其具备微孔吸附剂的特征。活化后吸附剂中的硫含量显著增加且硫形态以非氧化态硫为主,羰基等含氧官能团比原始石油焦更为丰富。
(2)SO2活化改性石油焦表现出优异的汞吸附性能,羰基、酯基以及非氧化态硫是Hg0的主要活性吸附位,其汞脱除能力由孔隙结构、含氧官能团、硫含量及其形态分布共同决定。吸附温度的升高会抑制对Hg0的物理吸附以及含氧、含硫官能团的化学吸附作用。烟气中较高的Hg0浓度会降低汞脱除效率,但对汞吸附速率有促进作用。
(3)SO2会与不饱和碳结合形成 C—S键,但在羰基上可能会与Hg0形成竞争吸附,对石油焦吸附剂的脱汞性能影响较小。O2易将Hg0氧化,而氧化态汞更容易与含氧、含硫官能团结合,从而促进对Hg0的脱除。热再生时汞化合物受热分解的过程伴随着吸附剂表面化学活性位的损失,导致再生后汞吸附性能大幅下降。
[1]ZHOU Q,DUAN Y F,ZHU C,et al.In-flight mercury removal and cobenefit of SO2and NO reduction by NH4Br impregnated activated carbon injection in an entrained flow reactor[J].Energy & Fuel,2015,29:8118-8125.
[2]LEE S H,RHIM Y J,CHO S P,et al.Carbon-based novel sorbent for removing gas-phase mercury[J].Fuel,2006,85(2):219-226.
[3]缪超,宋爱萍.我国高硫石油焦市场现状及预测[J].石油规划设计,2012,23(1):16-22.LIAO C,SONG A P.Situation and forecast of high sulfur petroleum coke market in China[J].Petroleum Planning & Engineering,2012,23(1):16-22.
[4]ZHUANG Y,THOMPSON J S,ZYGARLICKE C J,et al.Impact of calcium chloride addition on mercury transformations and control in coal flue gas[J].Fuel,2007,86(15):2351-2359.
[5]赵可,张华伟,陈江艳,等.改性石油焦脱除单质汞的实验研究[J].山东科技大学学报(自然科学版),2016,35(4):69-73.ZHAO K,ZHANG H W,CHEN J Y,et al.Removal of elemental mercury by the modified petroleum coke[J].Journal of Shandong University of Science and Technology(Natural Science),2016,35(4):69-73.
[6]洪亚光,段钰锋,朱纯,等.载溴高硫石油焦活性炭脱汞实验研究[J].中国电机工程学报,2014,34(11):1762-1768.HONG Y G,DUAN Y F,ZHU C,et al.Experimental study on mercury removal of high-sulfur petroleum coke activated carbon impregnated with bromine[J].Proceedings of the CSEE,2014,34(11):1762-1768.
[7]卓海波.石油焦制备活性炭工艺条件的优化及孔结构表征[D].青岛:中国石油大学,2007.ZHUO H B.Optimizing process for preparation of activated carbon from petroleum coke and characterization of its porosity[D].Qingdao:China University of Petroleum,2007.
[8]GAUR V,ASTHANA R,VERMA N.Removal of SO2by activated carbon fibers in the presence of O2and H2O[J].Carbon,2006,44:46-60.
[9]纪罗军,金苏闵.我国有色金属及烟气制酸环保技术进展与展望[J].硫酸工业,2016,(4):1-8.JI L J,JIN S M.Environmental protection technical progress and outlook of China’s nonferrous metallurgy and metallurgical acid production[J].Sulphuric Acid Industry,2016,(4):1-8.
[10]STACY W O,VASTOLA F J,WALKER JR P L.Interaction of sulfur dioxide with active carbon[J].Carbon,1968,6(6):917-923.
[11]ASASIAN N,KAGHAZCHI T,FARAMARZI A,et al.Enhanced mercury adsorption capacity by sulfurization of activated carbon with SO2in a bubbling fluidized bed reactor[J].Journal of the Taiwan Institute of Chemical Engineers,2014,(45):1588-1596.
[12]YANG C.Preparation,characterization and application of novel adsorbent from petroleum coke activated by sulfur dioxide[D].Toronto:University of Toronto,2002.
[13]MORRIS E A,JIA C Q.Effects of O2on characteristics of sulfur added to petroleum coke through reaction with SO2[J].Industrial and Engineering Chemistry Research,2010,49:12709-12717.
[14]MORRIS E A,CHOI R,JIA C Q.Sulfur dioxide as an activating agent for sulfur-impregnated activated carbon produced from dense petroleum coke[J].Journal of Sulfur Chemistry,2013,34(4):358-369.
[15]WEI Y Y,YU D Q,TONG S T,et al.Effects of H2SO4and O2on Hg0uptake capacity and reversibility of sulfur-impregnated activated carbon under dynamic conditions[J].Environmental Science and Technology,2015,49:1706-1712.
[16]杜鸿飞,段钰锋,佘敏.高硫石油焦热解过程及硫形态的变化特性[J].化工进展,2016,35(8):2420-2426.DU H F,DUAN Y F,SHE M.Research on pyrolysis process of high sulfur petroleum coke and the changes of sulfur species[J].Chemical Industry and Engineering Progress,2016,35(8):2420-2426.
[17]HUMERES E,MOREIRA R F P M,PERUCH M G B.Reduction of SO2on different carbons[J].Carbon,2002,40(5):751-760.
[18]HUMERES E,MOREIRA R F P M.Kinetics and mechanisms in flow systems:reduction of SO2on carbons[J].Journal of Physical Organic Chemistry,2012,25(11):1012-1026.
[19]HUMERES E,DEBACHER N A,SMANIOTTO A,et al.Selective insertion of sulfurdioxide reduction intermediates on grapheme oxide[J].Langmuir,2014,30(15):4301-4309.
[20]SMANIOTTO A,HUMERES E,DEBACHER N A,et al.Interconversion and selective reactivity of sulfur dioxide reduction intermediates inserted on graphene oxide[C]//15th European Symposium on Organic Reactivity (ESOR).Kiel,Germany,2015.
[21]HUMERES E,PERUCH M D B,MOREIRA R F P M,et al.Reduction of sulfur dioxide on carbons catalyzed by salts[J].International Journal of Molecular Sciences,2005,6(1/2):130-142.
[22]HUMERES E,CASTRO K M,MOREIRA R F P M,et al.Reactivity of the thermally stable intermediates of the reduction of SO2on carbons and mechanisms of insertion of organic moieties in the carbon matrix[J].Journal of Physical Chemistry,2008,112(2):581-589.
[23]ARONNIEMI M,SAINIO J,LAHTINEN J.Chemical state quantification of iron and chromium oxides using XPS the effect of the background subtraction method[J].Surface Science,2005,578(1/2/3):108-123.
[24]PIETRZAKR,WACHOWSKA H.The influence of oxidation with HNO3on the surface composition of high sulphur coals XPS study[J].Fuel Process.Technol.,2006,87(11):1021-1029.
[25]PUZIY A M,PODDUBNAYA O I,SOCHA R P,et al.XPS and NMR studies of phosphoric acid activated carbons[J].Carbon,2008,46(15):2113-2123.
[26]何川.高硫石油焦脱硫技术研究[D].长沙:中南大学,2013.HE C.Study on desulfurization technology of high-sulfur petroleum coke[D].Changsha:Central South University,2013.
[27]ZHANG H,ZHAO J T,FANG Y T,et al.Catalytic oxidation and stabilized adsorption of elemental mercury from coal-derived fuel gas[J].Energy and Fuel,2012,26:1629-1637.
[28]YAO Y X,VELPARI V,ECONOMY J.Design of sulfur treated activated carbon fibers for gas phase elemental mercury removal[J].Fuel,2014,116:560-565.
[29]ZHANG B,XU P,QIU Y,et al.Increasing oxygen functional groups of activated carbon with non-thermal plasma to enhance mercury removal efficiency for flue gases[J].Chemical Engineering Journal,2015,263:1-8.
[30]TONG LI,XU W Q,QI H,et al.Enhanced effect of O/N groups on the Hg0removal efficiency over the HNO3-modified activated carbon[J].Acta Physico-Chimica Sinica,2015,31(3):512-518.
[31]LIU J,CHENEY M A,WU F,et al.Effects of chemical functional groups on elemental mercury adsorption on carbonaceous surfaces[J].Journal of Hazardous Materials,2011,186(1):108-133.
[32]LIU W,VIDIC R D.Impact of flue gas conditions on mercury uptake by sulfur-impregnated activated carbon[J].Environmental Science and Technology,2004,34:154-159.
[33]SUN P,ZHANG B,ZENG X B,et al.Deep study on effects of activated carbon’s oxygen functional groups for elemental mercury adsorption using temperature programmed desorption method[J].Fuel,2017,200:100-106.
[34]沈彩琴.活性炭纤维表面吸附汞机理的密度泛函理论研究[D].杭州:浙江大学,2015.SHEN C Q.Density functional theory study on the mechanism of mercury adsorption by activated carbon fiber[D].Hangzhou:Zhejiang University,2015.
[35]SHAO H Z,LIU X W,ZHOU Z J,et al.Elemental mercury removal using a novel KI modified bentonite supported by starch sorbent[J].Chemical Engineering Journal,2016,29:306-316.
[36]LI Y H,LEE C W,GULLETT B K.Importance of activated carbon’s oxygen surface functional groups on elemental mercury adsorption[J].Fuel,2008,82:451-457.
[37]KARATEPE N,ORBA I,YAVUZ R,et al.Sulfur dioxide adsorption by activated carbon having different textural and chemical properties[J].Fuel,2008,87:3207-3215.
[38]RUMAYOR M,FERNANDEZ-MIRANDA N,LOPEZ-ANTON M A,et al.Application of mercury temperature programmed desorption(HgTPD) to ascertain mercury/char interactions[J].Fuel Processing Technology,2015,132:9-14.
[39]STAVROPOULOUS G G,SAMARAS P,SAKELLAROPOULOS G P.Effect of activated carbons modification on porosity,surface structure and phenol adsorption[J].Journal of Hazardous Materials,2008,151(2/3):414-421.
[40]HALL B,SCHAGER P,LINDQVIST O.Chemical reactions of mercury in combustion flue gases[J].Water,Air,Soil Pollut.,1991,56(1):3-14.
[41]吕维阳,刘盛余,能子礼超,等.载硫活性炭脱除天然气中单质汞的研究[J].中国环境科学,2016,36(2):382-389.LÜ W Y,LIU S Y,NENGZI L C,et al.Remove elemental mercury by sulfur-impregnated activated carbon in natural gas[J].China Environmental Science,2016,36(2):382-389.
[42]YANG J P,ZHAO Y C,ZHANG J Y,et al.Removal of elemental mercury from flue gas by recyclable CuCl2modified magnetospheres catalyst from fly ash (3):Regeneration performance in realistic flue gas atmosphere[J].Fuel,2016,173:1-7.
date:2017-05-15.
Prof.DUAN Yufeng,yfduan@seu.edu.cn
supported by the National Key Research and Development Program of China (2016YFB0600604).
Mercury adsorption characteristics of petroleum coke activated by SO2
WANG Chenping1,DUAN Yufeng1,SHE Min1,ZHU Chun1,YANG Zhizhong2
(1Key Laboratory of Energy Thermal Conversion and Control of Ministry of Education,Southeast University,Nanjing210096,Jiangsu,China;2Technology Center of Dongfang Boiler Group Company Limited,Dongfang Electric,Zigong643001,Sichuan,China)
Petroleum coke as a kind of by-product in petrochemical industry was chosen to prepare the mercury removal adsorbent with high sulfur and activity by SO2activation.The effects of adsorption temperature,inlet Hg0concentration,flue gas composition and thermal regeneration on mercury removal characteristic were investigated in a fixed bed reactor system.Meanwhile,the removal mercury mechanism was put forward by applying characterization methods,including surface area and porosity analyzer,elemental analyzer and X-ray photoelectron spectroscopy (XPS).The experimental results showed that the physical and chemical properties of SAPC were significantly improved.And carbonyl,ester and non-oxidized sulfur were the main active sites of Hg0capture.Furthermore,the mercury removal capacity decreased with increasing adsorption temperature.The mercury adsorption rate was faster,while the initial mercury removal efficiency became lower at elevated initial Hg0concentration.SO2had unconspicuous effect on mercury removal.Hg0on or close to surfaces was oxidized by the adsorbed oxygen,and mercuric ions were more readily bound to sulfurviathe Hg—S bond,while some will bind to oxygen.The absorption capacity of regenerated petroleum coke was weakened because of the loss of active sites in the regeneration process.
petroleum coke; mercury adsorption; sulfur dioxide; sulfur forms
TQ 534.9
A
0438—1157(2017)12—4764—10
10.11949/j.issn.0438-1157.20170621
2017-05-15收到初稿,2017-06-26收到修改稿。
联系人:段钰锋。
王晨平(1993—),男,硕士研究生。
国家重点研发计划项目(2016YFB0600604)。

