转Fat-1基因猪外源基因遗传稳定性分析
华文君,郑新民,华再东,毕延震,宋忠旭,任红艳
(湖北省农业科学院 畜牧兽医研究所/动物胚胎工程及分子育种湖北省重点实验室,湖北 武汉 430064)
转Fat-1基因猪外源基因遗传稳定性分析
华文君,郑新民,华再东,毕延震,宋忠旭,任红艳
(湖北省农业科学院 畜牧兽医研究所/动物胚胎工程及分子育种湖北省重点实验室,湖北 武汉 430064)
测定转Fat-1基因猪外源基因遗传稳定性,为转基因猪育种选择优质新材料提供基础数据。采用PCR和Southern印迹杂交方法对转Fat-1基因传代生产仔猪进行检测,了解Fat-1基因在猪基因组中的整合情况,统计传代猪转基因阳性比率,与自然基因单等位基因正常遗传比率进行差异显著性分析。结果显示,F2代传代仔猪Fat-1基因阳性比率为57.14%,F3代传代仔猪阳性比率为46.67%。F1代公猪外源Fat-1基因是1拷贝基因,传代配种母猪使用非转基因母猪,仔猪阳性比率与自然基因单等位基因正常遗传比率(50%)差异不显著。Fat-1基因在猪育种传代过程中遗传力没有下降,转Fat-1基因公猪能够稳定遗传生产后代猪。
Fat-1基因; 转基因猪; 遗传稳定性; 多聚不饱和脂肪酸
饮食中总脂肪和饱和脂肪的摄入量占总热量的比例不断减少,而ω-6多聚不饱和脂肪酸(ω-6 PUFAs)的摄入增加和ω-3多聚不饱和脂肪酸(ω-3 PUFAs)减少,导致ω-6与ω-3 PUFAs比例达到20∶1,甚至更高,这种情况对心血管疾病、慢性疾病具有明显影响[1],并且使超重和肥胖的患病率显著增加。红细胞(RBC)膜磷脂中ω-6 PUFAs及ω-6与ω-3 PUFAs比例增加可导致肥胖的风险增加。通过增加摄入二十碳五烯酸(EPA)和二十二碳六烯酸(DHA)能够减少疾病产生,ω-6/ω-3 PUFAs平衡对身体健康具有重要意义[2]。ω-3 PUFAs能够降低膜脂中胆固醇含量,增加细胞膜的流动性[3-4],降低心脑血管疾病产生的比例[5],具有抗炎、抗凝血等作用,还可抑制肿瘤生长[6-7],影响多种人类神经性疾病[8-9],食品中适量补充ω-3 PUFAs对身体保健具有多种功效。
人和哺乳动物缺少ω-3、ω-6多不饱和脂肪酸脱氢酶,不能够生成ω-3、ω-6 PUFAs,2种物质必须从食物中获取。秀丽线虫Fat-1基因编码的ω-3多聚不饱和脂肪酸脱氢酶具有将ω-6 PUFAs转化生成ω-3 PUFAs的能力[10-11]。采用转基因动物方法生产长链ω-3 PUFAs是解决ω-3 PUFAs食物短缺的有效方法之一,转Fat-1基因猪可提高猪肉营养价值,具有很好的应用前景。转Fat-1基因牛、猪已成功制备[12],转Fat-1基因猪ω-6/ω-3 PUFAs的比值从14.53下降到2.62[13]。
外源基因在转基因动物中能够稳定遗传是转基因动物新品种育种的重要研究内容之一,猪基因组是自然界长期自然选择进化形成的稳定基因组,通过基因工程技术人工整合的外源基因在猪基因组中的整合结构是否能够稳定遗传,需要进行转基因动物传代测试才能够明确。测试外源基因遗传稳定性对转基因猪育种选择优良个体,及改进转基因方法具有重要意义。本试验采用PCR和Southern印迹杂交方法对转Fat-1基因传代生产仔猪进行检测,了解Fat-1基因在猪基因组中的整合情况,统计阳性猪比率,以分析Fat-1基因在转基因猪中的遗传稳定性,为转基因猪育种选择优质新材料奠定基础。
1 材料和方法
1.1 主要试剂
基因组总DNA提取试剂盒、Southern印迹杂交检测试剂盒均购自美国生命技术公司,地高辛标记核酸检测试剂盒购自德国罗氏公司,限制性内切酶XbaⅠ购自美国Promega公司,2×PCR反应混合液购自日本TaKaRa公司。
1.2 转Fat-1基因猪配种传代
从猪场保种的转Fat-1基因猪中选择F1代转基因阳性耳号3028公猪,配种1头非转基因阴性母猪,从F2代生产仔猪中选取1头阳性公猪,在其12月龄配种1头阴性母猪,母猪产仔断奶后再与相同阳性公猪配种。及时保存生产仔猪样品,检测Fat-1基因在猪基因组中的整合情况。
1.3 PCR法检测转Fat-1基因猪
1.3.1 猪基因组总DNA提取 采集仔猪耳组织样品,用75%乙醇保存,每头仔猪取25 mg耳组织,记录仔猪样品编号和对应的仔猪耳号。应用基因组总DNA提取试剂盒提取总DNA,使用膜吸附法完成样品制备。每个样品加入180 μL组织消化液、20 μL蛋白酶K溶液,50 ℃消化12 h,加入20 μL RNase,37 ℃消化35 min。用200 μL洗脱液溶解DNA样品,测定DNA浓度,样品-20 ℃保存。
1.3.2 PCR法检测Fat-1基因 每个样品取DNA 120 ng,使用引物HFP1、HFP2扩增Fat-1 基因片段。特异扩增片段长度为600 bp。阳性对照为基因导入使用的质粒,阴性对照采用非转基因猪样品。
扩增引物序列为HFP1: 5′-GTGATGCTATTGCTTTATTTGTAAC-3′;HFP2: 5′-GGAGCAGTGGTGGAATGCCT-3′。PCR反应体系:2×PCR反应混合液12.5 μL,DNA样品120 ng,10 μmol/L的上、下游引物各1 μL,加ddH2O至总体积25 μL。反应条件:94 ℃ 2 min; 94 ℃ 30 s,62 ℃ 40 s,72 ℃ 45 s,30个循环;72 ℃延伸5 min。采用2%琼脂糖凝胶电泳检查扩增结果。PCR法检测14头F2代传代仔猪,15头F3代传代仔猪。
1.4 Southern印迹杂交分析Fat-1基因整合
PCR法检测得到的转Fat-1基因猪,通过苯酚抽提方法纯化其DNA样品,使用Southern印迹杂交检测Fat-1基因整合情况。PCR阳性猪、阴性猪总DNA各取15 μg,苯酚抽提1次,氯仿/异戊醇抽提1次,加2倍体积的无水乙醇沉淀DNA。-20 ℃冷冻后离心取沉淀,70%乙醇洗沉淀1次。DNA样品抽真空干燥后,加入20 μL ddH2O溶解,用10 μL限制性内切酶XbaⅠ于37 ℃消化7 h,将消化样品抽真空浓缩到15 μL。阳性对照为基因导入使用的质粒,阴性对照采用非转基因猪样品。
检测使用地高辛标记核酸检测试剂盒完成,PCR扩增Fat-1基因600 bp片段,回收纯化扩增产物作为Southern印迹杂交探针。样品用经碱变性、中和处理的1%琼脂糖凝胶电泳,转膜23 h,120 ℃烤膜30 min。对尼龙膜在42 ℃进行预杂交1 h、杂交过夜,在68 ℃水浴条件下洗膜2次。室温封阻尼龙膜、结合抗体、洗抗体,暗室避光进行免疫显色反应26 h,观察记录Southern印迹杂交带。阳性猪特异杂交带为1.8 kb,阴性猪没有杂交带。统计传代猪转基因阳性比率,与自然基因单等位基因正常遗传比率用SPSS 18.0统计软件进行差异显著性分析。
2 结果与分析
2.1 F2代转Fat-1基因传代猪的检测
F1代3028号阳性公猪(Fat-1基因1拷贝[14])配种3205号非转基因阴性母猪,生产F2代仔猪14头。用PCR法检测14头传代仔猪样品,共8头仔猪检测结果为转Fat-1基因阳性(图1),对应仔猪耳号分别为5001、5002、5004、5007、5008、5009、5010、5014号。F2代转基因阳性猪比率为57.14%,公猪外源基因为1拷贝基因,配种母猪是阴性母猪,仔猪转基因阳性比率与自然基因单等位基因正常遗传比率(50%)差异不显著,表明Fat-1基因能够稳定遗传到F2代仔猪。
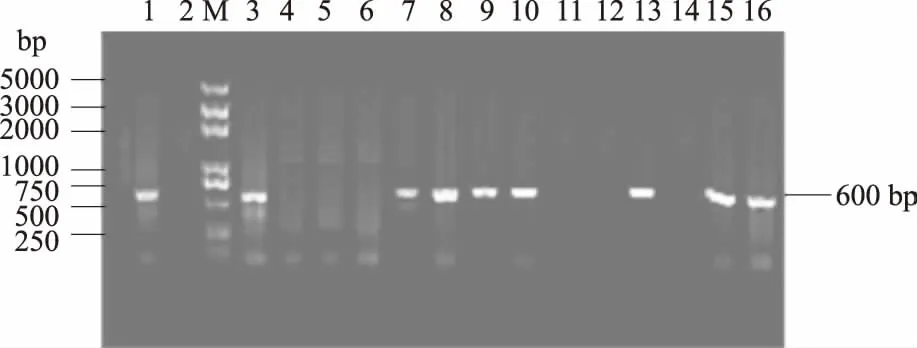
M:DNA分子标记;1:阳性对照;2:阴性对照;3—16:仔猪样品 图1 F2代转Fat-1基因猪检测
2.2 F3代转Fat-1基因传代猪的检测
2.2.1 第1次配种阳性仔猪检测 F2代转Fat-1基因5009号阳性公猪配种5012号阴性母猪,生产F3代仔猪8头。PCR法检测8头转Fat-1基因传代仔猪,得到5头阳性猪(图2),对应猪耳号分别为9010、9050、9060、9080、9090。疑似阳性猪1头,耳号为9070。6头猪样品经Southern印迹杂交分析,4个样品有1.8 kb特异杂交带,确认为Fat-1基因整合阳性,阳性猪耳号为9010、9050、9080、9090。仔猪阳性比率为50.00%,公猪携带1拷贝外源基因,阴性母猪配种,仔猪转基因阳性比率与自然基因单等位基因正常遗传比率(50%)相同。
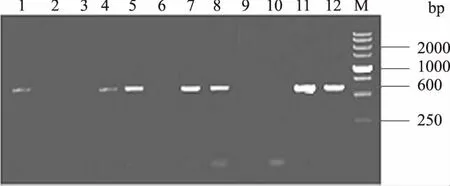
M:DNA分子标记;1—8:仔猪样品;9、10:阴性对照;11、12:阳性对照 图2 第1次配种F3代转Fat-1基因猪PCR检测
2.2.2 第2次配种阳性仔猪检测 F2代转Fat-1基因5009号阳性公猪再次配种5012号阴性母猪,生产F3代仔猪7头。PCR法检测7头转Fat-1基因传代仔猪,得到3头阳性猪(图3),对应猪耳号为9002、9004、9007。疑似阳性猪1头,耳号为9003。4头猪样品经Southern印迹杂交分析,其中3个样品有1.8 kb特异杂交带(图4),确认为Fat-1基因整合阳性,阳性猪耳号为9002、9004、9007。仔猪阳性比率为42.86%,公猪外源基因为1拷贝,配种母猪是阴性母猪,仔猪转基因阳性比率与自然单等位基因正常遗传比率(50%)差异不显著。
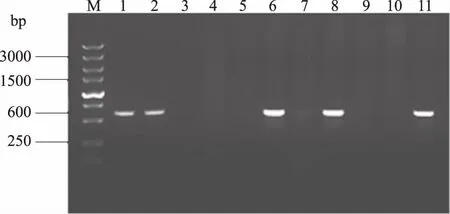
M:DNA分子标记;1、2:阳性对照;3、4:阴性对照;5—11:仔猪样品
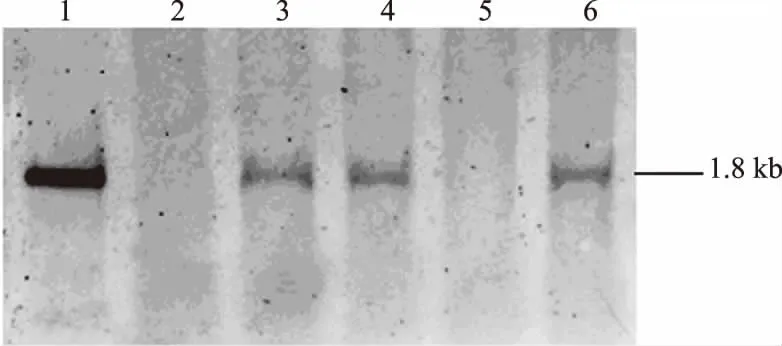
1:阳性对照;2:阴性对照;3—6:仔猪样品
F2代转Fat-1基因猪2次配种生产15头F3代仔猪,经过PCR和Southern杂交检测,7头猪为转基因整合阳性,仔猪阳性比率为46.67%,与自然单等位基因正常遗传比率(50%)差异不显著,表明Fat-1基因能够稳定遗传到F3代仔猪。
3 结论
本试验对转Fat-1基因猪中的外源基因遗传稳定性进行了测试分析,F2代传代仔猪Fat-1基因阳性比率为57.14%,F3代传代仔猪阳性比率为46.67%。F1代公猪外源Fat-1基因是1拷贝基因,配种母猪都是非转基因阴性母猪,传代仔猪阳性比率与自然基因单等位基因正常遗传比率(50%)差异不显著,Fat-1基因能够从F1代猪稳定遗传到F3代猪。可见,Fat-1基因在猪基因组中的整合稳定,猪育种传代过程中遗传力没有下降,转Fat-1基因耳号5009公猪能够为建立转Fat-1基因猪品系提供优良种质材料。
[1] Simopoulos A P.The importance of the omega-6/omega-3 fatty acid ratio in cardiovascular disease and other chronic diseases[J].Exp Biol Med,2008,233:674-688.
[2] Simopoulos A P.An increase in the omega-6/omega-3 fatty acid ratio increases the risk for obesity[J].Nutrients,2016,8(3):128-132.
[3] Terry P D,Rohan T E,Wolk A.In takes of fish and marine fatty acids and the rishs of cancers of the breast and prostate and of other hormone-related cancers:A review of the epidemiologic evidence[J].Am J Clin Nutr,2003,77(3):532-543.
[4] Andrea C,Damian M M,Maria A B,etal.Effect of ω-3 and ω-9 fatty acid rich oils on lipoxygenases and cyclooxygenases enzymes and on the growth of a mammary adenocarcinoma model[J].Lipids Health Dis,2010,9:112-117.
[5] Yam D,Peled A,Shwit Z M.Suppression of tumorgrowth and metastasis by dietary fish oil combined with vitamins E and C and cisplatin[J].Cancer Chemother Pharmacol,2001,47(1):34-40.
[6] Griffitts J,Saunders D,Tesiram Y A,etal.Non-mammalianFat-1 gene prevents neoplasia when introduced to a mouse hepatocarcinogenesis model:Omega-3 fatty acids prevent liver neoplasia[J].Biochim Biophys Acta,2010,18(10):1133-1144.
[7] Bellenger J,Bellenger S,Bataille A,etal.High pancreatic n-3 fatty acids prevent stz-induced diabetes inFat-1 mice:Inflammatory pathway inhibition[J].Diabetes,2011,60(4):1090-1099.
[8] Akbar M,Calderon F,Wen Z,etal.Docosahexaenoic acid:A positive modulator of Akt signaling in neuronal survival[J].Proc Natl Acad Sci USA,2005,102(31):10858-10963.
[9] Wan J B,Huang L L,Rong R,etal.Endogenously decreasing tissue n-6/n-3 fatty acid ratio reduces atherosclerotic lesions in apolipoprotein E-deficient mice by inhibiting systemic and vascular inflammation[J].Arterioscler Thromb Vasc Biol,2010,30(12):2487-2494.
[10] Spychalla J P,Kinney A J,Browse J.Identification of an animal omega-3 fatty acid desaturase by heterologous expression in Arabidopsis[J].Proc Natl Acad Sci USA,1997,94:1142-1147.
[11] Kang J X,Wang J,Wu L,etal.Transgenic mice:Fat-1 mice convert n-6 to n-3 fatty acids[J].Nature,2004,427:504.
[12] Wu X,Ouyang H,Duan B,etal.Production of cloned transgenic cow expressing omega-3 fatty acids[J].Transgenic Res,2012,21:537-543.
[13] Ren H Y,Zheng X M,Chen H X,etal.Transgenic pigs carrying a synthesized fatty acid desaturase gene yield high level of ω-3 PUFAs[J].Agricultural Sciences in China,2011,10:1603-1608.
[14] 华文君,华再东,郑新民,等.转hFat-1基因猪外源基因整合分析及拷贝数测定[J].江西农业学报,2014,26(11):99-101.
Analysis of Exogenous Gene Hereditary Stability in Fat-1 Transgenic Pigs
HUA Wenjun,ZHENG Xinmin,HUA Zaidong,BI Yanzhen,SONG Zhongxu,REN Hongyan
(Key Laboratory of Animal Embryo Engineering and Molecular Breeding of Hubei Province,Institute of Animal Science and Veterinary Medicine,Hubei Academy of Agricultural Sciences,Wuhan 430064,China)
In order to provide data for transgenic pig breeding selection of high quality new materials and establish experimental basis to improve transgenic method,Fat-1 transgenic pig exogenous gene genetic stability was tested and analysed.The integration ofFat-1 gene in pig genome andFat-1 gene genetic stability were detected by PCR and Southern blotting inFat-1 transgenic passage piglets.The transgenic positive rate of piglets was counted,and the heritability difference significance betweenFat-1 gene and natural single allele was analysed.The positive rate ofFat-1 gene in F2generation piglets was 57.14% and the positive rate of F3passage piglets was 46.67%.The exogenousFat-1 gene in F1generation poar was 1 copy gene and breeding sows were non-transgenic pigs.The heritability difference betweenFat-1 gene and natural single allele was not significant.TheFat-1 gene heritability did not decline during the passage of swine breeding,andFat-1 transgenic pig could stably produce moreFat-1 transgenic piglets.
Fat-1 gene; transgenic pigs; hereditary stability; PUFAs
S813.3
A
1004-3268(2017)11-0144-04
2017-06-10
转基因生物新品种培育重大专项(2016ZX08006002-006);湖北省农业科技创新中心项目(2017-620-004-001);湖北省农业科学院竞争性项目(2016jzxjh013);湖北省技术创新专项重大项目(2016ABA117)
华文君(1969-),男,湖北团风人,副研究员,本科,主要从事转基因动物和动物繁殖研究工作。
E-mail:huawenjun08@aliyun.com

