鸡传染性法氏囊病病毒弱毒株在鸡体连续传代后毒力增强的分子机理研究
宫世玲,王 嘉,毛娅卿,吴 涛,王 哲,蒋桃珍
(中国兽医药品监察所,北京100081)
传染性法氏囊病(Infectious bursal disease,IBD)是由鸡传染性法氏囊病病毒(Infectious bursal disease virus,IBDV)引起的一种的急性、高度接触性传染病,主要危害3~6周龄雏鸡。IBDV基因组由 A(3.2 kb)、B(2.8 kb)两个双链 RNA 节段构成,A片段包含两个部分重叠的开放阅读框(ORF),大ORF编码多聚蛋白 VP2-VP4-VP3,小 ORF编码VP5蛋白,是一种非结构蛋白;B片段编码VP1蛋白,是一种具有RNA聚合酶活性的多功能蛋白。其中VP2被证明与毒力密切相关[1],但也有研究表明VP2蛋白并非毒力决定的唯一因素,其他蛋白对病毒毒力和致病性也有影响[2-3]。尽管国内外学者对IBDV的毒力基因进行了广泛的研究,但其毒力因子至今仍未被确定。
对于IBDV来说,其毒力的判定标准主要有三个:死亡率、法氏囊的病理损伤值及囊体比的下降。其中死亡率主要是针对超强毒株,非超强毒株通常不引起鸡的死亡,故法氏囊的病理损伤值及囊体比的下降被广泛用于IBDV毒力的判定。而囊体比的下降较为简单直观,已被大多数研究所采用。将IBDV弱毒株在SPF鸡体内连续传代,发现弱毒株在鸡体内传代后囊体比大幅度下降,表明IBDV弱毒株在SPF鸡体内连续传代后毒力返强。为进一步研究弱毒株及其鸡体传代毒毒力变化与基因的关系,本试验测定了基础弱毒株及其鸡体传代毒的基因组编码区序列,并对其进行比较分析,以期从分子水平上为该病毒毒力相关位点的研究提供依据。
1 材料与方法
1.1 毒株、菌株和载体 IBDV弱毒株A、弱毒株B由本实验室保存;大肠杆菌JM109感受态细胞、pGEM-T载体均购于promega公司。21日龄SPF鸡购于北京梅里亚动保公司。
1.2 主要试剂 TRIzol、Reverse Transcription System为invitrogen公司产品;pfu高保真聚合酶为promega公司产品;DNA Marker、琼脂糖凝胶DNA回收试剂盒、质粒提取试剂盒为天根生化科技有限公司产品。
1.3 病毒在鸡体内传代 将IBDV弱毒株A和B分别在鸡体内连续传代,其中弱毒株B在鸡体内传代两次,每次传代后,观察法氏囊病变,计算囊体比(Bursa/Body Weight Ratio)和 B ∶B 指数(BBIX)。每代的法氏囊经研磨处理后继续传代,一部分法氏囊样品放在-80℃,用于病毒RNA的提取。
1.4 病毒基因组RNA的提取 采用TRIzol法提取基础弱毒株及鸡体内传代的各个代次囊毒的基因组RNA。
1.5 引物的设计与合成 参考GenBank中已发表的IBDV弱毒株序列,用Primer 5.0软件设计合成了4对引物(表1),用于基础弱毒株及其鸡体传代毒的基因组编码区序列的扩增。其中A片段分2部分进行扩增,分别为75~1687 bp,1506~3232 bp;基因组B片段分2部分进行扩增,分别为17~1521 bp,1365~2799 bp。
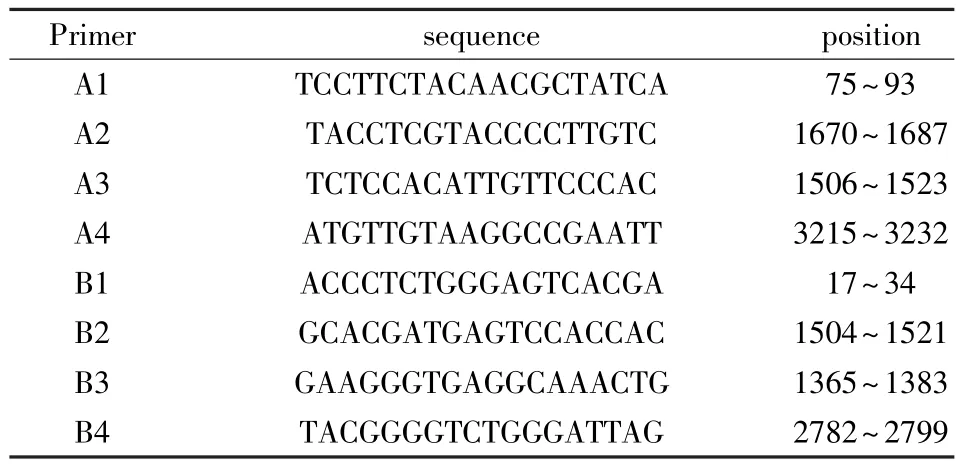
表1 引物序列及其位置
1.6 反转录-聚合酶链式反应(RT-PCR)用六聚体随机引物作为反转录引物,按反转录试剂盒说明书对提取的RNA进行反转录,并以反转录产物为模板,分别以 A1/A2、A3/A4、B1/B2、B3/B4 为引物进行PCR扩增。采用50 μL反应体系:10×Buffer 5 μL,dNTP 4 μL,上下游引物(10 μmol)各 2 μL,模板 5 μL,pfu 0.5 μL,ddH2O 31.5 μL;反应条件:95 ℃ 2 min;95 ℃ 40 s,55 ℃ 30 s,72 ℃ 3 min,35个循环;72 ℃10 min。 取 5 μL PCR 产物,用 1.0%琼脂糖凝胶电泳检查PCR扩增结果。
1.7 PCR产物的克隆和鉴定 PCR产物经纯化后,连接pGEM-T载体,转化大肠杆菌JM109感受态细胞,涂布含Amp、IPTG和X-Gal的LB平板,挑取白色菌落进行质粒提取,并进行PCR鉴定。
1.8 序列测定及比较分析 选取3~5个PCR阳性克隆,送立菲生物技术有限公司进行序列测定。所测定的基础弱毒株及在鸡体内传代后的各个代次囊毒的序列及其推导的氨基酸序列用DNASTAR 5.0软件中的Megalign进行比对分析。
2 结 果
2.1 病毒在鸡体内传代后的致病性变化 将基础IBDV弱毒株A和B在鸡体内连续传代至第5、第6代时,囊体比大幅度下降(图1-图3),B∶B指数下降(图4-图6),说明法氏囊萎缩严重,表明IBDV弱毒株在鸡体内传代后毒力返强。
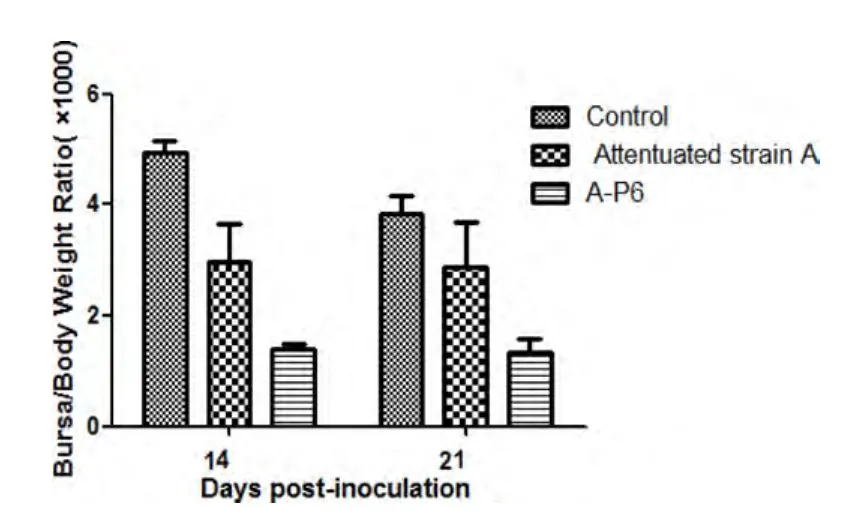
图1 14、21 d时弱毒株A及其鸡体传代毒P6的囊体比
图2 14、21 d时弱毒株B及其第一次鸡体传代毒P5的囊体比
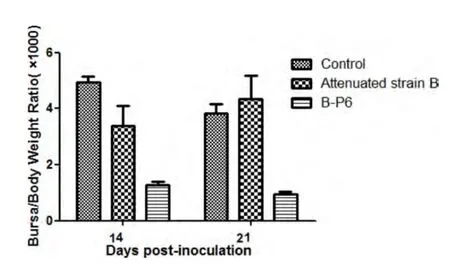
图3 14、21 d时弱毒株B及其第二次鸡体传代毒P6的囊体比
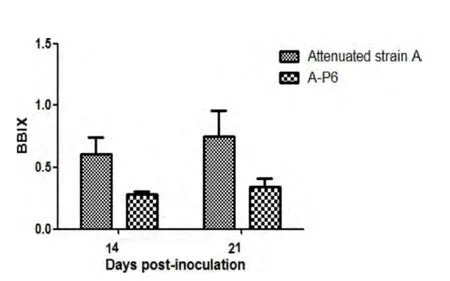
图4 14、21 d时弱毒株A及其鸡体传代毒P6的B∶B指数
图5 14、21 d时弱毒株B及其第一次鸡体传代毒P5的B∶B指数
图6 14、21 d时弱毒株B及其第二次鸡体传代毒P6的B∶B指数
2.2 IBDV基因的扩增及克隆鉴定 以提取的基础种毒及其在鸡体内传代后各个代次囊毒的RNA为模板,反转录后分别以引物 A1/A2、A3/A4、B1/B2、B3/B4 进行 PCR 扩增,得到了 1613、1726、1505和1435 bp的基因片段(图7),与预期片段大小相符。经PCR鉴定,得到了基因组各片段的阳性克隆(图8)。
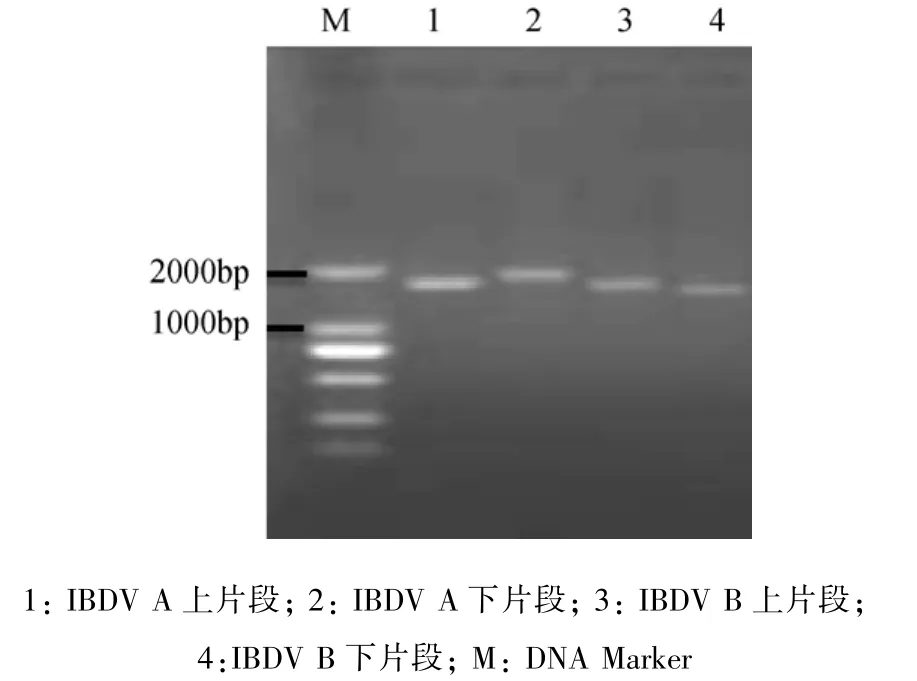
图7 IBDV RT-PCR扩增结果

图8 重组质粒pGEM-TA的PCR鉴定结果
2.3 序列的测定及比较分析 测序结果表明,成功地测出了基础种毒及在鸡体内传代后的各个代次囊毒的基因组编码区序列,各基因的阅读框完整,没有发生碱基的插入和缺失。通过对基础弱毒株及其鸡体传代毒的基因序列的比较分析,发现2株弱毒株在鸡体内连续传代过程中,一些氨基酸位点发生了规律性变异(表2)。

表2 弱毒株在鸡体内连续传代(P1-P5/P6)期间氨基酸的变异情况
IBDV弱毒株A在鸡体的传代过程中,基因组A片段VP5基因发生了一个碱基的突变:373(C→T),导致 VP5蛋白125位氨基酸 P→S的变异;VP2-VP4-VP3多聚蛋白基因发生了3个碱基的突变:339(C→T)、759(C→A)和 1899(C→T),但只有759位核苷酸的突变导致VP2蛋白253位氨基酸H→Q的变异,其他两个核苷酸的突变并未引起氨基酸的变异;B片段编码的VP1基因在鸡体的传代过程中,比较保守,并未发生任何核苷酸的突变。
IBDV弱毒株B第一次在鸡体的传代过程中,基因组A片段VP5基因发生了2个碱基的突变:238(A→G)和388(T→C),导致 VP5蛋白 80位氨基酸A→G和130位氨基酸C→R的变异;VP2-VP4-VP3多聚蛋白基因发生了4个碱基的突变:204(A→G)、354(T→C)、759(C→A)和 2332(G→A),其中759位核苷酸的突变导致VP2蛋白253位氨基酸H→Q的变异,2332位核苷酸的突变导致VP3蛋白778位氨基酸V→M的变异,其他两个核苷酸的突变并未引起氨基酸的变异;B片段编码的VP1基因在鸡体的传代过程中,比较保守,并未发生任何核苷酸的突变。
IBDV弱毒株B第二次在鸡体的传代过程中,基因组A片段VP5基因发生了2个碱基的突变:238(A→G)和 388(T→C),导致 VP5蛋白 80位氨基酸A→G和130位氨基酸C→R的变异;VP2-VP4-VP3多聚蛋白基因发生了5个碱基的突变:204(A→G)、354(T→C)、757(C→A)、1899(C→T)和2332(G→A),其中757位核苷酸的突变导致VP2蛋白253位氨基酸H→N的变异,2332位核苷酸的突变导致VP3蛋白778位氨基酸V→M的变异,其他三个核苷酸的突变并未引起氨基酸的变异;B片段编码的VP1基因在鸡体的传代过程中,比较保守,并未发生任何核苷酸的突变。
3 讨 论
病毒在易感动物体内传代后,会出现毒力返强现象。本实验将2株IBDV弱毒株在SPF鸡体内连续传代至第5、6代时,出现明显的法氏囊萎缩、B∶B指数下降,表明IBDV弱毒株在鸡体内连续传代后毒力返强。为进一步阐释哪些基因位点导致了上述毒力的变化,本实验测定了基础弱毒株及其在鸡体内传代后各个代次囊毒的基因组序列,通过比较分析基础弱毒株及其鸡体传代毒的各基因及推导的氨基酸序列,发现三次鸡体传代实验的结果都出现VP2蛋白253位氨基酸的替换;IBDV弱毒株B在鸡体内的两次传代实验出现了VP5蛋白80、130位氨基酸变异,VP3蛋白778位氨基酸变异,而弱毒株A在鸡体的传代过程中并未发生上述位点的变异。结果表明VP2蛋白253位氨基酸由H→Q或者H→N的变异能增强传染性法氏囊病病毒在鸡体内的致病性。
IBDV主要侵害鸡的中枢免疫器官—法氏囊,其中B淋巴细胞是主要的靶细胞。经典强毒株或者超强毒株不易在细胞上繁殖,但在细胞上连续传代后能适应细胞生长,并且对鸡的致病性降低[4]。序列分析[5]和后来的反向遗传学研究[6]表明 VP2高变区的几个特定的氨基酸(253、279、284、330)与IBDV的组织适应性及毒力相关。重组嵌合病毒的体内外致病性实验研究表明253Q、279D、284A参与了IBDV的毒力、细胞嗜性及致病性表型[7]。也有研究表明VP2蛋白不是IBDV超强毒株的唯一决定因子[8]。最近更多的研究表明基因组B片段编码的VP1蛋白(依赖于RNA的RNA聚合酶)对于IBDV在鸡体内的复制效率及毒力至关重要[9]。自然重配IBDV毒株的出现也表明基因组B片段对于超强IBDV毒株的致病性意义重大[10]。总之,越来越多的研究表明IBDV的毒力是多基因共同作用的结果。
然而 Yamaguchi和 Jackwood的研究发现将IBDV疫苗株在鸡体内连续传代后,VP2蛋白253位氨基酸由H突变为G或者Q、N,并伴随着毒力的增强;再将这些鸡体传代毒在细胞上培养,VP2蛋白253位氨基酸又回复突变为H,并伴随着毒力的丧失;然而VP2蛋白的279、284和330位氨基酸并没发生变异,表明仅VP2蛋白253位氨基酸的替换可能会增强传染性法氏囊病病毒在鸡体内的致病性[11-12]。 本实验从整个基因组水平上分析,发现弱毒株在鸡体内传代后,基因组B片段并未发生任何变异,VP2蛋白的279、284和330位氨基酸也没发生变异,仅VP2蛋白253位氨基酸发生了H→Q或者H→N的替换,更有效地证明了VP2蛋白253位氨基酸对于IBDV毒力的重要性。这些实验结果也都反映出疫苗株在田间应用中可能存在毒力返强的危险。
晶体学研究表明每一个VP2蛋白亚单位分为base、shell和 projection 三个结构域[13],253 位氨基酸位于projection中的两个亲水区之间,暴露在VP2蛋白表面。尽管VP2蛋白253位氨基酸残基的作用机制尚未明确,本文推测在该位点由组氨酸(H)变为谷氨酰胺(G)或者天冬酰胺(N),使该区域亲水性增强,可能更有利于IBDV在鸡体内与受体细胞相互作用,从而增强IBDV在鸡体内的致病性。本研究的结果表明VP2蛋白253位一个氨基酸的替换即可改变IBDV的毒力,该结果提示一个氨基酸变化就可能使弱毒株毒力返强,这对目前市场上IBDV疫苗株的安全性提出了质疑,提示进一步加强疫苗准入后的安全性评价及监管的重要性。
[1]Cui Xian-lan,Hadya S, Nagesha,et al.Identification of crucial residues of conformational epitopes on VP2 protein of infectious bursal disease virus by phage display[J].Virol Meth,2003,109(1):75-83.
[2]Miiller H.Replication of infectious bursal disease virus in lymphoid cells[J].Arch Virol,1986,87:191-203.
[3]MeihongLiua, Vikram N,Vakharia.VP1 protein of infectious bursal disease virus modulates thevirulence in vivo[J].Virology,2004, 330: 62-73.
[4]Yamaguchi T, Kondo T, Inoshima Y, et al.In vitro attenuation of highly virulent infectious bursal disease virus: some characteris⁃tics of attenuated strains[J].Avian Dis,1996, 40: 501-509.
[5]Yamaguchi T, Ogawa M, Inoshima Y, et al.Identification of sequence changes responsible for the attenuation of highly virulent infectious bursaldisease virus [J].Virology, 1996, 223:219-223.
[6]Lim B L, Cao Y, Yu T, Mo C W.Adaptation of very virulent infectious bursal disease virus to chicken embryonic fibroblasts by site-directed mutagenesis of residues 279 and 284 of viral coat protein VP2[J].Virol,1999,73: 2854-2862.
[7]Brandt M, Yao K, Liu M, et al.Molecular determinants of virulence,cell trophism,and pathogenic phenotype of infectious bursal disease virus[J].Virol, 2001,75, 11974-11982.
[8]Boot H J, terHuurne A H, Hoekman A A, et al.Rescue of very virulent and mosaic infectious bursal disease virus from cloned cDNA:VP2 is not the sole determinant of the very virulent type[J].Virol,2000,74 (15): 6701-6711.
[9]Liu M, Vakharia V N.VP1 protein of infectious bursal disease virus modulates the virulence in vivo[J].Virol,2004,330:62-73.
[10]Le Nouen C,Rivallan G,Toquin D,et al.Very virulent infectious bursal disease virus:reduced pathogenicity in a rare natural segment- B - reassorted solate[J].Gen Virol, 2006, 87:209-216.
[11]Yamaguchi T, Setiyono A, Kobayashi M, et al.Infectious bursal disease live vaccines:changes in the virus population during serial passage in chickens and chicken embryo fibroblast cells[J].Avian Dis,2000,44: 284-290.
[12]Jackwood D J, Sreedevi B, LeFever L J, et al.Studies on naturally occurring infectious bursal disease viruses suggest that a single amino acid substitution at position 253 in VP2 increases pathogenicity[J].Virology,2008,377: 110-116.
[13]Lee C C, Ko T P, Chou M, et al.Crystal structure of infectious bursal disease virus VP2 subviral particle at 2.6 A°resolution:implication in virion assembly and immunogenicity[J].Struct Biol, 2006, 155:74-86.

