成人型成骨不全并发心脏瓣膜病1例
赵琳琳 栾毅 何红
成人型成骨不全并发心脏瓣膜病1例
赵琳琳 栾毅 何红
患者男,37岁。因“反复心悸伴胸口隐痛3年”于2016年12月28日至我科门诊就诊。既往曾有多次不明原因骨折:足月顺产,出生时未见异常,发育与正常儿童无异,30年前第一次骨折,左侧前臂骨折,外固定处理,恢复良好;此后(7~16岁)无暴力下出现骨折共累计6次,部位限于双侧胫腓骨和骨盆,最严重的2次分别发生于右侧胫腓骨和右侧尺骨鹰嘴部,均采取手术治疗;1年前因交通意外造成肋骨骨折。否认高血压糖尿病史,否认风湿热及药物滥用史,否认吸烟史。父亲骨折3次(具体不详),主动脉瓣重度反流;母亲体健;弟弟无类似骨折病史;配偶体健;育有1子(目前8岁),自幼受外力后易骨折。体格检查:神志清,血压132/72mmHg,心率 85次 /min,呼吸 18次/min,体温 37℃,身高 163cm,体重 65kg,巩膜浅蓝,瞳孔等大等圆,听力正常,牙本质较好,口唇无紫绀,全身浅表淋巴结无肿大。颈静脉无充盈怒张,胸廓无畸形,脊柱无侧弯,两肺呼吸音清晰,心界无明显扩大,心尖部触及震颤,可闻及4/6级收缩期杂音,呈吹风样,心律齐,腹部软,肝脾未及肿大,四肢无畸形,无水肿。辅助检查:血常规,肝肾功能,碱性磷酸酶,血中微量元素,凝血功能,血沉等未见明显异常。血脂:TC 6.32mmol/L,TG 5.51mmol/L,HDL-C 1.06mmol/L,LDL-C 4.11mmol/L。常规十二导联心电图:窦性心律,左心室高电压。胸部X线平片:两肺纹理大致正常,未见实变;经胸超声心动图:二尖瓣后叶脱垂,考虑小腱索断裂,致对合不拢;二尖瓣中量反流(图1);基因检测结果(图2):成骨不全(osteogenesis imperfecta,OI),外周血基因组SNA测序发现致病基因为COL1A1,致病突变位于基因COL1A1外显子45,突变为c.3269delC,该突变可能导致COL1A1基因第1090以后发生移码和蛋白质截短(p.Gln1090Lysfs*18)。先证者本人为该突变的杂合子,其父亲也携带相同突变。

图1 患者超声心动图表现
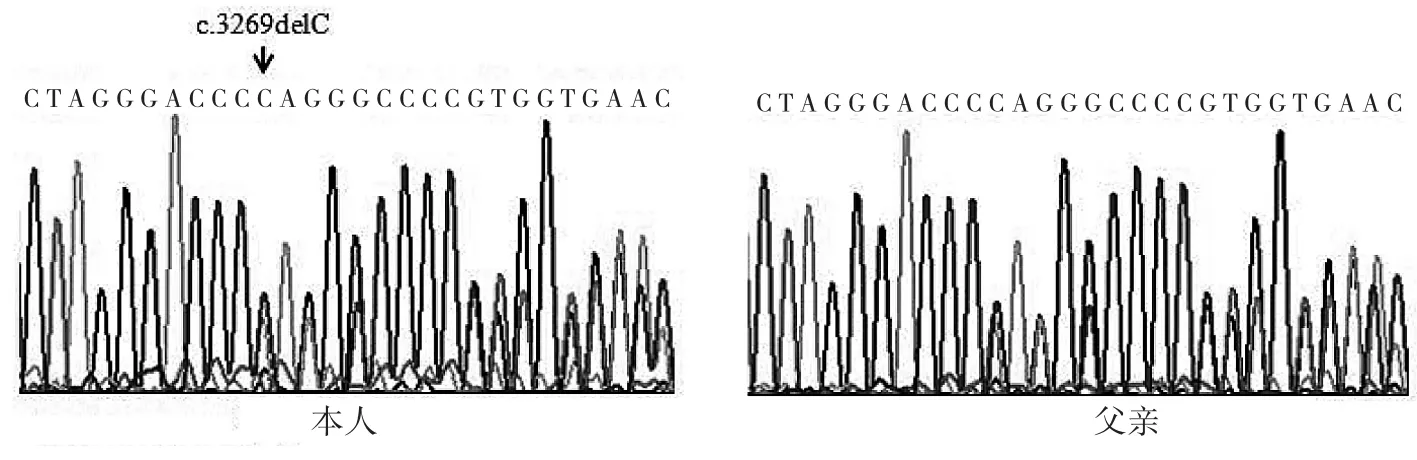
图2 患者及其父亲基因诊断结果
根据以上检查结果,诊断为“OI伴心脏瓣膜病、高脂血症”,予以琥珀酸美托洛尔缓释片(47.5mg/片,阿斯利康制药有限公司)口服控制心室率,阿司匹林肠溶片(100mg/片,拜耳医药保健有限公司)口服抗血小板聚集,辅以辅酶Q10营养心肌等对症支持治疗。因该患者无明显心功能不全症状,且心超提示二尖瓣中量反流,左心室舒张末期内径(LVEDd)为53mmm,左心室射血分数(LVEF)65%;未见有症状的重度二尖瓣反流和(或)左心室收缩功能障碍,且心超结果不符合LVEDd>70mm,左心室舒张末期容量指数(LVDEVI)>200ml/m2,LVEF <50% 等 条件,目前暂无外科手术指征。建议离院后定期复查心超,长期随访。
讨论OI又称脆骨病,是一组以骨骼脆性增加及胶原代谢紊乱为特征的全身性结缔组织疾病。其临床表现为骨脆性增加、骨关节进行性畸形等症状,还常常累及其他结缔组织,临床十分罕见。OI是一种常染色体遗传的先天性疾病,系由于多基因异常突变导致中胚层发育异常而使间充质组织发育不全、胶原形成障碍而造成的罕见遗传性疾病。90%的OI是编码I型胶原的基因COL1A1或COL1A2发生突变而引起的常染色体显性遗传疾病,其余OI则主要是由于调节I型胶原基因转录或翻译的基因(CRTAP、LEPRE1、PPIB、SERPINH1、FKBPIO 等) 发生突变所致。传统将OI分为Ⅰ~Ⅳ型,Glorieux、Ward、Cabral[1]等结合遗传缺陷特点又将5种罕见的亚型归入其中,将其改良为9种亚型,使得OI的分型逐渐趋于完善(表1)。
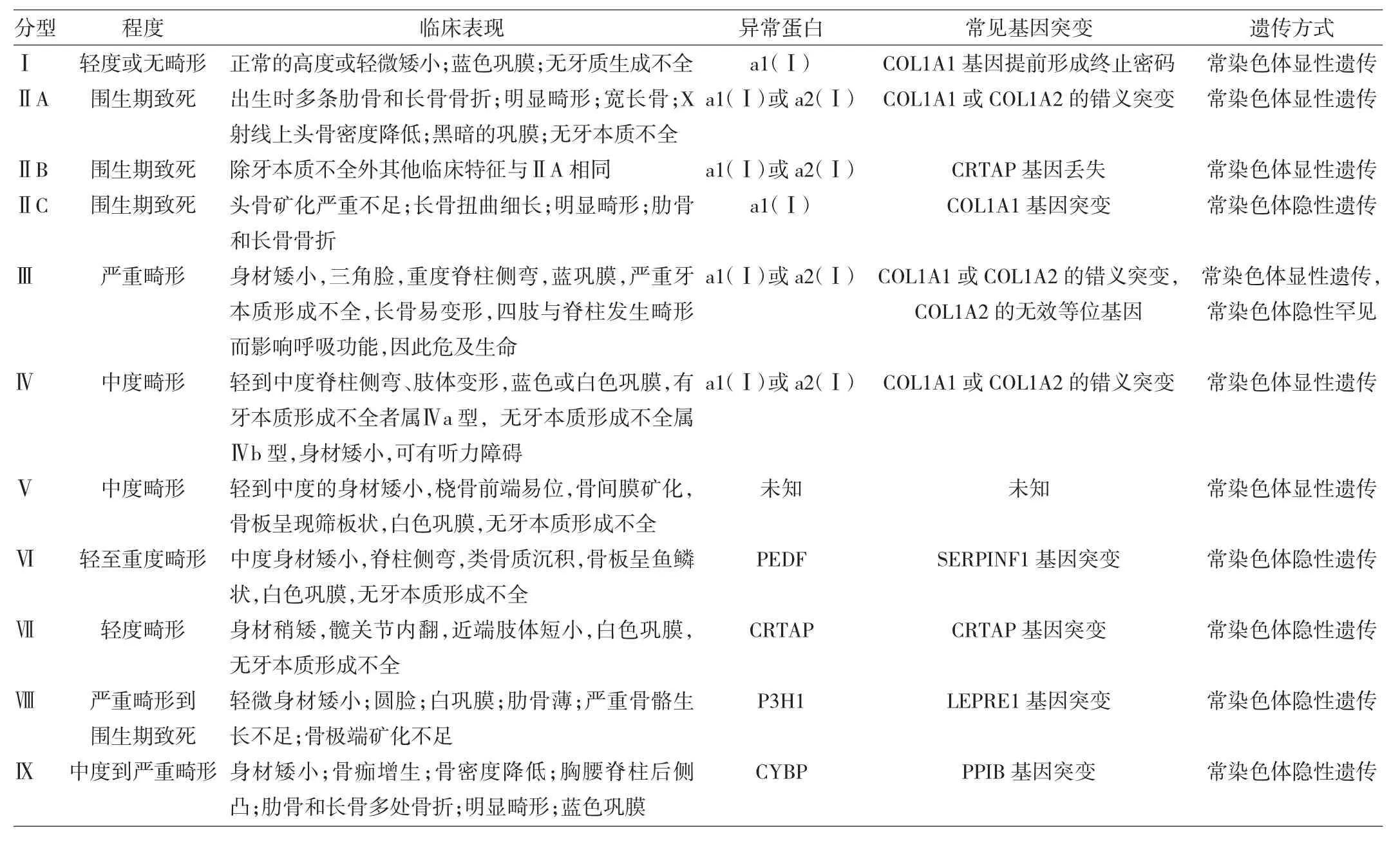
表1 OI的新分类
目前治疗OI主要是通过药物或进行外科手术,但随着遗传学的发展,基因治疗及干细胞移植将成为治疗该病的根本途径和主要研究热点。最新的研究发现将基因靶向定位(genetargeting)和诱导多能干细胞(iPSC)分化相结合可产生能生成正常胶原蛋白的特异性骨形成细胞,有望用于治疗OI[2]。
然而OI病变不仅限于骨骼,还常常累及其他结缔组织如眼、耳、牙齿、皮肤等,其特点是蓝巩膜、听力下降、牙本质发育不全及皮肤异常。同时,该病也是心脏瓣膜病的罕见病因之一,临床主要表现为主动脉瓣、二尖瓣反流,主动脉根部增宽以及因此而继发的血流动力学改变。本例患者为中青年男性,既往7~8次不明原因骨折,查体:蓝巩膜,体型矮小。辅助检查基因检测提示COL1A1突变,导致蛋白质截短,提示终止密码子形成,可诊断为OI(Ⅰ型),另患者因合并心脏瓣膜病,排除其他病因如高血压病,风湿性心瓣膜病,考虑OI并发心脏瓣膜病。本例OI合并二尖瓣脱垂,是OI伴发心脏瓣膜病临床中颇为罕见的类型之一。国内有关案例经验相对缺乏,国外也仅有个例伴发二尖瓣脱垂的报道,这些个体患有感染性心内膜炎(IE)的风险增加10~100倍。众所周知,IE患者的病死率较高(10%~30%)[3-4],故二尖瓣脱垂患者积极预防IE尤为重要,美国心脏协会强调需保持良好的口腔卫生,积极根除牙病,同时保留对预后不良或高危患者抗生素的预防治疗[4]。另外,据挪威OI注册表中99例患者瓣膜病的报告显示:有10.1%轻度和10.1%中度主动脉瓣关闭不全,57.5%轻度和7.1%中度二尖瓣反流[5]。此外,OI不仅仅累及心脏瓣膜,近年有新研究表明,其对心室结构和功能也具一定影响:成人OI患者左心室及右心室的舒缩功能较对照组均降低,根据回归分析显示,OI是一个重要独立的危险因素作用于右室心肌功能[6]。
虽然心脏瓣膜异常在OI中较为少见,但若合并严重的瓣膜性心脏病者,则需行人工瓣膜置换术或瓣膜成形术。此时,心脏手术病死率和并发症发病率的增加又与OI相关。OI患者行心脏外科手术的风险增加15%~25%,其原因是由于潜在的结缔组织疾病,引起组织和毛细血管脆性增加、血小板功能障碍、凝血机制异常等,从而导致大量出血或伤口愈合欠佳、迟缓[7-8]。上世纪90年代,OI患者行心外科手术的存活率不容乐观,据Thibault[9]报道的20例OI合并心脏瓣膜病患者,13例行心外科手术治疗,其中6例死于术后早期,4例行心脏瓣膜置换术者只有l例存活。随着医学研究的发展、前沿技术的不断涌现,术者们不断学习提高累积经验且乐于互相交流,现如今,局势较前有一定改善,然术后并发症的现象仍层出不穷。据2013年Najib等[8]报道的5例OI合并心脏瓣膜病的男性患者中,平均年龄为48.6岁,其中3例行主动脉瓣置换术(AVR),1例行AVR和二尖瓣修复成形术,另1例行二尖瓣修复成形术。手术过程中大多数患被注意到存有松散组织和出血的情况,术后5例患者LVEF均较前下降,其中1例需要植入双腔埋藏式除颤仪。由此可知,组织脆性和手术过程止血困难依然是外科治疗所面临的挑战。虽有文献报道OI患者行二尖瓣膜置换术生物瓣安全性优于机械瓣,但由于个体差异不同,外科术前仍需仔细评估与思考[10]。同时,OI患者术后心功能的改善、并发症的减少、存活率的上升及生活质量的提高也是临床治疗中可掌握和发展的新机遇。
[1]周琦,白露.成骨不全的相关研究进展[J].现代预防医学,2014,41(3):572-575.
[2]Deyle D R,Khan I F,Ren G,et al.Normal collagen and bone production by genetargeted human osteogenesis im-perfecta iPSCs[J].Mol Ther,2012,20(1):204-213.doi:10.1038/mt.2011.209.
[3]Que Y-A,Moreillon P.Infectious endocarditis[J].Nat Rev Cardiol2011,8:322-336 doi:10.1038/nrcardio.2011.43
[4]Vandersteen A M,Lund A M,Ferguson D J,et al.Four patients with Sillence type I osteogenesis imperfecta and mild bone fragility,complicated by left ventricular cardiac valvular disease and cardiac tissue fragility caused by type I collagen mutations[J].Am J Med Genet A,2014,164A(2):386-391.doi:10.1002/ajmg.a.36285.
[5]Radunovic Z,Wekre L L,Diep L M,et al.Cardiovascular abnormalities in adults withosteogenesis imperfecta[J].Am Heart J,2011,161(3):523-529.doi:10.1016/j.ahj.2010.11.006.
[6]Radunovic Z,Steine K.Prevalence ofCardiovascular Disease and Cardiac Symptoms:Left and Right Ventricular Function in Adults With Osteogenesis Imperfecta[J].Canadian Journal of Cardiology,2015,31(11):1386-1392.doi:10.1016/j.cjca.2015.04.016.
[7]Dimitrakakis G,Pericleous A,Dimitrakaki I A.Osteogenesis imperfecta in cardiac surgery[J].Asian Cardiovascular and Thoracic Annals,2013,21(1):116-117.doi:10.1177/0218492312463149.
[8]Najib MQ,Schaff H V,GanjiJ,et al.Valvular Heart Disease in Patients with Osteogenesis Imperfecta[J].2013,28(2):139-143.doi:10.1111/jocs.12064.
[9]Thibault G E.Clinical problem-solving.The heart of the matter[J].N Engl J Med,1993,329(19):1406-1410.doi:10.1056/NEJM199311043291909.
[10]Dimitrakakis G,Challoumas D,von Oppell U O.What type of valve is most appropriate for osteogenesis imperfecta patients?[J].Interactive Cardio-Vascular and Thoracic Surgery,2014,19(3):499-504.doi:10.1093/icvts/ivu152.
10.12056/j.issn.1006-2785.2017.39.22.2016-1007
310016 杭州,浙江大学医学院附属邵逸夫医院心内科
何红,E-mail::hehong179@163.com
2017-05-03)
沈昱平)

