分散液液微萃取-气相色谱法测定复杂食品基质中对羟基苯甲酸酯类
何浩,陈幸莺,*,梁林富,钟鹏鹏,蔡永,孙映球,赵娟
(1.湘潭市食品药品检验所,湖南湘潭411100;2.中南林业科技大学,湖南长沙410004)
分散液液微萃取-气相色谱法测定复杂食品基质中对羟基苯甲酸酯类
何浩1,陈幸莺1,*,梁林富2,钟鹏鹏1,蔡永1,孙映球1,赵娟1
(1.湘潭市食品药品检验所,湖南湘潭411100;2.中南林业科技大学,湖南长沙410004)
建立复杂食品基质中对羟基苯甲酸酯类及其钠盐的分散液液微萃取(Dispersive Liquid-Liquid Microextraction,DLLME)-气相色谱(Gas Chromatography,GC)检测方法。样品浸泡在水中,经煮沸和超声两个步骤提取目标物质。取4 mL待测液,调节pH后分别加入0.6 g氯化钠,0.3 mL四氯化碳和0.6 mL丙酮,手动和涡旋萃取,离心后取下层有机相分析,外标法定量。该方法在25 mg/kg~1 000 mg/kg范围内线性良好,r2为0.997 2~0.999 0,回收率为95.6%~99.2%,相对标准偏差均小于4.0。对羟基苯甲酸甲酯、乙酯、丙酯和丁酯的定量下限为1.2 mg/kg~3.2 mg/kg。
分散液液微萃取;气相色谱法;对羟基苯甲酸酸酯类;复杂食品基质
样品前处理是食品添加剂检测的一个重要步骤。食品基质复杂,各种添加剂和天然成分众多,食品中目标物质的提取和净化是一个复杂、繁琐和重要的工作。食品前处理的方法主要有液液萃取(liquid-liquid extraction,LLE)[1],固相萃取 (solid phase extraction,SPE)[2]、超临界萃取(supercritical fluid extraction,SFE)[3]。各种试剂消耗量小的微萃取技术得到较大发展,主要包括固相微萃取(solid-phase microextraction,SPME)[4]、溶剂微萃取(solvent microextraction,SME)[5]、液相微萃取(liquid phase microextraction,LPME)[6]、单液滴微萃取(single drop microextraction,SDME)[7]等。M Rezaee[8]等首次系统地提出了分散液液微萃取方法(dispersive liquid-liquid microextraction,DLLME),该方法汲取浊点萃取和均质液液萃取的优点,具有萃取效率高,平衡时间快,试剂使用少,回收率和准确率高等优点,是一个集萃取和富集于一体的前处理方法。
对羟基苯甲酸酯类,俗称尼泊金酯,是食品和化妆品中常用的一种广谱防腐剂。GB2760-2014《食品安全国家标准食品添加剂使用标准》[9]规定对羟基苯甲酸酯类及其钠盐可在醋、酱油、碳酸饮料及其酱制品中适量使用,其最大使用量为0.012 g/kg~0.5 g/kg。检测食品中对羟基苯甲酸酯类的方法主要有气相色谱法[10-12]、液相色谱法[13]、气质联用法[14]等。张茂升[15]等研究水中苯、甲苯、二甲苯的分散液液微萃取/气相色谱-氢离子火焰(DLLME/GC-FID)测定方法,韩熠[16]等研究饮料中4种对羟基苯甲酸酯类的测定方法。学者主要对萃取剂、分散剂的种类和体积、离子强度、萃取时间等做了研究。研究主要集中于液体样品中有机物的提取与测定,主要使用的萃取剂有三氯甲烷、四氯甲烷、二氯乙烯、乙酸乙酯、正辛醇等,分散剂主要有丙酮、乙腈、甲醇等。本文研究DLLME/GC-FID测定食品中对羟基苯甲酸甲酯、乙酯、丙酯、丁酯的方法,采用四氯化碳作为萃取剂、丙酮作为分散剂,实现复杂食品基质中对羟基苯甲酸酯类及其钠盐的同时提取和测定。
1 试验部分
1.1 仪器与试剂
GC2010plus型气相色谱仪(配FID检测器)、ATY224电子天平:日本岛津公司;HP-5石英毛细管柱(30 m×0.32 mm,0.25 μm):美国安捷伦公司;MS3数显型混匀器:德国IKA公司;TG16-WS台式高速离心机:湖南湘仪公司;HH-4恒温水浴锅:常州智博瑞仪器制造有限公司;KQ-500VDV型超声波清洗器:昆山市超声仪器有限公司;微量进样器(100 μL):上海安亭微量进样器厂。
对羟基苯甲酸甲酯、对羟基苯甲酸乙酯、对羟基苯甲酸丙酯标准品:中国食品药品检定研究院;对羟基苯甲酸丁酯:美国AccuStandard公司;丙酮、无水乙醇、三氯甲烷、四氯化碳(色谱纯)、盐酸(优级纯):国药集团化学试剂有限公司;乙腈(色谱纯):迪马科技有限公司;氯化钠、二水乙酸锌(分析纯):西陇化工股份有限公司;亚铁氰化钾(分析纯):天津市光复科技发展有限公司;B-广泛试纸(pH 1~14):上海三爱思试剂有限公司。
榨菜、酱油、食用槟榔等:当地超市。
1.2 试验方法
1.2.1 标准物质的配制
准确称取0.1 g(精确至0.000 1 g)对羟基苯甲酸甲酯、乙酯、丙酯和丁酯标准物质,用丙酮溶解后移入100 mL容量瓶中,定容摇匀,4种标准物质的浓度均为1 000 μg/mL,作为标准物质储备液,于-4℃保存。使用时用丙酮逐级稀释至所需浓度。
1.2.2 样品溶液的制备
准确称取样品约10 g于100 mL具塞比色管中,加去离子水至约80 mL,于沸水浴中放置0.5 h,取出后立即超声0.5 h(超声功率为500 W,超声频率为50 kHZ),冷却。加入5 mL 106 g/L亚铁氰化钾溶液,摇匀后加入5 mL 220 g/L乙酸锌溶液,定容,摇匀。静置0.5 h后用中速定性滤纸过滤至250 mL锥形瓶中,样品溶液备用。在榨菜样品中加入 1.6、200、1 000 μg标准物质,做加标回收试验。
1.2.3 样品溶液和标样前处理
用聚乙烯吸管吸取4.0 mL样品溶液至10 mL锥形离心管中,用(1+1)盐酸调节pH至2~5(用pH试纸检测),加入0.6 g氯化钠,摇匀。加入0.3 mL四氯化碳和0.6 mL丙酮,手动振荡200次后立即放在混匀器上,1 000 r/min涡旋60 s,再手动振荡100次,静置5 min后放入离心机中,3 000 r/min离心5 min,用微量进样器移取150 μL离心管底部有机相至1.5 mL进样瓶中,在进样瓶中补加0.85 mL丙酮,进样瓶在混匀器上涡旋10 s,上机。
分别移取含对羟基苯甲酸酯各 10、20、30、40、50、80 μg的标准使用液于10 mL锥形离心管中,定容至4 mL,加入 1滴(1+1)盐酸,加入 0.6 g氯化钠,摇匀。加入0.3 mL四氯化碳,加入一定体积的丙酮(使加入的丙酮和标准物质中带入的丙酮体积之和为0.6 mL),以下步骤同样品溶液的制备。外标法定量。
1.2.4 气相色谱条件
进样量:1 μL;分流比为 10∶1;色谱柱流量:1.49 mL/min;升温程序:80℃(保持 3 min),10℃/min到200℃,(保持3 min)再以20℃/min升温到250℃(保持9.5 min),程序升温总时间为30 min,进样口温度为220℃,检测器温度为260℃。
2 结果与讨论
2.1 萃取剂的选择
萃取剂应符合以下条件:第一,萃取剂的密度应显著大于水的密度,保证离心时萃取剂聚集于锥形离心管底部;第二,萃取剂在水中溶解度应很小,离心后能显著分层;第三,目标物质在有机相的溶解度应远远大于在水相的溶解度,确保萃取效率。本文比较二氯甲烷、三氯甲烷和四氯化碳作为萃取剂的萃取效率。3种试剂在20℃时密度为:二氯甲烷(1.325 g/mL)<三氯甲烷(1.484 0 g/mL)<四氯化碳(1.595 g/mL)。20℃时在水中溶解度为:二氯甲烷(20 g/L)<三氯甲烷(7 g/L)<四氯化碳(0.8 g/L)。因此,选用四氯化碳作为本次试验的萃取剂。
2.2 分散剂的选择
分散剂应选择在水相和有机相都有较高溶解度的物质,在水相中将目标物质提取后,将目标物质转移至萃取剂中。本次试验比较丙酮、乙醇和乙腈作为分散剂时的萃取效率。试验发现,在萃取剂四氯化碳0.3 mL,氯化钠0.6 g条件下,在乙醇和乙腈作为分散剂时,对羟基苯甲酸甲酯和乙酯在萃取剂四氯化碳中浓度很低,而在水相中浓度较高,萃取效率不高。丙酮作为分散剂则达到了预期的效果。
2.3 萃取剂体积的优化
萃取剂体积的大小对萃取效率有重大影响。萃取体积太小,会使水相中目标物质萃取不充分;萃取体积太大,将使水相中的丙酮转移至有机相中,降低了目标物质在萃取剂中的浓度。本次试验比较萃取剂四氯化碳在0.1 mL~0.5 mL条件下,对羟基苯甲酸甲、乙、丙、丁酯的峰面积变化,见图1。本文选用萃取剂体积为0.3 mL。

图1 对羟基苯甲酸甲、乙、丙、丁酯峰面积随四氯化碳体积变化图Fig.1 The peak areas of methyl,ethyl,propyl,butyl paraben with the change of the volume of carbon tetrachloride
2.4 分散剂体积的优化
分散剂体积的大小直接影响萃取剂在水相中微滴的形成和萃取效率。本次试验比较分散剂丙酮在0.1 mL~0.5 mL条件下,对羟基苯甲酸甲、乙、丙、丁酯的峰面积,见图2。
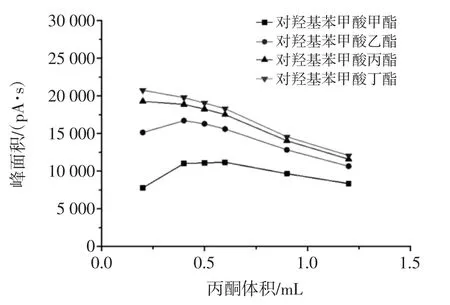
图2 对羟基苯甲酸甲、乙、丙、丁酯峰面积随丙酮体积变化图Fig.2 The peak areas of methyl,ethyl,propyl,butyl paraben with the change of the volume of acetone
对羟基苯甲酸乙酯、丙酯、丁酯的峰面积在丙酮体积在0.1 mL~0.4 mL时逐渐升高,丙酮体积在0.4 mL~1.2mL时逐渐降低。对羟基苯甲酸甲酯的峰面积在丙酮体积为0.1 mL~0.6 mL时逐渐升高,丙酮体积在0.6 mL~1.2 mL时逐渐降低。综合考虑,选择分散剂的体积为0.6 mL。
2.5 离子强度对萃取效率的影响
水相中适当的离子强度将使对羟基苯甲酸酯类的溶解度下降,有利于萃取效率的提高。在水相中分别加入 0.1 g~1.2 g氯化钠(25 g/L~300 g/L),离子强度(氯化钠添加量)见图3。

图3 对羟基苯甲酸甲、乙、丙、丁酯峰面积随离子强度变化图Fig.3 The peak areas of methyl,ethyl,propyl,butyl paraben with the change of the volume of ionic strength
由图3可知,氯化钠添加量为0.6 g(150 g/L)时,萃取效率达到最优值。
2.6 样品测试
四氯化碳0.3 mL,丙酮0.6 mL,氯化钠0.6 g的条件下,标准物质和食用槟榔样品色谱图见图4和图5,样品检验结果见表1。由表1可知,2个食用槟榔和1个酱油中检测出含有对羟基苯甲酸乙酯,其含量符合GB2760-2014《食品安全国家标准食品添加剂使用标准》[9]要求。
2.7 方法学评估
2.7.1 保留时间、标准曲线、r2、检出限和定量限
四氯化碳0.3 mL,丙酮0.6 mL,氯化钠0.6 g的条件下,标准曲线、r2、检出限和定量限见表2。

图4 对羟基苯甲酸甲、乙、丙、丁酯色谱图Fig.4 Chromatogram of methyl,ethyl,propyl,butyl paraben

图5 食用槟榔样品色谱图Fig.5 Chromatogram of edibleareca catechu
2.7.2 富集倍数、回收率和相对标准偏差
富集倍数(enrichment factor,EF)是反应DLLME方法性能的重要参数,其数值等于萃取后萃取剂中目标物质的浓度除以萃取前水相中目标物质的浓度。假设目标物质全部被萃取至萃取剂中,且萃取前后萃取剂和水相的体积不变,则富集倍数等于水相体积除以萃取剂体积,本次试验的富集倍数为13.3。虽然富集倍数不高,但完全能满足试验的要求。

表1 样品测试结果(n=3)Table 1 Test results of the sample(n=3)
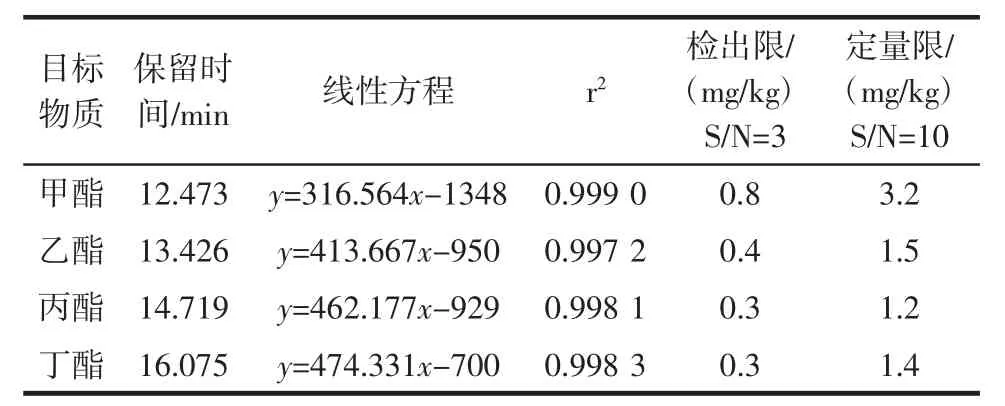
表2 保留时间、线性方程,r2、检出限和定量限(n=3)Table 2 Retention time,linear equation,r2,detection limit and limit of quantification(n=3)
在榨菜样品中添加对羟基苯甲酸酯类,做10、200、500 mg/kg三水平加标回收试验,回收率和相对标准偏差见表3。

表3 回收率和相对标准偏差(n=5)Table 3 Recovery rate and relative standard deviation(n=5)
线性范围为25 mg/kg~1 000 mg/kg。由表3可知,r2、相对标准偏差均能符合实验室质量控制要求[17],甲酯、乙酯、丙酯的回收率也能符合实验室质量控制要求,但丁酯的回收率达不到要求(90%~110%)。分析试验过程,甲酯、乙酯、丙酯和丁酯的水溶性依次变差,丁酯回收率低是样品前处理的过程引起的,引进系数f可以有效解决这一问题,f等于1除以回收率,本次试验f值为1.18。
2.8 创新点和试验改进
1)学者主要分析水样中目标物质的检测,而本文对复杂基质食品前处理转化为水样待测液后进行检测,提高了DLLME的适用范围。2)对羟基苯甲酸酯类在不同的食品中有不同的状态,大部分食品中以钠盐的形式存在,在一些食品中以酯类的形式存在。对羟基苯甲酸酯钠盐易溶于水,而酯类在冷水中溶解度小。本文采用沸水浴和超声两种提取方式,可以将食品中存在的钠盐和酯类完全提取出来,保证了回收率达到实验室要求。在添加萃取剂和分散剂之前,将待测样液pH值调至偏酸性,使对羟基苯甲酸酯钠盐转化为酯类,可提高萃取效率。3)本文在萃取剂的体积上作了较大改变,多数学者将萃取剂体积设为5 μL~100 μL,而本文将萃取体积改为300 μL。萃取剂体积的增大能提高萃取效率,减少萃取时间。将150 μL萃取剂移入样品瓶,定容至1 mL后,能实现自动进样器连续进样,也减少了相对标准偏差。4)本文将标准物质进行前处理后再进气相色谱分析,将萃取效率和萃取剂体积的变化影响降到最低,提高了试验的准确性和精密度。5)考虑到丁酯回收率不高的问题,引入系数f可以有效解决这一问题。
3 结论
本文建立复杂食品基质4种对羟基苯甲酸酯及其钠盐的液液微萃取-气相色谱检测方法。对萃取剂种类和体积、分散剂种类和体积以及离子强度等条件进行优化,得到了最佳萃取条件为待测液4 mL,四氯化碳0.3 mL,丙酮0.6 mL,氯化钠0.6 g,加标回收率为95.6%~99.2%,线性范围为 25 mg/kg~1 000 mg/kg,r2为0.997 2~0.999 0,RSD均小于4,是一种快速、准确、环保、节约的检测固态和液态食品中对羟基苯甲酸酯及其钠盐含量的方法。
[1]O Krüger,G Christoph,U Kalbe,et al.Comparison of stir bar sorptive extraction(SBSE)and liquid–liquid extraction(LLE)for the analysis of polycyclic aromatic hydrocarbons(PAH)in complex aqueous matrices[J].Talanta,2011,85(3):1428-34
[2]AL Heffernan,K Thompson,G Eaglesham,et al.Rapid,automated online SPE-LC-QTRAP-MS/MS method for the simultaneous analysis of 14 phthalate metabolites and 5 bisphenol analogues in human urine[J].Talanta,2016,151:224-233
[3]A Mariod,M Ismail,NFA Rahman,et al.Stability of rice bran oil extracted by SFE and soxhlet methods during accelerated shelf-life storage[J].Grasas Y Aceites,2014,65(1):13
[4]D Djozan,Y Assadi.Modified Pencil Lead as a New Fiber for Solid-Phase Microextraction[J].Chromatographia,2004,60(5):313-317
[5]LS de Jager,AR Andrews.Development of a rapid screening technique for organochlorine pesticides using solvent microextraction(SME)and fast gas chromatography(GC)[J].Analyst,2000,125(11):1943-1948
[6]谭小旺,宋燕西,魏瑞萍,等.三相中空纤维膜液相微萃取-高效液相色谱法测定水中痕量双酚A[J].分析化学,2012,40(9):1409-1414
[7]JPD Anjos,JBD Andrade.Simultaneous determination of pesticide multiresidues in white wine and rosé wine by SDME/GC-MS[J].Microchemical Journal,2015,120:69-76
[8]M Rezaee,Y Assadi,MRM Hosseini,et al.Determination of organic compounds in water using dispersive liquid–liquid microextraction[J].Journal of Chromatography A,2006,1116(1/2):1-9
[9]国家卫生和计划生育委员会.GB2760-2014食品安全国家标准食品添加剂使用标准[S].北京:中国标准出版社,2014
[10]国家卫生和计划生育委员会.GB/T5009.31-2016食品安全国家标准食品中对羟基苯甲酸酯类的测定[S].北京:中国标准出版社,2016
[11]谢敢爱,何浩.槟榔中对羟基苯甲酸酯类的快速测定-气相色谱法[J].商品与质量,2012(12):262
[12]陈幸莺.食品中12种防腐剂多通量测定方法的研究[J].食品与机械,2015,31(2):134-139
[13]山东省质量技术监督局.DB37/T1100-2008食品中对羟基苯甲酸酯类的测定高效液相色谱法[S].山东:中国标准出版社,2008
[14]郝鹏飞,徐琴,牟志春,等.气相色谱-质谱法同时测定葡萄酒中13种防腐剂[J].分析实验室,2013,32(7):108-112
[15]张茂升,黄佳蓉,郑向华.等.分散液液微萃取-气相色谱法测定水中苯、甲苯和二甲苯[J].分析实验室,2010,29(6):85-88
[16]韩熠,刘欣丽,贾晓宇.等.分散液液微萃取-气相色谱-质谱联用法测定饮料中4种对羟基苯甲酸酯类防腐剂[J].分析化学,2009,37(2):151
[17]国家质量技术监督检验检疫总局.GB/T 27404-2008实验室质量控制规范食品理化检验[S].北京:中国标准出版社,2008
Determination of p-hydroxy Benzoates in Complex Food Matrix Using Dispersive Liquid-Liquid Microextraction/Gas Chromatography
HE Hao1,CHEN Xing-ying1,*,LIANG Lin-fu2,ZHONG Peng-peng1,CAI Yong1,SUN Ying-Qiu1,ZHAO Juan1
(1.Xiangtan Institute for Food and Drug Control,Xiangtan 411100,Hunan,China;2.Central South University of Forestry and Technology,Changsha 410004,Hunan,China)
A dispersive liquid liquid microextraction(DLLME)and gas chromatographic(GC)method for the determination of p-hydroxy benzoates and its salts in complex food matrix was established.Sample was soaked in water,using boiling and ultrasound two steps to extract the target material.Take 4 mL sample solution,after adjusting pH,0.6 g sodium chloride,0.3 mL carbon tetrachloride and 0.6 mL acetone were added.Using manualandvortexextraction,aftercentrifugation,the organic phase was analyzed.The linearity was good in 25 mg/kg-1 000 mg/kg using this method,r2was 0.997 2-0.999 0,the recovery rate was 95.6%-99.2%,the relative standard deviation was less than 4.0.The lower limit of quantification for methyl,ethyl,propyl,butyl paraben was 1.2 mg/kg-3.2 mg/kg.
dispersive liquid-liquid microextraction;gas chromatography;p-hydroxy benzoates;complex food matrix
10.3969/j.issn.1005-6521.2017.23.028
湖南省食品药品监督管理局食品药品安全科技项目(R201715)
何浩(1986—),男(汉),工程师,硕士,研究方向:食品质量安全。
*通信作者
2017-04-21

