基于β-咔啉希夫碱的Al3+荧光探针的合成及其性能研究
韩雅莲,但飞君,刘璐璐,曾 敏,陈 玲,兰海闯
(三峡大学 生物与制药学院,湖北 宜昌 443002)
基于β-咔啉希夫碱的Al3+荧光探针的合成及其性能研究
韩雅莲,但飞君*,刘璐璐,曾 敏,陈 玲,兰海闯
(三峡大学 生物与制药学院,湖北 宜昌 443002)
以L-色氨酸甲酯盐酸盐和2-喹啉甲醛为原料,通过多步反应合成3-{N′-(2-羟基苯亚甲基)甲酰肼基}-1-(喹啉-2-基)-9H-β-咔啉(QCS),并通过1H NMR、13C NMR、ESI-MS对其结构进行了表征。探针QCS对Al3+有特异性响应,可在9~100 μmol/L范围定量检测Al3+,相关系数r2=0.999 1,检出限为4.40×10-9mol/L。在乙醇-水(体积比9∶1)的混合体系中,探针与Al3+的络合比为1∶1,络合常数Ka=(2.91±0.22)×103(mol/L)-1,且该探针与Al3+络合后的荧光强度在pH 5.0~8.0范围保持稳定,满足环境水样及生命体系的检测条件要求。
β-咔啉;喹啉;希夫碱;Al3+探针
铝是地壳中含量最多的金属元素,被广泛应用于建筑材料、电气传输、水净化和食品添加剂等领域[1]。但过量的铝会使植物枯萎甚至死亡,人体内铝积累过多时,易引起神经病症[2]。据世界卫生组织报道,人体内铝的日均摄入量为3~10 mg[3]。我国环境保护局标准规定饮用水中的Al3+浓度不高于0.05 mg/L[4],因此Al3+的检测至关重要。迄今报道的Al3+的检测方法包括电感耦合等离子体法、原子吸收法、离子质谱法等,荧光分析法因具有操作简便、灵敏性高、检出限低等优点,得到了广泛的应用[5]。由于Al3+水合作用强导致其络合能力弱,设计在水介质中高选择性和灵敏性的Al3+荧光探针成为科学家研究的热点与难点[6]。
希夫碱化合物含有N原子,可与金属离子形成配位键,是良好的配体[7],在荧光探针的构建中有着广泛应用[8]。近年来,Al3+荧光探针[9-10]多有报道。但以β-咔啉为荧光基团的Al3+荧光探针较少。β-咔啉具有吡啶并吲哚环的平面结构,是良好的发光体,可用于荧光材料的构建[11]。基于此,本课题组设计并合成了以β-咔啉为荧光基团,水杨酰腙为识别基团和连接体的荧光探针QCS,并对其进行了光谱性能分析和研究。结果表明QCS能够在乙醇-水(体积比9∶1)的混合体系中对Al3+进行定性和定量检测。
1 实验部分
1.1 试剂与仪器
400 MHz核磁共振波谱仪(TMS为内标,溶剂CDCl3,瑞士Bruker公司),ESI-MS质谱仪(德国Bruker公司),F-4600荧光光谱仪(日本Hitachi公司),UV-2600紫外-可见分光光度仪(日本Shimadzu公司),PHS-3C酸度计(上海雷磁仪器厂),WRS-1A型熔点仪(上海索光光电技术有限公司)。光谱测试中使用二次蒸馏水,14种金属硝酸盐固体[Al(NO3)3·9H2O、Ca(NO3)2·4H2O、Cr(NO3)3·9H2O、Mn(NO3)2、Fe(NO3)3·9H2O、Co(NO3)2·6H2O、Ni(NO3)2·6H2O、Cu(NO3)2·3H2O、Zn(NO3)2·6H2O、AgNO3、Cd(NO3)2·4H2O、Ba(NO3)2、Hg(NO3)2、Pb(NO3)2],其他试剂和原料均为分析纯(国药集团化学试剂有限公司)。
1.2 合成路线
1.2.13-甲酸甲酯-1-(喹啉-2-基)-9H-β-咔啉(化合物3)的合成参考文献[12]以L-色氨酸甲酯盐酸盐(化合物1)和2-喹啉甲醛(化合物2)为原料合成3-甲酸甲酯-1-(喹啉-2-基)-9H-β-咔啉,产率:35.69%。m.p.:220.8~222.2 ℃。ESI-MS(m/z):354.1767[M+H]+。1H NMR(400 MHz,CDCl3)∶δ11.92(s,1H),9.02(d,J=8.7 Hz,1H),8.95(s,1H),8.36(d,J=8.7 Hz,1H),8.29(d,J=8.4 Hz,1H),8.24(d,J= 7.9 Hz,1H),7.91(d,J=8.1 Hz,1H),7.86~7.77(m,1H),7.73(d,J=8.2 Hz,1H),7.69~7.55(m,2H),7.39(t,J=7.5 Hz,1H),4.11(s,3H)。
1.2.23-甲酰肼-1-(喹啉-2-基)-9H-β-咔啉(化合物4)的合成向250 mL烧瓶中,加入3.53 g(10 mmol) 3-甲酸甲酯-1-(喹啉-2-基)-9H-β-咔啉、50 mL乙醇和100 mL甘油,搅拌1 h;加入10.00 g(200 mmol)水合肼,回流4 h;冷却,抽滤,再用30 mL乙醇洗涤3次,真空干燥,得固体3.32 g,收率:94.05%。m.p.:263.9~261.9 ℃。ESI-MS(m/z):354.1834[M+H]+。1H NMR(400 MHz,DMSO):δ12.32(s,1H),10.24(s,1H),9.39(d,J=8.7 Hz,1H),9.00(s,1H),8.79(d,J=8.4 Hz,1H),8.60(d,J=8.8 Hz,1H),8.50(d,J=7.8 Hz,1H),8.12 ~ 8.06(m,2H),7.94~7.90(m,1H),7.73~ 7.67(m,2H),7.38(t,J=7.4 Hz,1H),4.68(s,2H)。
1.2.33-{N′-(2-羟基苯亚甲基)甲酰肼基}-1-(喹啉-2-基)-9H-β-咔啉(QCS)的合成合成路线如图1所示。向100 mL烧瓶中加入0.353 0 g(1 mmol) 3-甲酰肼-1-(喹啉-2-基)-9H-β-咔啉、0.122 0 g(1 mmol)水杨醛,15 mL乙醇和30 mL甘油,回流3 h,TLC跟踪反应完全,冷却,抽滤,再用10 mL乙醇洗涤,真空干燥,得QCS 0.389 1 g,收率:85.14%。m.p.>300 ℃。ESI-MS(m/z):458.174 6[M+H]+。1H NMR(400 MHz,DMSO):δ12.42(s,1H),12.31(s,1H),11.55(s,1H),9.39(d,J=8.7 Hz,1H),9.14(s,1H),9.04(s,1H),8.81(d,J=8.4 Hz,1H),8.67(d,J=8.7 Hz,1H),8.53(d,J=7.8 Hz,1H),8.14 ~ 8.08(m,2H),7.93(t,J=7.2 Hz,1H),7.74 ~ 7.69(m,2H),7.61(d,J=6.9 Hz,1H),7.42 ~ 7.33(m,2H),6.98(t,J=7.8 Hz,2H)。
1.3 荧光光谱测定方法
称取0.002 4 g化合物QCS,溶于10 mL DMF中配制成1.0×10-3mol/L的储备液,放置备用。测试均在乙醇-水(9∶1)混合液中进行,金属硝酸盐的浓度为1.0×10-2mol/L,所有测试重复3次。在一定量的乙醇-水(9∶1)混合溶液中加入盐酸或氢氧化钠调节pH值,配制pH 2.02、2.97、3.55、4.70、5.70、6.22、7.21、8.46、9.48、10.38、11.04、12.06、13.10的系列缓冲溶液。荧光参数λem为375 nm,Ex、Em的狭缝宽度均为5 nm,电压为500 V。
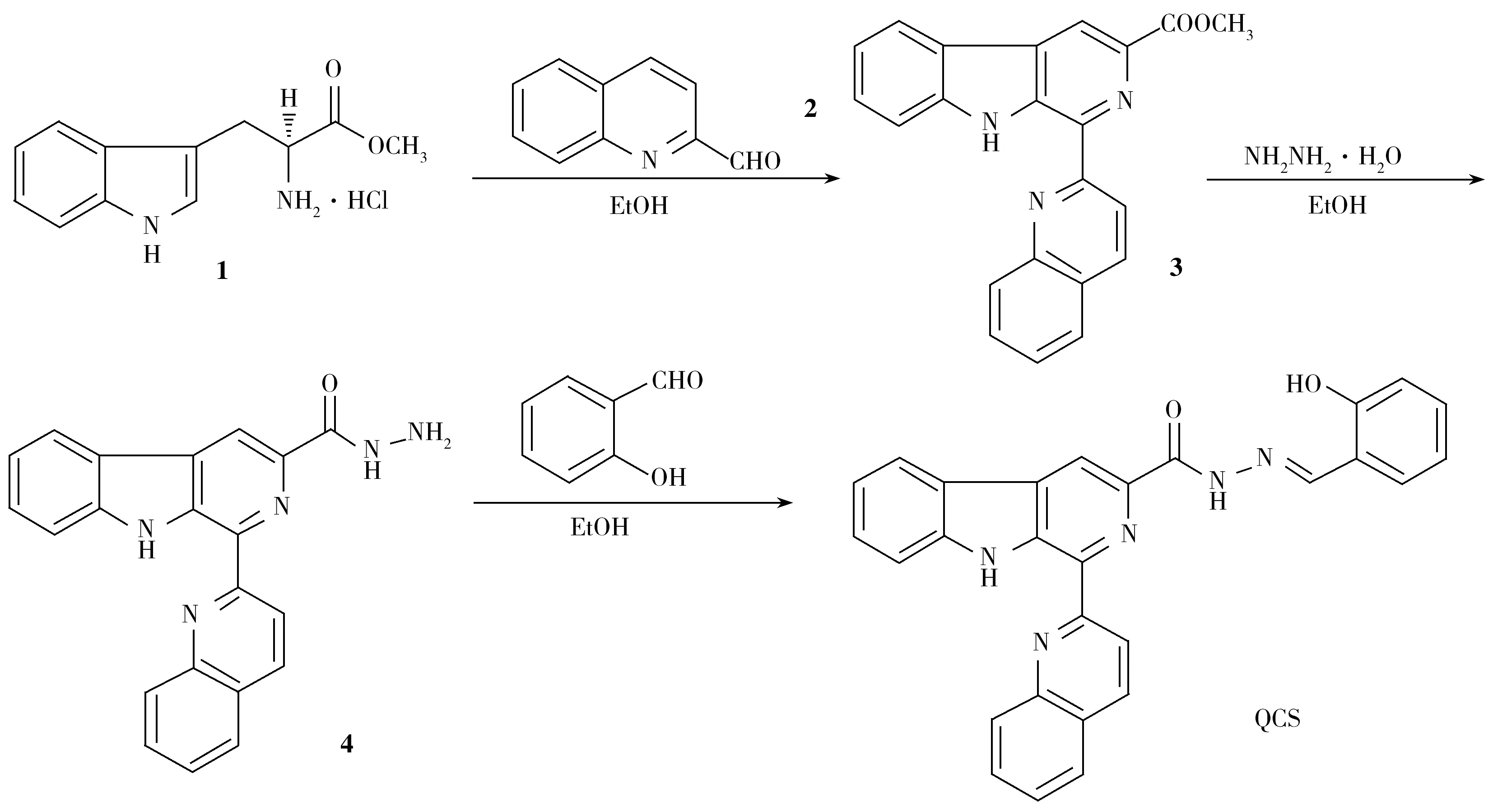
图1 QCS的合成路线Fig.1 Synthesis routes of QCS
2 结果与讨论
2.1 探针QCS对金属离子的识别
在乙醇-水(9∶1)混合溶液中,分别测定空白试样和探针QCS识别14种金属离子(Al3+、Ca2+、Cr3+、Mn2+、Fe3+、Co2+、Ni2+、Cu2+、Zn2+、Ag+、Cd2+、Ba2+、Hg2+、Pb2+)的荧光发射光谱,如图2A所示。同时,为了进一步考察探针QCS的选择性,进行了抗干扰测试,结果如图2B所示。

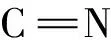
由图2B可见,当Al3+与其他金属离子共存时,除Cu2和Zn2+使体系发生荧光猝灭外,其他金属离子基本不会干扰探针QCS对Al3+的响应。推测Cu2+和Zn2+对其的干扰可能是Cu2+、Zn2+与QCS的络合能力比Al3+强。饮用水、自来水、铝厂废水等实际样品中一般不含Cu2+或Zn2+,故Cu2+和Zn2+对Al3+的检测无影响。实验结果表明探针QCS能够特异性识别Al3+。
2.2 不同浓度的Al3+对探针QCS荧光强度的影响
在混合液中,考察了不同浓度的Al3+(0~100 μmol/L)对探针QCS(10 μmol/L)荧光光谱的影响。结果显示,随着Al3+浓度的增加,在425 nm处的荧光强度不断增强并红移至490 nm处,且当Al3+过量时荧光强度仍有增强趋势,表明探针QCS与Al3+有良好的络合作用。在9~100 μmol/L浓度范围内,Al3+浓度(x)与相应的荧光强度(y)呈良好的线性关系,线性回归方程为y=-133.428 78+17.035 83x(r2=0.999 1)。表明在9~100 μmol/L浓度范围内,探针QCS可实现对Al3+的定量检测。依据公式LOD=3SD/b[14]计算得检出限为4.40×10-9mol/L,低于我国环境保护局标准规定饮用水中可存在Al3+的最高浓度,可用于监测饮用水的水质。
2.3 探针QCS对Al3+的响应测试
为了研究探针QCS的适用性,考察了pH值和时间对探针QCS识别Al3+的影响。荧光光谱结果显示,探针在一系列pH值缓冲溶液中未显示出明显的荧光发射。加入Al3+后,在pH 5.0~8.0条件下探针QCS结合Al3+后荧光强度保持稳定,但在碱性条件下,QCS-Al3+络合物的荧光强度随着pH值的增加而降低,推测是由于强碱影响了Al3+与探针QCS的络合[15]。该结果表明探针QCS能够满足环境水样及生命体系的检测条件。
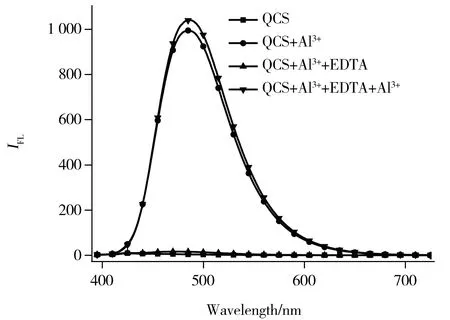
图3 探针QCS对Al3+的可逆荧光响应谱图(λex=375 nm)Fig.3 Reversible fluorescence response of QCS to Al3+(λex=375 nm)
QCS-Al3+络合物的荧光强度随着络合时间的增加而增强,500 s后荧光增强的速率趋于稳定,可认为探针QCS与Al3+的相互作用基本完成。表明探针QCS对Al3+的识别响应迅速。
2.4 探针QCS对Al3+的可逆性荧光响应
对靶向离子的可逆性检测是荧光探针的重要性质。向含有QCS和Al3+的混合液中加入EDTA后,490 nm处的荧光强度降低到未加入Al3+时的荧光强度,表明游离QCS可再生。再加入20 μL浓度为10-2mol/L的Al3+后,荧光再次恢复,如图3所示。因此,通过使用适量的络合剂EDTA可以证实探针QCS的可逆性,实现荧光探针的“off-on-off”功能[16]。
2.5探针QCS与Al3+的络合比与络合常数
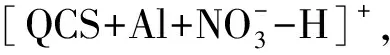
依据荧光定量滴定数据,通过Benesi-Hildebrand方程[18],以1/[Al3+]为横坐标(x),1/(F-F0)为纵坐标(y),线性拟合后得方程:y=-2.454 71×10-4+8.436 75×10-8x(r2=0.998 15),拟合后呈一条直线,进一步表明探针QCS与Al3+的络合比为1∶1,络合常数Ka=(2.91±0.22)×103(mol/L)-1。
2.6 机理的探究

3 结 论
本文设计并合成了一种新型探针QCS,其乙醇-水(9∶1)混合液中加入Al3+后可观察到荧光红移且强度增强580倍,该探针可以定性、定量检测Al3+且基本不受其他金属离子的干扰,检出限为4.40×10-9mol/L。探针QCS与Al3+的络合比为1∶1。同时探针QCS对Al3+的响应是可逆的,可以通过使用合适的络合剂如EDTA再循环,实现荧光探针的“off-on-off”功能。
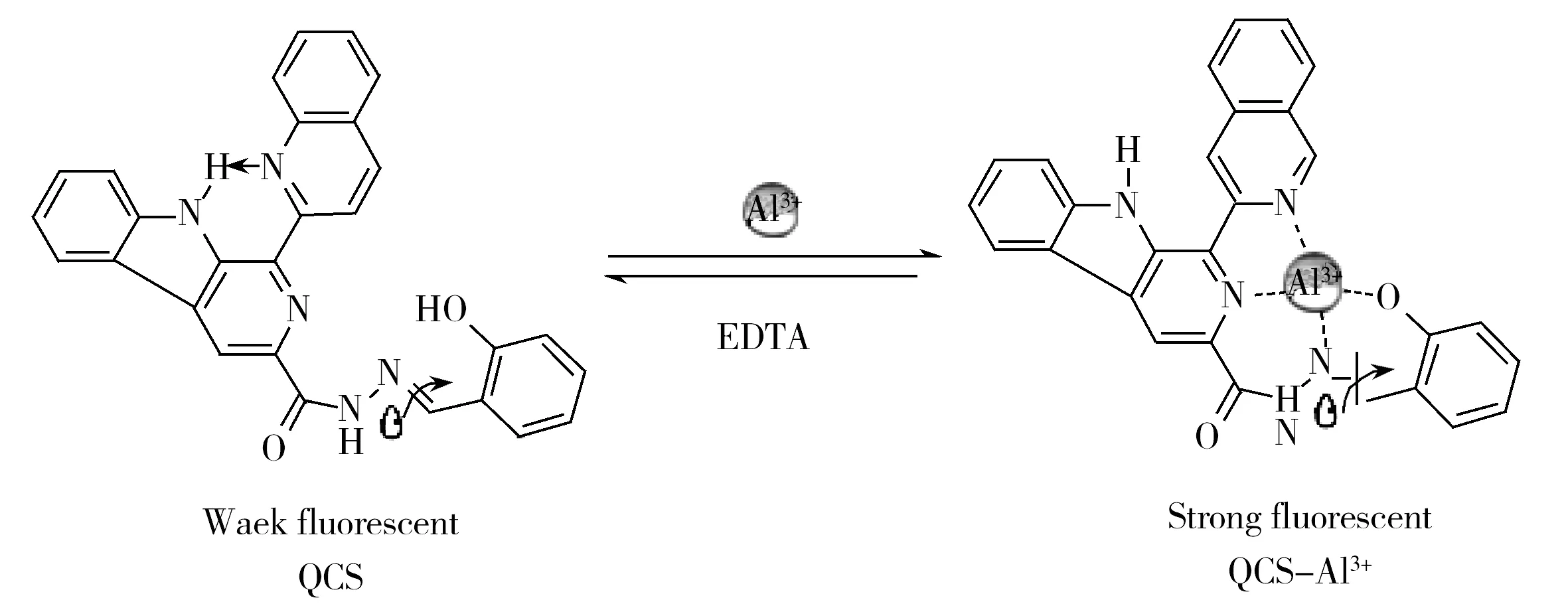
图4 探针QCS识别Al3+的可能机理Fig.4 The possible recognition mechanism of QCS for Al3+
[1] Li C Y,Zhou Y,Li Y F,Zou C X,Kong X F.Sens.ActuatorsB,2013,186:360-366.
[2] Sen B,Sheet S K,Thounaojam R,Jamatia R,Pal A K,Aguan K,Khatua S.Spectrochim.ActaPartA,2017,173:537-543.
[3] Gan X P,Li W,Li C X,Wu Z C,Liu D,Huang B,Zhou H P,Tian Y P.Sens.ActuatorsB,2017,239:642-651.
[4] Wang L,Qin W W,Tang X L,Dou W,Liu W S,Teng Q F,Yao X J.Org.Biomol.Chem.,2010,8(16):3751-3757.
[5] Ma T,Zhang J,Liu L Z,He Y,Zhang Z T.Chin.J.Org.Chem.(马拓,张瑾,刘龙珠,贺云,张尊听.有机化学),2014,34:1780-1785.
[6] Qin J C,Yang Z Y.J.Photochem.Photobiol.A,2015,303:99-104.
[7] Wang R,Jiang G Q,Li X H.Inorg.Chim.Acta,2017,455:247-253.
[8] Shi X Y,Wang H,Han T Y,Feng X,Tong B,Shi J B,Zhi J G,Dong Y P.J.Mater.Chem.,2012,22(36):19296-19302.
[9] Hossain S M,Singh K,Lakma A,Pradhan R N,Sing A K.Sens.ActuatorsB,2017,239:1109-1117.
[10] Sheet S K,Sen B,Thounaojam R,Aguan K,Khatua S.J.Photochem.Photobiol.A,2017,332:101-111.
[11] Laine A E,Lood C,Koskinen A M P.Molecules,2014,19(2):1544-1567.
[12] Ramesh S,Nagarajan R.J.Org.Chem.,2013,78(2):545-558.
[13] Liu T Q,Wan X J,Dong Y S,Li W B,Wu L S,Pei H,Yao Y W.Spectrochim.ActaPartA,2017,173:625-629.
[14] Manivannan P,Satheshkumar A,Elango K P.TetrahedronLett.,2014,55(45):6281-6285.
[15] Wen X Y,Fan Z F.Anal.Chim.Acta,2016,945:75-84.
[16] Hossain S M,Singh K,Lakma A,Pradhan R N,Singh A K.Sens.ActuatorsB,2017,239:1109-1117.
[17] Li Z Y,Yan J B,Yin Y,Xu D F,Sun X Q.J.Instrum.Anal.(李正义,严金贝,殷乐,徐德峰,孙小强.分析测试学报),2016,35(10):1306-1310.
[18] Jo T G,Bok K H,Han J,Lim M H,Kim C.DyesPigments,2017,139:136-147.
[19] Ponnuvel K,Kumar M,Padmini V.Sens.ActuatorsB,2016,227:242-247.
[20] Dong Z M,Wang W,Qin L Y,Feng J,Wang J N,Wang Y.J.Photochem.Photobiol.A,2017,335:1-9.
[21] Liu H Y,Dong Y S,Zhang B B,Liu F,Tan C Y,Tan Y,Jiang Y Y.Sens.ActuatorsB,2016,24:616-624.
Synthesis and Properties of Al3+Fluorescence Probe Based on β-Carboline and Schiff Base
HAN Ya-lian,DAN Fei-jun*,LIU Lu-lu,ZENG Min,CHEN Ling,LAN Hai-chuang
(College of Biology and Pharmacy,China Three Gorges University,Yichang 443002,China)
(2-Hydroxybenzylidene)-1-(quinolin-2-yl) -9H-pyrido[3,4-b] indole-3-carbohydrazide(QCS) was synthesized by a series of reactions withL-tryptophan methyl ester hydrochloride and 2-quinolinecarboxaldehyde as raw material. The structure of QCS was characterized by1H NMR,13C NMR and ESI-MS. The probe QCS has a specific response to Al3+,and the limit of detection was 4.40×10-9mol/L. QCS showed a good linearity in the concentration range of 9-100 μmol/L with a correlation coefficient(r2) of 0.999 1. In a mixed system of ethanol-water(9∶1,by volume),the binding ratio of QCS and Al3+was 1∶1,and the complexing constant was proved to be(2.91±0.22)×103(mol/L)-1in the fluorescence titration spectra. Furthermore,the fluorescent intensity of QCS-Al3+maintained stable in the pH 5.0-8.0,which satisfied the requirements for detection on environmental water samples and living cells.
β-carboline;quinolone;schiff base;Al3+fluorescent probe
2017-05-06;
2017-08-01
湖北省教育厅科学技术研究计划优秀中青年人才项目(Z2017044)
*
但飞君,博士,副教授,研究方向:有机合成与荧光分析,Tel:13477122150,E-mail:13477122150@163.com
10.3969/j.issn.1004-4957.2017.11.016
O433.4
A
1004-4957(2017)11-1387-05

