石墨烯/硫化钼近红外光催化性能的研究
张 欢,刘守清
(苏州科技大学 化学生物与材料工程学院,江苏 苏州215009;江苏省环境功能材料重点实验室,江苏 苏州 215009)
石墨烯/硫化钼近红外光催化性能的研究
张 欢,刘守清*
(苏州科技大学 化学生物与材料工程学院,江苏 苏州215009;江苏省环境功能材料重点实验室,江苏 苏州 215009)
采用水热法制备了石墨烯/硫化钼杂化材料。采用X射线衍射法、拉曼光谱法、透射电子显微镜法以及紫外-可见-近红外漫反射光谱法等对该杂化材料进行了表征。以此杂化材料为近红外光催化剂,催化降解了罗丹明B(RhB)。结果表明,当RhB溶液浓度为50.0 mg·L-1、溶液的pH值为7、溶液体积为50.0 mL、石墨烯/硫化钼催化剂量为0.05 g、近红外光辐射3 h时,50 mL溶液中RhB的降解率达到了96.5%;而以硫化钼为光催化剂时,RhB的降解率仅为75.5%。杂化光催化剂经过5次循环使用,其催化效率仍在90%以上,表明催化剂十分稳定。
石墨烯/硫化钼;杂化催化剂;近红外光;光催化
利用太阳能解决环境能源问题,起源于1972年Fujishima利用TiO2光电极电解水制氢[1],随后Carey在1976年报道了利用TiO2光催化氧化消除多氯二酚的毒性[2],从此,利用太阳能降解环境污染物迅速成为人们研究的热点。但是,TiO2只能利用占太阳能4%左右的紫外光,对TiO2进行掺杂[3-5]及开发Fe2O3、WO3、Bi2WO6等新型催化剂[6-7],虽然部分解决了对可见光的利用问题,但是占太阳能近50%的红外光尚需开发利用。在可见光光催化持续地被关注的同时,近年来,人们开始把光催化的研究前沿推进到近红外光的利用。Cao等报道了以In2TiO5为催化剂,以近红外光为驱动力,光催化制取了氢气[8];Peng等用酞菁染料敏化g-C3N4,通过近红外光辐射制取了氢气[9];Di等以NaYF4∶Yb,Tm为上转换材料,将近红外光转化为可被TiO2吸收利用的紫外光,通过TiO2光催化降解了亚甲蓝[10];Liu等用碳量子点与Cu2O组成了一种复合纳米结构,这种复合纳米结构材料可以利用近红外光催化降解有机染料[11]。
近几年来,二维材料由于其良好光学和电学特性受到了人们的广泛关注[12]。MoS2与石墨烯类似,具有二维平面结构[13]。作为一种半导体光催化剂,人们研究了MoS2在可见光辐射下的产氢特性[14-21]。而在近红外光的应用方面,文献仅报道了MoS2用于光热药物释放治疗癌症的研究[22]。作为一种半导体材料,MoS2的间接禁带宽度为1.29 eV[23],理论吸收边带可延伸至961 nm,可以吸收近红外光,这为近红外光光催化打下了科学基础。
另一方面,石墨烯(Graphene,G)是近年来研究碳材料的热点,是一种二维单原子层材料,其基本结构单元是六元环[24-25]。石墨烯结构中每个碳原子都提供一个p轨道电子形成离域π键,P电子可以自由移动,使得石墨烯具有较好的导电性[26]。将G与MoS2复合,有望制备对近红外光有催化活性的G/MoS2杂化光催化剂,以期实现对太阳能的充分利用。
笔者采用水热法制备G/MoS2光催化剂,以RhB为模拟污染物,研究近红外光催化降解RhB规律。
1 实验部分
1.1 G/MoS2纳米复合半导体材料的制备
1.1.1 MoS2的制备 取 1.21 g NaMoO4·2H2O(0.005 mol),1.56 g(NH2)2CS(0.020 mol),置于 100 mL 的烧杯中,搅拌直至全部溶解,然后转入聚四氟乙烯水热反应釜中,加入去离子水至反应釜总体积的80%,将反应釜密封,加热至200℃,反应24 h。然后将样品在室温下冷却,用去离子水洗涤,将可溶性物质除去。得到黑色的固体粉末,将其在40℃烘箱中干燥6 h,即得MoS2半导体材料。
1.1.2 氧化石墨(GO)的合成 准确称量 2.0 g石墨、1.0 g NaNO3于 200 mL烧杯中,加入 50 mL浓H2SO4再加入6.0 g KMnO4在温度低于20℃的条件下反应2 h。然后升温至35℃,反应35 min后向反应体系中加入一定量的去离子水,持续搅拌20 min,再用60 mL 5%的H2O2还原残留的高锰酸钾,至溶液成亮黄色,趁热过滤,并用5%的HCl和去离子水洗涤至无SO42-,在60℃真空干燥箱中充分干燥,即得氧化石墨样品,备用。
1.1.3 G/MoS2的制备 在合成MoS2的过程中,NaMoO4·2H2O与(NH2)2CS的混合溶液里面分别加入质量分数分别为1%、3%、5%、7%、9%的GO,200℃水热反应24 h,即得不同G含量的G/MoS2纳米杂化材料。
1.1.4 RhB溶液的配制 称取0.1 g RhB,定容至100 mL,即得浓度为1 mg·mL-1的RhB溶液。
1.1.5 分析表征 样品利用X射线衍射仪(XRD,D/max 2500 pC)、高分辨电镜(TEM,Tecnai G220)、傅里叶红外光谱仪(Spectrum BX,PerkinElmer Ltd,USA)、紫外/可见/近红外光谱仪(UV-Vis,U-4100)和 Raman 光谱仪(LabRAMHR800,France)等进行表征。
1.2 光催化反应
以100 mL的圆底烧杯为光反应器,用锡箔纸将烧杯的四壁包住,以避免紫外光和可见光进入反应体系,用λ>780 nm截止型滤光片覆盖在烧杯口上,以保证只有近红外光辐射进入光反应器。将300 W紫外-可见光灯置于反应器上方,在盛有一定浓度的RhB溶液中加入一定量的催化剂,磁力搅拌,反应过程中每隔20 min取样,离心分离,以紫外-可见分光光度计测定RhB在554 nm处的吸光度,以此计算RhB的降解率。

式中,C0为RhB的初始浓度,A0为初始溶液的吸光度,Ci为剩余RhB的浓度,Ai为剩余RhB的吸光度。
2 结果与讨论
2.1 X射线粉末衍射表征
图1是 MoS2、GO、G 和 G/MoS2样品的 XRD 粉末衍射谱。 在 2θ=14.2°、33.5°、39.5°、59.0°处的衍射峰分别对应于 MoS2的(002)、(100)、(103)和(110)晶面指标。MoS2与 G/MoS2的衍射峰与标准图谱(JCPDS37-1492)一致,因此,可以确定所得样品为MoS2(空间群为P36/mmc)[27]。
图1中曲线(b)是氧化石墨烯的衍射图,在8.5°处出现了氧化石墨的特征衍射峰,说明有大量含氧官能团引入石墨层间[28-29]。曲线(c)是经水热还原后的石墨烯衍射图,与曲线(b)比较可以看出,原有的8.5°处衍射峰消失,而在2θ=24.4°出现一衍射峰,并且峰形弥散、较宽,表明经过水热处理后,GO表面的官能团逐渐被还原,获得由单层或少层石墨烯层片形成的组装结构,晶体结构的完整性下降,无序度增加[28,30]。
曲线(d)是G/MoS2衍射图谱。与硫化钼相比,在相同位置处,出现了硫化钼所具有的晶面指标,同时在25.4°处出现了石墨烯的特征衍射峰,该峰位置出现位移,可能是由于硫化钼引入造成的。
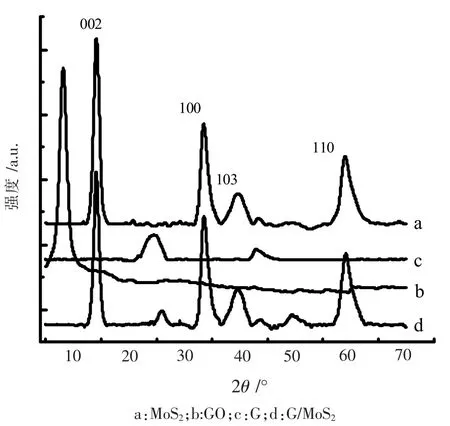
图1 样品的X射线粉末衍射图
2.2 拉曼光谱表征
MoS2单位晶胞是按照六角对称性堆垛而成,属于D6h4空间群(P36/mmc)。根据对称性,MoS2具有4个拉曼活性的振动模式:E2g2,E1g,E2g1,A1g[31]。 由图2(a)看出,位于385 cm-1以及408 cm-1处的拉曼峰分别归属于E2g1和A1g振动,这进一步表明所制备的样品是MoS2。
图2(b)和图2(c)分别代表氧化石墨烯和水热还原处理过的氧化石墨烯的拉曼光谱图。GO和还原氧化石墨烯材料在波数1 335 cm-1和1 600 cm-1附近处有两个重要的特征带,即D带和G带。G带是石墨结构的E2g振动模式,对应于碳原子sp2杂化,D峰是由sp3杂化的C-C单键的伸缩振动产生的,是石墨烯的缺陷和无序的度量。二者的强度比(ID/IG)常用来表征结构的无序程度。通过计算GO的ID/IG=1.27,G的ID/IG=1.88,说明水热处理过的石墨烯变成单层或少层石墨烯层片,sp2平面域的平均尺寸减小,无序度增加[32]。
图2(d)是G/MoS2的拉曼谱图,出现了硫化钼的特征E2g1和A1g振动模式,同时也出现了石墨烯的拉曼峰1 600 cm-1和1 335 cm-1,这进一步表明石墨烯与MoS2成功复合。

图2 拉曼光谱
2.3 透射电镜观察
图3(A)为石墨烯的TEM图,从图3中可知石墨烯为片状结构,也表明此法合成得到了石墨烯。图3(B)为硫化钼的TEM图,其层间距为0.629 nm,是(002)面的面间距,这表明该材料是硫化钼半导体材料。图3(C)为石墨烯/硫化钼杂化材料的TEM图。从图3中可以看出,(002)面的子纹清晰可见,周围则为石墨烯碳材料,这表明石墨烯与硫化钼生成了结构紧密的杂化材料。

图3 样品的透射电镜图
2.4 紫外可见红外漫反射表征
图4给出MoS2、G/MoS2和G样品的漫反射光谱。由图4知两个样品不但在300 nm附近有强吸收峰,在500-850 nm间也存在1个明显的吸收峰,所以样品在紫外区和可见光区具有良好的吸收性能。由于硫化钼负载了石墨烯,复合材料G/MoS2的吸收带发生红移,在近红外区域也具有很好的吸收,因而石墨烯大大提高了催化剂对太阳能的利用率。

图4 样品的紫外-可见-近红外光漫反射光谱
3 RhB降解实验
3.1 RhB的光催化降解
图5表示近红外光辐射下G/MoS2光催化降解RhB的曲线。曲线(a)显示,3 h时RhB降解率达到了96.5%。对比实验表明,当没有杂化催化剂存在时,即使红外光直接照射同浓度的RhB溶液,相同条件下RhB的降解率也只有4.3%,如曲线(d)所示。因此,比较曲线(a)与曲线(d)可知,杂化材料G/MoS2在利用近红外光降解RhB方面起了重要作用。将0.05 g G/MoS2催化剂置于相同浓度的RhB溶液中,在没有光照条件下,3 h后30.3%的RhB被吸附于催化剂表面如曲线(c)所示。在相同条件下,以单组份MoS2为催化剂时,RhB的降解率仅为75.5%如曲线(b)所示,而石墨烯与硫化钼组成的杂化催化剂的降解率显著高于单组分催化剂硫化钼的光催化效率。因此,石墨烯增强了硫化钼的光催化作用。
3.2 RhB初始浓度的影响
用G/MoS2催化剂降解不同初始浓度的RhB,在其他条件相同的情况下得降解曲线如图6所示。结果表明,ln(C0/Ct)与反应时间t成线性关系如图7所示。因此,RhB降解反应遵守一级反应动力学规律。据此可得表观动力学速率常数Kapp,其平均值为0.304 h-1。
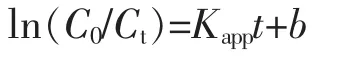

图5 近红外光催化降解RhB

图6 降解不同初始浓度的RhB

图7 ln(C0/Ct)与 t的线性关系图
3.3 催化剂稳定性和重复利用
通过多次循环实验来评价杂化催化剂的稳定性。图8是G/MoS2催化剂在近红外光辐射下连续5次近红外光催化降解RhB的降解率曲线。每一次实验持续3 h,每一次降解结束后,通过离心分离、去离子水洗涤得到催化剂,然后再继续循环使用该催化剂。在5次循环降解RhB后,RhB的降解率仍在90.6%以上。这说明G/MoS2催化剂比较稳定,可重复使用。
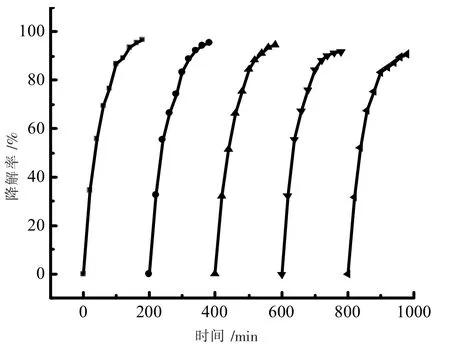
图8 G/MoS2重复循环利用实验
4 结语
采用水热法制备了石墨烯/硫化钼杂化材料,该杂化材料对近红外光具有光催化响应。以此杂化材料为光催化剂,在近红外光照射下可以有效地降解RhB。石墨烯/硫化钼杂化催化剂连续循环使用5次,RhB的降解率仍在90%以上,表明该杂化催化剂十分稳定。因此,该研究的结果表明,近红外光在环境保护领域具有重要的应用价值。
[1]FUJISHIMA A,HONDA K.Electrochemical photolysis of water at a semiconductor electrode[J].Nature,1972,238(5358):37-38.
[2]CAREY J H,LAWRENCE J,TOSINE H M.Photodechlorination of PCB's in the presence of titanium dioxide in aqueous suspensions[J].Bull Environ Contain Toxicol,1976,16(6):697-701.
[3]HOFFMANN M R,MARTIN S T,CHOI W,et al.Environmental applications of semiconductor photocatalysis[J].Chem Rev,1995,95(1):69-96.
[4]RIMEH D,PATRICK D,DIDIER R.Modified TiO2for environmental photocatalytic applications:A review[J].Ind Eng Chem Res,2013,52(10):3581-3599.
[5]BANERJEE S,PILLAI S C,FALARAS P,et al.New insights into the mechanism of visible light photocatalysis[J].J Phys Chem Lett,2014,5(15):2543-2554.
[6]MANEESHA M,DOO-MAN C.α-Fe2O3as a photocatalytic material:A review[J].Applied Catalysis A:General,2015,498(5):126-141.
[7]HE R A,CAO S W,YANG S.Recent advances in visible light Bi-based photocatalysts[J].Chinese Journal of Catalysis,2014,35(7):989-1007.
[8]WEI D,YAO L H,YANG S,et al.Band gap Engineering of In2TiO5for H2production under nearinfrared light[J].ACS Appl Mater Interfaces,2015,7(37):20761-20768.
[9]ZHANG X H,YU L J,ZHUANG C S,et al.Highly asymmetric phthalocyanine as a sensitizer of graphitic carbon nitride for extremely efficient Photocatalytic H2production under near-infrared light[J].ACS Catal,2013,4(1):162-170.
[10]TANG Y N,DI W H,ZHAI X S,et al.NIR-responsive photocatalytic activity and mechanism of NaYF4∶Yb,Tm@TiO2core-shell nanoparticles[J].ACS Catal,2013,3(3):405-412.
[11]LI H T,LIU R H,LIU Y,et al.Carbon quantum dots/Cu2O composites with protruding nanostructures and their highly efficient(near) infrared photocatalytic behavior[J].J Mater Chem,2012,22(34):17470-17475.
[12]张芸秋,梁勇明,周建新.石墨烯掺杂的研究进展[J].化学学报,2014,72(3):367-377.
[13]沈成,张菁,时东霞,等.退火对单层二硫化钼荧光特性的影响[J].化学学报,2015,73(9):954-958.
[14]史建平,马冬林,张艳锋,等.金箔上单层MoS2的控制生长及电催化析氢应用[J].化学学报,2015,73(9):877-885.
[15]CHANG K,MEI Z W,WANG T,et al.MoS2/graphene cocatalyst for efficient photocatalytic H2evolution under visible light irradiation[J].ACS Nano,2014,8(7):7078-7087.
[16]ZONG X,WU G P,YAN H J,et al.Photocatalytic H2evolution on MoS2/CdS catalysts under visible light irradiation[J].J Phys Chem C,2010,114(4):1963-1968.
[17]ZONG X,YAN H J,WU G P,et al.Enhancement of photocatalytic H2evolution on CdS by loading MoS2as cocatalyst under visible light irradiation[J].J Am Chem Soc,2008,130(23):7176-7177.
[18]YANG L,ZHONG D,ZHANG J Y,et al.Optical properties of metal-molybdenum disulfide hybrid nanosheets and their application for enhanced photocatalytic hydrogen evolution[J].ACS Nano,2014,8(7):6979-6985.
[19]LI Y X,WANG H,PENG S Q,et al.Tunable photodeposition of MoS2onto a composite of reduced graphene Oxide and CdS for synergic photocatalytic hydrogen generation[J].J Phys Chem C,2014,118(34):19842-19848.
[20]XIANG Q J,YU J G,JARONIEC M.Synergetic effect of MoS2and graphene as cocatalysts for enhanced photocatalytic H2production activity of TiO2nanoparticles[J].J Am Chem Soc,2012,134(15):6575-6578.
[21]MIN S X,LU G X.Sites for high efficient photocatalytic hydrogen evolution on a limited-layered MoS2cocatalyst confined on graphene sheetsthe role of graphene[J].J Phys Chem C,2012,116(48):25415-25424.
[22]YIN W Y,YAN L,YU J,et al.High-throughput synthesis of single-layer MoS2nanosheets as a near-infrared photothermal-triggered drug delivery for effective cancer therapy[J].ACS Nano,2014,8(7):6922-6933.
[23]MAK K F,LEE C G,HONE J,et al.Atomically thin MoS2:a new direct-gap semiconductor[J].Physical Review Letters,2010,105(13):474-479.
[24]VAN NOORDEN R.Moving towards a graphene world[J].Nature,2006,442(7100):228-229.
[25]STOLYAROVA E,RIM K T,RYU S M,et al.High-resolution scanning tunneling microscopy imaging of mesoscopic graphene sheets on an insulating surface[J].Proc Natl Acad Sci,2007,104(22):9209-9212.
[26]NOVOSELOV K S,GEIM A K,MOROZOV S V,et al.Two-dimensional gas of massless diracfermions in grapheme[J].Nature,2005,438(7065):197-200.
[27]田野,何俣,尚静,等.水热法合成MoS2层状材料及其结构表征[J].化学学报,2004,62(18):1807-1810.
[28]XU Y,SHENG K,LI C,et al.Self-assembled graphene hydrogel via a one-step hydrothermal process[J].ACS Nano,2010,4(7):4324-4330.
[29]SHEN J,LI T,LONG Y,et al.One-step solid state preparation of reduced graphene oxide[J].Carbon,2012,50(6):2134-2140.
[30]ZHOU Y,BAO Q,TANG L A L,et al.Hydrothermal dehydration for the “green” reduction of exfoliated graphene oxide to graphene and demonstration of tunable optical limiting properties[J].Chem Mater,2009,21(13):2950-2956.
[31]WU H H,YANG R,SONG B M,et al.Biocompatible inorganic fullerene-like molybdenum disulfide nanoparticles produced by pulsed laser ablation in water[J].ACS Nano,2011,5(2):1276-1281.
[32]STANKOVICH S,DIKIN D A,PINER R D,et al.Synthesis of graphene-based nanosheets via chemical reduction of exfoliated graphite oxide[J].Carbon,2007,45(7):1558-1565.
责任编辑:李文杰
Catalytic properties of graphene/molybdenum sulfide under near-infrared light irradiation
ZHANG Huan,LIU Shouqing*
(School of Chemistry,Biology and Materials Engineering,SUST,Suzhou 215009,China;Jiangsu Key Laboratory of Environmental Functional Materials,Suzhou 215009,China)
Graphene/MoS2hybrid material was synthesized by hydrothermal reaction for photocatalytic degradation of rhodamine B.The synthesized materials were characterized by X-ray diffraction,Raman spectroscopy,transmission electron microscope,ultraviolet-visible near-infrared diffuse reflection spectroscopy.Rhodamine B was degraded with the graphene/MoS2hybrid material as the near-infrared photocatalyst.The results show that a degradation ratio of 96.5%was achieved using 0.05 g graphene/MoS2photocatalyst in 50 mL solution containing 50 mg·L-1rhodamine B with pH=7 under infrared light irradiation for 3 h,whereas the degradation ratio for rhodamine B was only 75.5%under similar conditions using MoS2as photocatalyst.The catalytic efficiency is still over 90%after the hybrid catalyst was used for 5 runs,which indicates that the catalyst is quite stable.
graphene/MoS2;hybrid catalyst;near-infrared light;photocatalysis
X506
A
2096-3289(2017)04-0037-05
2016-03-04
国家自然科学基金资助项目(21576175)
张 欢(1990-),男,安徽广德人,硕士研究生,研究方向:光催化。
*通信作者:刘守清(1962-),男,博士,教授,硕士生导师,E-mail:shouqing_liu@163.com。

