GnRH-a促排周期中晚卵泡期孕酮上升的原因与策略
李元,龚斐*
(1.中南大学生殖与干细胞工程研究所,长沙 410008;2.中信湘雅生殖与遗传专科医院,长沙 410008)
GnRH-a促排周期中晚卵泡期孕酮上升的原因与策略
李元1,2,龚斐1,2*
(1.中南大学生殖与干细胞工程研究所,长沙 410008;2.中信湘雅生殖与遗传专科医院,长沙 410008)
GnRH-a促排过程中晚卵泡期孕酮(P)提前上升可能是肾上腺和卵巢来源共同作用结果,而这种P提前上升可能主要影响了子宫内膜容受性。在临床管理中如何避免晚卵泡期P上升显得尤为重要。首先寻找P上升原因,针对原因解决问题:如通过地塞米松降低基础P的影响;控制促排周期重组卵泡刺激素(rFSH)的剂量、及时添加合适的重组黄体生成素(rLH)制剂和稳定HCG日LH水平。而且,在不同卵巢反应性的人群中,P上升界定值及其意义不一。对于无法避免的晚卵泡期P上升的最佳策略为取消鲜胚移植,进行全胚冷冻。
促性腺激素释放激素类似物; 基础孕酮; 晚卵泡期; 孕酮上升; 子宫内膜容受性; 体外受精/卵胞浆内单精子注射
(JReprodMed2017,26(11):1095-1099)
在自然周期早卵泡期,由于卵泡内无血管供应,颗粒细胞和膜细胞缺乏合成大量孕酮(P)所需要的原材料胆固醇;同时膜细胞上黄体生成素(LH)受体不足,因此,早卵泡期P上升主要来源于肾上腺合成皮质醇的中间产物[1]。随着优势卵泡生长,雌激素分泌增加,LH分泌增加,LH与膜细胞LH受体结合后使胆固醇合成孕烯醇酮进而形成睾酮和雄烯二酮,后两者进入颗粒细胞成为雌激素的前体物质(排卵前按△5途径合成雌激素);LH峰后颗粒细胞和膜细胞黄素化有直接的血液供应,利用胆固醇合成孕酮和17α-羟孕酮(17a-OHP) 浓度增加(△4途径)[2]。然而与自然周期不一样的是:刺激周期由于外源性促性腺激素(Gn)的持续使用,多个卵泡发育导致整体外周血P浓度增加[3-4]。
在促性腺激素释放激素激动剂(GnRH-a)使用以前,晚卵泡期血清孕酮的上升是LH提前上升的结果,因此,定义为“提前黄素化(premature luteinization)”[5]。但在GnRH-a使用周期,仍有P提前上升;近13%~31.6% 的GnRH-a周期会出现晚卵泡期P上升[6-7];因此,在LH正常状态下的GnRH-a周期,P提前上升可能与提前黄素化无关,而主要与卵巢刺激相关[8]。本文就GnRH-a使用周期P上升对妊娠结局的影响及P上升的原因与对策进行综述,期望为临床解决难题。
一、P上升对妊娠结局的影响
生殖科临床医生都很关注HCG日P水平,源于HCG日P上升可能带来的不良结局。既往少量回顾性研究提示HCG日P上升组优胚率明显降低[9],但具体机制不清楚。而Meta分析和后续研究认为刺激周期P上升可能不会影响卵母细胞和胚胎质量[10-12]。
然而,对于HCG日P上升对内膜容受性的研究颇多。早在1997年,已有Ubaldi等[13]对HCG日P上升组的子宫内膜病理组织学观察,发现其发育提前(P<0.01),且HCG日P上升合并内膜发育提前超过3天者无一例妊娠。研究者发现刺激周期HCG 日P上升组与对照组相比,子宫内膜具有差异性表达的基因[14-15],这些差异性表达的基因功能主要表现为细胞粘附、发育、免疫系统等内膜正常发育表现的相关功能等。其中25个基因是作为子宫内膜容受性标志物,13个基因在上升组过度表达,这13个基因中的8个基因是孕激素应答元件(progesterone response elements,PRE)。因此,目前的观点都倾向于HCG日P上升产生的不良结局可能主要影响子宫内膜容受性。
二、P上升的原因
寻找HCG日P上升的原因则需要了解P的来源。孕激素生物合成需要两个酶促步骤:第一,由细胞色素P450scc催化的胆固醇向孕烯醇酮(P5)的转化;其次,其由3β-羟基类固醇脱氢酶(3βHSD)催化随后转化为孕酮[16]。卵巢在卵泡早期基本不合成孕酮,此时外周血P水平主要来源于肾上腺;当LH排卵峰发生时,排卵前卵泡的颗粒细胞黄素化,激活胆固醇侧链裂解酶/17-a羟化酶等,使胆固醇按△4途径转化为孕酮,开始分泌少量孕酮;排卵后,由于血管侵入颗粒细胞层,使黄体颗粒细胞内合成孕酮的胆固醇增加而使孕酮逐渐增加。因此,晚卵泡期P上升是肾上腺和卵巢来源共同作用的结果。
而在刺激周期持续相对大剂量的FSH刺激,使得颗粒细胞来源的P合成增多;足够LH状态下,P在膜细胞转化为雄激素,如果缺乏LH活性则代谢途径受阻,使得P累积量增加;刺激周期高雌激素状态使得颗粒细胞雄激素转化为雌激素途径被抑制,P间接累积量增加[3](图1)。既往文献提示:GnRH-a/GnRH-ant方案增加刺激周期rFSH剂量则增加P上升发生率[17-18]。且在GnRH-a方案中LH相对缺乏状态下,P代谢为雄激素过程受阻而使得P累积量增加;及时添加LH制剂可以相对降低HCG日P水平[19-20]。
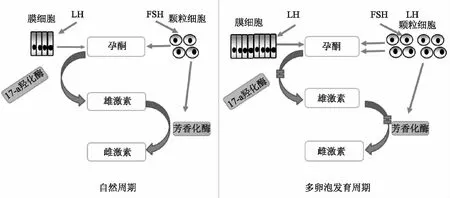
图1 自然周期和刺激周期P合成与代谢[3]
三、P上升的管理
定义P上升的切割值是判断是否存在P提前上升的前提,然而,既往文献对于P上升的定义存在争议。Venetis等[19]通过Meta分析对12个研究中的2 733例患者进行分析发现:P>0.9 ng/ml(2.853 nmol/L) 定义为P上升,P上升组临床妊娠率有下降趋势,但无统计学差异;Bosch 等[6]在一项前瞻性研究中定义HCG日P上升的切割值为1.2 ng/ml(3.804 nmol/L);一项4 032个周期的回顾性研究定义P上升的切割值为1.5 ng/ml(4.755 nmol/L)[20];而在2013年的一项研究分析发现,在卵巢高反应组P提前上升不影响妊娠结局,而对于卵巢正常/低反应人群P>1.5 ng/ml(4.755 nmol/L)则明显降低继续妊娠率[21];尚有对卵巢高反应者进行研究发现P>2.25 ng/ml(7.132 5 nmol/L)则继续妊娠率明显降低[22]。Papanikolaou等[23]和Huang 等[24]评估P上升对移植D3/D5胚胎妊娠结局的影响时发现:当P>1.0 ng/ml(3.17 nmol/L)时明显不利于D3胚胎移植成功率;Huang等[24]发现当P达到1.75 ng/ml(5.547 5 nmol/L) 时,移植D5囊胚也会产生不利影响,然而在2009年的研究中认为移植D5囊胚不会影响P上升者的妊娠结局[23]。目前,国内外大部分生殖中心采用HCG日P≥1.5 ng/ml(4.755 nmol/L)作为晚卵泡期P上升的切割值。
回顾性分析我院2016年01月~12月GnRH-a方案(n=9 931)HCG日P上升[≥1.5 ng/ml(4.755 nmol/L)]的相关数据,进行单因素和多因素分析发现HCG日P与基础P[OR1.282,95%CI(1.097,1.497)](P=0.002)、回收卵数[OR1.099,95%CI(1.071,1.127)](P<0.001)明显相关,HCG日P上升多来源于多个卵母细胞的发育,与卵巢反应性相关;然后,我们对GnRH-a方案不同卵巢反应性HCG日P上升发生率进行分析发现:高反应(获卵≥15个)、正常反应(获卵5~15个)、低反应(获卵≤4个)分别为4.23%、2.28%、0.68%(P=0.001),而卵巢高反应与正常反应组相比无统计学差异(P=0.431)。由此提示:对于低反应这类回收卵数较少的患者,HCG日P≥1.5 ng/ml (4.755 nmol/L)的切割值是否适合值得考虑。之后对GnRH-a方案卵巢低反应患者(获卵≤4个,AMH≤1.8 ng/ml,n=504)通过单因素、多因素分析后发现HCG日P与妊娠结局无明显相关[(0.48±0.27)ng/ml vs.(0.51±0.25)ng/ml ](P=0.309),而与患者年龄[OR0.936,95%CI(0.896,0.979)](P=0.004)、HCG日P/E2[OR0.425,95%CI(0.194,0.933)](P=0.033)、回收卵数[OR1.454,95%CI(1.189,1.777)](P<0.001)明显相关(数据待发表)。因此,对于不同卵巢反应的患者单纯以HCG日P作为判断妊娠与否的预测指标是不够精准的。可能还需参考其他指标,如HCG日P/E2。
既往文献对于HCG日P上升的影响因素进行分析发现:基础P水平对HCG日P水平的影响很大[OR12.21,95%CI(1.82,81.70)][25]。我院数据发现HCG日P与基础P[OR1.282,95%CI(1.097,1.497)](P=0.002)明显正相关(数据待发表)。早卵泡期孕酮上升主要来源于肾上腺;到晚卵泡期,P上升则主要来源于卵巢[1]。因此对于基础P上升者采用地塞米松负反馈可以抑制部分肾上腺来源的P分泌。我院2016年数据提示:使用地塞米松等干预后HCG日P上升发生率2.57%(256/9 931)(数据待发表),相对于既往文献报道的P上升发生率明显降低。回顾性分析2016年我院GnRH-a方案,基础P相对匹配状态下,使用地塞米松后会有一个迅速的P下降过程,但是在HCG日不管是否使用地塞米松,P仍有上升,但是较未使用对照组低(图2)。我院数据提示晚卵泡期P的上升不能由地塞米松的添加[OR0.806,95%CI(0.565,1.15)](P=0.234)而完全缓解(数据待发表)。说明肾上腺来源的P对于HCG日P上升有一定影响,但HCG日P部分来源于卵巢多卵泡的发育。
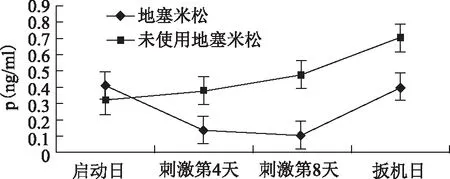
图2 血清孕酮水平波动曲线
即使经过严格的临床管理,如及时使用地塞米松,刺激周期控制rFSH剂量、及时添加rLH并控制HCG日LH水平等,仍有一部分人群HCG日P上升。这部分人群如强烈要求鲜胚周期移植者,部分研究者认为可以考虑囊胚培养后移植,但也是有争议的[22-23]。而全胚冷冻是目前国内外生殖中心所推荐的。我院对2016年1~12月因HCG日P上升而进行胚胎移植的患者进行回顾性分析发现:256个周期HCG日P上升者中38个周期要求鲜胚移植,余218个周期取消鲜胚移植全在冻胚周期移植;38个鲜胚移植者着床率(32.83%)、临床妊娠率(44.73%)均有明显下降趋势;而218个周期全在冻胚周期移植组与基线匹配的同期冻胚患者(n=218)助孕结局相比:着床率(44.44% vs.42.58%)(P=0.611)、临床妊娠率(60.47% vs.56.54%)(P=0.411)均无明显差异(数据待发表)。
GnRH-a方案促排过程中HCG日P上升与基础P和回收卵数明显相关。基础P上升主要来源于肾上腺;HCG日P上升与回收卵数即卵巢反应性明显相关,不同卵巢反应性HCG日P上升的界定值不一,且对于卵巢低反应综合评估HCG日P/E2具有更高临床妊娠预测价值;P上升的管理重在预防,充分的降调节,适时使用地塞米松、控制FSH剂量、适时添加LH制剂、不盲目追求多卵泡发育;对于经过干预后仍出现HCG日P上升者可考虑全胚冷冻,且不影响冻胚移植成功率。
[1] Kasum M,Radakovic B,Simunic V,et al. Preovulatory progesterone rise during ovarian stimulation for IVF[J].Gynecol Endocrinol,2013,29:744-7448.
[2] Chaffin CL,Dissen GA,Stouffer RL.Hormonal regulation of steroidogenic enzyme expression in granulosa cells during the peri-ovulatory interval in monkeys[J].Mol Hum Reprod,2000,6:11-18.
[3] Fleming R,Jenkins J.The source and implications of progesterone rise during the follicular phase of assisted reproduction cycles[J/OL].Reprod Biomed Online,2010,21:446-449.
[4] Kyrou D,Al-Azemi M,Papanikolaou EG,et al. The relationship of premature progesterone rise with serum estradiol levels and number of follicles in GnRH antagonist/recombinant FSH-stimulated cycles[J].Eur J Obstet Gynecol Reprod Biol,2012,162:165-168.
[5] Al-Azemi M,Kyrou D,Kolibianakis EM,et al. Elevated progesterone during ovarian stimulation for IVF[J/OL].Reprod Biomed Online,2012,24:381-388.
[6] Bosch E,Valencia I,Escudero E,et al. Prematureluteinization during gonadotropin-releasing hormone antagonist cycles and its relationship with in vitro fertilization outcome[J].Fertil Steril,2003,80:1444-1449.
[7] Venetis CA,Kolibianakis EM,Bosdou JK,et al. Progesterone elevation and probability of pregnancy after IVF:a systematic review and meta-analysis of over 60 000 cycles[J].Hum Reprod Update,2013,19:433-457.
[8] Lawrenz B,Beligotti F,Engelmann N,et al. Impact of gonadotropin-type on progesterone elevation during ovarian stimulation in GnRH antagonist cycles[J].Hum Reprod,2016,31:2554-2560.
[9] Huang B,Ren X,Wu L,et al. Elevated progesterone levels on the day of oocyte maturation may affect top quality embryo IVF cycles[J/OL].PLoS One,2016,11:e0145895.
[10] Santos-Ribeiro S,Polyzos NP,Haentjens P,et al. Live birth rates after IVF are reduced by both low and high progesterone levels on the day of human chorionic gonadotrophin administration[J].Hum Reprod,2014,29:1698-1705.
[11] Yang S,Pang T,Li R,et al. The individualized choice of embryo transfer timing for patients with elevated serum progesterone level on the HCG day in IVF/ICSI cycles:a prospective randomized clinical study[J].Gynecol Endocrinol,2015,31:355-358.
[12] Healy MW,Patounakis G,Conell MT,et al. Does a frozen embryo transfer ameliorate the effect of elevated progesterone seen in fresh transfer cycles?[J].Fertil Steril,2016,105:93-99.
[13] Ubaldi F,Bourgain C,Tournaye H,et al. Endometrial evaluation by aspiration biopsy on the day of oocyte retrieval in the embryo transfer cycles in patients with serum progesterone rise during the follicular phase[J].Fertil Steril,1997,67:521-526.
[14] Van Vaerenbergh I,Fatemi HM,Blockeel C,et al. Progesterone rise on HCG day in GnRH antagonist/rFSH stimulated cycles affects endometrial gene expression[J/OL].Reprod Biomed Online,2011,22:263-271.
[15] Labarta E,Martínez-Conejero JA,Alamá P,et al. Endometrial receptivity is affected in women with high circulating progesterone levels at the end of the follicular phase:a functional genomics analysis[J].Hum Reprod,2011,26:1813-1825.
[16] Thuesen LL,Smitz J,Loft A,et al. Endocrine effects of hCG supplementation to recombinant FSH throughout controlled ovarian stimulation for IVF:a dose-response study[J].Clin Endocrinol(Oxf),2013,79708-79715.
[17] Smitz J,Andersen AN,Devroey P.Endocrine profile in serum and follicular fluid differs after ovarian stimulation with HP-hMG or recombinant FSH in IVF patients[J].Hum Reprod,2007,22:676-687.
[18] Andersen AN,Devroey P,Arce JC.Clinical outcome following stimulation with highly purified hMG or recombinant FSH in patients undergoing IVF:a randomized assessor-blind controlled trial[J].Hum Reprod,2006,21:3217-3227.
[19] Venetis CA,Kolibianakis EM,Papanikolaou E,et al. Is progesterone elevation on the day of human chorionic gonadotrophin administration associated with the probability of pregnancy in in vitro fertilization? A systematic review and meta-analysis[J].Hum Reprod Update,2007,13:343-355.
[20] Bosch E,Labarta E,Crespo J,et al. Circulating progesterone levels and ongoing pregnancy rates in controlled ovarian stimulation cycles for in vitro fertilization:analysis of over 4000 cycles[J].Hum Reprod,2010,25:2092-2100.
[21] Griesinger G,Mannaerts B,Andersen CY,et al. Progesterone elevation does not compromise pregnancy rates in high responders:a pooled analysis of invitro fertilization patients treated with recombinant follicle-stimulating hormone/gonadotropin-releasing hormone antagonist in six trials[J].Fertil Steril,2013,100:1622-1628.
[22] Xu B,Li Z,Zhang H,et al. Serum progesterone level effects on the outcome of in vitro fertilization in patients with different ovarian response:an analysis of more than 10,000 cycles[J].Fertil Steril,2012,97:1321-1327.
[23] Papanikolaou EG,Kolibianakis EM,Pozzobon C,et al. Progesterone rise on the day of human chorionic gonadotropin administration impairs pregnancy outcome in day 3 single-embryo transfer,while has no effect on day 5 single blastocyst transfer[J].Fertil Steril,2009,91:949-952.
[24] Huang Y,Wang EY,Du QY,et al. Progesterone elevation on the day of human chorionic gonadotropin administration adversely affects the outcome of IVF with transferred embryos at different developmental stages[J].Reprod Biol Endocrinol,2015,13:82.
[25] Papaleo E,Corti L,Vanni VS,et al. Basal progesterone level as the main determinant of progesterone elevation on the day of hCG triggering in controlled ovarian stimulation cycles[J].Arch Gynecol Obstet,2014,290:169-176.
[编辑:谷炤]
The causes and countermeasures of premature progesterone elevation during the late follicular phase in GnRH-agonist cycles
LIYuan1,2,GONGFei1,2*
1.InstituteofReproductive&StemCellEngineering,CentralSouthUniversity,Changsha410008 2.Reproductive&GeneticHospitalofCITIC-XiangYa.Changsha410008
Emerging evidence shows that premature progesterone elevation during the late follicular phase in stimulated IVF cycles,which may be caused by the co-effect of adrenal and ovarian origin,does negatively affect the outcome of assisted reproductive techniques.The elevated peripheral progesterone level in the late follicular phase seems to effect on the endometrium,which may lead to asynchrony between the endometrium and developing embryo.The causes of premature progesterone elevation during ovarian stimulation are still unclear.However,recent studies point towards it is helpful that usage of dexamethasone,controlling the dose of rFSH and stabilizing the serum LH level on HCG day.Moreover,the definition and its significance of progesterone elevation are different in the patients with different ovarian response.Whole embryos frozen may be a good choice for unavoidable late follicular phase progesterone increased.
GnRH-analogues; Basal progesterone level; Late follicular phase; Progesterone rise; Endometrial receptivity; IVF/ICSI
10.3969/j.issn.1004-3845.2017.11.009
2017-08-23;
2017-08-30
国家自然科学基金(81501328)
李元,女,湖南岳阳人,硕士,医师,生殖医学专业.(*
,Email:lj_0305@126.com)

