蛋白质在膜表面的吸附特性及蛋白质存在的溶液环境对小檗碱膜透过行为的影响研究
李益群 徐丽 朱华旭 唐志书 李博 潘永兰 姚薇薇 付廷明 郭立玮

[摘要]为探索蛋白质在膜表面的吸附特性以及蛋白质存在的溶液环境对小檗碱膜透过行为的影响,以蛋白质、小檗碱为研究对象,配制模拟溶液,通过低场核磁共振技术、静态吸附实验以及膜分离实验探究蛋白质与陶瓷膜、小檗碱之间可能存在的相互作用,以蛋白质静态吸附量、膜过程相对通量、蛋白质截留率、小檗碱透过率及两者的吸附率为评价指标,同时测定膜过程中膜污染阻力分布、过膜前后粒径分布变化及膜表面电镜扫描(SEM),研究蛋白质在陶瓷膜上的吸附特性及对小檗碱膜过程的影响。结果表明,陶瓷膜对蛋白质具有吸附作用,且吸附模型符合Langmuir吸附模型,在模拟溶液的膜分离过程中,蛋白质是引起膜污染的主要因素,但在1 g·L-1蛋白质的浓度下,蛋白质的存在对小檗碱的膜过程没有显著影响。
[关键词]蛋白质; 小檗碱; 陶瓷膜微滤; 模拟体系; 吸附特性
[Abstract]In order to explore the adsorption characteristics of proteins on the membrane surface and the effect of protein solution environment on the permeation behavior of berberine, berberine and proteins were used as the research object to prepare simulated solution Low field NMR, static adsorption experiment and membrane separation experiment were used to study the interaction between the proteins and ceramic membrane or between the proteins and berberine The static adsorption capacity of proteins, membrane relative flux, rejection rate of proteins, transmittance rate of berberine and the adsorption rate of proteins and berberine were used as the evaluation index Meanwhile, the membrane resistance distribution, the particle size distribution and the scanning electron microscope (SEM) were determined to investigate the adsorption characteristics of proteins on ceramic membrane and the effect on membrane separation process of berberine The results showed that the ceramic membrane could adsorb the proteins and the adsorption model was consistent with Langmuir adsorption model In simulating the membrane separation process, proteins were the main factor to cause membrane fouling However, when the concentration of proteins was 1 g·L-1, the proteins had no significant effect on membrane separation process of berberine.
[Key words]protein; berberine; ceramic membrane microfiltration; simulation system; adsorption characteristics
陶瓷膜具有耐高温、耐腐蚀、机械强度高、化学稳定性好等特点,在生物醫药、石油化工、食品饮料、水处理等领域得到广泛的应用[12],尤其是在中药领域,凭借其对于中药水提液分离纯化的独特优势而具有广阔的应用前景[34],但中药水提液组成复杂多样,小分子药效物质的透过率不理想,严重制约了陶瓷膜在中药领域的推广应用,又缺少系统的研究方法,尤其是缺乏对高分子与膜、小分子与膜、高分子与小分子、高分子与高分子之间相互作用的研究手段,所以对膜过程机制的研究难以深入。
针对上述问题,本实验进行了初步的研究,以蛋白质、小檗碱为研究对象,建立模拟体系,通过静态吸附、膜分离实验等手段,考察陶瓷膜对蛋白质的吸附特性,研究蛋白质的存在对小檗碱膜过程的影响,为深入研究高分子对膜过程的影响及小分子的透过机制,优化设计特种分离膜奠定基础。
1材料
陶瓷膜装置(江苏久吾高科技股份有限公司,02 μm ZrO2单通道内压管式;外径12 mm,内径8 mm,管长220 mm;膜面积0005 m2);MicroMR23025V型低场核磁仪(纽迈分析仪器股份有限公司,共振频率23347 MHz;磁体温度3199~3201 ℃;探头线圈直径 25 mm);ZS90 型Malvern 纳米粒径测定仪(英国);Hitachi(日立)扫描电子显微镜S4800型(日本);Waters 2695 高效液相色谱分析仪(美国Waters公司,2998型紫外检测器,Empower工作站);ZORBAX SBC18色谱柱(美国安捷伦有限公司);Sartorius BL4100型电子分析天平(德国);Sartorius SQP型电子天平(德国);SHACA水浴恒温振荡器(金坛市盛蓝仪器制造有限公司)。endprint
盐酸小檗碱对照品(纯度867%,批号110713201212),购自中国食品药品检定研究院;盐酸小檗碱提取物(纯度 98%,批号20160228),购自南通飞宇生物科技有限公司;牛血清蛋白(CAS 9048468),购自Biosharp公司;甲醇(色谱纯,江苏汉邦科技有限公司);乙腈(色谱纯,美国 Merck 公司产品);水为超纯水;其余试剂均为分析纯。
2方法
21样品溶液配制
211蛋白质重水溶液的配制
精密称取牛血清蛋白001 g,置10 mL量瓶中,加重水溶解,定容至刻度,即得牛血清蛋白重水溶液,用于低场核磁检测。
212模拟溶液的配制
2121小檗碱模拟溶液根据本课题组前期研究[5],参照黄连解毒汤中小檗碱的质量浓度配制模拟溶液,得模拟溶液1(0201 4 g·L-1,pH 644)。
2122蛋白质模拟溶液根据本课题组前期研究[6],中药水提液中蛋白质质量浓度在01~40 g·L-1,配制模拟溶液2~7(蛋白质质量浓度分别为01,05,10,15,20,40 g·L-1,pH 642);选择模拟溶液4(蛋白质质量浓度10 g·L-1,pH 642)进行吸附动力学实验及膜分离实验。
2123小檗碱+蛋白质模拟溶液根据本课题组前期研究[56],配制小檗碱+蛋白质模拟溶液,得模拟溶液8(蛋白质质量浓度10 g·L-1,小檗碱质量浓度0201 4 g·L-1,pH 657)。
22陶瓷膜微滤实验
将陶瓷膜膜管装入膜装置中,实验温度为30 ℃,跨膜压差为015 MPa,加入超纯水预压30 min,之后继续加入超纯水,测定膜的纯水通量(J0),放出超纯水,分别加入模拟溶液1、模拟溶液4及模拟溶液8各4 500 mL,旁路循环至30 ℃,错流微滤,同时测定模拟溶液的膜过程通量(J),待渗透液体积达2 000 mL时停止过滤,收集渗透液、截留液与原液,检测各溶液中小檗碱、蛋白质含量。小檗碱透过率、蛋白质截留率及两者的吸附率计算公式如下。
透过率=CS/C0×100% (1)
截留率=[1-(CS×VS)/(C0×V0)]×100% (2)
吸附率=[(C0×V0)-(CS×VS)-(CJ×VJ)]/(C0×V0)×100% (3)
其中,C0为原液中蛋白质浓度,CS为渗透液中蛋白质浓度,CJ为截留液中蛋白质浓度,V0为原液体积,VS为渗透液体积,VJ为截留液体积。
23静态吸附实验
将整根陶瓷膜浸入600 mL蛋白质模拟溶液中,在摇床上振摇(150 r·min-1,30 ℃),测定原液与吸附后溶液的蛋白质浓度,计算吸附量。蛋白质吸附量计算公式如下。
静态吸附量=600×(C0 - C1)/S (4)
其中,C0为原液中蛋白质浓度;C1为吸附液中蛋白质浓度;S为陶瓷膜的表面积(0012 5 m2)。
24低场核磁共振实验
精密量取上述蛋白质重水溶液3 mL,加入供低场核磁测试的专用试管中,测量空白溶液的T2弛豫时间,将陶瓷膜截成长为1 cm的小段管式膜,置于装有重水溶液的试管中,分别在0,15,30,45,60,75,90,105,120,150,180,210,240 min时测定T2弛豫时间,绘制T2随时间的变化曲线。
25含量测定
251小檗碱含量测定[6]
2511色谱条件与系统适应性条件ZORBAX SBC18色谱柱(46 mm ×250 mm,5 μm);以乙腈为流动相(A),005%三乙胺01%磷酸水为流动相(B),梯度洗脱(0~5 min,10% A;5~7 min,10%~20% A;7~13 min,20% A;13~16 min,20%~30% A;16~25 min,30% A;25~27 min,30%~10% A;27~30 min,10% A);检测波长255 nm;柱温30 ℃;流速08 mL·min-1。
2512对照品溶液的配制精密称取盐酸小檗碱对照品0030 5 g,置10 mL量瓶中,加甲醇溶解,定容至刻度,在精密量取小檗碱对照品溶液1 mL,置10 mL量瓶中,加甲醇稀释并定容至刻度,即得浓度为0026 4 g·L-1的盐酸小檗碱对照品溶液。分別进样 2,4,6,8,10,15,20 μL,以峰面积为纵坐标(Y),对照品进样量为横坐标(X),绘制标准曲线,得回归方程 Y=5×106X-26 409,R2=0999 8。表明小檗碱在 0052 9~0529 μg呈良好的线性关系。
2513供试品溶液的制备精密量取模拟溶液过膜前后的原液、渗透液、截留液各1 mL,置10 mL量瓶中,加甲醇稀释并定容至刻度,摇匀,过022 μm的滤膜,即得供试品溶液。
252蛋白质含量测定
采用考马斯亮蓝染料比色法测定蛋白质的含量[7]。
253粒径分布测定
用Malvern纳米粒径测定仪分别测定小檗碱模拟溶液、蛋白质模拟溶液及混合模拟溶液过膜前后的粒径分布。
254膜阻力分布测定[8]
目前,DarcyPoiseuille[9] 定律过滤模型是膜分离技术中最常用来研究膜污染阻力分布的模型,以 Darcy 定律为基础得出下列过滤通量表达式。
J=ΔPμ×Rt(5)
其中,J为膜通量(L·m-2·h-1),ΔP为膜压差(Pa),μ为料液黏度(Pa·s),Rt为过滤阻力(m-1)。
但M MDaCin等[10] 指出采用上述阻力模型来比较各部分过滤阻力的相对大小时,往往过高估计浓差极化阻力而过低估计因溶质吸附引起的阻力,因此他对此模型进行了修正,本实验即采用MMDaCin修正后的阻力模型对膜污染阻力分布进行分析。该模型将总阻力(Dt)分为膜自身阻力(Dm)、表面沉积阻力(De)、堵塞阻力(Di)和浓差极化阻力(Dp),计算各部分阻力及占总阻力的百分比。endprint
255扫描电镜(SEM)分析
将污染后的陶瓷膜在35 ℃的烘箱中烘干12 h备用[11],将干净陶瓷膜与污染后的陶瓷膜敲碎,选取膜管同一位置的碎片,喷金后于扫描电镜上观察膜表面微观结构及污染物形态。
3结果与分析
31陶瓷膜在蛋白质模拟溶液中的静态吸附特性分析
低场核磁共振一般指恒定磁场强度低于05 T的核磁共振,其基本原理[12]是通過施加射频脉冲给予处于恒定磁场中的样品,使氢质子发生共振,质子所吸收的射频波能量以非辐射的方式释放后返回到基态,此过程被称为弛豫过程,又可分为横向弛豫(自旋自旋弛豫)和纵向弛豫(自旋晶格弛豫),可分别用T1和T2表示其弛豫时间,样品内部氢质子所处物理化学环境及存在状态决定了弛豫时间的长短。本实验测定的T2弛豫时间反映了蛋白质中氢质子所处的物理化学环境,其值随时间的变化与氢质子所受的束缚程度及其自由度有关,蛋白质与陶瓷膜之间的相互作用是影响氢质子T2弛豫时间的主要因素。
随着蛋白质重水溶液与陶瓷膜接触时间的增加,T2弛豫时间不断减小,表明蛋白质重水溶液中氢质子所受的束缚越大,即自由度越小,表明陶瓷膜对蛋白质存在吸附作用,从而使T2弛豫时间不断减小,见图1。从趋势上看,前60 min T2弛豫时间下降幅度明显,120 min后逐渐趋于平缓,表明陶瓷膜对蛋白质的吸附在240 min后逐渐达到饱和。
为了从量上确定陶瓷膜对蛋白质的吸附作用,进一步研究了陶瓷膜对蛋白质的吸附量随时间、浓度的变化情况。
蛋白质静态吸附量随时间的增加而增加,在240 min后吸附达到饱和,饱和吸附量为533 g·m-2,见图2。经拟合发现,陶瓷膜对蛋白质的吸附符合一级动力学吸附模型,拟合方程为y=5213 46[1-exp(-0013 72x)],R2=0951 0。由方程可得出理论饱和吸附量为521 g·m-2,与实际相符合。观察陶瓷膜对蛋白质吸附量随时间的变化的趋势,可以发现在0~240 min变化趋势与低场核磁共振实验中T2弛豫时间的变化趋势类似,由此两者相互印证了陶瓷膜对蛋白质的吸附特性符合一级动力学吸附模型。
陶瓷膜在不同质量浓度(01~40 g·L-1)的模拟溶液中对蛋白质的吸附量的变化情况,可见随着蛋白质模拟溶液浓度的增大,陶瓷膜对蛋白质的吸附量也随之增加,经拟合发现陶瓷膜对蛋白质的静态吸附模型符合Langmuir吸附模型,拟合方程为y=831x120/(1+053x120),R2=0985 07,见图3。
32小檗碱膜透过行为及蛋白质对其膜过程的影响
321膜通量比较
因为膜的自身阻力不同,所以采用相对通量
(J/J0)来比较模拟溶液的膜过程,由于小檗碱溶液浓度较低,且膜通量与纯水通量接近,膜过程所需时间较短,相对通量远大于蛋白质模拟溶液、蛋白质+小檗碱混合模拟溶液的相对通量,因此只列出后2种溶液的相对通量变化进行比较,见图4。蛋白质模拟溶液的相对通量要大于蛋白质与小檗碱混合模拟溶液的相对通量,但两者膜通量衰减幅度相差不大,蛋白质模拟溶液的起始相对通量为023,终点时相对通量为019,加入小檗碱后起始相对通量为021,终点时相对通量为016。推测由于小檗碱的加入,使得混合模拟溶液的相对通量小于蛋白质模拟溶液的相对通量,但由于主要污染物都为蛋白质,所以两者的相对通量衰减幅度相同。
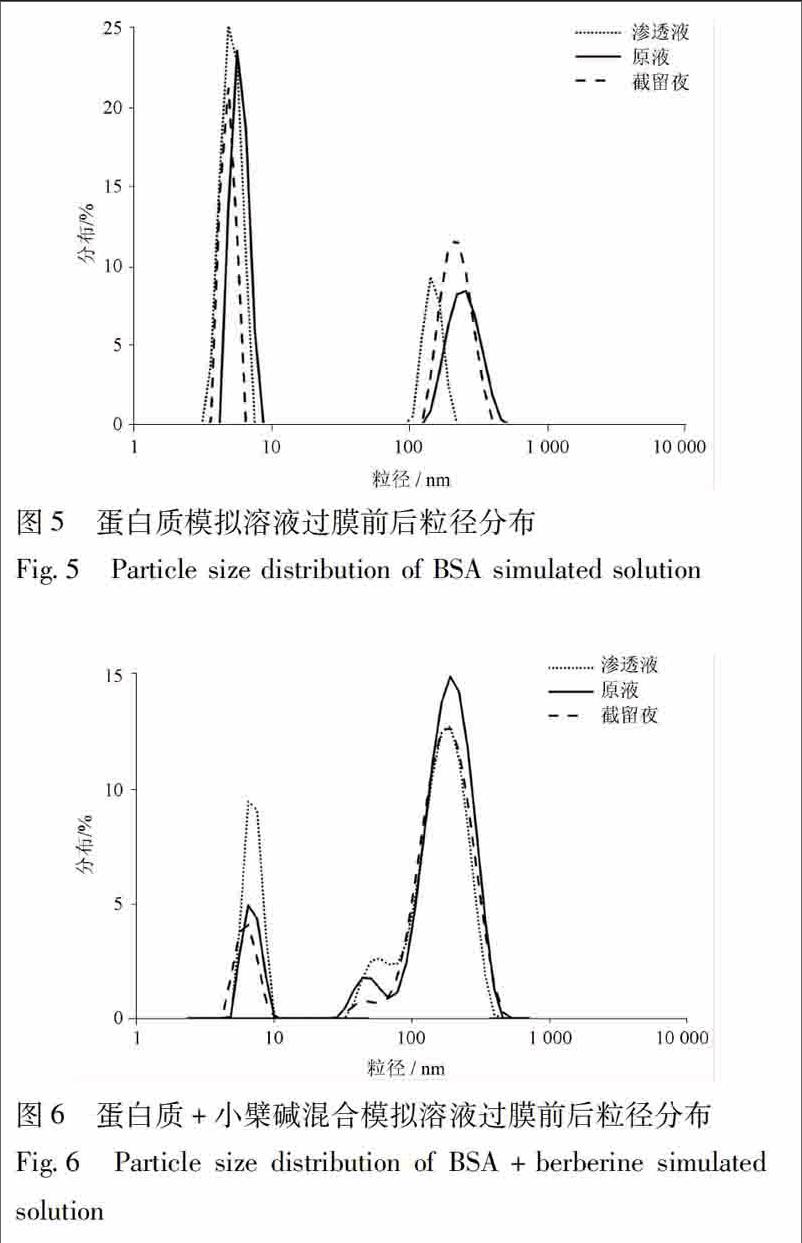
322粒径分布
蛋白质模拟溶液及混合模拟溶液过膜前后的原液、渗透液和截留液的粒径分布图见图5,6,由于小檗碱溶液中粒径太小,达不到检测的最低要求,因此只列出蛋白质模拟溶液、混合模拟溶液的粒径分布图。蛋白质模拟溶液的粒径大小有2个分布范围,一部分粒子的粒径大小<10 nm,推测为游离的蛋白质,一部分粒子的粒径>100 nm,推测为蛋白质团聚体,渗透液、原液和截留液的粒径分布类似,但渗透液中>100 nm的峰较原液、截留液明显左移,而<10 nm的峰粒径分布类似,推测其原因可能是由于溶液中蛋白质团聚体大部分被截留,一些粒径较小的团聚体则能顺利通过产生的结果,也可能是由于渗透液中一些游离的蛋白质重新团聚形成了新的团聚体,从而与原液略有差别。
蛋白质与小檗碱混合模拟溶液粒径分布与蛋白质模拟溶液有所不同,主要差别是混合模拟溶液中的粒子大小在10~100 nm也有分布,推测其原因是由于小檗碱的存在使得蛋白质团聚体发生了改变,小檗碱可能与蛋白质结合形成了新的团聚体,从而有了新的粒径分布范围,这也有可能是导致其膜通量差异的原因。
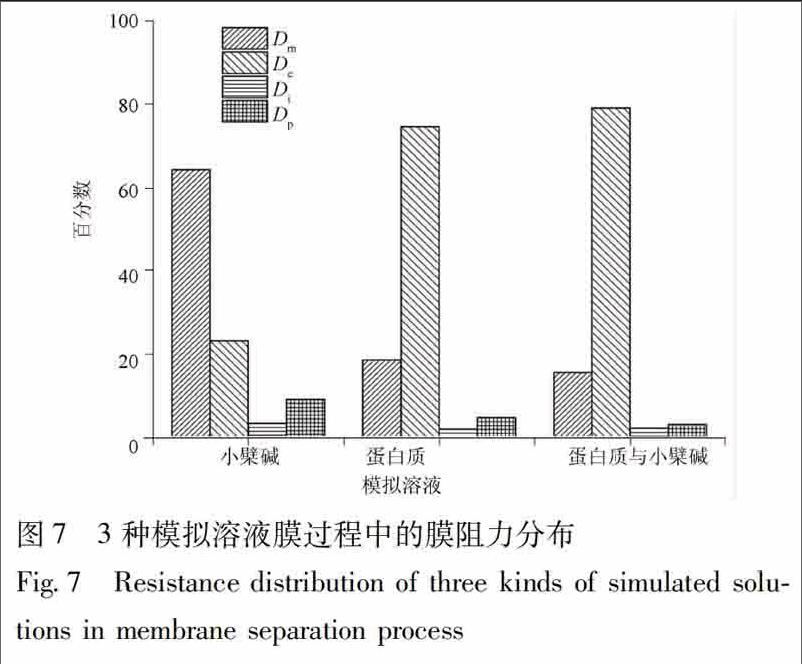
323膜阻力分布
小檗碱模拟溶液在膜过程中膜自身阻力(Dm)所占比例较高,而蛋白质模拟溶液、混合模拟溶液膜过程中表面沉积阻力(De)所占比例最大,可见,蛋
白质对膜过程的影响主要是通过沉积在膜表面来实现的,由低场核磁共振实验及静态吸附实验的结果可以确定陶瓷膜对蛋白质具有吸附作用,因此可以推测在膜过程中,蛋白质首先吸附在膜表面,进而在跨膜压差的作用下沉积在膜表面形成凝胶层,从而引起膜污染,导致膜通量的下降。同时混合模拟溶液的表面沉积阻力(De)所占比例大于蛋白质模拟溶液中表面沉积阻力(De)所占比例,这也是混合模拟溶液相对通量小于蛋白质模拟溶液的原因,见图7。
324小檗碱透过率、高分子截留率及两者吸附率比较
小檗碱模拟溶液的小檗碱透过率、吸附率较混合模拟溶液高,但两者之间没有显著性差异,混合模拟溶液中蛋白质的截留率、吸附率较蛋白质模拟溶液有所增加,但同样没有显著性差异,由此可推测蛋白质虽然是导致膜污染的主要因素,但在1 g·L-1
的质量浓度下,蛋白质对小檗碱的透过率没有显著影响,见表1。相比于蛋白质的静态吸附量,膜过程中陶瓷膜对蛋白质的吸附量显著增加,结合膜阻力分布可知,所增加的吸附量是由于蛋白质的在膜表面沉积所致。endprint
325扫描电镜
空白陶瓷膜表面粗糙,由微小颗粒堆积而成,从表面上可以清晰的观察到膜孔,见图8。滤过蛋白质模拟溶液的陶瓷膜表面被蛋白质覆盖,放大之后污染形成的凝胶层上可以观察到细小的孔,推测是膜孔未完全被污染物覆盖所致。滤过小檗碱模拟溶液的陶瓷膜表面污染物呈不规则块状,与蛋白质污
4讨论
陶瓷膜使用壽命长,易清洗,在中药领域具有广阔的应用前景,本实验使用浓度为1%的NaOH溶液清洗陶瓷膜,清洗1 h,其超纯水通量均能恢复到初始超纯水通量的80%左右,可见陶瓷膜具有良好的再生性能,可重复使用。
小檗碱是黄连解毒汤中的主要药效成分,采用陶瓷膜精制的方法是为了去除高分子成分,保留大量药效成分,但在实际应用过程中,高分子物质会导致严重的膜污染,小分子药效成分不能完全透过,为了探究高分子造成膜污染的机制以及小分子的透过机制,本实验采用系统模拟的方法,初步考察了蛋白质在陶瓷膜上的吸附特性以及对小檗碱膜过程的影响。
本实验通过低场核磁共振技术证明了陶瓷膜对蛋白质存在吸附作用,并通过静态吸附实验进一步证明了陶瓷膜对蛋白质的吸附作用符合一级动力学吸附模型及Langmuir吸附模型。蛋白质吸附在膜表面是形成膜污染的基础,结合蛋白质模拟溶液膜过程相关参数可知,蛋白质对陶瓷膜的污染形式主要是通过表面沉积来实现的。
小檗碱模拟溶液过膜后,小檗碱透过率为7787%,吸附率为2156%,小檗碱与蛋白质混合模拟溶液过膜后,小檗碱透过率为7565%,吸附率为2072%,2种溶液的透过率与吸附率之间没有显著性差异,由此可见在此条件下,蛋白质对小檗碱的膜过程没有显著影响。探究小檗碱透过率低的原因,推测其原因一方面是陶瓷膜对小檗碱的吸附作用,一方面是小檗碱在膜过程中的“受限传递”。因此,小檗碱在膜表面的吸附作用以及其“受限传递”的机制将是进一步研究的重点。
本实验考察了陶瓷膜对蛋白质的吸附作用以及蛋白质的存在对小檗碱膜过程的影响,是研究陶瓷膜过程中小分子透过机制和高分子物质的污染机制的一种尝试,为研究其他高分子物质对膜过程的影响,以及小分子药效物质的透过机制提供一种思路,同时为深入研究中药水提液的膜过程、优化设计中药特种分离膜奠定基础。
[参考文献]
[1]漆虹, 曹义鸣 2014年我国陶瓷膜应用新进展[J]. 膜科学与技术, 2015, 35(3): 131.
[2]王姣, 姜忠义, 吴洪, 等. 中药有效成分和有效部位分离用膜[J]. 中国中药杂志, 2005, 30(3): 165.
[3]曹静杰, 董新法, 董应超, 等. 无机陶瓷膜分离技术应用研究进展[J]. 广州化工, 2014, 41(2): 314.
[4]曹云台, 郭立玮, 施栋磊, 等. 陶瓷膜应用于中药精制的研究进展[J]. 中草药, 2010, 42(9): 19.
[5]刘静, 郭立玮, 朱华旭, 等. 基于系统模拟方法的3种溶液环境对小檗碱膜过程影响及其机制初探[J]. 膜科学与技术, 2017, 37(3): 104.
[6]潘永兰 中药水提液无极陶瓷膜膜污染基础数据库的建立及数据的关联分析[D]. 南京:南京中医药大学, 2009.
[7]董洁, 郭立玮, 文红梅, 等. 中药水提液种蛋白质含量测定方法研究[J]. 现代中药研究与实践, 2009, 22(6): 40.
[8]李博, 张连军, 郭立玮, 等. 基于溶液环境调节理论的黄连解毒汤陶瓷膜微滤过程的预处理研究[J]. 中国中药杂志, 2014, 39(1): 59.
[9]黄仲涛, 曾昭槐, 钟邦克, 等. 无机膜技术及其应用[M]. 北京: 中国石化出版社, 1999.
[10]DalCin M M, Mclellan F, C N Striez, et al Membrane performance with a pulp mill effluent: relative contributions of fouling mechanisms[J]. J Membrane Sci, 1996, 120(2): 273.
[11]Ao L, Liu W J, Zhao L, et al Membrane fouling in ultrafiltration of natural water after pretreatment to different extents[J]. J Environ Sci, 2016, 43: 234.
[12]杨赫鸿, 李沛军, 孔保华, 等. 低场核磁共振技术在肉品科学研究中的应用[J]. 食品工业科技, 2012,33 (13): 400
[责任编辑孔晶晶]endprint

