电化学传感器检测环境中多氯联苯的研究进展
蒋宇婷,陈 文*
(1.成都理工大学 材料与化学化工学院,四川 成都 610059;2.矿产资源化学四川省高校重点实验室,四川 成都 610059)
电化学传感器检测环境中多氯联苯的研究进展
蒋宇婷1,2,陈 文1,2*
(1.成都理工大学 材料与化学化工学院,四川 成都 610059;2.矿产资源化学四川省高校重点实验室,四川 成都 610059)
多氯联苯(PCBs)为环境中持久性有毒有机污染物之一,对生态环境产生了严重的危害。随着科研人员对PCBs危害性认识的深入,PCBs监测方法的研究日益增多。该文概述了近年来国内外PCBs的主要分析方法,重点介绍了电化学传感器检测PCBs的研究成果,指出了目前电化学传感器检测PCBs存在的问题,并对电化学传感器在PCBs检测中的发展前景进行了展望。
多氯联苯;电化学传感器;分析方法;研究进展
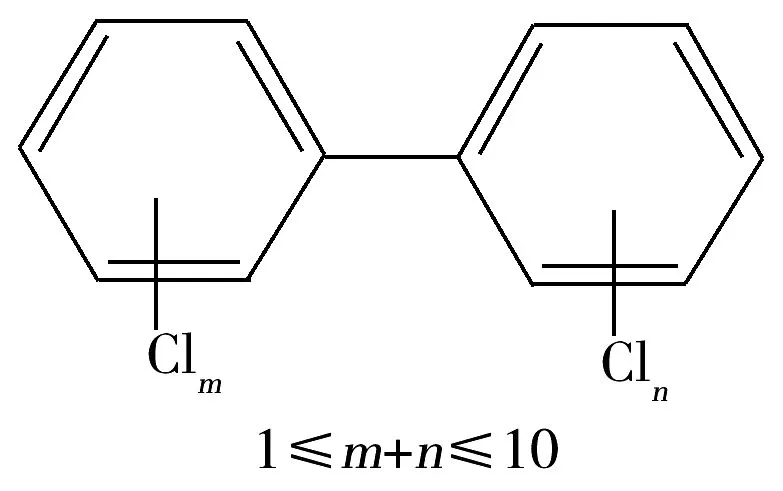
图1 多氯联苯的结构通式Fig.1 General structure of polychlorinated biphenyls
多氯联苯(Polychlorinated biphenyls,简称 PCBs,又名氯化联苯),是一类具有高稳定性的氯代烃类化合物,属于人工合成的工业品。在联苯的2个苯环上可连有不同数目、不同位置的氯原子,共有209种异构体,这些同系物多为非共平面结构,只有其中的4种非邻位取代和8种邻位取代 PCB具有共平面结构,称为共平面 PCB(Co-PCBs)。PCBs结构通式见图1。
1 概 述

虽然PCBs已被停产禁用,但因其曾大量使用,且理化特性极为稳定,可通过地表径流、大气沉降和含 PCB 固体废弃物的弃置进入土壤,且由于具有半挥发性等特征,可从土壤和水体中进入大气,在整个生态环境中形成持久性残留,因此对环境样品中PCBs的准确监测任重而道远。
由于PCBs的危害性,各国均非常重视环境中PCBs的监控,尤其对于环境水体的指标要求。日本在1982年12月登记的法规中规定废水中PCBs 的排放标准为0.003 mg·L-1(PCBs总量),欧共体在1983年1月登记的饮用水法规中规定了PCBs的最高允许浓度0.1 pg·L-1(每种物质分开)、 0.5 pg·L-1(PCBs 总量)。我国是《斯德哥尔摩公约》的签约国,于1989年将PCBs列入“水中优先控制污染物黑名单”并于1992年实施了“含多氯联苯废物污染控制标准”(GB13015-91),新颁布的《地表水环境质量标准》(GB3838-2002)中规定,集中式生活饮用水、地表水源地水中PCBs的含量不得超2×10-5mg·L-1[4]。
2 分析方法介绍
2.1 化学分析法
PCBs在环境中的浓度较低、组分复杂,准确定性和定量存在一定难度。目前,国际上公认的较为常用而有效的方法为气相色谱法(GC)[5-6]及气相色谱-质谱联用法(GC-MS,GC-MS/MS)[7-9]等化学分析法,这些方法分离能力强、耗时相对较短,并可进行多组分分析。但其操作技术要求较高,设备昂贵,仪器体积较大,无法应用于样品的现场检验,尤其使用GC测定Aroclor样品时,极易出现假阳性[10];GC-MS方法具有良好的分离特性,已能对PCBs的几十种同系物进行同时定量检测,且精确度很高,但在大批量样品的简捷快速检测方面仍受到限制,方法前处理技术的进一步优化仍是今后的主要研究方向。
2.2 生物分析法
随着生物科学的不断发展及其与其他科学的交叉延伸,生物分析技术亦被引入到PCBs检测领域。相对而言,生物学方法无需复杂的前处理过程,在大批量样品筛查方面具有较大优势。目前常见的生物分析法有免疫分析法、SERS分析技术及其他生物检测等方法。
2.2.1免疫分析法免疫分析法是一类常见的分析方法,它是以抗原与抗体的特异性反应为基础的一种分析技术,具有特异性较强、检测方便、耗时较短、成本较低等优点,但该方法的灵敏度总体不高,在痕量污染物的检测方面受到限制。免疫分析包括酶联免疫法和其它免疫法,在对PCBs的免疫检测研究方面,国外在20世纪 90 年代即开始用免疫方法检测环境中毒性较大的共平面PCBs[11-12],近年来,国内外在各类PCBs总量和单量的免疫测定方面也有较多的研究[13-16]。尤其是上海交通大学庄惠生教授研究团队[17-19]用当前比较先进的实时荧光PCR(rt-PCR)作为抗原抗体结合物的检测手段,通过制备特异性的PCBs多克隆抗体建立了环境中PCBs的rt-IPCR测定方法,检出限分别达1.5 fg·mL-1、1.72 pg· L-1和2.55 pg· L-1,检测灵敏度取得了很大的进展,但依然未能实现现场检测。另外,PCR需对靶分子进行级联放大后才能检测,耗时较长,而且难以实现真正意义上的定量测定[20]。该技术有待进一步优化,以提高其稳定性和重现性。
2.2.2表面增强拉曼光谱分析技术基于纳米或其它材料对检测基底进行粗糙改性,使痕量被测物的拉曼光谱信号增强,从而获得物质结构等信息的表面增强拉曼光谱(SERS)分析研究正成为一个热点。SERS技术不但具有拉曼光谱的大部分优点,能够提供更丰富的化学分子的结构信息,可实现实时、原位探测,而且灵敏度高,数据处理简单,准确率高,是非常强有力的痕量检测工具。近年,用于PCBs的方法研究也在逐步开展[21-24],因其不仅能提供分子的结构信息,而且具有很高的灵敏度,因此对PCBs异构体的识别鉴定更具优势。目前基底的重现性和稳定性的改善是该方法研究的主要目标,相信随着材料科学和纳米技术的发展,表面增强拉曼光谱作为一种迅速发展的检测技术,在环境污染物痕量分析方面的应用具有广阔的发展空间。
2.2.3其他生物检测技术PCBs的生物学分析技术还包括可对环境污染样品进行筛选和半定量的基因重组法[25],该法快速、灵敏,检测限可达2.5 ng·mL-1;可实时检测样品的表面胞质团的共振检测方法(SPR)[26-28];灵敏、快速但存在背景干扰的以芳香烃受体为基础的生物分析法[29-30];以及经美国EPA批准的一种基于芳香受体的新型生物检测方法——CALUX检测法[31]。
2.3 电化学方法
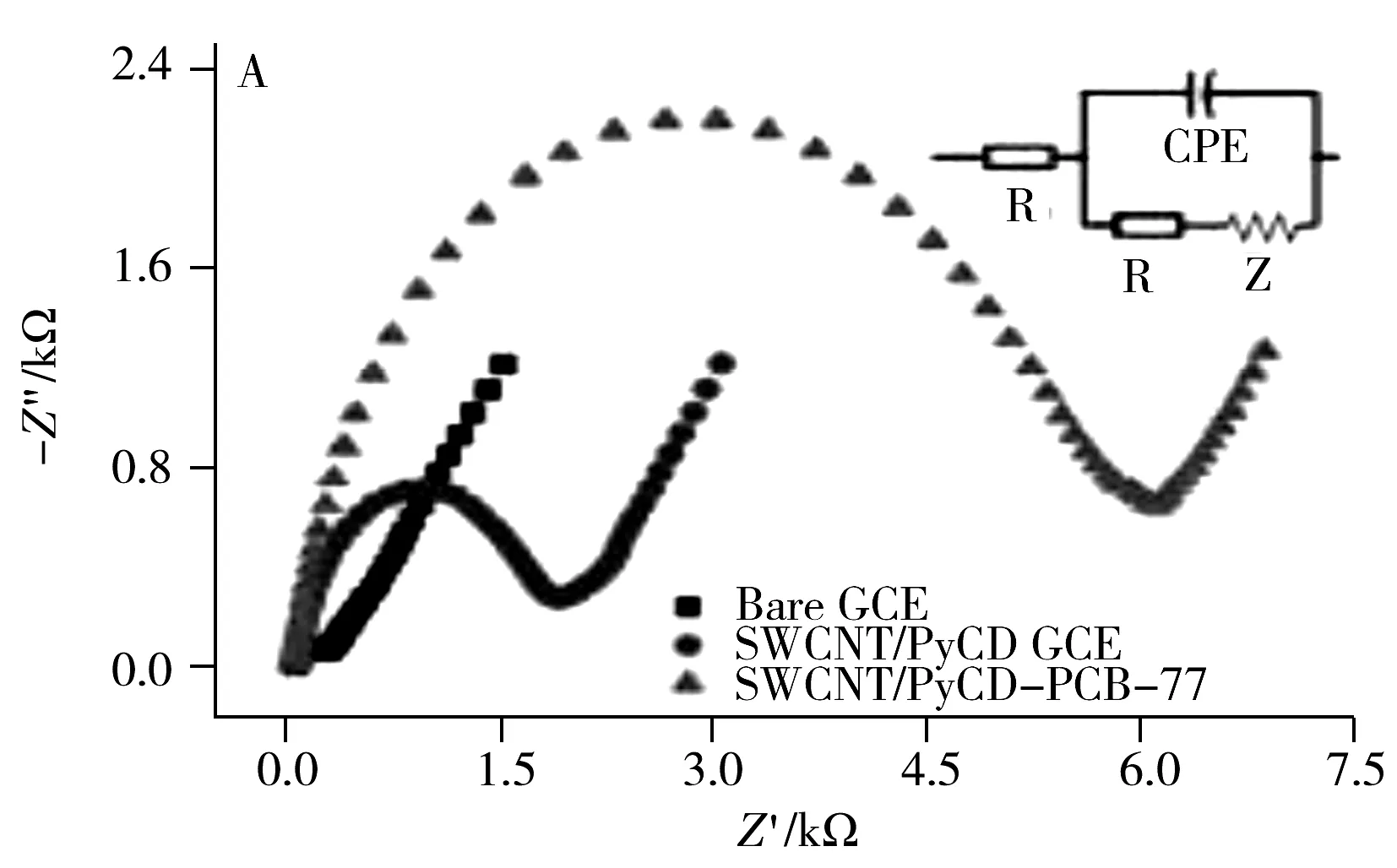
电化学方法因具有灵敏度高、选择性好、操作简便和响应快等特点而受到研究者的青睐,其中电化学传感器对环境污染物质的研究一直是近年的研究热点。对环境中多氯联苯的电化学传感器检测方法,主要通过电流、电位或阻抗等电化学信号来直接或间接分析待测物质。如Wei等[32]详细研究了利用单壁碳纳米管/芘环糊精(SWCNT/PyCD)复合膜传感器的交流阻抗变化进行3,3′,4,4′-四氯联苯(PCB-77)检测的方法。即当PCB分子通过PyCD主体的空腔捕获,PCB-复合物的形成会阻碍电化学过程,从而阻碍氧化还原探针 [Fe(CN)6]3-/4-进入电极表面,导致电子转移电阻增加,电子转移电阻的增加幅度与主体捕获的PCB分子数量有关(图2)。
而在电化学传感器中,电化学生物传感器是应用较多的电化学分析方法。由于生物传感器的识别元件是酶、受体、抗体等具有特异性识别能力的生物大分子,所以其特异性识别作用和快速催化作用的特点可以满足快速、特异性,能够实现即时和在线检测的要求[20],因而成为电化学传感器研究的热点之一。电化学生物传感器主要包括电化学酶传感器、电化学免疫传感器和电化学脱氧核糖核酸(DNA)生物传感器。
电化学酶传感器是一种由生物酶膜与各种电极如气敏电极、氧化还原电极等电化学电极组合而成或将酶膜直接固定在基体电极上制成,利用生化反应所产生或消耗的物质的量,通过电化学装置转换成电信号,进而选择性地测定出某种成分的传感器[33]。
电化学免疫传感器是一种基于抗原抗体特异性识别功能将抗体或抗原和电极组合而成的用以监测抗原、抗体反应的传感器[34]。
电化学脱氧核糖核酸(DNA)生物传感器,通常由一条直序列的单链DNA分子与电化学电极组成,是一种利用单链DNA(ssDNA)作为敏感元件通过共价键合或化学吸附固定在固体电极表面,加上识别杂交信息的电活性指示剂(称为杂交指示剂)共同构成的检测特定基因的装置[35]。
上述传感器在制备的过程中,一般为了实现更好的传感效应,会在酶、抗体或DNA识别单元与基底电极复合的过程中使用具有优异导电性能及生物亲和性的材料,诸如石墨烯、碳纳米管及金属纳米材料等,而石墨烯在电化学传感器上的使用较多。
2.3.1石墨烯在PCBs电化学传感器中的应用进展近年来,石墨烯因其独特的单原子结构而具有一系列的特殊性质,如量子霍尔效应、良好的导热导电效应、较高的载流子迁移率、超大的比表面积及边缘磁性行为,已成为电化学传感器的理想材料,在环境污染物质的电化学传感检测方面应用非常广泛[36-38]。而纳米材料除具备上述相似性质外,还具有特殊的光学性质、催化性质、光电化学性质以及良好的吸附能力和生物兼容性等特点,被广泛应用于各类传感器研究[39-41]。纳米材料还能显著提高生物分子的吸附量,同时放大电信号,从而使传感器的灵敏度、寿命、稳定性等得以提高[42]。将石墨烯和纳米材料结合,其各种优良效应的协同作用将使电化学传感器具备更强的分析性能。伴随着科技的快速发展,人们对电化学传感器的灵敏度要求越来越高。目前,采用纳米技术提高电化学传感器的灵敏度已成为国内外的研究热点,研究方向主要集中在碳纳米管和石墨烯传感器的制备和产业化方面。
基于石墨烯的PCBs电化学传感器研究,国内外均有报道。比利时安特卫普大学的Rather等[43]以氧化石墨烯(GO)为酪氨酸酶(Tyr)和氧化锌量子点(ZnO QD)组成的杂交结构的扩增平台,构建了检测OH-PCB的电化学传感器,检出限为0.15 μmol/L。济南大学的周长利教授团队[44]利用大环分子β-环糊精与还原的氧化石墨烯(ERGO)在电极表面形成聚合物,构建了PCBs的电化学传感器,其检出限为1.58×10-13mol/L。石墨烯在电化学传感器上的优异表现可见一斑。
2.3.2PCBs电化学免疫传感器研究进展文献中关于PCBs的电化学传感器的报道,以生物传感器,尤其是免疫传感器居多。南非约翰内斯堡大学的Nomngongo等[45]将辣根过氧化物酶固定在聚苯胺修饰的铂电极表面,研制出PCBs等有机污染物的酶传感器。该传感器对PCB-1、PCB-28、PCB-101的检出限分别为0.022、0.016、0.019 μg·L-1。该研究采用的酶固定于电极表面的修饰物之上,当抗原与抗体结合后,对酶的抑制作用需通过电极表面进行传递,在作用时间和效率上均不及酶直接修饰在抗体上快速和高效。
而美国国立大学化学系的Bender等[46]早在1998年就基于PCB和抗PCB抗体固定的导电聚合物基质之间的特异性结合,提出检测水中PCBs的直接电化学免疫传感器。该免疫传感器的检测范围为0.3~100 ng·mL-1,Aroclor 1242的相关系数为0.997。Aroclors 1242、1248、1254和1016的方法检测限为3.3、1.56、0.39、1.66 ng·mL-1,信噪比(S/N)为0.5的免疫传感器在氯化苯甲醚、苯和酚的存在下显示出对PCB的高选择性。来自工业废水、轧机和海产品工厂预处理水(0.5、50 ng·mL-1)的加标Aroclors 1242和1254的生物燃料的回收率为103%~106%。该方法可用于废水和地下水的连续检测。可以看出,无标记免疫传感器的检出限相对较高,对于痕量、超痕量分析样品需要进行浓缩富集,增加了分析的操作单元。
2000年,意大利佛罗伦萨大学Laschi等[47]以辣根过氧化物酶(HRP)与Ag或抗体缀合固定于丝网印刷电极上,采用过氧化氢和二茂铁羧酸(FCA)为探针,研制出一次性PCBs酶联免疫电化学传感器,并对食品中的PCBs残留进行了检测,检测范围在10-10~10-8mol/L之间。该方法的优点是分析时间(30 min)较微量滴定测定板(14 h)短。2015年,该研究团队[48]又在上述研究的基础上,以碱性磷酸酶为标记,研制出一次性丝网印刷酶联免疫电化学传感器并用于食品中PCBs残留检测。2005年和2007年,该团队成员Centi[49-50]先后提出一种包括磁性颗粒和碳基丝网印刷电极(SPCE)的一次性免疫磁电化学传感器,分别用于土壤中Aroclor 1248 PCB(检出限为0.4 ng·mL-1)和牛奶样品中PCB-28和PCB-77(检出限分别为4 ng·mL-1和28.65 pg·mL-1)的检测。该研究基于PCB和示踪剂PCB-碱性磷酸酶(AP)对磁珠表面抗体直接免疫竞争后被磁性石墨电极捕获,再通过AP对α-萘酚磷酸盐的酶促反应而进行电化学检测(图3)。
上述一次性碳基丝网印刷(磁性)电极检测PCBs的方法,分析快速,对食品的检测结果也满足分析要求,最大的优势是避免了分析过程中电极的污染和表面的再生,同时电极体积小,便于携带,更易于实现现场检测。但是一次性电极面临两个主要的问题:一是制造规格和性能的统一性和稳定性问题;二是废弃电极材料的绿色回收问题。因此上述两个问题的解决,对电化学传感器的应用具有重要意义。
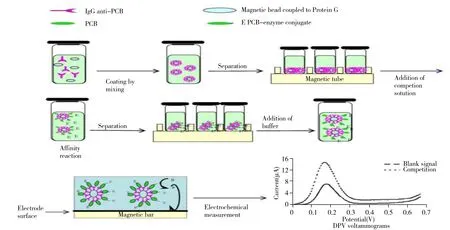
图3 磁性颗粒-碳基丝网印刷电极免疫传感器免疫反应、磁分离、电化学测量和DPV伏安分析的示意图[49]Fig.3 Schematic representation of the immunochemical reaction,magnetic separation,electrochemical measurement and DPV voltammograms[49]
另外,南非开普敦半岛科技大学Khesuoe等[36]最近研制出基于纳米银掺杂的聚苯胺修饰玻碳电极基底,以戊二醛(GA)共价键固定PCB抗体的电化学免疫传感器。该传感器对PCB28的检出限(LOD)和定量下限(LOQ)分别为0.063 ng·mL-1和0.209 ng·mL-1,其中纳米银的作用不可小觑。但是因氯化苄(BnCl)和PCB 180与PCB28的相似性,该传感器只适于PCBs总量的检测(图4)。
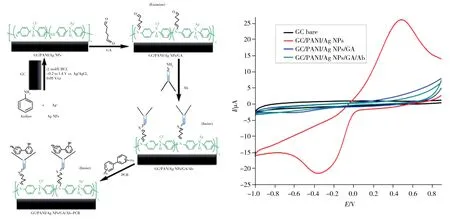
图4 PCBs纳米免疫传感器制作机理及玻碳电极免疫修饰前后的CV图[39]Fig.4 Immunosensor fabrication mechanism scheme and stepwise immobilization CV responses in PBS-ACN(99.6∶0.4,by volume)[39]
我国科研人员在PCBs免疫传感器的研究方面也取得了进展,上海交通大学庄惠生研究团队[40]构建了一种基于L-半胱氨酸、壳聚糖、戊二醛和纳米金层层自组装技术的新型无标记、高灵敏电流型3,3′,4,4′-四氯联苯(PCB77)免疫传感器,该传感器以铁氰化钾作为氧化还原探针,通过检测铁氰根离子在传感器电极上的响应电流间接检测样品中的PCB77。该方法用纳米金将电活性物质固定在电极表面,减少了媒介体对检测溶液的污染,提高了传感器的灵敏度和使用寿命,但传感器的选择性有待进一步提高。天津农学院的刘源等[51]进行了PCBs免疫传感器的设计,主要优化了传感器硬件系统和软件程序方面的设置,PCBs的检测值在1.25~10.00 ng/mL 范围内有很好的线性关系,电化学工作站 CH660A 测试值与检测系统测试值的相关系数为0.994 8。免疫传感器选择性不佳的问题较为突出,如何制备高特异性的免疫传感器仍是电化学工作者今后研究的方向。
2.3.3PCBs电化学脱氧核糖核酸(DNA)生物传感器研究进展近年来,核酸适体(Aptamer)的出现使得筛选针对各种靶标的高亲和力与强特异性的适体成为可能。与普通抗体相比,核酸适体有低分子量、自身稳定性强、变性复性快速、易功能性修饰与标记以及作为优良的纳米器件等诸多优点,也可以识别很多靶分子,其中包括有机染料、金属离子、可卡因等。因此,核酸适体在检测、诊断和治疗方面有更大的发展潜力[52]。
基于此,电化学脱氧核糖核酸(DNA)生物传感器多见诸于多类物质的分析研究,但关于PCBs检测的研究较少。比利时安特卫普大学 Pilehvar等[41]构建了将适体通过酰胺键固定在羧基化的多壁碳纳米管(MWCNT-COOH)修饰的玻碳电极表面的DNA生物传感器用于人血中OH-PCB的检测,线性范围为0.16~7.5 μmol/L,检测限达10-8mol/L。其中羧化多壁碳纳米管的羧基不仅可以结合DNA适配体以捕获更多被测物,同时其纵向电子快速传导性能缩短了被测物与传感器之间的传输时间。
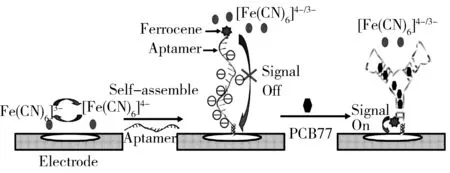
图5 适配体/Au 生物传感器的分析过程示意图[53]Fig.5 Schematic diagram of the fabrication process of the Aptamer/Au biosensor[53]
近期,中国水产科学研究院Wu等[53]研究开发了基于DNA适配体改性的Au电极(Aptamer/Au)的电化学生物传感器用于PCB77的高选择性快速检测(图5)。该传感器通过SELEX分离的适体(通过指数富集的配体的系统演化)和用电活性二茂铁(Fc)修饰的3′-DNA适体分别作为生物识别元件和信号放大分子,用以高选择性和灵敏性测定PCB77,其检测范围为0.2~200 μg·L-1,检出限(LOD)为0.01 μg·L-1。Aptamer/Au生物传感器可以区分PCB77与潜在的共存干扰物(即PCB同源物和苯衍生物)。因此,该传感器是PCB77选择性和快速现场测定的潜在工具。
目前关于PCBs核酸适配体电化学生物传感器的研究报道虽不多,但基于核酸适配体的高特异性优势,相信未来此类传感器对PCBs的检测方法研究会越来越多,终将充分探明此类电化学生物传感器的作用机理,研制出高效、灵敏、高选择性的PCBs电化学生物传感器。
3 结论与展望
电化学传感器技术与以往的传统方法相比具有诸多优势,如检测速度较快,操作简便,可进行实时检测,可与其他技术联用,特异性强以及无污染等特点。在环境监测领域的研究应用已经深入到各个角落,但目前大部分处于基础应用研究过程中,局限于实验室,真正实际应用仍有大量的难题需要攻克。比如电极制作的统一性和稳定性等问题;另外,在检测气体时需要传感器的微型化;进行室外检测时,检测环境和条件难以达到要求。而且,目前大多数电化学传感器只能对单一污染物进行分析,缺乏对某一类污染物的系统性研究等[54]。此外,电化学生物传感器在制造工艺上较难,并且由于使用的材料是具有生命活性的物质,其寿命常受环境中各种有害气体以及微生物的侵袭而失活,有些酶甚至一旦离开了生物活体,其寿命就大大降低[55]。因此,要制备廉价而使用寿命长的传感器确属不易。
虽然电化学传感器存在对温度非常敏感,使用的温度范围有限;使用寿命易受温度、压力和湿度的影响等问题,需要在使用寿命、再生性、稳定性等方面投入更多的研究精力,但是随着新型功能化纳米材料的不断涌现,譬如具有良好生物相容性的纳米粒子,能为生物材料提供一个可以有效保持其活性的类似生物分子本体环境的微环境,而纳米粒子的表面效应也会进一步提高生物分子的活性等[56],电化学生物传感器的一些缺陷将被克服。随着科技的不断发展,制作工艺的不断完善,专业生产设备的更新换代,电化学传感器在使用寿命、再生性、稳定性等方面的问题将会逐一得到解决。
相信电化学传感器技术的不断改进与创新会使其在环境监控(诸如对环境中PCBs这一类持久性污染物质等的监控)、医疗领域和工农业生产中展示更大的应用价值,未来有望实现对废气排放、污水排放的现场检验和郊野环境的动态无人实时监测[54]。
[1] Shen P.Chin.J.Chem.Edu.(沈平.化学教育),2005,6:6-9.
[2] Hu W L,Wang Q.Chin.J.HealthLab.Technol.(胡文兰,王勤.中国卫生检验杂志),2012,22(9):2262-2266.
[3] Xu W X,Yang R D,Zhang G.SichuanEnviron.(徐文兴,杨汝德,张广.四川环境),2008,27(2):89-93.
[4] Chen H Y,Zhuang H S,Yang G X.Environ.Chem.(陈寒玉,庄惠生,杨光昕.环境化学),2011,30(5):953-957.
[5] Diao C P,Yu X T,Li C,Yang X,Sun A L,Liu R M.J.Sep.Sci.,2016,39(10):1926-1934.
[6] Mokbel H,Dine E J A,Elmoll A,Liaud C,Millet M.Environ.Sci.Pollut.Res.,2016,23(8):8053-8063.
[7] Stancheva M,Georgieva S,Makedonski L.FoodControl,2017,72(B):205-210.
[8] Huang D M,Shi Y F,Qian B L,Wang Y,Jiang C J.J.Instrum.Anal.(黄冬梅,史永富,钱蓓蕾,王媛,姜朝军.分析测试学报),2008,27(Z1):183-186.
[9] Marder M E,Panuwet P,Hunter R E,Ryan P B,Marcus M,Barr D B.J.Anal.Toxic.,2016,40(7):511-518.
[10] Guo W C.FujianAnal.Test.(郭维超.福建分析测试),2014,23(1):42-48.
[11] Chiu Y W,Carlson R E,Marcus K L,Karu A E.Anal.Chem.,1995,679(21):3829-3839.
[12] Lawruk T S,Lachman C E,Jourdan S W,Fleeker J R,Hayes M C,Herzong D P,Rubio F M.Environ.Sci.Technol.,1996,30(2):695-700.
[13] Fránek M,Deng A P,Kolá V,Socha J.Anal.Chim.Acta,2001,444(1):131-142.
[14] Endoa T,Okuyama A,Matsubara Y,Nishi K,Kobayashi M,Yamamura S,Morita Y,Takamura Y,Mizukami H,Tamiya E.Anal.Chim.Acta,2005,531(1):7-13.
[15] Tsutsumi T,Amakura Y,Okuyama A,Tanioka Y,Sakata K,Sasaki K,Maitani T.Chemosphere,2006,65(10):467-473.
[16] Terakado S,Ohmura N,Park S U,Lee S M,Glass T R.Anal.Sci.,2013,29(10):963-969.
[17] Chen H Y,Zhuang H S.Anal.Bioanal.Chem.,2009,394(4):1205-1211.
[18] Yang G X,Zhuang H S,Chen H Y.Anal.Bioanal.Chem.,2014,406(6):1693-1700.
[19] Yang G X,Zhuang H S,Chen H Y,Ping X Y,Bu D.Sensor.ActuatorsB,2015,214:152-158.
[20] Lu D Q,Pang G C.FoodSci.(鲁丁强,庞广昌.食品科学),2014,35(8):6-10.
[21] Zhou Q,Yang Y,Ni J,Li Z C,Zhang Z J.PhysicaE:Low-dimensionalSystemsandNanostructures,2010,42:1717-1720.
[22] Xu W,Meng G W,Huang Q,Hu X Y,Huang Z L,Tang H B,Zhang J X.Appl.Surf.Sci.,2013,271:125-130.
[23] Robbins T H.Rsc.Adv.,2014,4(38):19654-19657.
[24] Lu Y,Yao G,Sun K,Huang Q.Phys.Chem.Chem.Phys.,2015,17(33):21149.
[25] Xu T,Kong F X,Sun C,Tan J K,Han X B,Yan R.Environ.Sci.(徐挺,孔繁翔,孙成,谈健康,韩小波,阎荣.环境科学),2004,25(1):45-48.
[26] Shimomura M,Nomura Y,Zhang W,Sakino M,Lee K H,Ikebukuro K,Karube I.Anal.Chim.Acta,2001,434(2):223-230.
[27] Rogers K R.Anal.Chim.Acta,2006,568(1/2):222-231.
[28] Li L,Zhang G,Zhao J L,Gu D Y,He Y H,Ma S H.ActaSci.Circum.(李莉,张广,赵继伦,顾大勇,何永红,马绥华.环境科学学报),2010,30(10):2004-2010.
[29] Behnisch P,Hosoe K,Shiozaki K,Komatsu T,Schramm K W,Sakai S.Environ.Sci.Pollut.Res.,2002,9(5):337-344.
[30] Tsutsumi T,Miyoshi N,Sasaki K,Maitani T.Anal.Chim.Acta,2008,617(1/2):177-183.
[31] Croes K,Van Langenhove K,Elskens M,Desmedt M,Roekens E,Kotz A,Denison M S,Baeyens W.Chemosphere,2011,82(5):718-724.
[32] Wei Y,Kong L T,Yang R,Wang L,Liu J H,Huang X J.Chem.Commun.,2011,47:5340-5342.
[33] Liu J,Yin L F,Dai Y R,Jiang F,Niu J F.ProgressinChemistry(刘佳,殷立峰,代云容,江帆,牛军峰.化学进展),2012,24(1):131-143.
[34] Zhong T S,Liu G D,Shen G L,Yu R Q.Chem.Sens.(钟桐生,刘国东,沈国励,俞汝勤.化学传感器),2002,22(1):7-14.
[35] Zhang W Y,Pan W P,Li K,Que X D,Ma X G,Qian L N.ChineseJournalofPublicHealthEngineering(张雯艳,潘维平,李凯,阙肖冬,马兴钢,钱丽娜.中国卫生工程学),2002,1(3):188-189.
[36] Park H,Kim J Y,Haque A M J,Choi S Y,Kim T H,Hong J D,Kim K.Bull.KoreanChem.Soc.,2012,33(12 ):4219-4222.
[37] Tan X C,Hu Q,Wu J W,Li X Y,Li P F,Yu H C,Li X Y,Lei F H.Sens.ActuatorsB,2015,220:216-221.
[38] Xue F,Gao Z Y,Sun X M,Yang Z S,Yi L F,Chen W.J.Electrochem.Soc.,2015,162(6):H338-H344.
[39] Khesuoe M P,Okumua F O,Matoetoe M C.Anal.Methods,2016,8:7087-7095.
[40] Zhang Y,Zhuang H S,Chen H Y.Chem.J.Chin.Univ.(张岩,庄惠生,陈寒玉.高等学校化学学报),2013,34(5):1092-1098.
[41] Pilehvar S,Ahmad R J,Dardenne F,Robbens J,Blust R,De W K.Biosens.Bioelectron.,2014,54:78-84.
[42] Yin H S,Ai S Y,Shi W J,Zhu L S.Sens.ActuatorsB,2009,137(2):747-753.
[43] Rather J A,Pilehvar S,Wael K D.Sens.ActuatorsB,2014,190:612-620.
[44] Zheng X L,Li H L,Xia F Q,Tian D,Hua X X,Qiao X Y,Zhou C L.Electrochim.Acta,2016,194:413-421.
[45] Nomngongo P N,Ngila J C,Msagati T A M,Gumbi B P,Iwuoha E I.Phys.Chem.Earth,2012,50/52:252-261.
[46] Bender S,Sadik O A.Environ.Sci.Technol.,1998,32:788-797.
[47] Laschi S,Mascini M,Scortichini G,Fránek M,Mascini M.J.Agric.FoodChem.,2003,51(7):1816-1822.
[48] Laschi S,Fránek M,Mascini M.Electroanalysis,2015,12(16):1293-1298.
[49] Centi S,Laschi S,Fránek M,Mascini M.Anal.Chim.Acta,2005,538:205-212.
[50] Centi S,Silva E,Laschi S,Palchetti I,Mascini M.Anal.Chim.Acta,2007,594:9-16.
[51] Liu Y,Wu H Y,Yu Y P,Chang R K,Wang L P.HubeiAgric.Sci.(刘源,吴海云,于亚平,常若葵,王利鹏.湖北农业科学),2015,54(18):4593-4595.
[52] Sun M Q,Cao F Q,Hu X L,Zhang Y R,Lu X W,Zeng L B.J.Forens.Med.(孙美琪,曹芳琦,胡小龙,张玉荣,陆鑫薇,曾立波.法医学杂志),2014,30(5):346-349.
[53] Wu L D,Qi P P,Fu X C,Liu H,Li J C,Wang Q,Fan H.J.Electroanal.Chem.,2016,771:45-49.
[54] Liu L H,Che W S,Sun J,Chen L H,Dai L M,Yang L,Zhu D Y.Technol.Inn.Appl.(刘立红,车文实,孙晶,陈丽华,代立梅,杨柳,朱道玉.科技创新与应用),2017,(1):43.
[55] Tong W,Zhang J M,Zhang L.ActaAcad.Med.CPAF(佟巍,张纪梅,张丽.武警医学院学报),2008,17(1):62-64.
[56] Yang H P,Chen S G,Li C H,Chen D C,Ge Z C.Prog.Chem.(杨海朋,陈仕国,李春辉,陈东成,戈早川.化学进展),2009,21(1):210-216.
Research Progress of Determination of Polychlorinated Biphenyls in Environmental Samples by Electrochemical Sensors
JIANG Yu-ting1,2,CHEN Wen1,2*
(1.College of Materials and Chemistry & Chemical Engineering,Chengdu University of Technology,Chengdu 610059,China;2.Mineral Resources Chemistry Key Laboratory of Sichuan Higher Education Institution,Chengdu 610059,China)
Polychlorinated biphenyls(PCBs) are one of the persistent toxic organic pollutants in the environment,which have caused serious harm to the ecological environment.Many monitoring methods for PCBs have been developed rapidly because the researchers have paid more and more attention on their perniciousness.The main analytical methods for PCBs at home and abroad in recent years are summarized in this paper,especially the investigation on determination of PCBs using electrochemical sensors.and the insufficients of these researches are also pointed out.The foreground of electrochemical sensors in application of determining PCBs are prospected.
polychlorinated biphenyls;electrochemical sensor;analytical method;research progress
10.3969/j.issn.1004-4957.2017.10.020
O646;X131
A
1004-4957(2017)10-1279-08
2017-04-22;
2017-06-08
*
陈 文,博士(后),教授,研究方向:分析化学,Tel:028-84079012,E-mail:chenwen2010@foxmail.com