2,4,6-三磺酸基间苯二酚硝化
——反应动力学与过程优化
张化良,曾 涛,叶光华,周静红,周兴贵
华东理工大学化工学院,化学工程联合国家重点实验室,上海 200237
2,4,6-三磺酸基间苯二酚硝化
——反应动力学与过程优化
张化良,曾 涛,叶光华,周静红,周兴贵
华东理工大学化工学院,化学工程联合国家重点实验室,上海 200237
采用管式反应器与间歇反应器串联的方式考察了 2,4,6-三磺酸基间苯二酚(TSR)选择性硝化制备 2-磺酸基-4,6-二硝基间苯二酚(DNRS)的过程。建立了三步串联硝化反应宏观动力学模型以及等温均相间歇反应器模型(BR),对实验数据进行优化拟合估计动力学参数;将获得的动力学参数应用于一维定态轴向扩散管式反应器模型(LM)中,并与实验值进行对比验证。结果表明,三步串联硝化反应的表观活化能分别为 57.66,40.05,130.89 kJ/mol;轴向扩散降低了串联硝化反应中间产物的选择性及收率,目标产物 DNRS的最大收率随着管式反应器管径的增加而减小。分析比较了LM模型与BR模型的计算结果,并对管式反应器的放大进行了模拟计算。研究结果可用于TSR硝化反应器的设计和过程的优化。
2,4,6-三磺酸基间苯二酚 硝化反应 宏观动力学 过程优化
聚对苯撑苯并二噁唑(PBO)纤维是20世纪60年代美国空军开发的一种在国防军工、航空航天等领域有着重要应用价值的有机高性能纤维,具有超高强度和模量、优异的耐热性和阻燃性[1],在防护器材、消防器材与运动器材等众多领域中得到广泛应用。
4,6-二氨基间苯二酚(DAR)是合成 PBO纤维的重要中间体,其合成路线种类较多[2-4],其中熊本行宏等[3]提出的间苯二酚三磺化合成方法具有原料价廉易得,原子利用率较高,能够满足高分子量PBO对DAR高纯度的要求等优势,因此广受关注。该工艺以间苯二酚(RS)为原料,采用发烟硫酸磺化得到2,4,6-三磺酸基间苯二酚(TSR),然后经硝化得到2-磺酸基-4,6-二硝基间苯二酚(DNRS),并经水解、还原后得到DAR,如图1所示。
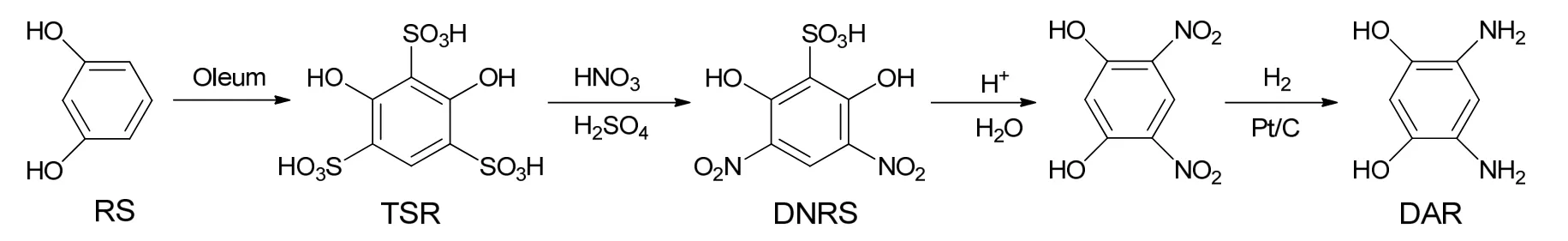
图1 间苯二酚三磺化法合成DAR路线Fig.1 Synthesis route of DAR by sulfonation of resorcinol
2,4,6-三磺酸基间苯二酚(TSR)选择性硝化对该合成路线的DAR总收率起到决定性作用。硝酸先在浓硫酸作用下生成硝酰阳离子作为亲电试剂进攻苯环,因2位的磺酸基及1、3位的羟基造成位阻效应,因此硝酰阳离子优先依次进攻4、6位生成2,4-二磺酸基-6-硝基间苯二酚(DSRN)与DNRS。

2 硝化反应动力学确定
2.1 硝化反应动力学模型
大量研究表明[5,7,8],硝基苯在硝硫混酸中的硝化反应服从二级反应的规律[7,8]。本研究的 TSR硝化过程亦可认为是二级反应(对硝酸和有机物分别为一级)[5]。由于混酸的强氧化性,DMSO(F)溶剂也将被硝化,也消耗部分硝酸。但由于 DMSO大量过量,因此其硝化反应可视为仅对硝酸为一级反应。TSR的硝化反应及各物质的反应速率如下:

2.2 动力学参数估计及模型校验
首先测定了DMSO的硝化反应动力学,忽略TSR硝化对其影响,按一级反应处理得其速率常数,结果见表 1。根据阿累尼乌斯方程拟合得到 DMSO硝化反应的活化能Ea4和指前因子A4分别为16.01 kJ/mol,1.07×10-5。

表1 各硝化反应动力学参数Table 1 Rate constants of nitration reactions
根据图 3所示的间歇硝化反应实验结果,用上述的动力学方程式(1)~(5)拟合得到的动力学参数见表1。用阿累尼乌斯方程拟合得到了TSR硝化反应过程中各步硝化反应的反应活化能和指前因子,如表2所示。

表2 各步硝化反应的表观活化能及指前因子Table 2 The activation energies and pre-exponential factors for the steps in the TSR nitration
从表2可看出,DNRS进一步硝化为三硝化物TNR的反应活化能远远高于前两步硝化过程的活化能,因此温度升高将显著提高目标产物DNRS过度硝化的速率,由此大幅度降低其选择性。因此,对这一串联硝化反应,为了提高目标产物DNRS的收率,必须精确控制反应温度。
采用拟合的动力学方程计算得到的各物质浓度变化与实验值的比较如图3所示。可看出动力学模型对实验结果的拟合较好,同时也说明前期对TSR硝化反应对有机物和硝酸分别为一级的假定是合适的。

图3 各物质浓度变化的计算值与实验值比较Fig.3 Comparison of experimental and predicted concentration of components
为了进一步校验所获得的动力学参数的可靠性,将获得的动力学参数用于建立 TSR硝化过程连续管式反应器模型进行模拟计算,并与实验值进行比较。假定反应在等温条件下进行,各物料在入口混合均匀。实验中流体在细管内流动的Re为5.42,为层流流动,采用一维轴向扩散反应器模型来计算反应结果。TSR及其硝化产物的分子扩散系数分别采用Wilke and Chang公式(6)计算[9],并取平均值作为反应物系的分子扩散系数。反应器的长径比L/dt为9 943。选择Taylor表达式(7)计算轴向有效扩散系数[10]。

采用打靶法求解该模型,进行了不同反应温度及不同反应器管长的模拟计算,计算结果和实验结果的比较如图4所示。从图4可以看到模拟结果与实验结果吻合很好(残差平方和为0.4%),这从另一方面证明了获取的动力学参数是可靠的。

图4 管式反应器内模拟值与实验值Fig.4 Comparison of simulated and experimental results in tubular reactor
3 反应过程优化
理论上对串联反应,任何返混都对提高中间产物的收率不利,最佳的反应器是全混式间歇反应器。但间歇反应器在体积较大时不易实现混合的均匀性,也不易于精确控温。而微型或小型反应器在原料预混合和温控方面有很大优势,但如果存在返混收率会下降。因此,采用一维轴向扩散模型模拟考察了微型或小型反应器管径对收率的影响,由于管内温度变化平缓,在反应器模型中只考虑浓度扩散,不考虑温度扩散,也不考虑反应过程中可能出现的产物析出问题。
对置于水浴的连续流动管式反应器,管外对流传热系数取α1为400 W/(m2·K),管内为层流流动状态的硫酸反应体系的传热系数的计算采用式(8)[11]:

微通道反应器的总传热系数K采用式(9)进行计算[12],W/(m2·K)(以管道内表面积为基准的传热系数):

设定进口体积流率不变,仍然维持在1.433×10-7m3/s,模拟考察了不同管式反应器内径时的反应,表3中列出了在不同反应温度下间歇反应器中能获得的最大收率(表3的第2列),不同管径反应器中可获得的最大收率(表3的第5列),以及可能出现的最大温升(表3的第6列)。

表3 管径放大计算结果对比Table 3 The calculation results for tubular reactor of different diameters
结果表明,管径增加,目标产物最佳收率会有所下降,温度越低,管径对最优收率的影响越小,而且温度对收率的影响更加敏感。因为DNRS进一步硝化活化能最高,温度是决定收率的控制因素。此外可以看出,即使利用管径为7 mm的管道,温升最高也只有0.41 ℃,几乎可忽略不计。
如果仅仅考虑DNRS收率,最优反应器为间歇反应器(在温度可控的前提下)。但由于该反应在初始阶段物料物性(粘度)差异大、流速差异大,不易混合均匀,同时副产物TNR的选择性对温度很敏感,因此需要考虑如何促进原料预混合提高反应速率以及在反应初始阶段控制反应温升的问题。微型管式反应器对提高硝化反应速率和实现温度控制十分有利,但在反应后期过渡硝化产物TNR将析出堵塞管道,层流流动也会降低反应收率及选择性。从实际角度, 管道反应器+间歇反应器组合是更合理的方式:一方面促进原料预混合(提高反应速率),另一方面有利于实现温度的精确控制。根据表4中的计算结果,可以预测即使采用较大直径的管道反应器也不会出现大的温升,至于管道直径增加后的返混问题,可采用管道式静态混合器加以解决。采用小通道反应器与间歇反应器组合这种操作方式,不仅能避免微反应器中堵塞问题和因层流流动引起的收率下降温度,又能使总的反应时间缩短,并实现反应的平稳和安全操作。
4 结 论
a)研究了TSR选择性硝化反应动力学,确定了反应动力学参数。三步硝化反应活化能Ea1,Ea2,Ea3分别为57.66,40.05,130.89 kJ/mol。因此,温度控制是提高串联硝化中间产物DNRS收率的决定性因素。
b)建立了连续管式反应器的轴向扩散模型。模拟结果表明,管径增加后,最佳收率会有所下降,温度越低,管径对最优收率的影响越小。
c)为了兼顾物料预混合、传热强化、返混和固体析出对最优收率和稳定操作的影响,在管式反应器后串联间歇反应器是合理的选择。
符号说明
c—— 浓度,mol/LRe—— 雷诺数
DAB—— 分子扩散系数,m2/sT—— 温度,K
Dea—— 有效扩散系数,m2/su—— 物料流速,m/s
dt—— 管径,mmU—— 传热系数,W/(m2·K)
Ea—— 表观活化能,kJ/molvA—— 溶质在正常沸点下的分子体积,cm3/(g·mol)
k1,2,3—— 反应速率常数,L/(mol·s)α—— 冷却介质及溶剂传热系数,W/(m2·K)
k4—— 反应速率常数,s-1δ—— 管壁厚度,mm
L—— 微通道反应器长度,mλ—— 热导率,W/(m·K)
MB—— 溶剂相对分子质量,g/molμB—— 溶剂粘度,mPa·s
Pem—— 传质Péclet数ρ—— 密度,kg/m3
Pr—— 普朗特数φ—— 溶剂的缔合参数
R—— 理想气体常数,J/(mol·K)ΔH—— 反应焓,kJ/mol
[1]Pop E, Mann D, Cao J, et al. Negative differential conductance and hot phonons in suspended nanotube molecular wires [J]. Phys Rev Lett, 2005, 95(15):155505.
[2]Dow Chemical Co. Synthesis of 4,6-diamnoresrcinol: US, 5371291 [P]. 1994-12-06.
[3]熊本行宏, 楠本昌彦. 4,6-二氨基间苯二酚的制备方法: 中国, 1276369 [P]. 2000-12-13.
[4]Behre H, Fiege H, Blank H U, et al. Process for preparing 4,6-diaminoresorcinoldihydrochloride: US, 6093852 [P]. 2000-07-25.
[5]吕春绪. 硝酰阳离子理论 [M]. 北京: 兵器工业出版社, 2006:102-106.
[6]Lin X Y, Wang K, Zhang J S, et al. Liquid-liquid mixing enhancement rules by microbubbles in three typical micro-mixers [J]. Chem Eng Sci, 2015, 127:60-71.
[7]Miller R C, Noyce D S, Vermeulen T. Kinetics of aromatic nitration [J]. Ind Eng Chem, 1964, 56(6):43-53.
[8]Gillespie R J. Hughes, E D, Ingold, C K. et al. Kinetics and mechanism of aromatic nitration [J]. Nature, 1949, 163(4146):599-599.
[9]Wilke C R, Chang P. Correlation of diffusion coefficients in dilute solutions [J]. AIChE J, 1955, 1(2):264-270.
[10]Levenspiel O, Levenspiel C. Chemical reaction engineering [M]. New York etc.: Wiley, 1972: 339-341.
[11]张 奕. 传热学 [M]. 南京: 东南大学出版社, 2004: 120-130.
[12]陈敏恒, 丛德滋, 方图南, 等. 化工原理 [M]. 北京: 化学工业出版社, 2006:208-209.
Nitration Process of 2,4,6-Trisulfonate Resorcinol-Reaction Kinetics and Process Optimization
Zhang Hualiang, Zeng Tao, Ye Guanghua, Zhou Jinghong, Zhou Xinggui
State Key Laboratory of Chemical Engineering, East China University of Science and Technology, Shanghai 200237, China
Nitration of 2,4,6-trisulfonate resorcinol (TSR) in a tube and a batch reactor was carried out to produce 2-sulfo-4,6-dinitroresorcin (DNRS). Nitration of TSR involves three reactions in series, and in addition, the nitration of the solvent,i.e. DMSO. Kinetics was established and the parameters obtained by fitting the experimental data from the batch reactor. The obtained kinetics was verified by the experiments on the tube reactor. Then simulation was performed for the tube reactor by assuming plug flow, and the results were compared to the case where dispersion effect due to laminar flow was considered. The results show that the temperate rise in the tube is negligible, and isothermal condition can be assumed. Because of the axial dispersion, increasing the tube diameter will decrease the yield of DNRS. However, the reaction temperature has more remarkable effect on the yield.
2,4,6-trisulfonate resorcinol; nitration reaction; apparent kinetics; process optimization
TQ203.6
A
1001—7631 ( 2017 ) 03—0193—06
10.11730/j.issn.1001-7631.2017.03.0193.06
2017-04-19;
2017-05-12。
张化良(1991—),男,硕士研究生;周静红(1971—),女,教授,通讯联系人。E-mail:jhzhou@ecust.edu.cn。

