壳聚糖/脲醛树脂微胶囊的制备和控释性能
, , , ,
(1.华东理工大学化学工程研究所,上海 200237; 2.中化化肥有限公司成都研发中心,成都 610015)
壳聚糖/脲醛树脂微胶囊的制备和控释性能
叶鹏飞1,陈葵1,纪利俊1,朱家文1,盛勇2
(1.华东理工大学化学工程研究所,上海200237;2.中化化肥有限公司成都研发中心,成都610015)
以脲醛树脂(UF)/壳聚糖(CS)复合材料为壳材,以溶解了阿维菌素的二甲苯为芯材,研究脲醛树脂(UF)/壳聚糖(CS)缓控释农药微胶囊的制备方法。改变壳层聚合过程中作为交联剂的甲醛的引入方式,制备得到一系列微胶囊。通过红外光谱仪、粒度分布仪、扫描电镜等对微胶囊的化学结构、组成成分、形貌特征进行表征,发现在缩聚阶段引入甲醛可以提高微胶囊壳层中壳聚糖的含量,进而提高微胶囊的包覆率和缓释效果。在优化条件下制备得到的微胶囊粒径7.14μm,包覆率大于70%。
微胶囊; 壳聚糖; 脲醛树脂; 缓释农药
脲醛树脂(UF)是由尿素和甲醛聚合而成的高分子材料,具有原料价格便宜、制备条件温和、耐磨性好等优点[1],此外,树脂中的氮元素还可以作为潜在的氮源供给植物利用[2],因此,UF是一种良好的缓释农药微胶囊(MCP)壁材。UF降解性差、水溶性低、脆性大[3],尤其是降解性差的缺点限制了其在缓控释农药微胶囊中的应用。壳聚糖(CS)是一种天然的氨基多糖高分子物质,分子中含有大量甙键、羟基和胺基,在酸性溶液中具有溶解性,在自然条件下容易降解,且生物相容性好[4-7]。用CS改性UF,通过改变CS的含量可以调控复合材料的降解性;同时,CS中含有的大量亲水基团,可以提高复合材料的吸水溶胀性能,间接提高复合材料降解性能。CS的相对分子质量在106左右,在复合材料的构建过程中其空间位阻影响壳聚糖与树脂的缩聚嵌入[8],因此,鲜有关于将UF和CS复合使用的报道。
Qu等[9]用UF和羧甲基化壳聚糖合成蛇笼树脂,其膨胀性能和稳定性能良好,在纯水、盐酸、NaOH溶液中均不脱序游离,对金属有很强的吸收能力,因此,可以用蛇笼树脂作为添加剂对其他壁材进行改性或直接以此为膜材来制备微胶囊。Wang等[10]将CS溶液和UF预聚液加到芯材乳化液中,利用乳化剂十二烷基硫酸钠对CS中氨基的吸引,在乳化液表面形成一层凝胶,再逐渐将pH降至3,使得UF预聚液中的羟基和CS中的氨基交联,形成微胶囊。这是一个双层膜结构的微胶囊,内膜层为壳聚糖,外膜层以脲醛树脂为主。因此,控制缓释速率的主要步骤是较难降解的脲醛树脂外壳层的降解速率,而壳聚糖控制缓释速率的作用较弱。一般复合材料壳层微胶囊中控制缓释速率的步骤是易降解材料的降解速率[11],因此在UF/CS单一混合壳层中,CS的降解速率决定了整个微胶囊的破裂速率,进而决定了农药的释放速率。
本文研究将UF/CS共混形成单一壳层微胶囊的制备方法,并且通过在UF制备过程的缩聚阶段引入甲醛将壳聚糖羟甲基化,提高了微胶囊壳层中CS的含量,使微胶囊达到更好的缓释效果和包覆效果。
1 实验部分
1.1原料
阿维菌素(AV)原药:纯度98.5%,邹平德睿商贸有限公司;甲醛:质量分数为37.0%~40.0%,上海凌峰化学试剂有限公司;尿素:纯度≥99%,上海凌峰化学试剂有限公司;邻二甲苯:纯度≥98.0%,上海凌峰化学试剂有限公司;司班80 (Span-80):化学纯,国药集团化学试剂有限公司;吐温80:化学纯,国药集团化学试剂有限公司;壳聚糖:国药集团化学试剂有限公司;无水乙醇:分析纯,国药集团化学试剂有限公司。
1.2微胶囊的制备
1.2.1 阿维菌素乳化液的制备 将0.2 g阿维菌素和2 mL邻二甲苯混合加热至阿维菌素溶解在邻二甲苯中;冷却至室温,加入Span-80,得到油相;另取一定量吐温80 (Tween-80)溶于50 mL水中,得到水相;将水相倒入油相,在300 r/min转速下搅拌乳化1 h,得到乳化液。
1.2.2 UF预聚液的制备 设预聚开始时刻为t1,称量5 g尿素和一定质量的甲醛(F1),混合溶解得到无色透明溶液;用氢氧化钠溶液调节尿素甲醛混合液的pH为10;70 ℃下恒温反应1 h,得到预聚液。
1.2.3 微胶囊的包覆 设缩聚开始时刻为t2,将预聚液、乳化液、CS溶液和一定质量的甲醛(F2)混合,调节pH=3.5;将混合液移入夹套瓶,60 ℃恒温反应,转速300 r/min。设缩聚反应1 h的时刻为t3,加入一定质量的甲醛(F3)继续反应2 h。
反应结束后过滤,并用水洗涤滤饼,40 ℃干燥24 h,得到微胶囊。
实验制备了4组微胶囊(MCP-1,MCP-2,MCP-3,MCP-4)来比较其形貌、粒度及缓释性能差异。制备微胶囊所用原料用量见表1。实验中尿素(U)和甲醛(F)溶液质量比为1∶2。

表1 各组微胶囊的加料方式
1.3包覆率的测定
将制备所得的微胶囊悬浊液直接干燥,得到未包覆的阿维菌素和微胶囊的混合固体,称量其质量为mMCP,取其中 0.5 g,用30 mL乙醇浸没形成悬浊液,70 ℃下加热3 min;将悬浊液转移至100 mL容量瓶定容;从容量瓶中量取大约40 mL悬浊液在转速10 000 r/min下离心10 min;移取1 mL上清液,定容至50 mL;测定50 mL容量瓶中溶液的吸光度A。
(1) 在波长245 nm时,测定阿维菌素乙醇溶液的浓度(c1)与吸光度A标准曲线方程:
c1=25.97A-0.161 9,R2=0.995
(1)
(2) 滤液中阿维菌素的质量m1
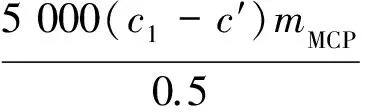
(2)
式中,c′为未包覆阿维菌素的空白微胶囊(MCP-0)的浓度。
(3) 包覆率K

(3)
式中,m2为最初用于包覆的阿维菌素的质量。
1.4微胶囊分解缓释实验
称取1 g微胶囊装入透析袋,再装入1粒搅拌子,将透析袋两端扎紧后没入盛有200 mL体积分数为30%乙醇溶液的棕色广口瓶中,用凡士林密封瓶口,将广口瓶室温静置。每隔一段时间,从广口瓶中移取2 mL溶液至比色皿,再分别往广口瓶和比色皿中加入2 mL体积分数为30%的乙醇溶液,测定吸光度,并通过标准曲线法求得溶液中阿维菌素浓度。乙醇溶液中阿维菌素的浓度对吸光度的标准曲线为
c2=27.18A-0.068 1,R2=0.993 3
(4)
溶液中阿维菌素的浓度
cn=2c2
1.5微胶囊表征
微胶囊研磨后用溴化钾压片制样,用Nicolet 6700型红外光谱分析仪(美国Thermo electron公司)测定微胶囊红外光谱,确定微胶囊结构;使用Nova NanoSEM 450型场发射扫描电镜观察微胶囊形貌特征;使用Mastersize3000型粒度分析仪测定微胶囊粒径分布。
2 结果与讨论
2.1微胶囊的红外分析

2.2微胶囊包覆率的测定
4组微胶囊包覆率的测定结果见表2,少量悬浮的脲醛树脂颗粒会吸收紫外光,MCP-1的包覆率最低,这主要是因为UF易收缩、脆性大,不容易在乳化液滴表面形成包裹。CS是一种长链高分子,可以改善UF的力学性能,提高微胶囊的包覆率。

图1 微胶囊红外吸收光谱Fig.1 IR spectra of MCP

表2 MCP的包覆率
2.3微胶囊形貌分析
用扫描电子显微镜来分析微胶囊的形貌,结果示于图2。微胶囊表面粗糙,表面无裂缝或破损,说明包覆良好。由于微胶囊表面的--OH和--NH2相互之间可以形成氢键,或者在甲醛的作用下发生交联反应,微胶囊易团聚。由图2可以看出,MCP-1和MCP-2团聚严重;和MCP-1和MCP-2相比,MCP-3和MCP-4粒径趋于缩小,分散性提高。因此,分批加入甲醛可以改善微胶囊的分散性。
2.4微胶囊粒径分布
微胶囊的粒径分布结果见表3,其中Dv指分割粒径。4组微胶囊的粒径均小于100 μm,属于微米级颗粒。图3所示为微胶囊粒径分布图。MCP-2的峰宽大于MCP-1,说明壳聚糖使得微胶囊粒径分布变宽。比较MCP-2、MCP-3和MCP-4的平均粒径D[3,2]可知,随着甲醛加入次数的增加,平均粒径减小,说明分批加料可以减弱微胶囊颗粒之间的黏连。虽然MCP-4的粒径最小,但是它在图3中有一个很大的拖尾,粒径分布不够集中。因此,MCP-3的平均粒径较小,且分布较为集中,是较为理想的微胶囊。

图2 微胶囊的SEM图片Fig.2 SEM images of MCP

表3 微胶囊的粒径分布结果

图3 微胶囊粒径分布图Fig.3 Size-grading images of MCP
2.5微胶囊缓释动力学
UF/CS微胶囊的破裂速率与壳层材料中CS的含量有关。在壳层降解破裂之后,微胶囊的油相从壳层溢出,进入水相,形成不稳定的水包油体系,然后阿维菌素从油相扩散进入水相。由于二甲苯密度比水小,挥发性强,微胶囊中芯材质量相对于缓释体系中水的质量来说很小,所以假定微胶囊释放出的乳化液滴能在较短的时间内上浮至水面,破乳挥发。微胶囊破裂的裂缝很大,所以药物释放的控制步骤不是油相从壳层进入水相形成水包油的过程,而是阿维菌素从油相扩散进入水相的过程。
对微胶囊的缓释性能进行测定,缓释结果如图4所示。采用一级动力学方程对其进行拟合[12]
c=-c0e-kt+ktn+c0
(6)
式中:k表示动力学常数;c0表示油相阿维菌素在水相中对应的饱和浓度;c表示缓释液中阿维菌素的浓度;tn表示微胶囊破裂所需时间。tn与壳层中CS的含量直接相关,tn越大,表示微胶囊越难破裂,壳层中壳聚糖含量越低;tn越小,表示微胶囊越容易破裂,壳层中壳聚糖含量越高。

图4 微胶囊缓释曲线Fig.4 Controlled release curves of MCP
对实验数据进行拟合,结果见表4。R2均大于0.97,说明是缓释过程符合一级动力学特征,结果理想。

表4 缓释方程拟合表
分析表4可知,在含有CS的3组微胶囊中,壳层破裂时间tn的顺序为MCP-2>MCP-3>MCP-4,说明这3组微胶囊中CS含量大小为MCP-4>MCP-3>MCP-2。因此分批加入甲醛可以提高微胶囊壳层中壳聚糖的含量。这是因为在缩聚阶段引入的甲醛可以将CS羟甲基化,羟甲基化的CS和反应体系中的羟甲基脲交联反应,并扩展为空间网状结构,这样形成的壳层中CS含量较高。4组微胶囊中阿维菌在水相中饱和浓度的关系为MCP-4>MCP-3>MCP-2>MCP-1,后3组壳层掺杂了CS的微胶囊缓释终点的溶液中阿维菌素的浓度大于壳层没有掺杂CS的微胶囊,说明CS提高了微胶囊对阿维菌素的包覆效果。MCP-1的动力学常数k和MCP-2接近,说明预聚合时一次性加入甲醛并不能明显改善CS交联进入壳层的效果,但是实验中加入CS可以改善微胶囊的包覆效果。这可能是因为在溶液中加入CS,提高了反应体系的黏度,降低了刚刚包覆好的微胶囊剪切破裂的可能性。MCP-3和MCP-4中阿维菌在水相中饱和浓度明显大于前两组,说明缩聚阶段加入的甲醛可以和CS先预聚,生成的羟甲基可以迅速和其他胺基反应,促进了CS交联进入壳层,并且提高了包覆率。
3 结 论
采用原位聚合法,以CS改性的UF为壁材,以溶解了阿维菌素的二甲苯为芯材,制备得到镶嵌有CS的UF微胶囊壳层缓释农药微胶囊。研究表明,分阶段加入甲醛,可以改变UF/CS的交联过程,提高CS在微胶囊的复合壳层中的含量,提高农药的包覆率和缓释效率。通过在缩聚阶段分次导入甲醛制备所得的MCP-3的平均粒径为7.14 μm、包覆率为70.39%,其缓释性能良好,是较理想的缓释微胶囊。
[1] 邹洪涛.环境友好型包膜缓释肥料研制及其养分控释机理的研究[D].沈阳:沈阳农业大学,2007:16-19.
[2] 郭振铎,于曦,刘彤,等.高效缓释化肥甲醛脲[J].天津师范大学学报(自然科学版),1998,18(4):41-44.
[3] ZHANG Y H,GU J Y,TAN H Y,etal.Fabrication,performances,and reaction mechanism of urea-formaldehyde resin adhesive with isocyanate[J].Journal of Adhesion Science & Technology,2013,27(20):2191-2203.
[4] KWEON H Y,UM Y,PARK H.Structural and thermal characteristics of antheraea pernyi silk fibroin/chitosan blend film[J].Polymer,2001,42(15):6651-6656.
[5] PUTTIPIPATKHACHORN S,NUNTHANI J,YAMAMOTOC K,etal.Drug physical state and drug-polymer interaction on drug release from chitosan matrix films[J].Journal of Controlled Release,2001,75(1/2):143-153.
[6] 曲丽君,张吉强,郭肖青,等.N-乙酰化壳聚糖膜的制备及其结构与性能表征[J].印染助剂,2011,28(9):17-19.
[7] YONG S K,SRIVASTAVA M,KUNHIKRISHNAN A,etal.Environmental applications of chitosan and its derivatives[J].Reviews of Environmental Contamination & Toxicology,2015,233:1-43.
[8] GUAN Y,QI X M,CHEN G G,etal.Facile approach to prepare drug-loading film from hemicelluloses and chitosan[J].Carbohydrate Polymers,2016,153:542-548.
[9] QU R J,SUN Y Z,WANG C H,etal.Syntheses and properties of carboxymethyl chitosan/urea-formaldehyde snake-cage resins[J].Journal of Applied Polymer Science,2002,84(2):310-317.
[10] WANG R G,HU H L,HE X D,etal.Synthesis and characterization of chitosan/urea-formaldehyde shell micro-capsules containing dicyclopentadiene[J].Journal of Applied Polymer Science,2011,121(4):2202-2212.
[11] 赵媛,陈宜昭,王娟,等.纳米纤维素/聚乳酸复合材料的降解性能[J].包装工程,2016(11):20-26.
[12] 李扬,王仲妮.阿司匹林/壳聚糖聚集体的形成和释放行为[J].中国海洋药物,2016,35(6):72-78.
PreparationandSustained-ReleaseofMicrocapsulesConsistingofChitosan/Urea-FormaldehydeResin
YEPeng-fei1,CHENKui1,JILi-jun1,ZHUJia-wen1,SHENGYong2
(1.ChemicalEngineeringResearchCenter,EastChinaUniversityofScienceandTechnology,Shanghai200237,China;2.ChengduR&DCenterofSinochemFertilizerCompanyLimited,Chengdu610015,China)
A series of microcapsules were prepared with urea-formaldehyde resin (UF)/chitosan (CS) as the shell,and avermectin xylene solution as the core.The chemical structure,composition and morphology of the microcapsules were characterized by FT-IR,GSD and SEM,and the sustained-release properties were studied.The results show that the formaldehyde introduced in the pre-polymerization stage of the polycondensation can increase the content of chitosan in shell layer.Therefore,the encapsulation rate of avermectin and sustained-release rate of the microcapsules are improved.Under optimized preparation conditions,the particle size of MCP is7.14μm and encapsulation efficiency is more than70%.
microcapsule; chitosan; urea-formaldehyde resin; sustained-release pesticide
TB332
A
1006-3080(2017)05-0627-05
10.14135/j.cnki.1006-3080.2017.05.005
2016-12-26
叶鹏飞(1991-),男,河南人,硕士生,主要研究方向为缓释农药微胶囊。E-mail:ypf1_2_6@126.com
陈 葵,E-mail:chenkui@ecust.edu.cn

