乌司他丁联合醒脑静注射液治疗重度颅脑损伤的临床研究
王华民,齐平建,于 东,史 进,董虹廷,付 浩,李钦涛,陈 洋(南阳市中心医院神经外一科,河南南阳473000)
乌司他丁联合醒脑静注射液治疗重度颅脑损伤的临床研究
王华民*,齐平建#,于 东,史 进,董虹廷,付 浩,李钦涛,陈 洋(南阳市中心医院神经外一科,河南南阳473000)
目的:探讨乌司他丁注射液联合醒脑静注射液治疗重度颅脑损伤的临床效果及安全性。方法:选取2014年9月-2015年11月我院收治的重度颅脑损伤患者120例作为研究对象,按照治疗方案将患者分为乌司他丁组、醒脑静组和联合组,各40例。3组患者入院后均及时给予常规治疗。在常规治疗基础上,乌司他丁组患者给予乌司他丁注射液20万单位,ivgtt,bid;醒脑静组患者给予醒脑静注射液20 mL,ivgtt,qd;联合组患者给予乌司他丁注射液联合醒脑静注射液,用法同上(两药间隔1 h滴注)。3组患者均连续治疗14 d。观察3组患者治疗前后的血清炎症因子[C反应蛋白(CRP)、白细胞介素1(IL-1)、IL-6和肿瘤坏死因子α(TNF-α)]和颅脑损伤血清学指标[神经元特异性烯醇化酶(NSE)、髓鞘碱性蛋白(MBP)和S100B蛋白(S100B)]水平、格拉斯哥昏迷(GCS)评分、治疗后的格拉斯哥预后(GOS)评分,并记录治疗过程中不良反应发生情况。结果:治疗前,3组患者血清炎症因子、颅脑损伤血清学指标和GCS评分比较,差异均无统计学意义(P>0.05)。治疗后,3组患者炎症因子水平均较治疗前显著降低,乌司他丁组显著低于醒脑静组,联合组显著低于两单药组,差异均有统计学意义(P<0.05);3组患者颅脑损伤血清学指标水平和GCS评分均显著改善,且联合组均显著优于两单药组,差异均有统计学意义(P<0.05),但乌司他丁组与醒脑静组比较,差异均无统计学意义(P>0.05)。治疗后6个月,联合组患者GOS评分[(4.17±0.81)分]显著优于乌司他丁组[(3.05±0.97)分]和醒脑静组[(2.97±0.89)分],差异均有统计学意义(P<0.05);但乌司他丁组与醒脑静组比较,差异无统计学意义(P>0.05)。治疗过程中,联合组患者的不良反应发生率(27.50%)显著低于乌司他丁组(50.00%)和醒脑静组(42.50%),差异均有统计学意义(P<0.05);但乌司他丁组与醒脑静组比较,差异无统计学意义(P>0.05)。结论:乌司他丁注射液联合醒脑静注射液可显著降低重度颅脑损伤患者血清炎症因子水平,减轻颅脑损伤,保护脑组织,改善患者近期预后,且安全性较高。
乌司他丁注射液;醒脑静注射液;重度颅脑损伤;炎症因子;颅脑损伤血清学指标
重度颅脑损伤是外科常见危急重症,主要以创伤和应激反应为特点,可引起严重的全身炎症反应综合征(SIRS)、机体内环境紊乱和脑氧代谢失衡,发生率可高达40%[1]。乌司他丁是从人体尿液中提取的广谱蛋白酶抑制剂,其在抑制炎症反应、细胞凋亡和减轻脑水肿等方面发挥着积极的作用,对重型颅脑损伤患者的治疗具有一定的临床价值[2-3]。醒脑静注射液能明显改善患者脑水肿和脑缺氧症状,增强组织细胞耐缺氧能力和对中枢神经系统的平衡调节作用,缓解神经系统症状,促进清醒和神经功能的恢复,改善预后[4]。研究发现乌司他丁注射液联合醒脑静注射液可显著抑制急性脑出血患者的炎症反应,保护脑组织,减轻脑水肿,同时能加强促醒作用,改善微循环和脑出血预后[5]。鉴于此,本研究探究了乌司他丁注射液联合醒脑静注射液治疗重度颅脑损伤的临床效果及安全性,旨在为其临床治疗提供参考。
1 资料与方法
1.1 纳入与排除标准
纳入标准:(1)颅脑创伤后24 h内;(2)颅脑CT检测确诊为颅脑损伤;(3)格拉斯哥昏迷(GCS)评分3~8分,并伴有不同程度的意识障碍;(4)年龄>18岁;(5)患者家属均知情同意并签署知情同意书。
排除标准:(1)合并癫痫、脑部肿瘤等疾病者;(2)合并精神障碍性疾病者;(3)颅脑创伤前合并急性或慢性感染性疾病者;(4)严重肝肾功能不全者;(5)对本研究药物存在禁忌证或严重过敏者;(6)失血性休克者。
1.2 研究对象
本研究方案经医院医学伦理委员会审核通过后,选取2014年9月-2015年11月我院急诊外科和神经外科收治的重度颅脑损伤患者120例作为研究对象,按照治疗方案将其分为乌司他丁组、醒脑静组和联合组,各40例。3组患者的年龄、性别、致伤原因和损伤类型等一般资料比较,差异均无统计学意义(P>0.05),具有可比性,详见表1。
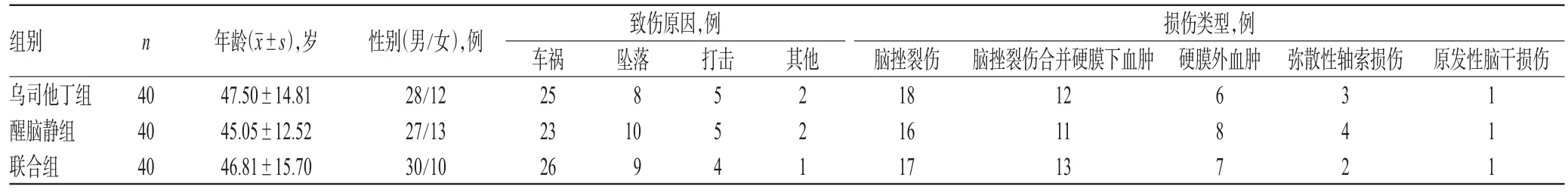
表1 3组患者一般资料比较Tab 1Comparison of general information of patients among 3 groups
1.3 研究方法
3组患者入院后均及时给予常规治疗,包括保持呼吸道畅通、吸氧、降低颅内压、止血、维持水电解质/酸碱平衡、营养支持、控制血压/血糖等;患者若存在手术指征则及时给予开颅清除血肿术或去骨板减压术。乌司他丁组患者在常规治疗基础上给予乌司他丁注射液(广东天普生化医药股份有限公司,批准文号:国药准字H20040506,规格:2 mL∶10万单位)20万单位,ivgtt,bid;醒脑静组患者在常规治疗基础上给予醒脑静注射液(无锡济民可信山禾药业股份有限公司,批准文号:国药准字Z32020563,规格:10 mL/支)20 mL,ivgtt,qd;联合组患者在常规治疗基础上给予乌司他丁注射液联合醒脑静注射液,用法同上(两药间隔1 h滴注)。3组患者均连续治疗14 d。
1.4 观察指标
(1)观察3组患者治疗前后的血清炎症因子[C反应蛋白(CRP)、白细胞介素1(IL-1)、IL-6和肿瘤坏死因子α(TNF-α)]水平。采用免疫透射比浊法测定CRP,采用放射免疫分析(RIA)法测定其余3项指标,试剂盒均购自深圳晶美生物工程有限公司。(2)观察3组患者颅脑损伤血清学指标[神经元特异性烯醇化酶(NSE)、髓鞘碱性蛋白(MBP)和S100B蛋白(S100B)]水平。采用酶联免疫吸附测定(ELISA)法检测,试剂盒均购自武汉博士德生物工程有限公司。(3)观察3组患者治疗前后GCS评分[6]。其包括睁眼反应、语言反应和肢体运动3个方面,总分13~14分为轻度昏迷,9~12分为中度昏迷,3~8分为重度昏迷。(4)观察3组患者治疗6个月后的格拉斯哥预后评分(GOS)[7-8]。5分为痊愈良好(恢复正常生活,可有轻度缺陷),4分为中度残疾(尚可独立生活,可在保护下工作),3分为重度残疾(生活不能自理,需要照顾),2分为植物生存(仅存在眼部活动和睡眠周期),1分为死亡。(5)记录3组患者治疗过程中不良反应的发生情况。
1.5 统计学方法
采用SPSS 20.0软件对数据进行统计分析。计量资料以±s表示,采用F检验;计数资料和等级资料均以例数或率表示,前者采用χ2检验,后者采用秩和检验。P<0.05为差异有统计学意义。
2 结果
2.1 3组患者治疗前后血清炎症因子水平比较
治疗前,3组患者血清CRP、IL-1、IL-6和TNF-α比较,差异均无统计学意义(P>0.05)。治疗后,3组患者上述炎症因子水平均较治疗前显著降低,乌司他丁组水平显著低于醒脑静组,联合组水平显著低于两单药组,差异均有统计学意义(P<0.05),详见表2。
表2 3组患者治疗前后血清炎症因子水平比较(±s)Tab 2Comparison of levels of serum inflammatory factors among 3 groups before and after treatment(±s)
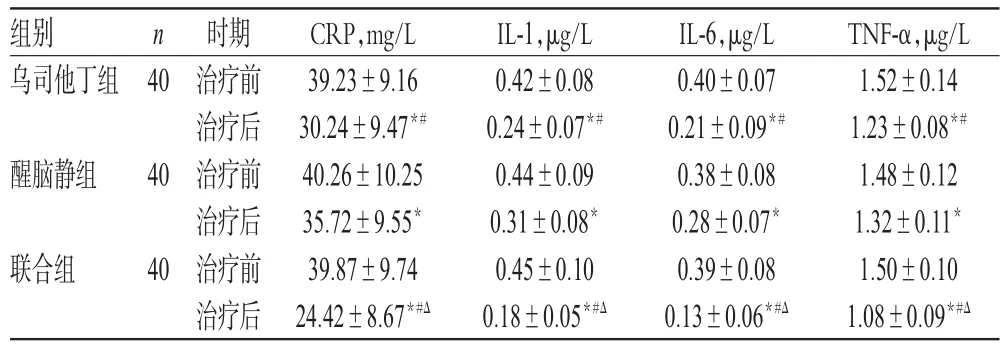
表2 3组患者治疗前后血清炎症因子水平比较(±s)Tab 2Comparison of levels of serum inflammatory factors among 3 groups before and after treatment(±s)
注:与治疗前比较,*P<0.05;与醒脑静组比较,#P<0.05;与乌司他丁组比较,ΔP<0.05Note:vs.before treatment,*P<0.05;vs.Xingnaojing group,#P<0.05;vs.ulinastatin group,ΔP<0.05
TNF-α,μg/L 1.52±0.14 1.23±0.08*#1.48±0.12 1.32±0.11*1.50±0.10 1.08±0.09*#Δ组别乌司他丁组n 40醒脑静组40联合组40时期治疗前治疗后治疗前治疗后治疗前治疗后CRP,mg/L 39.23±9.16 30.24±9.47*#40.26±10.25 35.72±9.55*39.87±9.74 24.42±8.67*#Δ IL-1,μg/L 0.42±0.08 0.24±0.07*#0.44±0.09 0.31±0.08*0.45±0.10 0.18±0.05*#Δ IL-6,μg/L 0.40±0.07 0.21±0.09*#0.38±0.08 0.28±0.07*0.39±0.08 0.13±0.06*#Δ
2.2 3组患者治疗前后颅脑损伤血清学指标比较
治疗前,3组患者血清NSE、MBP和S100B水平比较,差异均无统计学意义(P>0.05)。治疗后,3组患者上述颅脑损伤血清学指标水平均显著降低,且联合组水平显著低于两单药组,差异均有统计学意义(P<0.05);乌司他丁组与醒脑静组比较,差异均无统计学意义(P>0.05),详见表3。
表3 3组患者治疗前后颅脑损伤血清学指标比较(±s)Tab 3Comparison of serologic indexes of craniocerebral injury among 3 groups before and after treatment(±s)
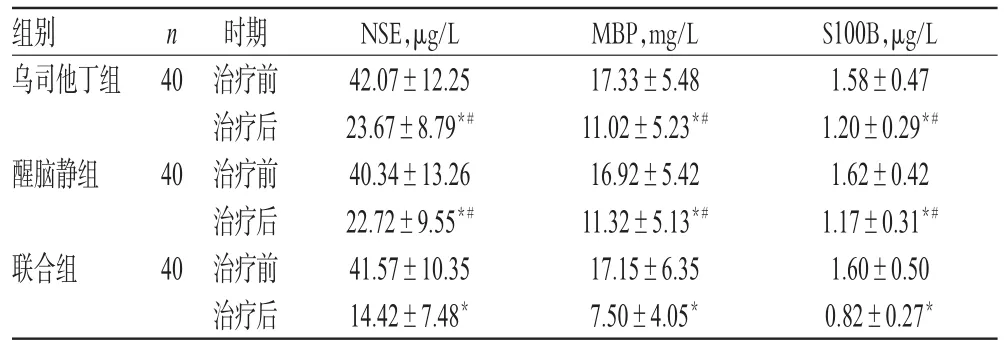
表3 3组患者治疗前后颅脑损伤血清学指标比较(±s)Tab 3Comparison of serologic indexes of craniocerebral injury among 3 groups before and after treatment(±s)
注:与治疗前比较,*P<0.05;与联合组比较,#P<0.05Note:vs.before treatment,*P<0.05;vs.combination group,#P<0.05
S100B,μg/L 1.58±0.47 1.20±0.29*#1.62±0.42 1.17±0.31*#1.60±0.50 0.82±0.27*组别乌司他丁组n 40醒脑静组40联合组40时期治疗前治疗后治疗前治疗后治疗前治疗后NSE,μg/L 42.07±12.25 23.67±8.79*#40.34±13.26 22.72±9.55*#41.57±10.35 14.42±7.48*MBP,mg/L 17.33±5.48 11.02±5.23*#16.92±5.42 11.32±5.13*#17.15±6.35 7.50±4.05*
2.3 3组患者治疗前后GCS评分比较
治疗前,3组患者GCS评分比较,差异均无统计学意义(P>0.05)。治疗后3、7、14 d,3组患者GCS评分均较治疗前显著升高,差异有统计学意义(P<0.05)。治疗后7、14 d,联合组患者GCS评分显著高于两单药组,差异均有统计学意义(P<0.05);乌司他丁组与醒脑静组比较,差异均无统计学意义(P>0.05),详见表4。
表4 3组患者治疗前后GCS评分比较(±s,分)Tab 4Comparison of GCS scores among 3 groups before and after treatment(±s,score)

表4 3组患者治疗前后GCS评分比较(±s,分)Tab 4Comparison of GCS scores among 3 groups before and after treatment(±s,score)
注:与治疗前比较,*P<0.05;与联合组比较,#P<0.05Note:vs.before treatment,*P<0.05;vs.combination group,#P<0.05
治疗后14 d 9.42±1.98*#9.45±2.07*#11.47±2.25*组别乌司他丁组醒脑静组联合组n 40 40 40治疗前6.34±0.92 6.28±1.06 6.30±0.87治疗后3 d 7.48±1.13*7.52±1.17*7.60±1.05*治疗后7 d 7.90±1.15*#7.88±1.26*#9.67±1.22*
2.4 3组患者治疗后GOS评分比较
治疗后6个月,联合组患者GOS评分[(4.17±0.81)分]显著优于乌司他丁组[(3.05±0.97)分]和醒脑静组[(2.97±0.89)分],差异均有统计学意义(P<0.05);但乌司他丁组与醒脑静组比较,差异无统计学意义(P>0.05)。
2.5 3组患者治疗过程中不良反应发生情况比较
治疗过程中,联合组患者的不良反应发生率(27.50%)显著低于乌司他丁组(50.00%)和醒脑静组(42.50%),差异均有统计学意义(P<0.05);但乌司他丁组和醒脑静组比较,差异无统计学意义(P>0.05),详见表5。
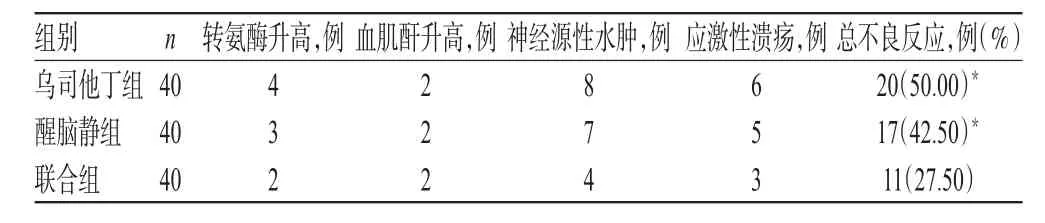
表5 3组患者不良反应发生情况比较Tab 5Comparison of the occurrence of ADR among 3 groups
3 讨论
据流行病学调查结果显示,我国颅脑损伤的发病率已超过0.1%,其中重度颅脑损伤约占20%,病死率高达30%~50%,成为急诊科常见的急危重症之一[9]。重度颅脑损伤救治不及时或方法不当,均易诱发严重的应激反应。重度颅脑损伤患者昏迷时间较长,且多伴有并发症,病情进展快,如何尽早恢复患者的神经功能、提高临床疗效、改善预后是其治疗的关键。
乌司他丁作为一种内源性保护物质,可显著减少胰蛋白酶、弹性蛋白酶和脂类水解酶等多种蛋白酶释放,抑制炎症因子的表达和释放;稳定溶酶体膜,抑制溶酶体酶释放,减少蛋白分解;同时抑制氧自由基生成,改善微循环,提高缺血和炎症状态下心、脑、肝、肾等脏器实质细胞对缺氧的耐受能力,并减轻组织和脏器损伤[10]。近年来,乌司他丁注射液已被广泛应用于急性重症胰腺炎、脓毒症、SIRS、多器官功能衰竭和颅脑损伤等疾病的临床治疗,其有效性和安全性已得到较多研究的证实[10-11]。醒脑静注射液是经安宫牛黄丸组方制成的注射剂,其有效成分包括麝香、冰片、郁金和栀子等,具有清热泻火、凉血解毒和开窍醒脑之功效。研究显示,醒脑静注射液能通过血脑屏障直接作用于中枢神经系统,进而改善大脑血氧供应,调节能量代谢,清除氧自由基,减轻脑组织水肿,防止脑疝形成;同时可改善高热、中毒和卒中等引起的意识障碍[12-13]。张建军等[14]的研究发现,醒脑静注射液可有效控制重度颅脑损伤患者的高热反应,有助于患者安全度过疾病急性期,加快苏醒,提高生活质量。余丹凤等[15]的研究发现,醒脑静注射液能提高重度颅脑损伤患者1周内的清醒率,且能降低患者血清炎症因子水平,降低肺部感染发生率。
本研究的结果显示,治疗后3组患者炎症因子水平均较治疗前显著降低,联合组显著低于两单药组,乌司他丁组显著低于醒脑静组(P<0.05)。可见,乌司他丁注射液和醒脑静注射液均可显著抑制重度颅脑损伤患者急性期炎症因子的释放,控制患者炎症水平;乌司他丁的抗炎效果优于醒脑静,两药联合使用的抗炎效果优于单一用药。NSE、MBP和S100B均高度特异性地存在于中枢神经系统,在脑组织受损后透过血脑屏障释放入血,其血清水平的增加提示神经元的损伤,故三者均为评估急性颅脑损伤病情及预后的敏感指标[16]。本研究结果提示,治疗后3组患者血清NSE、MBP和S100B水平均较治疗前显著降低,联合组显著低于两单药组(P<0.05),但乌司他丁组和醒脑静组比较,差异均无统计学意义(P>0.05)。这说明乌司他丁注射液联合醒脑静注射液能更有效地减轻脑组织损伤,加速脑组织损伤后的康复。GCS评分可客观反映颅脑损伤患者的昏迷程度,GOS评分可反映患者短期的预后情况。本研究结果显示,联合组患者治疗后7、14 d的GCS评分以及治疗6个月后的GOS评分均显著优于两单药组(P<0.05),但乌司他丁组和醒脑静组比较,差异均无统计学意义(P>0.05)。这表明乌司他丁注射液联合醒脑静注射液可显著减轻重度颅脑损伤患者的昏迷程度,改善近期预后,提高生活质量。此外,联合组患者的总不良反应发生率明显低于两单药组,表明乌司他丁注射液联合醒脑静注射液具有较高的安全性,同时可显著减少治疗过程中的肝肾损伤、神经源性水肿和应激性溃疡发生的风险。
综上所述,乌司他丁注射液联合醒脑静注射液可显著降低重度颅脑损伤患者血清炎症因子水平,减轻颅脑损伤,保护脑组织,改善患者近期预后,且安全性较高。然而,本研究的样本量较小,且并未对3组患者进行长期跟踪随访,故本研究结论仍需大样本、高质量的随机对照研究加以验证。
[1]Brain Trauma Foundation,American Association of Neurological Surgeons,Congress of Neuroloical Surgeons,et al.Guidelines for the management of severe traumatic brain injury:Ⅺ Ⅴhyperventilation[J].J Neurotrauma,2007,24(Suppl 1):S87-S90.
[2]Hui L,Shen F,Chang H,et al.Effects of ulinastatin on cerebral oxygen metabolism and CRP levels in patients with severe traumatic brain injury[J].Exp Ther Med,2014,7(6):1683-1686.
[3]Wang X,Zhuang X,Wei R,et al.Protective effects of acanthopanax vs.ulinastatin against severe acute pancreatitis-induced brain injury in rats[J].Int Immunopharmacol,2015,24(2):285-298.
[4]Xu M,Su W,Xu QP,et al.Effect of Xingnaojing injection on cerebral edema and blood-brain barrier in rats following traumatic brain injury[J].Chin J Traumatol,2010,13(3):158-162.
[5]韩世伟,赵义,任吉祥.乌司他丁联合醒脑静治疗急性脑出血的疗效研究[J].广州中医药大学学报,2015,32(1):19-22.
[6]李继禄,杨洪菊,郭桂华,等.格拉斯哥昏迷评分动态曲线的记录及临床意义[J].中华创伤杂志,2005,21(9):708-709.
[7]Leng YX,Yang SG,Song YH,et al.Ulinastatin for acute lung injury and acute respiratory distress syndrome:a systematic review and meta-analysis[J].World J Crit Care Med,2014,3(1):34-41.
[8]Qin ZS,Tian P,Wu X,et al.Effects of ulinastatin administered at different time points on the pathological morphologies of the lung tissues of rats with hyperthermia[J].Exp Ther Med,2014,7(6):1625-1630.
[9]赵成之,陈建良.急性颅脑损伤的流行病学研究进展[J].中华神经医学杂志,2006,5(3):319-321.
[10]郭华,陈炅,索冬卫.奥曲肽联合乌司他丁治疗急性重症胰腺炎临床疗效及安全性分析[J].中华医学杂志,2015,95(19):1471-1474.
[11]Li G,Li T,Li Y,et al.Ulinastatin inhibits oxidant-induced endothelial hyperpermeability and apoptotic signaling[J].Int J Clin Exp Pathol,2014,7(11):7342-7350.
[12]卢志刚,刘芸.醒脑静注射液对急性脑梗死血瘀证患者疗效及相关指标的影响[J].中国药房,2016,27(21):2898-2900.
[13]郭晓明,刘文科.醒脑静注射液对重型颅脑损伤患者肠黏膜通透性及血浆二胺氧化酶的影响[J].中国老年学杂志,2015,35(8):2114-2115.
[14]张建军,朱镇宇,张俊.醒脑静注射液在治疗重症颅脑损伤中抗高热和促醒作用的疗效观察[J].中国中西医结合急救杂志,1999,6(1):5-7.
[15]余丹凤,沈盛晖,张庚,等.醒脑静注射液对重症颅脑损伤患者细胞因子及肺部感染的影响[J].中国中西医结合急救杂志,2005,12(5):289-291.
[16]Brouns R,de Vil B,Cras P,et al.Neurobiochemical markers of brain damage in cerebrospinal fluid of acute ischemic stroke patients[J].Clin Chem,2010,56(3):451-458.
Clinical Study of Ulinastatin Combined with Xingnaojing Injection in the Treatment of Severe Craniocerebral Injury
WANG Huamin,QI Pingjian,YU Dong,SHI Jin,DONG Hongting,FU Hao,LI Qintao,CHEN Yang(Dept.One of Neurosurgery,Nanyang Central Hospital,Henan Nanyang 473000,China)
OBJECTIVE:To explore clinical efficacy and safety of Ulinastatin injection combined with Xingnaojing injection in the treament of severe craniocerebral injury(CCI).METHODS:A total of 120 severe CCI patients selected from our hospital during Sept.2014-Nov.2015 were divided into ulinastatin group,Xingnaojing group and combination group according to therapy plan,with 40 cases in each group.Three groups were given routine treatment timely after admission.On the basis of routine treatment,Ulinastatin group additionally
Ulinastatin injection 200 000 U,ivgtt,bid;Xingnaojing group additionally received Xingnaojing injection 20 mL,ivgtt,qd;combination group additionally received Ulinastatin injection combined with Xingnaojing injection,same usage as above(with 1 h intervals).Three groups received therapy for consecutive 14 d.Serum inflammatory factors(CRP,IL-1,IL-6,TNF-α),serologic indexes of craniocerebral injury[neuron specific enolase(NSE),myelin basic protein(MBP),S100B protein(S100B)]and GCS scores before and after treatment as well as GOS scores after treatment were all observed in 3 groups.The occurrence of ADR was recorded during treatment.RESULTS:Before treatment,there was no statistical significance in serum inflammatory factors,serologic indexes of craniocerebral injury or GCS scores among 3 groups(P>0.05).Compared to before treatment,inflammatory factors of 3 groups were decreased significantly after treatment,the ulinastatin group was significantly lower than the Xingnaojing group,combination group was significantly lower than two single drug groups,with statistical significance(P<0.05).Levels of serologic indexes of craniocerebral injury and GCS scores of 3 groups were improved significantly,and the combination group was significantly better than the two single drug groups,with statistical significance(P<0.05).There was no statistical significance between ulinastatin group and Xingnaojing group(P>0.05).Six months after treatment,GOS score of combination group(4.17±0.81)was significantly better than those of ulinastatin group(3.05±0.97)and Xingnaojing group(2.97±0.89),with statistical significance(P<0.05);there was no statistical significance between ulinastatin group and Xingnaojing group(P>0.05).Duringtreatment,the incidence of ADR in combination group(27.50%)was significantly lower than ulinastatin group(50.00%)and Xingnaojing group(42.50%),with statistical significance(P<0.05);there was no statistical significance between ulinastatin group and Xingnaojing group(P>0.05).CONCLUSIONS:Ulinastatin injection combined with Xingnaojing injection can significantly decrease serum inflammatory factor levels,relieve craniocerebral injury,protect cerebral tissue and improve shortterm prognosis with good safety.
Ulinastatin injection;Xingnaojing injection;Severe craniocerebral injury;Inflammatory factor;Serlolgic index of craniocerebral injury
R651.1
A
1001-0408(2017)29-4119-04
DOI10.6039/j.issn.1001-0408.2017.29.24
*主治医师,硕士。研究方向:神经外科。电话:0377-6300091。E-mail:huaminw@163.com
#通信作者:主任医师。研究方向:神经外科。电话:0377-6300091。E-mail:qipingjian@163.com
2016-09-26
2017-07-30)
(编辑:陶婷婷)

