重组人透明质酸酶促皮下注射扩散研究
姜廷,杨伟,张金龙,吕鹏,侯利华,陈薇
军事医学科学院 生物工程研究所,北京 100071
重组人透明质酸酶促皮下注射扩散研究
姜廷,杨伟,张金龙,吕鹏,侯利华,陈薇
军事医学科学院 生物工程研究所,北京 100071
目的:探究重组人透明质酸酶(rHuPH20)促皮下注射药物的扩散能力,解决皮下快速给药和大体量给药难题。方法:以台盼蓝模拟联用药物作为可视化示踪剂,研究rHuPH20对皮下注射药物扩散速率的影响;用生理盐水造新西兰兔水肿模型,研究rHuPH20对皮下注射输液量的影响。结果:rHuPH20可极大地增加皮下注射药物的扩散速率和输液量。结论:rHuPH20作为扩散剂使用,可弥补传统皮下注射微小输液量的缺陷,满足皮下注射不同输液量的需求,在替代药物静脉输液方面具有潜在应用价值。
透明质酸;透明质酸酶;皮下输液;扩散作用
皮下注射是经典的微量体积注射方式,注射液必须经由皮肤间质进入作用靶点,而这种由胶原蛋白、弹性蛋白、纤维连接蛋白和透明质酸(hy⁃aluronic acid,HA)等结构性大分子组成的皮肤间质,具有复杂的三维立体结构,限制了皮下注射的扩散速率和输液量[1]。其中HA是皮肤间质复杂立体结构的“基架”,同时HA的亲水性促使水分子嵌入网状结构内部,构成网状实体弹性结构,阻碍了注射液的扩散吸收[2]。我们利用重组人透明质酸酶rHuPH20对皮下HA的酶解作用[3],破坏皮肤间质立体结构,降低其结构致密性和黏弹性,进而增加了皮下注射药物的扩散速率和输液量。rHuPH20作为扩散剂辅助皮下注射是一种新的皮下给药方式,相比于传统皮下注射具有快速扩散吸收、大体量输液和高生物利用度等优势,满足了大体量皮下注射和快速给药的需求。
1 材料与方法
1.1 材料
新西兰兔(雄性,3 kg)购自中国食品药品检定研究院;BALB/c裸鼠(雄性,7周龄)购自北京维通利华实验动物技术有限公司;rHuPH20(1.1×105U/mg)由军事医学科学院生物工程研究所抗体与疫苗研究室制备和提供;移液器为Gilson公司产品;台式离心机为Hitachi公司产品;盐酸氯胺酮购自福建古田药业有限公司;台盼蓝购自Sigma公司;注射用生理盐水购自国药集团化学试剂有限公司;其他试剂为国产分析纯产品。
1.2 rHuPH20促皮下注射扩散效果观察
以BALB/c裸鼠为研究对象,以台盼蓝模拟联用药物作为可视化示踪剂,通过监测台盼蓝的扩散速率,评价rHuPH20的促扩散作用。将BALB/c裸鼠随机分成5组,每组8只(表1),称重后,腹腔注射盐酸氯胺酮(150 mg/kg)麻醉,标记背部正中左侧1 cm处为给药位点,各组给药位点处皮下注射示踪染料2%台盼蓝20 μL,1 min后皮下注射rHuPH20,注射结束立刻用卡尺测量台盼蓝染色面积,并以此为初始时间节点,观察并记录2、5、10、20、30 min时染色扩散横向直径D1和纵向直径D2,根据面积计算公式(Area=D1×D2×π/4)计算各时间节点的台盼蓝扩散面积。

表1 rHuPH20促皮下注射扩散实验
1.3 rHuPH20增加皮下注射输液量和治疗皮下水肿药效评价
以新西兰兔为研究对象,皮下注射大体量生理盐水制造水肿模型。造模前预注射rHuPH20,评价rHuPH20对皮下注射输液量的影响;造模后注射rHuPH20,以水肿体积为指标,评价rHuPH20治疗水肿的药效。耳缘静脉注射盐酸氯胺酮(150 mg/kg)麻醉新西兰兔,彻底麻醉后用剃毛器剃除背部及左侧绒毛,裸露表皮,背部正中左侧2 cm处标记注射位点,进行皮下注射,记录水肿体积。实验分为3组:第1组皮下注射生理盐水125 mL(对照);第2组皮下注射生理盐水125 mL,水肿模型完成后,注射 100 μL rHuPH20(1000 IU/mL)(考察rHuPH20治疗皮下水肿效果);第3组预先注射100 μL rHuPH20(1000 IU/mL),2 min后皮下注射生理盐水125 mL(考察rHuPH20对皮下注射输液量的影响)。
2 结果
2.1 rHuPH20促皮下注射扩散作用
如图1,时间节点为10 min时,注射rHuPH20各组示踪染料扩散面积显著大于对照组,且高剂量rHuPH20组示踪染料扩散面积高于低剂量组,证明rHuPH20促进皮下注射药物扩散,且具有一定的剂量依赖性。

图1 rHuPH20促皮下注射药物扩散实验
采用二维测量法测定不同时间皮下注射示踪染料的扩散面积(表2)。0 min时,各组之间的台盼蓝扩散面积差异无统计学意义(P>0.05),即初始扩散面积无显著性差异;测量扩散终点(30 min)时,各rHuPH20注射组与对照组示踪染料扩散面积差异有统计学意义(P<0.05),其中10 U、50 U和100 U rHuPH20组分别为对照组扩散面积的157%、173%和173%。表明rHuPH20具有良好的促扩散作用。

表2 不同剂量rHuPH20对台盼蓝扩散的影响
为进一步研究rHuPH20酶活浓度与扩散速率的关系,对各组数据进行了深度分析。统计不同酶解时间台盼蓝扩散面积增加量与初始面积的百分比,获得各组在不同时间节点内台盼蓝的扩散速率,并绘制扩散速率曲线图(图2)。不同酶解时间示踪染料扩散速率数据类型为一个重复测量因素的两因素设计一元定量资料,统计方法为混合效应模型法(mixed effects model),以P<0.05为差异有统计学意义,统计软件为SAS 9.2(表3)。各酶解时间节点组间两两比较结果表明,2 min时,各组之间的台盼蓝扩散速率有显著性差异(P<0.05),表明扩散速率与rHuPH20酶活浓度具有剂量关系,经100 U rHuPH20处理后台盼蓝扩散速率为对照组的748%;10、20和30 min时,50 U和100 U rHuPH20组促台盼蓝扩散速率无显著差异(P>0.05);30 min时,10 U 和 50 U rHuPH20组、50 U和100 U rHuPH20组扩散作用无显著性差异(P>0.05),表明rHuPH20促扩散作用随时间推移逐渐降低。
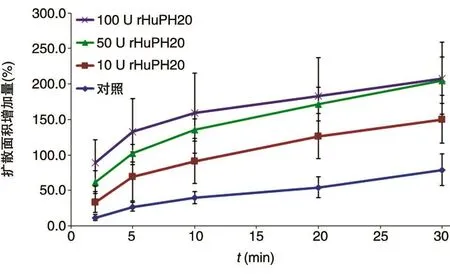
图2 不同时间节点扩散面积增加量与初始面积的百分比

表3 组间两两比较统计结果
2.2 rHuPH20治疗皮下水肿和增加皮下注射输液量
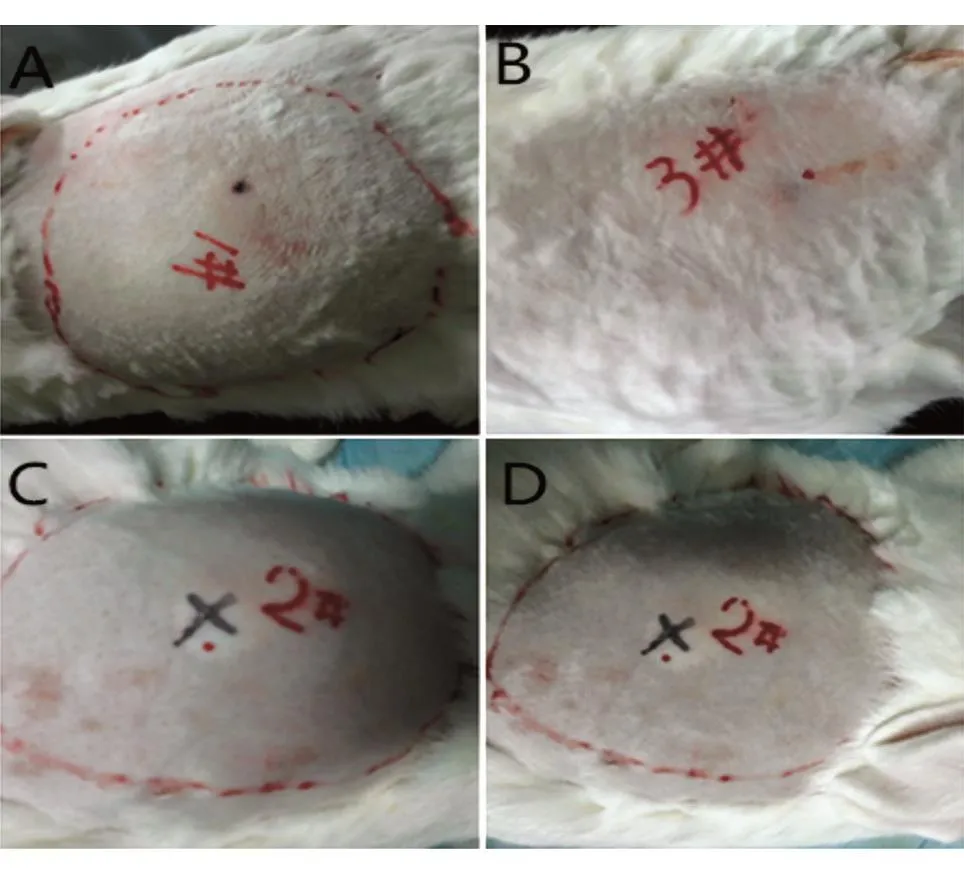
图3 新西兰兔脊背左侧大体量注射生理盐水制造水肿模型,造模前注射和造模后注射rHuPH20对水肿体积的影响
如图3A所示,皮下注射生理盐水125 mL造成局部皮下水肿,水肿体积为60.2 cm3(约10 h后水肿消失,解剖发现皮下有块状白色凝胶);而造模前预注射 100 μL rHuPH20(1000 IU/mL)2 min后,皮下注射生理盐水125 mL未发生组织形变和肿胀(图3B),表明在不引起组织损伤的条件下,rHuPH20可显著提高皮下注射输液量。皮下注射生理盐水125 mL后,造成局部皮下水肿,水肿体积为70.2 cm3(图3C);而造模后注射100 μL rHuPH20(1000 IU/mL),局部皮下水肿逐渐减小,20 min后水肿消失(图3D),证明rHuPH20可以有效治疗局部皮下水肿。
3 讨论
自1940年始,从动物组织提取的透明质酸酶已应用于临床实验性治疗,但低纯度引起的高免疫原性和毒性作用限制了其在临床上的推广。21世纪初,美国Halozym公司利用基因重组技术在CHO细胞中表达了rHuPH20,并于2005年经美国FDA批准成为第一个上市的rHuPH20药物,随后rHuPH20注射剂和PEG-rHuPH20相继于2010和2016年上市,但国内在rHuPH20制剂上还存在空白。本实验室建立了高纯度rHuPH20制备方法,拟利用rHuPH20解决皮下注射快速给药和大体量输液难题。我们用rHuPH20酶解皮肤间质中的HA,破坏了皮肤间质结构致密性和黏弹性,显著提高了皮下注射药物的扩散速率和输液量。在本实验条件下,100 U rHuPH20预处理后皮下注射示踪染料初始扩散速率可提高6.48倍,经条件优化后可得到10倍甚至几十倍初始扩散速率,在急性病症治疗和三防(防生、防化、防核)解毒中具有潜在应用价值。同时,rHuPH20在体内半衰期较短[4],意味着rHuPH20可能带来的皮肤组织损伤和炎症反应极小。
rHuPH20作为辅助扩散剂用于皮下注射是一种新型的“大体量皮下给药方式”,相比于静脉注射,具有技术要求低、操作简单、成本低廉和输液效率高等优势,可替代静脉注射而成为慢性疾病患者自助型注射类药物给药方式,如糖尿病患者注射胰岛素[5];替代不便于静脉注射环境和条件的大体量注射方式,如皮肤烧伤患者的输液[6];为因溶解度、生物利用度和稳定性等因素限制而不能进行静脉注射的药物提供新的给药途径。这种大体量注射方式可弥补传统皮下注射微小输液量的缺陷,满足皮下注射不同输液量的需求。
[1]Bookbinder L H,Hofer A,Haller M F,et al.A re⁃combinanthuman enzyme for enhanced interstitial transport of therapeutics[J].J Control Rel,2006,114(2):230-241.
[2]Bian S,He M,Sui J,et al.The self-crosslinking smart hyaluronic acid hydrogels as injectable three-di⁃mensional scaffolds for cell culture[J].Colloids Surf B Biointerfaces,2016,140:392-402.
[3]Chen K J,Sabrina S,Safory N S,et al.Constitutive expression of recombinant human hyaluronidase PH20 by Pichia pastoris[J].J Biosc iBioeng,2016,122(6):673-678.
[4]Vaughn D E,Muchmore D B.Use of recombinant hu⁃man hyaluronidase to accelerate rapid insulin ana⁃logue absorption:experience with subcutaneous injec⁃tion and continuous infusion[J].Endocr Pract,2011,17(6):914-921.
[5]Garg S K,Buse J B,Skyler J S,et al.Subcutaneous injection of hyaluronidase with recombinant human in⁃sulin compared with insulin lispro in type 1 diabetes[J].Diabetes,Obes Metab,2014,16(11):1065-1069.
[6]Buehner M,Pamplin J,Studer L,et al.Oxalate ne⁃phropathy after continuous infusion of high-dose vita⁃min C as an adjunct to burn resuscitation[J].J Burn Care Res,2016,37(4):374-383.
Study of rHuPH20 Pharmacological Property on Facilitat⁃ing Diffusion of Subcutaneous Injection
JIANG Ting,YANG Wei,ZHANG Jin-Long,LYU Peng,HOU Li-Hua*,CHEN Wei*
Beijing Institute of Biotechnology,Beijing 100071,China
Objective:To study the recombinant human hyaluronidase rHuPH20 property of improving the diffu⁃sion of subcutaneous injection so as to realize quick subcutaneous injection and high-dose subcutaneous injection.Methods:Trypan blue was used as a visualized tracer to simulate combined medicine to study influence of rH⁃uPH20 on diffusion rate of subcutaneous injection.The New Zealand rabbit model of subcutaneous oedema was made by subcutaneous injection of saline to study influence of rHuPH20 on doses of subcutaneous injection.Re⁃sults:Subcutaneous co-administration of rHuPH20 greatly improves diffusion rate and doses of subcutaneous infu⁃sion.Conclusion:rHuPH20 can be co-administraed as diffusion agent to makes up the defects of traditional sub⁃cutaneous injection and meet the needs of various doses of subcutaneous injection,which has potential to replace the intravenous infusion.
hyaluronic acid;hyaluronidase;subcutaneous delivery;diffusion
R91;Q75
A
1009-0002(2017)05-0647-04
10.3969/j.issn.1009-
*Co-corresponding authors,HOU Li-Hua,E-mail:houlihua@sina.com;CHEN Wei,E-mail:cw0226@foxmail.com
2017-04-17
姜廷(1986- ),女,硕士研究生,(E-mail)18518920805@163.com
侯利华,(E-mail)houlihua@sina.com;陈薇,(E-mail)cw0226@foxmail.com

